Анализ на синдром ди джорджи
Генетическое исследование, позволяющее выявить причинный фактор – мутацию (отсутствие или недостаточное функционирование некоторых генов (или их частей) на 15-й отцовской хромосоме (синдром Прадера – Вилли) или мутацию материнского генетического материала аналогичного генетического региона (синдром Ангельмана, а также мутация (выпадение одного из участков) 22-й хромосомы, ведущая к гипоплазии вилочковой и паращитовидной желез (синдром Ди Джорджи).
Синонимы русские
Тест на синдромы “смежных генов”, FISH-тест на генетические аномалии, FISH-анализ на Прадера – Вилли, Ангельмана, Ди Джорджи.
Синонимы английские
The test for syndromes of “adjacent genes”, FISH analysis on Prader-Willy syndrome (PWS), FISH analysis for Angelman syndrome (AS), FISH analysis for Di George syndrome (DGS), FISH-test for genetic abnormalities.
Метод исследования
Дифференциальное окрашивание хромосом.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Исследование проводится в состоянии сытости, не рекомендуется сдавать кровь на данное исследование натощак.
- Исключить (по согласованию с врачом) прием антибактериальных и химиотерапевтических препаратов в течение 14 дней до исследования.
- Исследование рекомендуется проводить не ранее чем через 2 недели после перенесенных инфекционных/острых воспалительных заболеваний.
Общая информация об исследовании
Цитогенетический анализ проводится методом флуоресцентной гибридизации in situ (FISH, от англ. fluorescence in-situ hybridization), который является одним из самых современных методов диагностики хромосомных аномалий. Подробнее с методом можно ознакомиться здесь (https://helix.ru/kb/item/12-052).
Одним из преимуществ FISH-теста является его способность определять микроделеции, которые не выявляются с помощью классического кариотипирования или полимеразной цепной реакцией (ПЦР). Это имеет особое значение при диагностике микроделеционных синдромов, например Прадера – Вилли, Ангельмана, Ди Джорджи. Делеции – это хромосомные перестройки, при которых происходит потеря участка хромосомы. Микроделеции часто характеризуются сложным клиническим и поведенческим фенотипом, возникающим в результате дисбаланса нормального количества генов, расположенных в этом конкретном сегменте хромосом.
Микроделеционные синдромы определяются как группа клинически узнаваемых расстройств, характеризующихся небольшой утратой хромосомного сегмента, охватывающего несколько соседних генов, каждый из которых потенциально может вносить свой вклад в фенотип. Эти синдромы называют еще синдромами “смежных генов”. Большинство клинически значимых микроделеций, по-видимому, происходят спорадически, но в ряде случаев может обнаруживаться наследственная связь.
Велокардиофациальный синдром – наиболее частая известная интерстициальная делеция, обнаруженная у человека с частотой 1 из 4000 живорождений. Большинство потерь являются результатом события de novo, и только около 5-10% наследуются аутосомно-доминантным способом. Для диагностики этого синдрома используется несколько диагностических меток, включая синдром (аномалию) Ди Джорджи (DGS).
Синдром Ди Джорджи связан с делецией 22q11.2 и встречается у 1:3000-1:20000 новорождённых, с одинаковой частотой как у мальчиков, так и у девочек. Клинически он проявляется нарушениями иммунной системы, вплоть до тяжелого иммунодефицита из-за недоразвитости или отсутствия тимуса, гипопаратиреозом, пороками сердца, расщелиной неба, умственной отсталостью разной степени выраженности, катарактой (помутнение хрусталика). Также могут быть пороки развития мочевыделительной системы, проблемы с питанием. Больные, как правило, низкого роста и с характерными чертами лица (подбородок и рот маленькие, переносица расширена).
Синдром Прадера – Вилли (75% случаев) и 80% случаев возникновения синдрома Ангельмана связаны с микроделецией 15q11-13. Идентифицированы различные молекулярные механизмы, приводящие к этой потере. Примечательно, что при этом каждый из синдромов может сопровождаться и другими мелкими “молекулярными поломками”.
Синдром Прадера-Вилли (PWS) представляет собой сложное мультисистемное расстройство, характеризующееся множеством клинических проявлений. Встречается патология у 1:12000-1:15000 новорождённых, которые в большинстве случаев рождаются преждевременно. Как правило, пациенты с данной аномалией небольшого роста, с короткими конечностями, имеют типичные черты лица: небольшой лоб, миндалевидной формы глаза, недоразвитую верхнюю челюсть, тонкую верхнюю губу и опущенные углы рта. С самого рождения наблюдается гиперфагия (неконтролируемое потребление пищи) и в результате – ожирение, тяжелая мышечная гипотония. Также характерны гипогонадизм (синдром, сопровождающийся недостаточностью функций половых желез и нарушением синтеза половых гормонов) с недостаточным ростом во время полового созревания, нарушения терморегуляции и дневная сонливость.
Синдром Прадера – Вилли рассматривается как многоэтапное расстройство, характеризующееся тремя различными фазами:
- Первая, “гипотоническая фаза”, характеризуется разной степенью выраженности гипотонии во время неонатального периода и раннего младенчества, слабым криком, гипотермией, гипогенитализмом и слабым рефлексом сосания. В течение первого года дети с PWS дружелюбные, спокойные и ласковые.
- “Гиперфагическая фаза” обычно начинается в 1-2 года, характеризуется повышенным аппетитом, ранним началом детского ожирения, физической бездеятельностью, сниженной болевой чувствительностью, нарушенной терморегуляцией, психомоторной отсталостью, трудностью сочетанной речи и умственными нарушениями. Одновременно с изменением структуры питания меняется и поведение детей – оно становится социально неадекватным и неправильно эмоционально окрашенным (например, немотивированные вспышки гнева), появляются упрямство, лабильность настроения, импульсивность, беспокойство и обсессивно-компульсивные симптомы.
- Третья фаза – “подростковый возраст и взрослая жизнь”. На этом этапе преобладают проблемы со здоровьем, связанные с ожирением (например, сколиоз, гипертония, гиперхолестеринемия, остеопороз и т.д.). Около 10% подростков и взрослых имеют серьезные психиатрические проблемы. Примечательно, что психотические эпизоды у пациентов с PWS имеют много общих черт, включая острое начало, полиморфную и колеблющуюся симптоматику с тревогами, агитацией, аномальными верованиями и слуховыми галлюцинациями. Эти эпизоды классифицируются как острый циклоидный психоз.
Синдром Ангельмана (AS) встречается примерно у 1:10000-30000 новорождённых, и с первых лет жизни наблюдается задержка умственного и неврологического развития. Способность к невербальному общению сохранена, больные понимают больше, чем способны выразить.
К типичным чертам при данной патологии относятся брахицефалия (короткоголовость), микроцефалия (недоразвитость черепа, маленькая голова), большой рот с широко расставленными зубами, нижнечелюстной прогнатизм (выпячивание нижней челюсти, затрагивающее более низкую треть лица), глубокие и голубые глаза и гипопигментация, практически постоянная улыбка. “Типичное лицо” становится очевидным в возрасте от одного года до четырех лет, и с увеличением возраста происходит огрубление и усиление характерных черт. У пациентов с AS наблюдается гипотония с гипертонией конечностей и высокий риск развития сколиоза. Все пациенты имеют умственную отсталость с различными речевыми расстройствами. С первых лет жизни отмечаются различные неврологические нарушения (например, дрожание уголков рта, выталкивание языка, немотивированное хлопанье руками, тики). У 80% детей в возрасте от 1 мес. до 5 лет встречаются эпилептические припадки. Их трудно контролировать, и они могут быть разнообразными, начиная от атипичного отсутствия судорог, тонико-клонических припадков, миоклонических приступов и тонических приступов до эпилептического статуса. Модели ЭЭГ, наблюдаемые у пациентов с синдромом Ангельмана, очень характерны и наблюдаются у пациентов с/без судорог и могут играть важную диагностическую роль в соответствующем клиническом контексте. Уже через 10 недель после рождения могут наблюдаться приступы легко спровоцированного продолжительного смеха. Дети, как правило, гиперактивны, имеют пониженную способность концентрировать внимание и различные нарушения сна. С возрастом походка становится медленная, атаксическая и жесткая с характерным положением поднятых рук с изгибами запястий и локтей (дерганная походка марионетки). Характерны нарушения координации, хаотичные движения рук и ног. Люди с AS плохо переносят душные помещения и повышенную температуру. Кроме классических проявлений синдрома, существуют разнообразные вариации, связанные с различными генетическими причинами. Например, более мягкая эпилепсия отмечена у пациентов со спонтанной мутацией материнской копии, которая вызывает отсутствие преобразования в мозге копии гена UBE3A.
FISH-анализ позволяет достоверно диагностировать общеизвестные микроделеционные синдромы и является стандартным диагностическим методом при данной патологии. Исследование позволяет установить этиологию заболевания и сделать прогноз по дальнейшему его течению.
Для чего используется исследование?
- Для диагностики микроделеций.
Когда назначается исследование?
- Пренатальная диагностика при подозрении на наличие отклонений в развитии плода.
- Постнатальная диагностика генетической патологии у ребенка при наличии соответствующих клинических признаков.
- При планировании последующих беременностей, если в семье есть ребенок с микроделеционным синдромом.
Что означают результаты?
Положительный результат говорит о наличии в исследуемом образце микроделеции.
Отрицательный результат указывает на отсутствие искомой микроделеции, но не может достоверно опровергать заболевание, так как синдром может быть вызван другим генетическим сбоем (например, однородительской дисомией, транслокацией родительских хромосом). В процентном соотношении вероятность этого значительно меньше, но все же возможна.
Синдром Прадера-Вилли:
- встречается у 1:25000- 1:10000 новорождённых;
- с помощью обычного исследования хромосомного состава кариотипа выявить данную патологию невозможно.
Синдром Ангельмана:
- встречается примерно у 1:10000 новорождённых;
- с первых лет жизни наблюдается задержка умственного и неврологического развития.
Синдром Ди Джорджи:
- встречается у 1:3000-1:20000 новорождённых, в равной доле как у мальчиков, так и у девочек;
- характерна триада симптомов: гипоплазия тимуса и паращитовидной железы, врождённый порок сердца;
- 5-10% – аутосомно-доминантный тип наследования.
Важные замечания
FISH-тест часто используется совместно с другими методами молекулярной и цитогенетической диагностики.
Также рекомендуется
[40-006] Беременность – Пренатальный скрининг трисомий I триместра беременности (синдром Дауна)
[16-001] Исследование кариотипа
[40-007] Беременность – Пренатальный скрининг трисомий II триместра беременности
Кто назначает исследование?
Педиатр, врач-генетик, эндокринолог, невролог.
Литература
- Shaffer, L.G., Ledbetter, D.H., and Lupski, J.R. 2001, Molecular cytogenetics of contiguous gene syndromes: mechanisms and consequences of gene dosage imbalance. In: The Metabolic & Molecular Bases of Inherited Disease, C. R. Scriver, A. L. Beaudet, W. S. Sly, and D. Valle (Eds.), McGraw-Hill, Medical Publishing Division, New York, St. Louis, San Francisco, Auckland, Bogota, Caracas, Lisbon, London, Madrid, Mexico City, Milan, Montreal, New Delhi, San Juan, Singapore, Sudney, Tokyo, Toronto, 1291.
- Microdeletions and Molecular Genetics, Annick VOGELS and Jean-Pierre FRYNS. Center for Human, University of Leuven, Herestraat 49, B-3000 Leuven, Belgium, 2004-02.
- Di George, A. 1965, A new concept of the cellular basis of immunity. J. Pediatr., 67, 907.
- Clinical spectrum and molecular diagnosis of Angelman and Prader-Willi syndrome patients with an imprinting mutation.Saitoh S, Buiting K, Cassidy SB, Conroy JM, Driscoll DJ, Gabriel JM, Gillessen-Kaesbach G, Glenn CC, Greenswag LR, Horsthemke B, Kondo I, Kuwajima K, Niikawa N, Rogan PK, Schwartz S, Seip J, Williams CA, Nicholls RD, Am J Med Genet. 1997;68(2):195.
Источник

Синдром Ди Джорджи – генетическое заболевание, относящееся к группе первичных иммунодефицитов и, наряду с ослаблением иммунитета, характеризующееся многочисленными пороками развития. Симптомами этого состояния являются частые бактериальные инфекции со склонностью к тяжелому течению, врожденные пороки сердца, аномалии развития лица и другие нарушения. Диагностика синдрома Ди Джорджи основывается на исследовании сердца, щитовидных и паращитовидных желез, изучении иммунологического статуса и данных молекулярно-генетических анализов. Лечение только симптоматическое, включает хирургическую коррекцию пороков сердца и аномалий лица, заместительную иммунологическую терапию, борьбу с бактериальными и грибковыми инфекциями.
Общие сведения
Синдром Ди Джорджи (гипоплазия тимуса и паращитовидных желез, велокардиофациальный синдром) – генетическое заболевание, обусловленное нарушением эмбрионального развития третьего и четвертого фарингеальных мешков. Впервые это состояние было описано в 1965 году американским педиатром Анджело Ди Джорджи, который классифицировал его как врожденную аплазию тимуса и паращитовидных желез. Дальнейшие исследования в области генетики помогли определить, что нарушения при этом заболевании выходят далеко за рамки первичного иммунодефицита. Это дало основание для появления другого названия синдрома Ди-Джорджи. С учетом наиболее часто поражаемых органов (небо, сердце, лицо) некоторые специалисты именуют данную патологию велокардиофациальным синдромом. Ряд современных исследователей разграничивают эти два состояния и считают, что «истинный» велокардиофациальный синдром не сопровождается выраженными иммунологическими нарушениями. Встречаемость синдрома Ди Джорджи составляет 1:3 000-20 000 – такое значительное расхождение данных обусловлено тем, что достоверная и четкая граница между этим заболеванием и велокардиофациальным синдромом до сих пор не установлена. Поэтому один и тот же больной, по мнению разных специалистов, может иметь либо первичный иммунодефицит, сопровождающийся сопутствующими нарушениями, либо многочисленнее пороки развития на фоне снижения иммунитета.

Синдром Ди Джорджи
Причины синдрома Ди Джорджи
Генетическая природа синдрома Ди Джорджи заключается в повреждении центральной части длинного плеча 22-й хромосомы, где предположительно располагаются гены, кодирующие ряд важных факторов транскрипции. Удалось идентифицировать один из этих генов – TBX1, продуктом его экспрессии является белок под названием T-box. Он относится к семейству протеинов, контролирующих процессы эмбриогенеза. Доказательством взаимосвязи синдрома Ди Джорджи и TBX1 является тот факт, что незначительный процент больных не имеет выраженных повреждений 22-й хромосомы, присутствуют только мутации в этом гене. Также высказываются предположения о роли делеций иных хромосом в развитии данного заболевания. Так, аналогичные синдрому Ди Джорджи проявления выявлялись при наличии повреждений 10-й, 17-й и 18-й хромосом.
В большинстве случаев синдрома Ди Джорджи делеция 22-й хромосомы захватывает порядка 2-3 миллионов пар оснований. Чаще всего данный генетический дефект возникает спонтанно во время формирования мужских или женских половых клеток – то есть, носит герминативный характер. Лишь десятая часть всех случаев заболевания представляет собой семейную форму с аутосомно-доминантным характером наследования. Патогенез синдрома Ди Джорджи сводится к нарушению формирования особых эмбриональных образований – фарингеальных мешков (главным образом, 3-го и 4-го), которые являются предшественниками ряда тканей и органов. Главным образом, они отвечают за формирование неба, паращитовидных желез, тимуса, сосудов средостения и сердца, поэтому при синдроме Ди Джорджи возникают пороки развития именно этих органов.
Симптомы синдрома Ди Джорджи
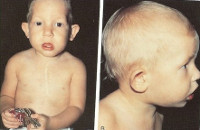
Многие проявления синдрома Ди Джорджи определяются сразу после рождения ребенка, отдельные пороки развития (например, сердца) можно выявить еще раньше – на профилактических ультразвуковых исследованиях. Чаще всего первыми обнаруживаются аномалии развития лица – расщепление неба, иногда в сочетании с «заячьей губой», прогнатия нижней челюсти. Зачастую младенцы с синдромом Ди Джорджи имеют небольшой рот, маленький нос с расширенной переносицей, деформированные или недоразвитые хрящи ушных раковин. При относительно легком течении заболевания все вышеперечисленные симптомы могут быть выражены довольно слабо, даже расщепление твердого неба может возникать только в задней его части и выявляться лишь при тщательном осмотре у отоларинголога.
В первые месяцы жизни больного синдромом Ди Джорджи на первый план выступают проявления врожденных пороков сердца – это может быть как тетрада Фалло, так и отдельные нарушения: дефект межжелудочковой перегородки, незаращение артериального протока и ряд других. Они сопровождаются цианозом, сердечно-сосудистой недостаточностью и при отсутствии квалифицированной медицинской помощи (в том числе и хирургической) могут приводить к ранней смерти больных. Другим распространенным нарушением у детей с синдромом Ди Джорджи считаются судороги и тетания, обусловленная гипоплазией паращитовидных желез и последующей гипокальциемией.
Следующим важнейшим проявлением синдрома Ди Джорджи, отличающим его от других разновидностей велокардиофациального синдрома, является выраженный первичный иммунодефицит. Он развивается по причине аплазии или недоразвития тимуса и поэтому в большей степени затрагивает клеточный иммунитет. Однако из-за тесных взаимосвязей между гуморальным и клеточным отделами иммунной системы это приводит к общему ослаблению защитных сил организма. Больные с синдромом Ди Джорджи крайне чувствительны к вирусным, грибковым и бактериальным инфекциям, которые нередко принимают затяжное и тяжелое течение. Некоторые исследователи отмечают наличие умственной отсталости различной степени, иногда могут наблюдаться судороги неврологического происхождения.
Диагностика синдрома Ди Джорджи
Для определения синдрома Ди Джорджи применяют метод физикального общего осмотра, кардиологические исследования (ЭхоКГ, электрокардиограмма), УЗИ щитовидной железы и тимуса, иммунологические пробы. Вспомогательную роль играет проведение общего и биохимического анализов крови, изучение анамнеза больного, генетические исследования. При осмотре больных синдромом Ди Джорджи могут определяться характерные для заболевания нарушения – расщепление твердого неба, аномалии строения лица, патологии ЛОР-органов. В анамнезе, как правило, выявляются частые эпизоды вирусных и грибковых инфекций, принимающих тяжелое течение, судороги, обусловленные гипокальциемией, нередко обнаруживается обширное кариозное поражение зубов.
На ультразвуковых исследованиях вилочковой железы отмечается значительное уменьшение массы или даже полное отсутствие органа (агенезия). ЭхоКГ и другие кардиологические методы диагностики выявляют многочисленные пороки сердца (например, дефект межжелудочковой перегородки) и сосудов средостения. Иммунологические исследования подтверждают значительное падение уровня Т-лимфоцитов. Это же явление наблюдается в периферической крови и нередко сочетается с уменьшением концентрации белков-иммуноглобулинов. Биохимическое изучение крови свидетельствует о снижении уровня кальция и гормонов паращитовидной железы. Врач-генетик может выполнить поиск делеций в 22-й хромосоме посредством флуоресцентной гибридизации ДНК или мультиплексной полимеразной цепной реакции.
Лечение синдрома Ди Джорджи
Специфического лечения синдрома Ди Джорджи на сегодняшний момент не существует, используют только паллиативные и симптоматические методики. Очень важно как можно раньше выявить врожденные пороки сердца и при необходимости произвести их хирургическую коррекцию, поскольку именно сердечно-сосудистые нарушения являются наиболее частой причиной неонатальной смерти при этом заболевании. Значительную опасность представляют собой судорожные приступы, обусловленные гипокальциемией, что требует своевременной коррекции электролитного баланса плазмы крови. Помощь хирургов при синдроме Ди Джорджи также может потребоваться для устранения пороков развития лица и неба.
Из-за выраженного иммунодефицита любые признаки бактериальной, вирусной или грибковой инфекции являются поводом для срочного применения соответствующих препаратов (антибиотиков, противовирусных и фунгицидных средств). Для улучшения иммунного статуса больного синдромом Ди Джорджи может производиться заместительное вливание иммуноглобулинов, полученных из донорской плазмы. В отдельных случаях осуществлялась пересадка вилочковой железы, которая стимулировала образование собственных Т-лимфоцитов – это способствовало улучшению качества жизни больных.
Прогноз и профилактика синдрома Ди Джорджи
Прогноз синдрома Ди Джорджи большинством исследователей оценивается как неопределенный, так как данное заболевание характеризуется значительной вариабельностью симптомов. В тяжелых случаях имеется высокий риск ранней неонатальной смерти из-за сочетания сердечно-сосудистых и иммунологических нарушений. Более доброкачественные формы синдрома Ди Джорджи требуют достаточно интенсивной паллиативной терапии, особенно важно уделять внимание лечению и профилактике вирусных и грибковых инфекций. Интеллектуальное развитие больных несколько замедлено, однако при правильной педагогической и психологической коррекции проявления задержки развития можно нивелировать. Из-за частого спонтанного характера мутаций профилактика синдрома Ди Джорджи не разработана.
Источник
