Атипичный гемолитико уремический синдром википедия
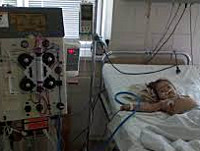
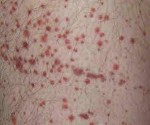
Гемолитико-уремический синдром – острое патологическое состояние, характеризующееся одновременным развитием микроангиопатической гемолитической анемии, тромбоцитопении и азотемии. Гемолитико-уремический синдром может проявляться кровавой диареей, абдоминальными болями, бледностью и иктеричностью кожи и склер, пастозностью лица, петехиями на коже, анурией, поражением ЦНС, печени, поджелудочной железы и сердца. Диагноз гемолитико-уремического синдрома основан на характерных клинических признаках, результатах общего и биохимического анализа крови и мочи, коагулограммы, бакпосева кала. Лечение гемолитико-уремического синдрома включает патогенетическую, симптоматическую и заместительную терапию.
Общие сведения
Гемолитико-уремический синдром (болезнь Гассера) – тяжелое полиэтиологическое расстройство, проявляющееся сочетанием неиммунной гемолитической анемии, тромбоцитопении и острой почечной недостаточности. Гемолитико-уремический синдром наблюдается преимущественно у детей грудного и младшего возраста (с 6 мес. до 4 лет), но также встречается у детей старшего возраста и редко у взрослых. Ежегодно в расчете на 100 тыс. детского населения регистрируются 2-3 случая гемолитико-уремического синдрома у детей до 5 лет и 1 случай у детей до 18 лет. Поскольку гемолитико-уремический синдром – одна из частых причин острой почечной недостаточности у детей, то от своевременности его диагностики и лечения зависит исход заболевания.

Гемолитико-уремический синдром
Классификация гемолитико-уремического синдрома
В зависимости от этиологии и клинических особенностей разделяют гемолитико-уремический синдром диареяассоциированный – Д+ (типичный) и не ассоциированный с диареей – Д- (спорадический или атипичный). Д+ гемолитико-уремический синдром чаще встречается у детей раннего и младшего возраста, является эндемическим (распространен в Поволжье, Московском регионе); недиарейный – более свойственен детям старшего возраста и взрослым.
По тяжести течения выделяют легкую и тяжелую формы гемолитико-уремического синдрома. Легкая форма гемолитико-уремического синдрома подразделяется на тип А (анемия, тромбоцитопения и азотемия) и тип Б (триада симптомов в сочетании с судорожным синдромом или артериальной гипертензией); тяжелая – на тип А (триада симптомов в сочетании с анурией длительностью более суток) и тип Б (триада симптомов в сочетании с анурией, артериальной гипертензией и судорожным синдромом).
Причины гемолитико-уремического синдрома
У детей частыми причинами гемолитико-уремического синдрома являются острая кишечная инфекция (90%) и инфекции верхних дыхательных путей (10 %).
Основное значение в развитии Д+ гемолитико-уремического синдрома имеет энтерогеморрагическая Е. coli, продуцирующая специфический шига-подобный веротоксин, способный избирательно повреждать эндотелиальные клетки сосудов почек и головного мозга. Наибольшее сродство веротоксина с эндотелием капилляров почек наблюдается у детей первых 3 лет жизни. Веротоксин вызывает эндотелиальный апоптоз и лейкоцитозависимое воспаление, а также запускает цепь патологических реакций, приводящих к гемолизу эритроцитов, агрегации и деструкции тромбоцитов, локальной активации процесса коагуляции и внутрисосудистого отложения фибрина, развитию ДВС-синдрома. Такими же свойствами обладает шигатоксин S. dysenteriae I типа. Развивающиеся микроциркуляторные нарушения (микроангиопатическая гемолитическая анемия, тромбоцитопения и микротромбозы) приводят к ишемическим изменениям в органах мишенях. При гемолитико-уремическом синдроме на фоне ОКИ наиболее часто поражаются капилляры клубочков почек, что может приводить к снижению скорости гломерулярной фильтрации, ишемии или некрозу клубочков, вторичной дисфункции или некрозу почечных канальцев, при массивном поражении – к ОПН.
Заражение энтерогеморрагической Е. coli может произойти при контакте с животными (кошками, крупным рогатым скотом) или инфицированным человеком; употреблении недостаточно термически обработанных мясных изделий, непастеризованных молочных продуктов, фруктовых соков, загрязненной воды. Для гемолитико-уремического синдрома характерна сезонность: на фоне ОКИ – преимущественно теплое время года (июнь-сентябрь), на фоне вирусных инфекций – зимне-весенний период.
Д- гемолитико-уремический синдром может быть постинфекционным, лекарственным, поствакцинальным, наследственным, связанным с системными заболеваниями соединительной ткани, идиопатическим. В 40% случаев развитие Д- гемолитико-уремического синдрома обусловлено респираторной инфекцией, возбудителем которой является S. pneumoniae, разрушающий мембраны эритроцитов, тромбоцитов и эндотелиоцитов с помощью фермента нейраминидазы. Вирусы ветряной оспы, ВИЧ, гриппа, Эпштейна-Барра, Коксаки также могут быть причиной гемолитико-уремического синдрома.
Установлена связь между развитием гемолитико-уремического синдрома у взрослых и употреблением некоторых медикаментов (циклоспорина А, митомицина С, эстроген – содержащих контрацептивов, противоопухолевых препаратов), трансплантацией костного мозга, злокачественными новообразованиями, системной красной волчанкой и антифосфолипидным синдромом, беременностью. Выявлены семейные случаи гемолитико-уремического синдрома с аутосомным типом наследования обусловленные дефектом системы комплемента, нарушением обмена простациклина, недостаточностью антитромботических факторов и др.
В основе гемолитико-уремического синдрома может лежать активация тромбоцитов иммунными комплексами (например, комплексом антиген – антитело после прививок живыми вакцинами против полиомиелита, против ветряной оспы, против кори, АКДС).
Симптомы гемолитико-уремического синдрома
В клинической картине гемолитико-уремического синдрома различают продромальный период, разгар заболевания и восстановительный период. Продолжительность продромального периода составляет от 2 до 7 суток. Для него характерно появление признаков поражения ЖКТ или дыхательных путей.
Гемолитико-уремический синдром на фоне ОКИ, вызванной энтеропатогенной Е. coli, имеет ярко выраженную симптоматику. Развиваются симптомы гастроэнтерита или колита (часто кровавая диарея), тошнота, рвота, абдоминальные боли, лихорадка. Постепенно общее состояния ребенка ухудшается, повышенная возбудимость сменяется вялостью.
В период разгара гемолитико-уремического синдрома превалируют проявления гемолитической анемии, тромбоцитопении и ОПН: бледность и иктеричность кожного покрова, склер и слизистых оболочек; пастозность век, голеней; кожный геморрагический синдром в виде петехий или экхимозов, иногда – носовые кровотечения, в тяжелых случаях – снижение диуреза (олигурия или анурия). Тяжесть и продолжительность дизурии зависит от степени и глубины повреждения почек.
Гемолитико-уремический синдром может проявляться полиорганной патологией: поражением ЦНС, печени, поджелудочной железы, сердца, артериальной гипертензией. В 50% случаев гемолитико-уремического синдрома наблюдаются неврологические нарушения: подергивания мышц, гиперрефлексия, децеребрационная ригидность, гемипарезы, судороги, ступор, кома (особенно выраженные у детей первых лет жизни). Выявляются гепатоспленомегалия, кардиомиопатия, тахикардия, аритмия.
В самых тяжелых случаях возможно легочное кровотечение, развитие отека легких, синдрома «ригидного легкого», сердечно-легочной недостаточности, отека головного мозга. Поражение ЖКТ может проявляться эзофагитом, энтероколитом, гепатитом, панкреатитом, а также некрозом, перфорацией, инвагинацией кишечника.
Продолжительность гемолитико-уремического синдрома обычно составляет 1-2 недели, затем наступает стабилизация и в 70% случаев – постепенное восстановление нарушенных функций: улучшение выделения мочи, повышение уровня тромбоцитов, нормализация уровня гемоглобина. При тяжелом течении наступает либо летальный исход вследствие экстраренальных поражений, либо формирование ХПН.
Диагностика
Диагноз гемолитико-уремического синдрома основан на выявлении характерных клинических признаков, осложняющих течение ОКИ или ОРВИ: гемолитической анемии, тромбоцитопении, ДВС-синдрома, азотемии.
При гемолитико-уремическом синдроме в крови обнаруживаются анемия, анизоцитоз и полихроматофилия эритроцитов (наличие фрагментированных форм), присутствие свободного гемоглобина, снижение количества тромбоцитов, лейкоцитоз, умеренная непрямая гипербилирубинемия, возрастание уровня мочевины и креатинина, гипонатриемия, гиперкалиемия, ацидоз (в олигоанурической стадии ОПН), гипоальбуминемия.
Моча приобретает коричневато-ржавый цвет, в ней могут появиться фибриновые комки, отмечается гематурия, протеинурия, гемоглобинурия. У детей с ОКИ выполняют бактериологическое исследование кала на выявление штаммов энтеропатогенной Е. coli. При тяжелых неврологических нарушениях возможно проведение КТ головного мозга и люмбальной пункции для исключения кровотечения и менингита.
Дифференциальная диагностика гемолитико-уремического синдрома проводится с неотложными хирургическими состояниями (аппендицитом, кишечной непроходимостью, окклюзией мезентериальных сосудов, перфорацией кишечника, дивертикулом подвздошной кишки), ишемическим колитом, септицемией с ДВС-синдромом, вирусным или бактериальным гастроэнтеритом, тяжелой степенью дегидратации при кишечных токсикозах, тромботической тромбоцитопенией.
Лечение гемолитико-уремического синдрома
Лечение гемолитико-уремического синдрома определяется периодом развития заболевания и тяжестью поражения почечной ткани. Чем раньше ребенок с гемолитико-уремическим синдромом поступает в стационар, тем выше вероятность его успешного и полного излечения. Патогенетическая терапия включает нормализацию агрегатного состояния крови с использованием антиагрегантов, гепаринотерапии; улучшение микроциркуляции (трентал, эуфиллин); коррекцию антиоксидантного статуса (витамины А и Е).
При бактериальной этиологии гемолитико-уремического синдрома назначаются антибиотики широкого спектра действия; при инфекции, вызванной энтеропатогенной Е. coli, прием антибиотиков и препаратов, замедляющих моторику кишечника, не рекомендуется. При олигоанурии показана коррекция водно-электролитных расстройств, подавление реакций метаболического распада и инфекционного процесса. Для коррекции тяжелой анемии используется инфузия эритроцитарной массы.
В половине случаев типичного гемолитико-уремического синдрома необходимо раннее проведение заместительной терапии: обменного плазмафереза, перитонеального диализа или гемодиализа. Гемодиализ проводится ежедневно в течение всего олигоуремического периода. В случае развития терминальной стадии ХПН показана трансплантация почки.
Прогноз гемолитико-уремического синдрома
Гемолитико-уремический синдром имеет серьезный прогноз, летальность у маленьких детей во время острой фазы заболевания составляет 3-5%, у 12% развивается терминальная ХПН, у 25% происходит снижение клубочковой фильтрации. Плохой прогноз имеют атипичные наследственные, аутоиммунные и связанные с беременностью формы гемолитико-уремического синдрома.
Классическая форма гемолитико-уремического синдрома у детей раннего возраста с преимущественным поражением почечных клубочков протекает более благоприятно. В случае Д+ гемолитико-уремического синдрома наблюдается лучший исход по сравнению с недиарейным синдромом, сопровождающимся частыми рецидивами и высокой летальностью.
Источник
Атипичный гемолитико-уремический синдром (аГУС) – это редкое, системное, угрожающее жизни заболевание с неблагоприятным прогнозом.[1][2][3][4] Основу аГУС, который поражает как детей, так и взрослых, составляет тромботическая микроангиопатия (TMA).[4][5] При ТМА происходит образование тромбов в мелких кровеносных сосудах (сосуды микроциркуляторного русла) различных органов, что приводит к поражению последних , в результате внезапного или постепенного прогрессирования которого развивается полиорганная недостаточность.[1][3][4] Причиной аГУС в большинстве случаев является хроническая (постоянная) неконтролируемая активация системы комплемента, части иммунной системы организма, действие которой в норме направлено на уничтожение возбудителей инфекций и удаление иммунных комплексов и отмерших клеток.[4][5][6][7][8] Разрушительное действие системы комплемента на собственные ткани организма предотвращают особые белки, в норме регулирующие процессы активации комплемента. Однако при аГУС эта регуляция нарушается – главным образом вследствие мутаций в генах белков-регуляторов комплемента, что обусловливает нарушения их функций.[6][8] Сбои в действии контролирующих механизмов приводят к чрезмерной активации системы комплемента, которая начинает атаковать собственные ткани организма.[7][8] Быстрая диагностика и раннее начало адекватной терапии улучшают прогноз заболевания и снижают риск развития жизнеугрожающих осложнений ТМА, в том числе терминальной почечной недостаточности, инсульта или острого инфаркта миокарда.[4][9][10][11]
Классификация
аГУС – это одна из форм ГУС (гемолитико-уремического синдрома). В структуре ГУС у детей на долю аГУС приходится 5-10% случаев, в то время как у взрослых большинство случаев ГУС представляют собой аГУС[12].В большинстве случаев ГУС у детей вызван инфицированием бактериями Escherichia coli, продуцирующими шига-токсин. Индуцированная инфекцией форма болезни в современной классификации называется STEC-ГУС.[12] Ранее она носила название Д+ ГУС, т.е. ГУС, связанный с диареей, в противоположность (Д-ГУС), т.е. не ассоциированому с диареей или атипичному (аГУС). Сегодня эту терминологию следует считать устаревшей,[13], поскольку у 30% пациентов с аГУС заболевание начинается с диареи .[12]
Эпидемиология
аГУС классифицируют на спорадический или семейный,[2][14] его распространенность не зависит от расы, пола и географического положения.[12] Как и у всех редких заболеваний, данные по заболеваемости аГУС ограничены. Европейский реестр, в котором зарегистрированы 167 пациентов детского возраста, приводит данные о 3,3 случаях на миллион детей и более низкой распространенности у взрослых.[15][16] Недавно проведенное исследование 214 пациентов с аГУС выявило сходные данные по заболеваемости у детей (41,6%) и взрослых (58,4%).[17] По данным сайта Orphanet (портал, посвященный редким заболеваниям и орфанным препаратам), распространенность аГУС составляет от 1 до 9 на миллион человек.[18]
Патогенез
Основным механизмом развития аГУС является хроническая неконтролируемая активация системы комплемента, приводящая к повреждению эндотелия сосудов, и, вследствие этого, повреждению органов.[5][6] В норме система комплемента атакует и разрушает патогены, например бактерии, вирусы и измененные клетки организма, и удаляет клеточные обломки.[7][8][19] Существует 3 различных пути активации комплемента: классического, лектинового и альтернативного.[8] В первых 2 путях активация комплемента происходит только в результате связывания с иммунными комплексами или особыми микроорганизмами, соответственно, а альтернативный путь активен постоянно, что приводит к непрерывному образованию мембраноатакующего комплекса (МАК), вызывающего лизис клеток.[19] Чтобы избежать комплемент-опосредованного повреждения здоровых тканей и органов, организму важно жестко регулировать систему комплемента, что осуществляется с помощью белков регуляции комплемента[14]. Генетические изменения белков регуляции комплемента (таких, как CFH, CFB, CFI, MCP и тромбомодулин) вследствие мутаций в генах, кодирующих синтез этих белков, нарушают хрупкое равновесие альтернативного пути активации комплемента при аГУС.[6][20][21][22] Возникающая в результате постоянная неконтролируемая активация комплемента приводит к непрерывному повреждению клеток эндотелия (клетки, выстилающие внутреннюю поверхность кровеносных сосудов),[4][9][20][21] что сопровождется постоянной активацией тромбоцитов и белых кровяных телец, индуцируя процессы микротромбообразования и воспаления в сосудистом русле жизненно важных органов и, следовательно, их ишемию, приводящую к необратимому поражению, полиорганной недостаточности и даже смерти.[23][24]
Клиническая картина
аГУС часто начинается с неспецифических симптомов: недомогания и утомляемости.[12] У подавляющего большинства пациентов наблюдается поражение почек, включая терминальную почечную недостаточность (ТПН).[6] При этом, наряду с повышением креатинина крови,[25][26][27] снижением расчетной скорости клубочковой фильтрации (рСКФ),[4][26] могут отмечаться и другие симптомы: снижение диуреза, отеки,[5] тяжелая или злокачественная артериальная гипертензия,[5]протеинурия.[25]
Кроме почек, также могут страдать другие системы организма:
• У трети пациентов развивается внепочечный тромбоз.[28]
• Неврологические нарушения: около половины пациентов имеют признаки поражения головного мозга:[29]спутанность сознания[30], инсульта,[29][30]судороги,[29][30]кому[29][31] и энцефалопатию[5]
• Поражение сердечно-сосудистой системы: у 43% пациентов с аГУС отмечаются признаки поражения сердца и сосудов, включая кардиомиопатию с развитием сердечной недостаточности;[25][32] инфаркт миокарда,[11][32] высокое артериальное давление (артериальная гипертензия [1][25][32] и диффузную васкулопатию.[6]
• Поражение желудочно-кишечного тракта: у 37% пациентов имеются симптомы со стороны ЖКТ:[3] боль в животе,[10] рвота [33] или диарея.[13] В наиболее тяжелых случаях отмечаются признаки панкреатита,[33]гастроэнтерита,[5]Колит,[10]некроза печени [5]
• Осложнения со стороны зрения: поражение сосудов глаза.[34]
• Поражения кожи :[35] изъязвления, петехиальная сыпь.[36]
• Легочные осложнения[11]
Триггерами аГУС могут быть различные состояния, которые сопровождаются дополнительной активацией системы комплемента и, следовательно, высоким риском развитияТМА.[5][16][36][37]
• Диарея / гастроэнтерит
• Инфекции верхних дыхательных путей
• Беременность и роды
• Злокачественная артериальная гипертензия
• Трансплантация почки и костного мозга
• Гломерулопатия
• Системные заболевания, например, системная красная волчанка (СКВ) и склеродермия
• Злокачественные новообразования
Прогноз
В отдаленной перспективе прогноз при аГУС неблагоприятный.[20] До 79% пациентов с аГУС умирают или получают необратимое повреждение почек (развитие терминальной почечной недостаточности) в течение 3 лет от начала заболевания при применении только поддерживающей терапии.[5]Трансплантация почки при ТПН пациентам с аГУС ранее проводилась редко из-за высокой частоты отторжения трансплантата, достигающей 90% при некоторых видах мутаций. Возможно также развитие аГУС в трансплантате de novo.[14] В связи с этим большинство пациентов с аГУС, достигших ТПН, получают лечение диализом, что сопряжено с ухудшением прогноза.[38][39] Предпринимаются попытки комбинированной трансплантации печени и почки при аГУС, хотя эта сложная процедура сопровождается высоким уровнем смертности (1 из 2 случаев).[40]
Диагностика
аГУС манифестирует клиническими признаками ТМА (тромбоцитопения, микроангиопатический гемолиз и симптомы нарушения функции органов, в первую очередь, острое почечное повреждение).[4] Поскольку аГУС – не единственное заболевание, вызывающее системную ТМА, исключительно важно провести дифференциальную диагностику. К другим основным причинам ТМА относятся тромботическая тромбоцитопеническая пурпура (ТТП) и гемолитико-уремический синдром, вызванный Escherichia coli, продуцирующей шига-токсин (STEC-ГУС).[4][41][42]
После подтверждения TMA с помощью с помощью диагностических тестов, выявляющих тромбоцитопению, микроангиопатический гемолиз и показатели нарушения функции органов, чрезвычайно важно провести дифференциальную диагностику с целью выявления основного заболевания. Анализ на активность ADAMTS-13 может разграничить ТТП и аГУС, а анализ на шига-токсин может выявить STEC-ГУС:[4]
• Активность ADAMTS-13, равная 5% или менее, подтверждает диагноз ТТП.
• Положительный анализ на шига-токсин в крови или кале подтверждает диагноз STEC-ГУС.
• Активность ADAMTS-13 более 5% и отсутствие шига-токсина в анализе кала повышает вероятность подтверждения диагноза аГУС.
При отсутствии результатов анализа на ADAMTS-13 уровень креатинина сыворотки (SCr) и количество тромбоцитов у пациентов с TMA могут служить предиктором активности ADAMTS-13.[43] Уровень креатинина сыворотки выше 150-200 мкмоль/л (более 1,7-2,3 мг/дл) или количество тромбоцитов выше 30 000/мм3 практически исключает диагноз тяжелой недостаточности ADAMTS-13 и, следовательно, ТТП.[43]
Хотя аГУС – это генетическое заболевание, у 30-50% пациентов генетическую мутацию выявить не удается.[1][4][5][44] Поэтому генетический анализ представляется ненадежным методом диагностики заболевания.[1][4] Не каждая известная генетическая мутация имеет прогностическое значение.[4] Последнее соображение, в сочетании с ограниченной доступностью генетического анализа из-за его высокой стоимости и длительного ожидания результатов, позволяет заключить, что для первоначальной диагностики и выбора тактики лечения аГУС генетический анализ не является необходимым.[4][45]
Лечение
Плазмообмен / инфузии плазмы (ПО/ИП)
Хотя ПО/ИП широко применяется, не существует статистически достоверных контролируемых исследований безопасности и эффективности этого метода при аГУС.[46] У некоторых пациентов отмечалось улучшение гематологических показателей,[4] у других нарушения регуляции комплемента и ТМА сохранялись, несмотря на плазмозамещающую терапию.[45][47] Это может объясняться тем, что ПО/ИП недостаточно для удаления мутантных факторов комплемента или восполнения недостающих факторов,[9][38] что приводит к неполному клиническому ответу.[4][48]
Американское общество афереза присвоило рекомендации по применению плазмозамещающей терапии при лечении аГУС категорию доказательности 2C/слабая в связи с «низким» и «очень низким» качеством доказательств в пользу её применения.[49]
Постоянный диализ
Пациентам с аГУС при развитии ТПН, как правило, начинается диализная терапия, при которой 5-летняя выживаемость составляет 50%.[50] Поскольку у пациентов с аГУС на диализе сохраняется системная и неконтролируемая активация комплемента,[34] активность комплемента у них выше, чем у диализных пациентов, получающих этот вид лечения в связи с другими заболеваниями.[51] В связи с этим у пациентов с аГУС, находящихся на диализе, сохраняется риск внепочечной ТМА.[34][51][52][53][54][55][56]
Трансплантация
Хотя больным аГУС выполняется трансплантация почки, она не влияет на неконтролируемую активацию комплемента, которая приводит к прогрессирующей системной ТМА.[45] В зависимости от генетической мутации до 90% пациентов с аГУС переносят рецидив заболевания после трансплантации почки.[13][45] Продолжающаяся после пересадки почки неконтролируемая активация комплемента приводит к отторжению трансплантата, которое у большинства пациентов не удается предотвратить с помощью плазмозамещающей терапии.[6][57] Комбинированная трансплантация печени и почки возможна только у очень малого числа пациентов из-за ограниченного количества донорских органов. Кроме того, воспаление и ТМА развиваются в других органах, обусловливая высокий риск неблагоприятного исхода, который многим врачам и пациентам представляется чрезмерным.[5][6]
Экулизумаб
Экулизумаб – это гуманизированное моноклональное антитело, которое связывает C5 компонент комплемента, отвечающий за активацию мембраноатакующего комплекса (МАК),[9][58] и таким образом подавляет неконтролируемую активность терминального комплекса комплемента.[58] В России, как и в Европе, на сегодняшний день Экулизумаб является единственным ингибитором активности комплемента, одобренным для лечения аГУС у детей и взрослых.
Литература
[1][2][3][4][5][6][7][8][9][10][11][12][13][14][15][16][17][18][19][20][21][22][23][24][25][26][27][28][29][30][31][32][33][34][35][37][36][38][39][40][41][42][59][43][44][45][46][60][47][48][49][50][51][52][53][54][55][56][57][58]
Примечания
- ↑ 1 2 3 4 5 6 Kavanagh, D., et al. (2006) Atypical haemolytic uraemic syndrome. From Br Med Bull 77-78, 5-22.>
- ↑ 1 2 3 Caprioli, J., et al. (2006) Genetics of HUS: the impact of MCP, CFH, and IF mutations on clinical presentation, response to treatment, and outcome. From Blood 108(4), 1267-1279.>
- ↑ 1 2 3 4 Langman, C. (2012) Systemic Multi-Organ Complications In Atypical Hemolyticuremic Syndrome (aHUS): Retrospective Study In A Medical Practice Setting. From Haematologica 97(s1), 195-196: Abstract 0490.>
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Laurence, J. (2012) Atypical hemolytic uremic syndrome (aHUS): making the diagnosis. From Clin Adv Hematol Oncol 10(10 Suppl 17), 1-12.>
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 Noris, M., et al. (2010) Relative role of genetic complement abnormalities in sporadic and familial aHUS and their impact on clinical phenotype. From Clin J Am Soc Nephrol 5(10), 1844-1859.>
- ↑ 1 2 3 4 5 6 7 8 9 Loirat, C., et al. (2008) Complement and the atypical hemolytic uremic syndrome in children. From Pediatr Nephrol 23(11), 1957-1972.>
- ↑ 1 2 3 4 Meri, S. (2007) Loss of self-control in the complement system and innate autoreactivity. From Ann N Y Acad Sci 1109, 93-105.>
- ↑ 1 2 3 4 5 6 Walport, M. J. (2001) Complement. First of two parts. From N Engl J Med 344(14), 1058-1066.>
- ↑ 1 2 3 4 5 Legendre, C. M., et al. (2013) Terminal complement inhibitor eculizumab in atypical hemolytic-uremic syndrome. From N Engl J Med 368(23), 2169-2181.>
- ↑ 1 2 3 4 Ohanian, M., et al. (2011) Eculizumab safely reverses neurologic impairment and eliminates need for dialysis in severe atypical hemolytic uremic syndrome. From Clin Pharmacol 3, 5-12.>
- ↑ 1 2 3 4 Sallee, M., et al. (2010) Myocardial infarction is a complication of factor H-associated atypical HUS. From Nephrol Dial Transplant 25(6), 2028-2032.>
- ↑ 1 2 3 4 5 6 Loirat, C., et al. (2011) Atypical hemolytic uremic syndrome. From Orphanet J Rare Dis 6, 60.>
- ↑ 1 2 3 4 Zuber, J., et al. (2011) New insights into postrenal transplant hemolytic uremic syndrome. From Nat Rev Nephrol 7(1), 23-35.>
- ↑ 1 2 3 4 Noris, M., et al. (2009) Atypical hemolytic-uremic syndrome. From N Engl J Med 361(17), 1676-1687.>
- ↑ 1 2 Zimmerhackl, L. B., et al. (2006) Epidemiology, clinical presentation, and pathophysiology of atypical and recurrent hemolytic uremic syndrome. From Semin Thromb Hemost 32(2), 113-120.>
- ↑ 1 2 3 Campistol, J. M., et al. (2013) An update for atypical haemolytic uraemic syndrome: diagnosis and treatment. A consensus document. From Nefrologia 33(1), 27-45.>
- ↑ 1 2 Fremeaux-Bacchi, V., et al. (2013) Genetics and outcome of atypical hemolytic uremic syndrome: a nationwide French series comparing children and adults. From Clin J Am Soc Nephrol 8(4), 554-562.>
- ↑ 1 2 Orphanet from https://www.orpha.net/consor/cgi-bin/Disease_Search.php?lng=EN&data_id=779&Disease_Disease_Search_diseaseGroup=aHUS&Disease_Disease_Search_diseaseType=Pat&Disease(s)/group. accessed 2014(03 June).
- ↑ 1 2 3 Meri, S., et al. (2008) Encyclopedia of Life Sciences (ELS), John Wiley & Sons, Ltd, Chichester.
- ↑ 1 2 3 4 Hirt-Minkowski, P., et al. (2010) Atypical hemolytic uremic syndrome: update on the complement system and what is new. From Nephron Clin Pract 114(4), c219-235.>
- ↑ 1 2 3 Noris, M., et al. (2012) STEC-HUS, atypical HUS and TTP are all diseases of complement activation. From Nat Rev Nephrol 8(11), 622-633.>
- ↑ 1 2 Sellier-Leclerc, A. L., et al. (2007) Differential impact of complement mutations on clinical characteristics in atypical hemolytic uremic syndrome. From J Am Soc Nephrol 18(8), 2392-2400.>
- ↑ 1 2 Caprioli, J., et al. (2003) Complement factor H mutations and gene polymorphisms in haemolytic uraemic syndrome: the C-257T, the A2089G and the G2881T polymorphisms are strongly associated with the disease. From Human Molecular Genetics 12(24), 3385-3395.>
- ↑ 1 2 Sullivan, M., et al. (2011) Age-related penetrance of hereditary atypical hemolytic uremic syndrome. From Annals of Human Genetics 75(6), 639-647.>
- ↑ 1 2 3 4 5 Neuhaus, T. J., et al. (1997) Heterogeneity of atypical haemolytic uraemic syndromes. From Arch Dis Child 76(6), 518-521.>
- ↑ 1 2 3 Stahl, A. L., et al. (2008) Factor H dysfunction in patients with atypical hemolytic uremic syndrome contributes to complement deposition on platelets and their activation. From Blood 111(11), 5307-5315.>
- ↑ 1 2 Ariceta, G., et al. (2009) Guideline for the investigation and initial therapy of diarrhea-negative hemolytic uremic syndrome. From Pediatr Nephrol 24(4), 687-696.>
- ↑ 1 2 Muus, P., et al. (2013) from 18th European Hematology Association (EHA), Abstract B1774.
- ↑ 1 2 3 4 5 George, J. N. (2010) How I treat patients with thrombotic thrombocytopenic purpura: 2010. From Blood 116(20), 4060-4069.>
- ↑ 1 2 3 4 Vesely, S. K., et al. (2003) ADAMTS13 activity in thrombotic thrombocytopenic purpura-hemolytic uremic syndrome: relation to presenting features and clinical outcomes in a prospective cohort of 142 patients. From Blood 102(1), 60-68.>
- ↑ 1 2 Noris, M., et al. (2005) Complement factor H mutation in familial thrombotic thrombocytopenic purpura with ADAMTS13 deficiency and renal involvement. From J Am Soc Nephrol 16(5), 1177-1183.>
- ↑ 1 2 3 4 Noris, M., et al. (2014) Cardiovascular complications in atypical haemolytic uraemic syndrome. From Nat Rev Nephrol 10(3), 174-180.>
- ↑ 1 2 3 Dragon-Durey, M. A., et al. (2010) Clinical features of anti-factor H autoantibody-associated hemolytic uremic syndrome. From J Am Soc Nephrol 21(12), 2180-2187.>
- ↑ 1 2 3 4 Larakeb, A., et al. (2007) Ocular involvement in hemolytic uremic syndrome due to factor H deficiency–are there therapeutic consequences?. From Pediatr Nephrol 22(11), 1967-1970.>
- ↑ 1 2 Ardissino, G., et al. (2014) Skin involvement in atypical hemolytic uremic syndrome. From Am J Kidney Dis 63(4), 652-655.>
- ↑ 1 2 3 Fang, C. J., et al. (2008) Advances in understanding of pathogenesis of aHUS and HELLP. From British Journal of Haematology 143(3), 336-348.>
- ↑ 1 2 Liszewski, M. K., et al. (2011) Too much of a good thing at the site of tissue injury: the instructive example of the complement system predisposing to thrombotic microangiopathy. From Hematology Am Soc Hematol Educ Program 2011, 9-14.>
- ↑ 1 2 3 Heinen, S., et al. (2013) Monitoring and modeling treatment of atypical hemolytic uremic syndrome. From Mol Immunol 54(1), 84-88.>
- ↑ 1 2 Nester, C., et al. (2011) Pre-emptive eculizumab and plasmapheresis for renal transplant in atypical hemolytic uremic syndrome. From Clin J Am Soc Nephrol 6(6), 1488-1494.>
- ↑ 1 2 Bresin, E., et al. (2006) Outcome of renal transplantation in patients with non-Shiga toxin-associated hemolytic uremic syndrome: prognostic significance of genetic background. From Clin J Am Soc Nephrol 1(1), 88-99.>
- ↑ 1 2 Benz, K., et al. (2010) Thrombotic microangiopathy: new insights. From Curr Opin Nephrol Hypertens 19, 242-247.>
- ↑ 1 2 Zipfel, P. F., et al. (2010) Thrombotic microangiopathies: new insights and new challenges. From Curr Opin Nephrol Hypertens 19(4), 372-378.>
- ↑ 1 2 3 Zuber, J., et al. (2012) Use of eculizumab for atypical haemolytic uraemic syndrome and C3 glomerulopathies. From Nat Rev Nephrol 8(11), 643-657.>
- ↑ 1 2 Kavanagh, D., et al. (2011) Atypical hemolytic uremic syndrome, genetic basis, and clinical manifestations. From Hematology Am Soc Hematol Educ Program 2011, 15-20.>
- ↑ 1 2 3 4 5 Kavanagh, D., et al. (2010) Atypical hemolytic uremic syndrome. From Curr Opin Hematol 17(5), 432-438.>
- ↑ 1 2 Loirat, C., et al. (2010) Plasmatherapy in atypical hemolytic uremic syndrome. From Semin Thromb Hemost 36(6), 673-681.>
- ↑ 1 2 Reidl M, et al. (2011) Initiale Plasmatherapie bei Patienten mit atypischem HUS: kein negativer Vorhersagewert für das Outcome nach einem Jahr. From Klinische Padiatrie 223, Abstract P031.>
- ↑ 1 2 Sarode, R., et al. (2013) Thrombotic thrombocytopenic purpura: 2012 American Society for Apheresis (ASFA) consensus conference on classification, diagnosis, management, and future research. From J Clin Apher.>
- ↑ 1 2 Szczepiorkowski, Z. M., et al. (2010) Guidelines on the use of therapeutic apheresis in clinical practice–evidence-based approach from the Apheresis Applications Committee of the American Society for Apheresis. From J Clin Apher 25(3), 83-177.>
- ↑ 1 2 ERA-EDTA Registry Annual Report 2011: “European Renal Association-European Dialysis and Transplant Association Registry”, The Netherlands: Academic Medical Center, Department of Medical Informatics.
- ↑ 1 2 3 Bekassy, Z. D., et al. (2013) Eculizumab in an anephric patient with atypical haemolytic uraemic syndrome and advanced vascular lesions. From Nephrol Dial Transplant 28(11), 2899-2907.>
- ↑ 1 2 Davin, J. C., et al. (2010) Maintenance of kidney function following treatment with eculizumab and discontinuation of plasma exchange after a third kidney transplant for atypical hemolytic uremic syndrome associated with a CFH mutation. From Am J Kidney Dis 55(4), 708-711.>
- ↑ 1 2 Malina, M. , et al. (2011) Peripheral gangrenes in children with atypical hemolytic uremic syndrome. From Pediatr Nephrol 26, 1591-1731. Poster PS1592-FRI-1476.>
- ↑ 1 2 Remuzzi, G., et al. (2005) Hemolytic uremic syndrome: a fatal outcome after kidney and liver transplantation performed to correct factor h gene mutation. From Am J Transplant 5(5), 1146-1150.>
- ↑ 1 2 Vergouwen, M. D., et al. (2008) Proximal cerebral artery stenosis in a patient with hemolytic uremic syndrome. From AJNR Am J Neuroradiol 29(5), e34.>
- ↑ 1 2 Loirat, C., et al. (2010) Non-atheromatous arterial stenoses in atypical haemolytic uraemic syndrome associated with complement dysregulation. From Nephrol Dial Transplant 25(10), 3421-3425.>
- ↑ 1 2 Le Quintrec, M., et al. (2013) Complement genes strongly predict recurrence and graft outcome in adult renal transplant recipients with atypical hemolytic and uremic syndrome. From Am J Transplant 13(3), 663-675.>
- ↑ 1 2 3 Keating, G. M. (2013) Eculizumab: a review of its use in atypical haemolytic uraemic syndrome. From Drugs 73(18), 2053-2066.>
- ↑ Mody, R. K., et al. (2012) Infections in pediatric postdiarrheal hemolytic uremic syndrome: factors associated with identifying shiga toxin-producing Escherichia coli. From Archives of Pediatrics and Adolescent Medicine 166(10), 902-909.>
- ↑ Zuber, J., et al. (2013) Targeted strategies in the prevention and management of atypical HUS recurrence after kidney transplantation. From Transplant Rev (Orlando) 27(4), 117-125.>
![]()
Эта страница в последний раз была отредактирована 23 октября 2020 в 08:57.
Источник
