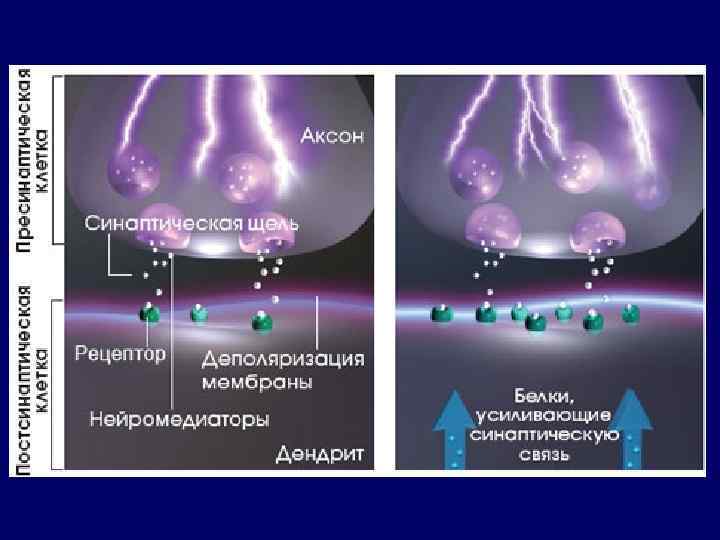
Болевые синдромы в анестезиологии и реаниматологии
Анестезиология и реаниматологияМарина Александровна Колесникова
39. Боль
Боль – это неприятное сенсорное и эмоциональное состояние, обусловленное реальным либо потенциальным патологическим влиянием на ткани.
В ЦНС боль проводится по двум основным проводящим путям.
Специфический путь – задние рога спинного мозга, специфические ядра таламуса, кора задней центральной извилины. Этот путь является малонейронным, быстрым, проводит пороговую, эмоционально неокрашенную, точно локализованную боль (эпикритическая боль).
Неспецифический путь – задние рога спинного мозга, неспецифические ядра таламуса, кора лобной и теменной долей диффузно. Проводит подпороговую, эмоционально окрашенную, плохо локализованную боль. Является медленным, многонейронным, так как образует многочисленные коллатерали к продолговатому мозгу, ретикулярной формации, лимбической системе, гиппокампу. Подпороговые болевые импульсы подвергаются суммации в таламусе. Проводимые по неспецифическому болевому пути импульсы возбуждают эмоциональные центры лимбической системы, вегетативные центры гипоталамуса, продолговатого мозга. Поэтому боли сопутствуют страх, тягостные переживания, учащение дыхания, пульса, подъем АД, расширение зрачка, диспепсические расстройства. Действию болевой ноцецептивной системы противодействует антиноцецептивная система, основные нейроны которой локализованы в околоводопроводном сером веществе (сильвиев водопровод соединяет III и IV желудочки). Их аксоны образуют нисходящие пути к продолговатому и спинному мозгу и восходящие пути к ретикулярной формации, таламусу, гипоталамусу, лимбической системе, базальным ганглиям и коре. Медиаторами этих нейронов являются пентапептиды: метэнкефалин и лейэнкефалин, имеющие в качестве концевых аминокислот соответственно метионин и лейцин. Энкефалины возбуждают опиатные рецепторы. В энкефалинергических синапсах опиатные рецепторы находятся на постсинаптической мембране, но эта же мембрана является пресинаптической для других синапсов. Опиатные рецепторы ассоциированы с аденилатциклазой и вызывают ее ингибирование, нарушая в нейронах синтез цАМФ. В итоге уменьшается вход кальция и освобождение медиаторов, включая медиаторы боли – пептиды: субстанция P, холецистокинин, соматостатин, глутаминовая кислота. Опиатные рецепторы возбуждаются не только медиаторами – энкефалинами, но и другими компонентами антиноцецептивной системы – гормонами головного мозга (эндорфинами). Пептидные агонисты опиатных рецепторов образуются при протеолизе пептидных веществ мозга: проопиокортина, проэнкефалинов А и В. Все эти пептиды образуются в гипоталамусе. Опиатные рецепторы возбуждают рецепторы во всех структурах головного мозга, участвующих в проведении и восприятии боли, формировании эмоционально окрашенных реакций на боль. При этом уменьшается выделение медиаторов боли и ослабляются все реакции, сопровождающие боль.
Следующая глава >
Похожие главы из других книг:
1.8. Боль и сон
В новом формируемом направлении «Медицина сна» важное место занимают болевые синдромы. До недавнего времени вопросы представленности, выраженности болевых синдромов в цикле сон — бодрствование и их влияния на качество жизни человека практически не
Боль древняя и современная: протопатическая и эпикритическая боль
Впервые об этих типах боли заговорил английский врач Г. Гед, посвятивший годы своей жизни изучению болевых ощущений. Причем, ряд опасных экспериментов он ставил над собой: в частности, разрезал и вновь
Боль в ухе
Боль в ухе, как правило, является признаком воспалительного процесса. Однако она может быть следствием травмы или попадания в ухо постороннего предмета, поэтому маленьким детям, неспособным объяснить характер боли, необходимо немедленно вызвать врача.
Боль
Это самый заметный симптом при остром геморрое. Боль любого заставит задуматься о том, что надо бы посетить врача. Поистине она — сторожевой пес здоровья.Чрезмерное натуживание при запоре, усердие не по силам при работах на даче, купание жарким днем в холодной реке,
Боль
Боль — это неприятное ощущение, возникающее в ответ на повреждающие раздражители. В процессе эволюции она приобрела значение могучего средства самосохранения, являясь оборонительной реакцией организма на вредные воздействия. Однако постоянная боль из защитного
Боль
Давайте еще раз вернемся к вопросу о том, что такое боль. В принципе, с ней все ясно, надо поставить последний штрих.Однажды я присутствовал на сеансе Диалога Голосов. У клиента — женщины — вышла наружу субличность, которая, когда у нее спросили имя, ответила, что ее
Боль
Она может появляться во время дефекации и после нее, а также при ходьбе и в положении сидя. Однако боль не является характерным признаком геморроя. В основном ее появление говорит о наличии сопутствующего воспаления, тромбоза и ущемления геморроидальных узлов или о
10. БОЛЬ
В этой главе мы рассматриваем боль, не связанную с травмой.Существуют общие правила помощи, действующие вне зависимости от интенсивности боли и ее локализации.Основное правило состоит в том, что у ребенка ничего не должно болеть. Это мама и папа (а в еще большей
10.2. БОЛЬ В УХЕ
Срочно нужен врач, если:? боль в ухе возникла у ребенка младше 3 месяцев;? умеренная боль длится более 3 часов;? даже слабовыраженная боль длится более суток;? боль в ухе сочетается с:• головной болью;• болью в мышцах шеи.Неотложная помощь:? в соответствии с
Боль
Боль бьет тревогу, лучше всех информируя о разрушении.Своеобразие боли характеризует злобу:
С помощью таблицы страхов Вы можете еще точнее локализовать свою боль и найти для нее правильное определение.Головная боль – злоба из-за того, что меня не любят, что мною
Боль
Боль бьет тревогу, лучше всех информируя о разрушении.Своеобразие боли характеризует злобу:
С помощью таблицы страхов Вы можете еще точнее локализовать свою боль и найти для нее правильное определение.Головная боль – злоба из-за того, что меня не любят, что мною
Боль в ухе
Что делать?1. Вставить в слуховой проход ватку, смоченную спиртом. Сверху положить спиртовой компресс.2. НПВА3. АнтибиотикиСпиртовой компресс: В марле (3-4 слоя) прорезается небольшое круглое отверстие. Марля смачивается спиртом или водкой и надевается на больное
Боль в ухе
— Боль в ухе, причиной которой стало воспаление или простудное заболевание, можно уменьшить при помощи паровой ванночки с использованием яблочного уксуса: нагрейте смесь 1 л яблочного уксуса и 2 л воды. Наклоните голову боком так, чтобы поднимающийся от сосуда
Боль
Пастернак посевной помогает снизить боль при ее травмотологическом или физиологическом происхождении.Рецепт 13 столовые ложки сухих корней пастернака обварить кипятком, завернуть в марлевую ткань. Прикладывать подушечки к больным местам. Средство успокаивает и
Источник
Лекция № 11. Боль и анальгетики
1. Боль
Боль – это неприятное сенсорное и эмоциональное состояние, обусловленное реальным либо потенциальным патологическим влиянием на ткани.
В ЦНС боль проводится по двум основным проводящим путям.
Специфический путь – задние рога спинного мозга, специфические ядра таламуса, кора задней центральной извилины. Этот путь является малонейронным, быстрым, проводит пороговую, эмоционально неокрашенную, точно локализованную боль (эпикритическая боль).
Неспецифический путь – задние рога спинного мозга, неспецифические ядра таламуса, кора лобной и теменной долей диффузно. Проводит подпороговую, эмоционально окрашенную, плохо локализованную боль. Является медленным, многонейронным, так как образует многочисленные коллатерали к продолговатому мозгу, ретикулярной формации, лимбической системе, гиппокампу. Подпороговые болевые импульсы подвергаются суммации в таламусе. Проводимые по неспецифическому болевому пути импульсы возбуждают эмоциональные центры лимбической системы, вегетативные центры гипоталамуса, продолговатого мозга. Поэтому боли сопутствуют страх, тягостные переживания, учащение дыхания, пульса, подъем АД, расширение зрачка, диспепсические расстройства. Действию болевой ноцецептивной системы противодействует антиноцецептивная система, основные нейроны которой локализованы в околоводопроводном сером веществе (сильвиев водопровод соединяет III и IV желудочки). Их аксоны образуют нисходящие пути к продолговатому и спинному мозгу и восходящие пути к ретикулярной формации, таламусу, гипоталамусу, лимбической системе, базальным ганглиям и коре. Медиаторами этих нейронов являются пентапептиды: метэнкефалин и лейэнкефалин, имеющие в качестве концевых аминокислот соответственно метионин и лейцин. Энкефалины возбуждают опиатные рецепторы. В энкефалинергических синапсах опиатные рецепторы находятся на постсинаптической мембране, но эта же мембрана является пресинаптической для других синапсов. Опиатные рецепторы ассоциированы с аденилатциклазой и вызывают ее ингибирование, нарушая в нейронах синтез цАМФ. В итоге уменьшается вход кальция и освобождение медиаторов, включая медиаторы боли – пептиды: субстанция P, холецистокинин, соматостатин, глутаминовая кислота. Опиатные рецепторы возбуждаются не только медиаторами – энкефалинами, но и другими компонентами антиноцецептивной системы – гормонами головного мозга (эндорфинами). Пептидные агонисты опиатных рецепторов образуются при протеолизе пептидных веществ мозга: проопиокортина, проэнкефалинов А и В. Все эти пептиды образуются в гипоталамусе. Опиатные рецепторы возбуждают рецепторы во всех структурах головного мозга, участвующих в проведении и восприятии боли, формировании эмоционально окрашенных реакций на боль. При этом уменьшается выделение медиаторов боли и ослабляются все реакции, сопровождающие боль.
2. Анальгезирующие лекарственные средства
Анальгетик (ацетилсалициловая кислота, парацетамол, морфин) – это лекарственное средство, уменьшающее боль разного генеза. Лекарственные средства, уменьшающие боль, спровоцированную лишь определенным причинным фактором, или устраняющие специфический болевой синдром, например антацидные средства, эрготамин (мигрень), карбамазепин (невралгия), нитроглицерин (стенокардия), не относятся к классическим анальгетикам. Кортикостероиды подавляют воспалительную реакцию и обусловленную ею боль, но, несмотря на широкое их использование с этими целями, они также не представляют собой классические анальгетики.
Анальгетики классифицируются на наркотические, действующие на структуры ЦНС и вызывающие сонливость, например опиоиды, и ненаркотические, действующие главным образом на периферические структуры, например, парацетамол, ацетилсалициловая кислота.
Дополнительные средства, усиливающие действие анальгетиков
Препараты этой группы сами по себе не являются анальгетиками, но при боли используются в сочетании с анальгезирующими средствами, так как могут изменять отношение к боли, ее восприятие и нивелировать беспокойство, страх, депрессию (трициклические антидепрессанты могут даже вызывать уменьшение потребности в морфине у больного в терминальном состоянии). Такими средствами могут быть психотропные препараты, а также воздействующие на механизмы болевых ощущений, например устраняющие спазм гладкой и поперечнополосатой мускулатуры.
Наркотические анальгетики – растительные и синтетические средства, избирательно уменьшающие восприятие боли, повышающие переносимость боли в результате уменьшения эмоциональной окраски боли и ее вегетативного сопровождения, вызывают эйфорию и лекарственную зависимость. Наркотические анальгетики снижают проведение и восприятие боли лишь в границах ЦНС, подавляют в основном неспецифический путь. Средства данной группы возбуждают опиатные рецепторы, создают действие, аналогичное эффектам пептидов антинорецецептивной системы. Поэтому главными механизмами обезболивания становятся следующие: расстройство проведения болевого импульса с аксона I нейрона, тело которого располагается в спинальном ганглии, на II нейрон, находящийся в желатинозной субстанции задних рогов спинного мозга. Подавление суммации подпороговых импульсов в таламусе. Снижение участия в болевой реакции продолговатого мозга, гипоталамуса, лимбической системы (неакцентированное отношение к боли).
Классификация наркотических анальгетиков и их антагонистов
Классификация следующая.
1. Производные пипередин-фенантрена:
1) морфин;
2) кодеин (метилморфин, в 5–7 раз слабее морфина как анальгетик);
3) этилморфин (дионин, равен по силе морфину).
2. Производные фенилпипередина:
1) промедол (в 3–4 раза слабее морфина);
2) фентанил (в 100–400 раз сильнее морфина).
3. Производные дифенилметана:
1) пиритрамид (дипидолор) – равен морфину;
2) трамадол (трамал) – несколько уступает морфину.
4. Агонисты-антагонисты:
1) агонисты опиатных рецепторов и антагонисты опиатных рецепторов – бупренорфин (норфин) (в 25–30 раз сильнее морфина);
2) агонисты опиатных рецепторов и антагонисты опиатных рецепторов – пентазоцин (лексир) (в 2–3 раза слабее морфина) и буторфанол (морадол) (равен морфину).
Агонисты-антагонисты намного реже и слабее полных агонистов вызывают эйфорию и лекарственную зависимость.
Налорфин – самостоятельно (например, при отравлении барбитуратами) и при легком отравлении морфином оказывает обезболивающее действие, вызывает миоз, брадикардию, усугубляет угнетение дыхательного центра. При тяжелом отравлении морфином и другими агонистами вытесняет их из опиатных рецепторов дыхательного центра и восстанавливает дыхание. Вызывает дисфорию, раздражительность, депрессию, нарушение фокусировки взора.
Полные антагонисты опиатных рецепторов
Налоксон – самостоятельного действия не имеет, эффективен как антидот при отравлениях наркотическими анальгетиками.
Применять наркотические анальгетики следует только при острой боли кратковременно.
Наиболее часто используют при травмах, ожогах, инфаркте миокарда, перитоните (после уточнения диагноза и решения вопроса об операции). Наркотические анальгетики входят в состав литических смесей для потенцирования наркоза. Препараты этой группы применяют при послеоперационной боли в комбинации с М-холиноблокаторами и миотропными спазмолитиками. Их назначают для прекращения печеночной (пентазоцин) и почечной (промедол) колик. Хроническая боль является противопоказанием для назначения наркотиков, исключение – запущенные формы злокачественной опухоли (дипидолор, трамадол, агонисты-антагонисты).
Наркотические анальгетики комбинируют с психотропными средствами для проведения специальных видов обезболивания.
Нейролептаналгезия – это обезболивание комбинацией фентанила (сильный, действует 30–40 мин) и дроперидола (мягкий нейролептик). Дроперидол оказывает мягкое седативное действие, купирует эмоциональные реакции и уменьшает тонус скелетной мускулатуры. Также важными эффектами дроперидола являются противорвотный и противошоковый. Дозы дроперидола – 1: 50. Комбинированный препарат – таламонал. Нейролептаналгезию применяют при малотравматических операциях, в области нейрохирургии и в кардиологии при инфаркте миокарда и др. Атальгезия или транквилоанальгезия – фентанил в сочетании с сильным транквилизатором типа сибазона, феназепама. Основной недостаток – это сильное угнетение дыхания фентанилом и сохранение сознания.
Источник

БОЛЬ В АНЕСТЕЗИОЛОГИИ И РЕАНИМАТОЛОГИИ Доц. Николаев Леонидович Проф. Кукушкин Михаил Львович ГБОУ ДПО РМАПО Кафедра анестезиологии и реаниматологии Лаборатория патофизиологии боли ГУ НИИ общей патологии и патофизиологии РАМН

Хроническая боль – это боль, продолжающаяся сверх нормального периода заживления и длящаяся более трех месяцев. (IASP)

ХРОНИЧЕСКАЯ БОЛЬ – ГЛОБАЛЬНАЯ ПРОБЛЕМА • Одна треть пациентов испытывает боль постоянно – 24 часа в день – 365 дней в году • Согласно исследованию «Боль в Европе» (2003) 30% людей, испытывающих боль, очень подавлены ею и «не могут больше ее терпеть» . Source: Pain in Europe, 2003

Распространенность хронической боли 12%-70% (m=22%) имеют хроническую боль От хронической боли страдает каждый пятый взрослый житель Европы (19% или 75 млн. человек) Павленко С. С. и соавт. , 2002; Bonica J. J. , 1990; Fordyce W. E. , 1995; Crombie I. K. , 1997; Jensen M. K. et al. , 2003; fon Korff M. , Leresche L. , 2005; Leresche L. , 2006
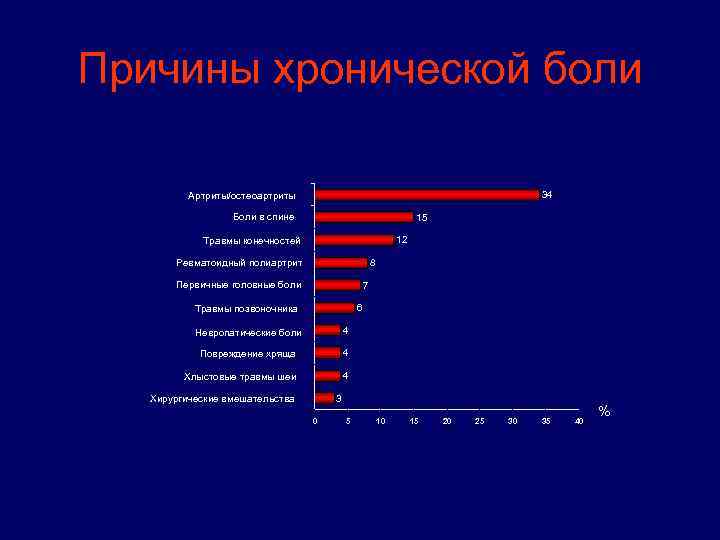
Причины хронической боли 34 Артриты/остеоартриты Боли в спине 15 12 Травмы конечностей Ревматоидный полиартрит 8 Первичные головные боли 7 6 Травмы позвоночника Невропатические боли 4 Повреждение хряща 4 Хлыстовые травмы шеи 4 3 Хирургические вмешательства 0 5 10 15 20 25 30 35 40 %

Идентификация и устранение повреждения при хронической боли часто не сопровождается исчезновением боли
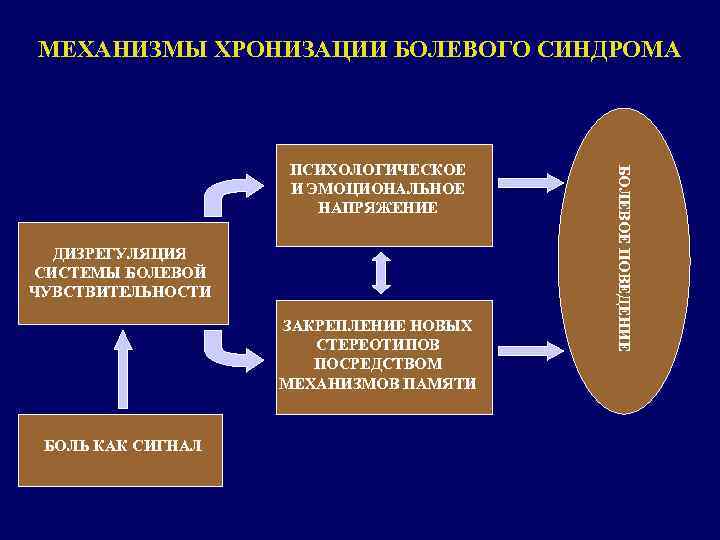
МЕХАНИЗМЫ ХРОНИЗАЦИИ БОЛЕВОГО СИНДРОМА ДИЗРЕГУЛЯЦИЯ СИСТЕМЫ БОЛЕВОЙ ЧУВСТВИТЕЛЬНОСТИ ЗАКРЕПЛЕНИЕ НОВЫХ СТЕРЕОТИПОВ ПОСРЕДСТВОМ МЕХАНИЗМОВ ПАМЯТИ БОЛЬ КАК СИГНАЛ БОЛЕВОЕ ПОВЕДЕНИЕ ПСИХОЛОГИЧЕСКОЕ И ЭМОЦИОНАЛЬНОЕ НАПРЯЖЕНИЕ
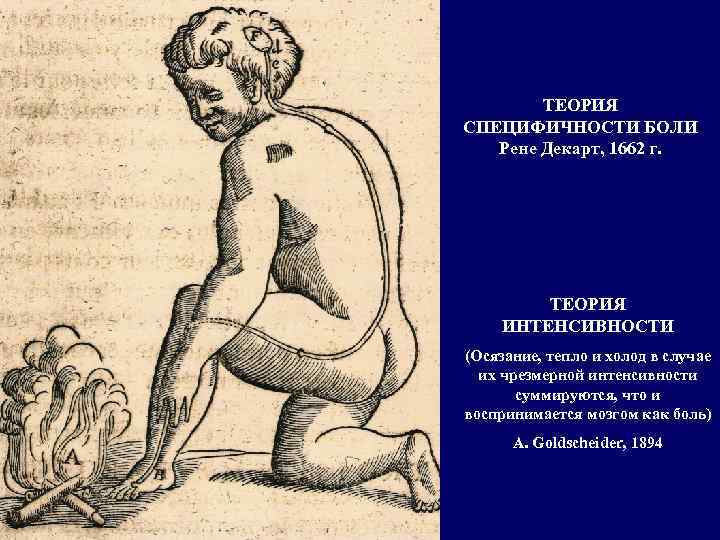
ТЕОРИЯ СПЕЦИФИЧНОСТИ БОЛИ Рене Декарт, 1662 г. ТЕОРИЯ ИНТЕНСИВНОСТИ (Осязание, тепло и холод в случае их чрезмерной интенсивности суммируются, что и воспринимается мозгом как боль) A. Goldscheider, 1894
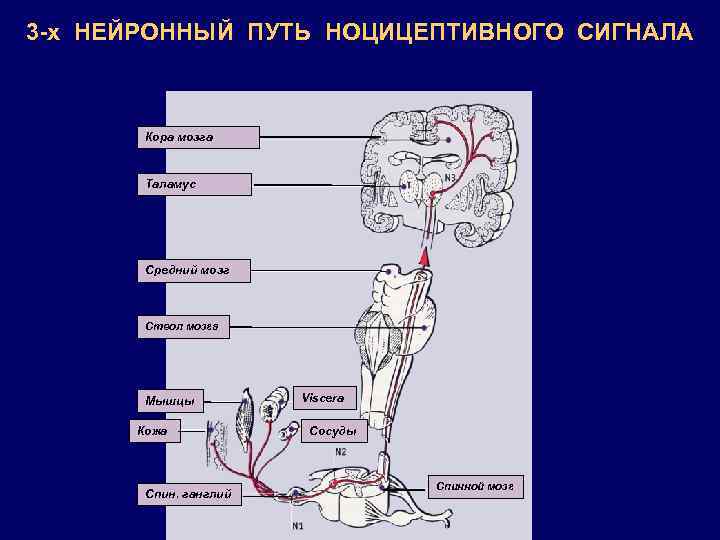
3 -х НЕЙРОННЫЙ ПУТЬ НОЦИЦЕПТИВНОГО СИГНАЛА Кора мозга Таламус Средний мозг Ствол мозга Мышцы Кожа Спин. ганглий Viscera Сосуды Спинной мозг
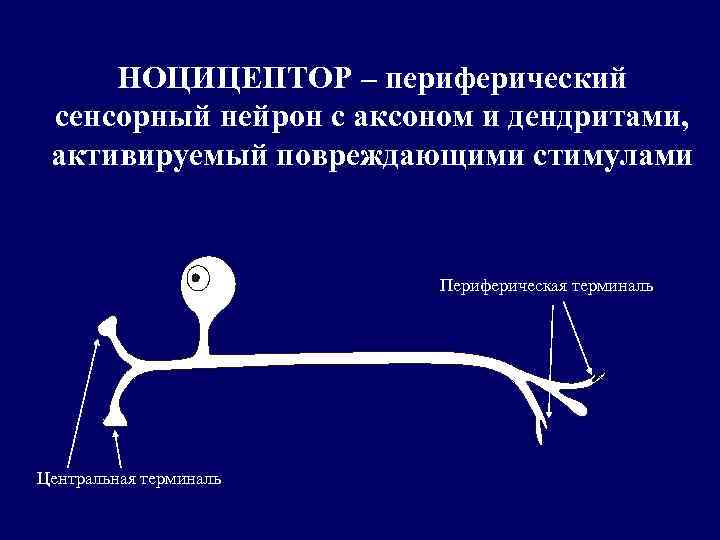
НОЦИЦЕПТОР – периферический сенсорный нейрон с аксоном и дендритами, активируемый повреждающими стимулами Периферическая терминаль Центральная терминаль

КЛАССИФИКАЦИЯ НОЦИЦЕПТОРОВ В ЗАВИСИМОСТИ ОТ МЕХАНИЗМА ВОЗБУЖДЕНИЯ РАЗЛИЧАЮТ: 1. МЕХАНОНОЦИЦЕПТОРЫ 2. ТЕРМОНОЦИЦЕПТОРЫ 3. ПОЛИМОДАЛЬНЫЕ НОЦИЦЕПТОРЫ КОЖА 1. ВЫСОКОПОРОГОВЫЕ А-ДЕЛЬТА МЕХАНОНОЦИЦЕПТОРЫ (5 -50 м/с) 2. А-ДЕЛЬТА МЕХАНО-ТЕРМОНОЦИЦЕПТОРЫ (3 -20 м/с) 3. С-ПОЛИМОДАЛЬНЫЕ НОЦИЦЕПТОРЫ (

ТИПЫ ВИСЦЕРАЛЬНЫХ НОЦИЦЕПТОРОВ ВИСЦЕРАЛЬНЫЕ НОЦИЦЕПТОРЫ ПО МЕХАНИЗМУ ВОЗБУЖДЕНИЯ ЯВЛЯЮТСЯ ПОЛИМОДАЛЬНЫМИ И МОГУТ ОДНОВРЕМЕННО АКТИВИРОВАТЬСЯ: • Механическими, термическими и химическими стимулами (42%) • Механическими и термическими стимулами (31%) • Механическими и химическими стимулами (27%)

ПЕРИФЕРИЧЕСКИЕ МЕДИАТОРЫ НОЦИЦЕПЦИИ – ТКАНЕВЫЕ АЛГОГЕНЫ, ВЫДЕЛЯЮЩИЕСЯ ВО ВНЕКЛЕТОЧНУЮ СРЕДУ ПРИ ПОВРЕЖДЕНИИ: а. ТУЧНЫХ КЛЕТОК (ГИСТАМИН, ИОНЫ К+ и Н+) б. ТРОМБОЦИТОВ (СЕРОТОНИН, АДФ) в. МАКРОФАГОВ (ИНТЕРЛЕЙКИНЫ, ФНО, СЕРОТОНИН) г. ЭНДОТЕЛИЯ (ИНТЕРЛЕЙКИНЫ, ФНО, ЭНДОТЕЛИНЫ, ПРОСТАГЛАНДИНЫ) – АЛГОГЕНЫ, ЦИРКУЛИРУЮЩИЕ В ПЛАЗМЕ КРОВИ: а. БРАДИКИНИН б. КАЛЛИДИН – АЛГОГЕНЫ, СЕКРЕТИРУЮЩИЕСЯ ИЗ ПЕРИФЕРИЧЕСКИХ ОКОНЧАНИЙ С-АФФЕРЕНТОВ: а. СУБСТАНЦИЯ Р б. НЕЙРОКИНИН А в. КАЛЬЦИТОНИН ГЕН-РОДСТВЕННЫЙ ПЕПТИД
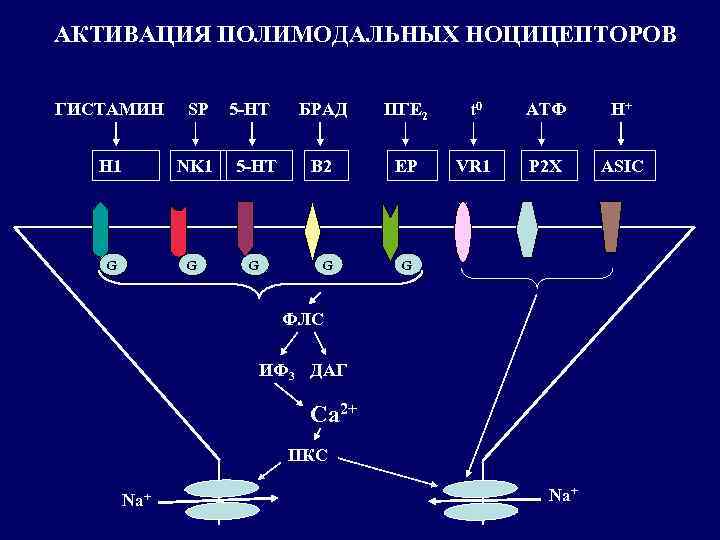
АКТИВАЦИЯ ПОЛИМОДАЛЬНЫХ НОЦИЦЕПТОРОВ ГИСТАМИН SP 5 -HT H 1 NK 1 5 -HT G G G БРАД ПГЕ 2 t 0 АТФ H+ B 2 EP VR 1 P 2 X ASIC G G ФЛС ИФ 3 ДАГ Са 2+ ПКС Na+
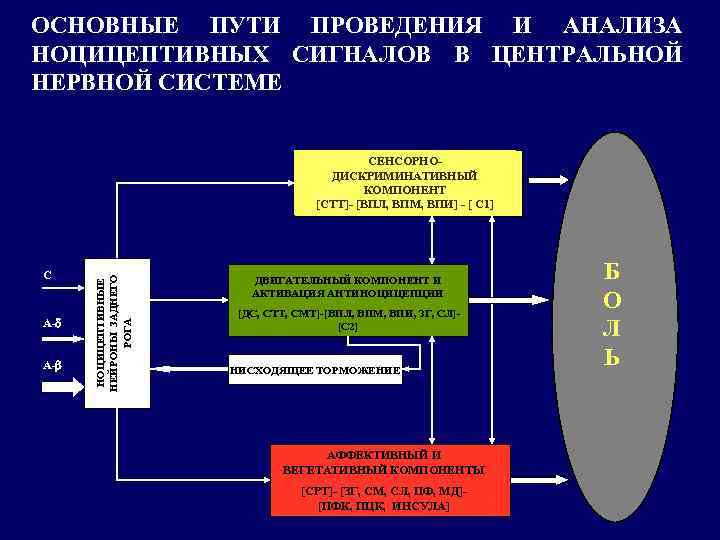
ОСНОВНЫЕ ПУТИ ПРОВЕДЕНИЯ И АНАЛИЗА НОЦИЦЕПТИВНЫХ СИГНАЛОВ В ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЕ С А-d А-b НОЦИЦЕПТИВНЫЕ НЕЙРОНЫ ЗАДНЕГО РОГА СЕНСОРНОДИСКРИМИНАТИВНЫЙ КОМПОНЕНТ [СТТ]- [ВПЛ, ВПМ, ВПИ] – [ С 1] ДВИГАТЕЛЬНЫЙ КОМПОНЕНТ И АКТИВАЦИЯ АНТИНОЦИЦЕПЦИИ [ДС, СТТ, СМТ]-[ВПЛ, ВПМ, ВПИ, ЗГ, СЛ][С 2] НИСХОДЯЩЕЕ ТОРМОЖЕНИЕ АФФЕКТИВНЫЙ И ВЕГЕТАТИВНЫЙ КОМПОНЕНТЫ [СРТ]- [ЗГ, СМ, СЛ, ПФ, МД][ПФК, ПЦК, ИНСУЛА] Б О Л Ь
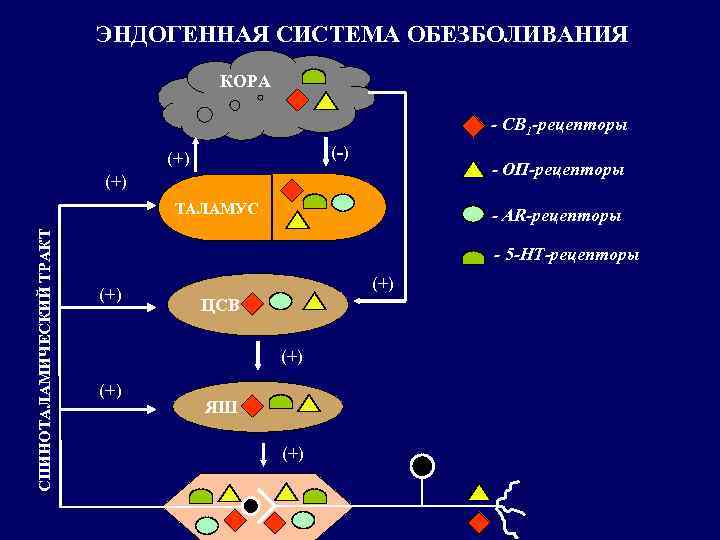
ЭНДОГЕННАЯ СИСТЕМА ОБЕЗБОЛИВАНИЯ КОРА – СВ 1 -рецепторы (-) (+) – ОП-рецепторы (+) СПИНОТАЛАМИЧЕСКИЙ ТРАКТ ТАЛАМУС – AR-рецепторы – 5 -HT-рецепторы (+) ЦСВ (+) ЯШ (+)

Необходимо помнить, что активность, возникающая в ноцицепторах или в ноцицептивных путях при повреждающих стимулах, не является болью, а представляет собой процесс обнаружения и передачи сигнала Taxonomy Committee of the International Association for the Study of Pain Конечная оценка (восприятие и осознание) ноцицептивных сигналов нашим мозгом в виде болевого ощущения, эмоции, переживания зависит от множества психологических факторов.
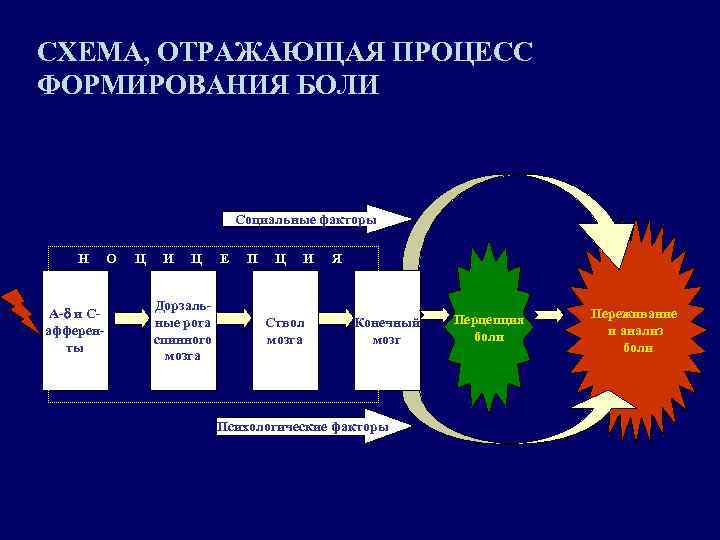
СХЕМА, ОТРАЖАЮЩАЯ ПРОЦЕСС ФОРМИРОВАНИЯ БОЛИ Социальные факторы Н А-d и Сафференты О Ц И Ц Дорзальные рога спинного мозга Е П Ц И Ствол мозга Я Конечный мозг Психологические факторы Перцепция боли Переживание и анализ боли
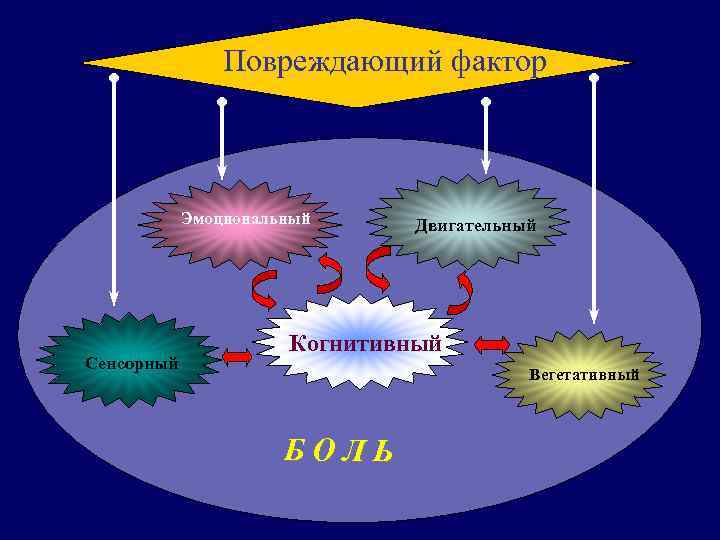
Повреждающий фактор Эмоциональный Сенсорный Двигательный Когнитивный Вегетативный БОЛЬ

БОЛЬ – это неприятное ощущение и эмоциональное переживание, связанное с действительным или возможным повреждением тканей или описываемое в терминах такого повреждения (IASP)

ОЩУЩЕНИЕ БОЛИ МОЖЕТ ВОЗНИКАТЬ НЕ ТОЛЬКО ПРИ ПОВРЕЖДЕНИИ ТКАНИ ИЛИ В УСЛОВИЯХ РИСКА ПОВРЕЖДЕНИЯ ТКАНИ, НО ДАЖЕ ПРИ ОТСУТСТВИИ КАКОГО-ЛИБО ПОВРЕЖДЕНИЯ ИНТЕРПРЕТАЦИЯ ЧЕЛОВЕКОМ БОЛЕВОГО ОЩУЩЕНИЯ, ЕГО ЭМОЦИОНАЛЬНАЯ РЕАКЦИЯ И ПОВЕДЕНИЕ МОГУТ НЕ КОРРЕЛИРОВАТЬ С ТЯЖЕСТЬЮ ПОВРЕЖДЕНИЯ

Больные, которые боятся анестезии или операции, хуже переносят боль и её бывает очень трудно купировать

Непреодолимый страх, боязнь боли и опасения неблагоприятного исхода операции испытывают 84% пациентов Московец О. Н. и соавт, 2003

• из 25 млн. пациентов оперированных в 1989 г. в США, 6 млн. испытывали сильные и очень сильные послеоперационные боли, а еще 3 млн. – боли средней интенсивности (J. Bonica, 1990). • средняя интенсивность боли на протяжении первых суток после операции достигает 60% от максимально возможной (Kuhn S. et al. , 1990). • адекватность обезболивания, которая оценивалась пациентом как «безболевой комфорт» , не превышала 50%. (Owen H. , 1990). • от выраженного болевого синдрома в послеоперационном периоде страдают от 30 до 75% пациентов (Carr D. , Goudas L. , 1999, Chauvin M. , 1999).

Боль вызывает: 1) усиление симпатической реакции организма с последующей тахикардией, усилением сократимости и потребления кислорода 2) снижает физическую активность, что может привести к венозному застою, повышенному риску тромбоза глубоких вен и эмболии легочной артерии 3) оказывает неблагоприятное влияние на перистальтику кишечника и мочевого тракта, что, в свою очередь, ведет к послеоперационному парезу кишечника, тошноте, рвоте и задержке мочи.

ОСНОВНЫЕ ФАКТОРЫ, ВЛИЯЮЩИЕ НА ИНТЕНСИВНОСТЬ И ДЛИТЕЛЬНОСТЬ ПОСЛЕОПЕРАЦИОННОГО БОЛЕВОГО СИНДРОМА ü локализация, характер и продолжительность операции, включая тип разреза и объем травмы ü наличие или отсутствие хирургических осложнений ü физиологические и психологические особенности пациента ü наличие предоперационной боли Moore D. , 1990, Aida S. et al. , 1999, Carragee E. , 1999
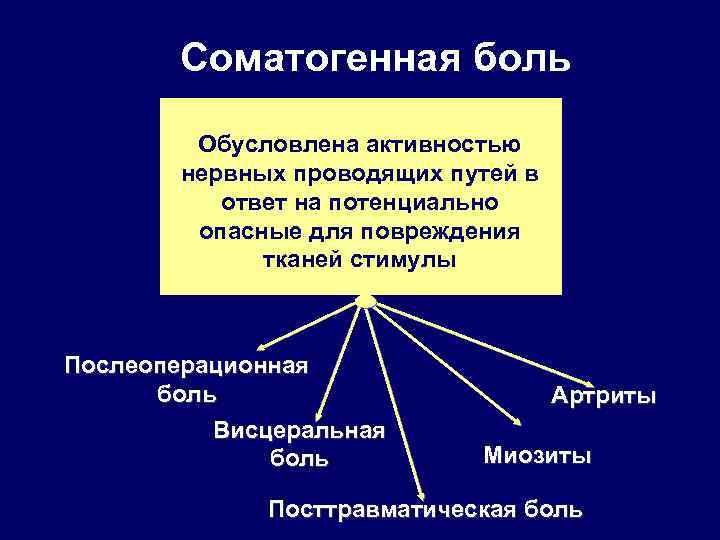
Соматогенная боль Обусловлена активностью нервных проводящих путей в ответ на потенциально опасные для повреждения тканей стимулы Послеоперационная боль Висцеральная боль Артриты Миозиты Посттравматическая боль

КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ СОМАТОГЕННЫХ БОЛЕВЫХ СИНДРОМОВ ЗОНЫ ПОСТОЯННОЙ БОЛЕЗНЕННОСТИ ЗОНЫ ПЕРВИЧНОЙ И ВТОРИЧНОЙ ГИПЕРАЛЬГЕЗИИ
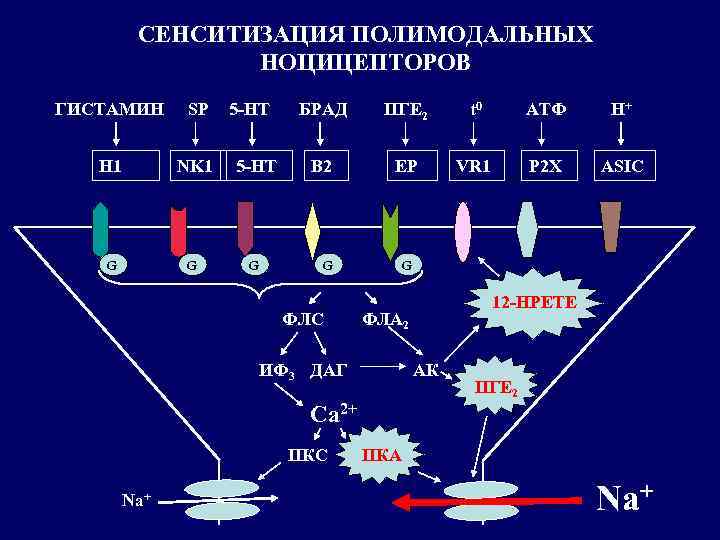
СЕНСИТИЗАЦИЯ ПОЛИМОДАЛЬНЫХ НОЦИЦЕПТОРОВ ГИСТАМИН SP 5 -HT H 1 NK 1 5 -HT G G G БРАД ПГЕ 2 t 0 АТФ H+ B 2 EP VR 1 P 2 X ASIC G ФЛС G 12 -HPETE ФЛА 2 ИФ 3 ДАГ АК ПГЕ 2 Са 2+ ПКС Na+ ПКА Na+
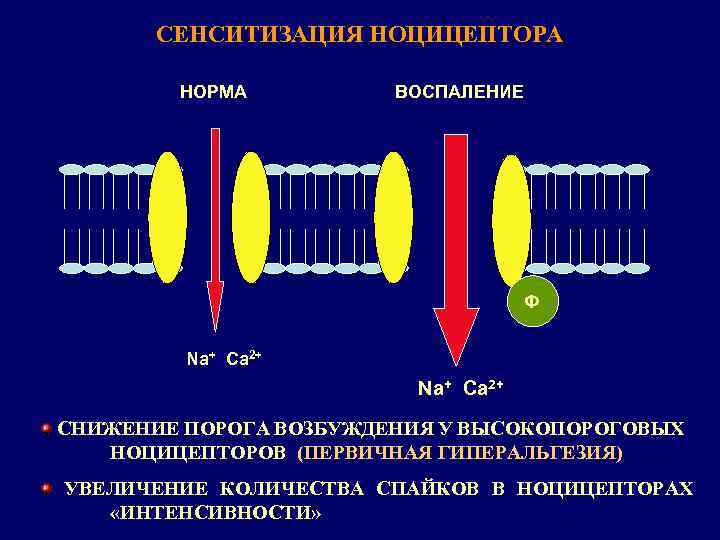
СЕНСИТИЗАЦИЯ НОЦИЦЕПТОРА НОРМА ВОСПАЛЕНИЕ Ф Na+ Ca 2+ СНИЖЕНИЕ ПОРОГА ВОЗБУЖДЕНИЯ У ВЫСОКОПОРОГОВЫХ НОЦИЦЕПТОРОВ (ПЕРВИЧНАЯ ГИПЕРАЛЬГЕЗИЯ) УВЕЛИЧЕНИЕ КОЛИЧЕСТВА СПАЙКОВ В НОЦИЦЕПТОРАХ «ИНТЕНСИВНОСТИ»
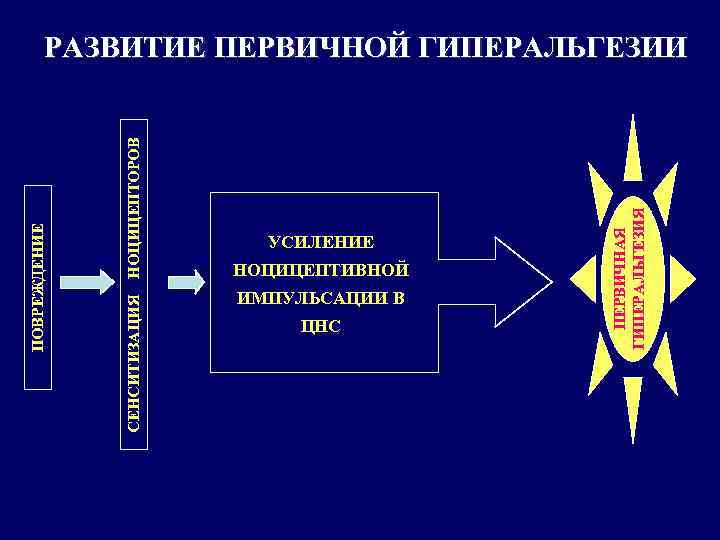
УСИЛЕНИЕ НОЦИЦЕПТИВНОЙ ИМПУЛЬСАЦИИ В ЦНС ПЕРВИЧНАЯ ГИПЕРАЛЬГЕЗИЯ НОЦИЦЕПТОРОВ СЕНСИТИЗАЦИЯ ПОВРЕЖДЕНИЕ РАЗВИТИЕ ПЕРВИЧНОЙ ГИПЕРАЛЬГЕЗИИ
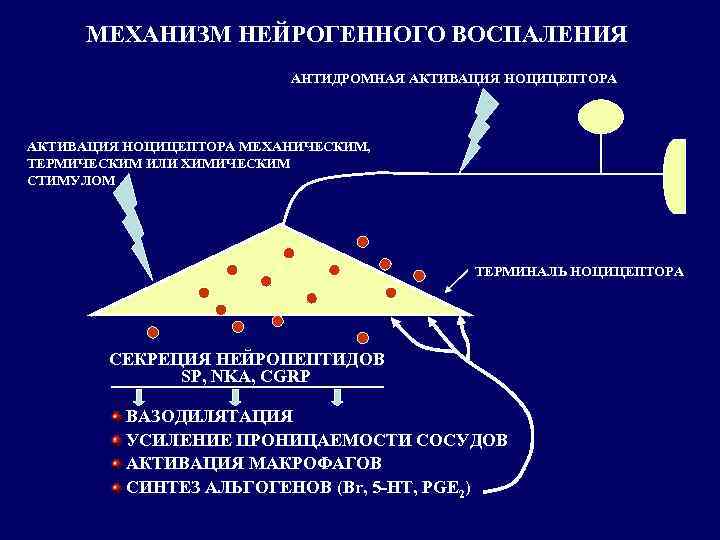
МЕХАНИЗМ НЕЙРОГЕННОГО ВОСПАЛЕНИЯ АНТИДРОМНАЯ АКТИВАЦИЯ НОЦИЦЕПТОРА МЕХАНИЧЕСКИМ, ТЕРМИЧЕСКИМ ИЛИ ХИМИЧЕСКИМ СТИМУЛОМ ТЕРМИНАЛЬ НОЦИЦЕПТОРА СЕКРЕЦИЯ НЕЙРОПЕПТИДОВ SP, NKA, CGRP ВАЗОДИЛЯТАЦИЯ УСИЛЕНИЕ ПРОНИЦАЕМОСТИ СОСУДОВ АКТИВАЦИЯ МАКРОФАГОВ СИНТЕЗ АЛЬГОГЕНОВ (Br, 5 -HT, PGE 2)
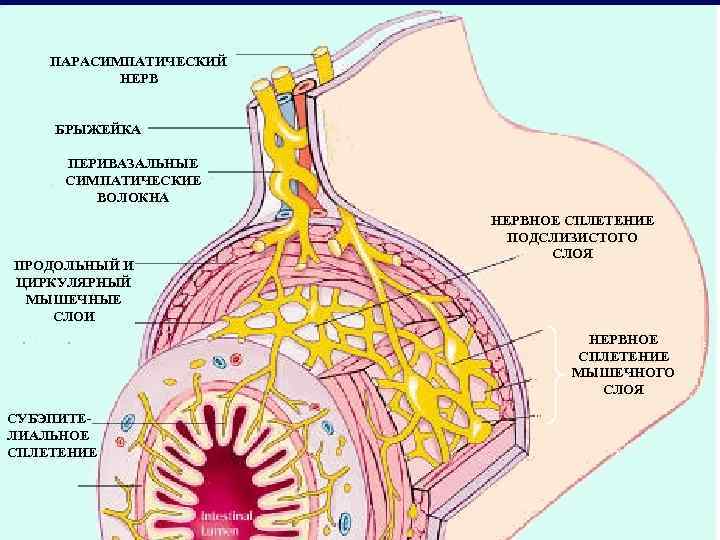
ПАРАСИМПАТИЧЕСКИЙ НЕРВ БРЫЖЕЙКА ПЕРИВАЗАЛЬНЫЕ СИМПАТИЧЕСКИЕ ВОЛОКНА ПРОДОЛЬНЫЙ И ЦИРКУЛЯРНЫЙ МЫШЕЧНЫЕ СЛОИ НЕРВНОЕ СПЛЕТЕНИЕ ПОДСЛИЗИСТОГО СЛОЯ НЕРВНОЕ СПЛЕТЕНИЕ МЫШЕЧНОГО СЛОЯ СУБЭПИТЕЛИАЛЬНОЕ СПЛЕТЕНИЕ

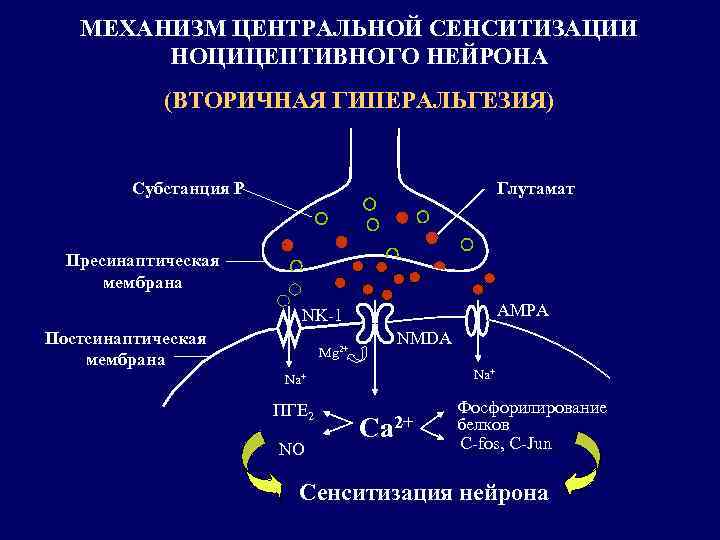
МЕХАНИЗМ ЦЕНТРАЛЬНОЙ СЕНСИТИЗАЦИИ НОЦИЦЕПТИВНОГО НЕЙРОНА (ВТОРИЧНАЯ ГИПЕРАЛЬГЕЗИЯ) Субстанция Р Глутамат Пресинаптическая мембрана AMPA NK-1 Постсинаптическая мембрана Mg 2+ NMDA Na+ ПГЕ 2 NO Ca 2+ Фосфорилирование белков C-fos, C-Jun Сенситизация нейрона