Чем отличается болезнь от синдрома кушинга
Дифференциация болезни и синдрома Иценко-Кушинга
Определенные трудности могут быть при дифференциальной диагностике между болезнью Иценко — Кушинга и синдромом Иценко — Кушинга, возникающим при развитии кортикостеро-мы надпочечника. При гормональном обследовании в обоих случаях обнаруживают значительное увеличение суммарных 17-0КС в моче (до 20—25 мг в сутки), в то время как 17-КС мочи остаются в пределах нормы или незначительно повышаются.
После введения кортизона или декеаметазона при болезни Иценко — Кушинга 17-КС мочи снижаются, а при злокачественной опухоли надпочечника этого не происходит. Однако иногда 17-КС мочи при болезни Иценко — Кушинга повышаются до 68,8 мг в сутки [Васюкова Е. И.]. Некоторые авторы объясняют это ускоренным переходом глюкокортикоидов в 17-КС, в результате чего уровень 17-ОКС мочи может снижаться.
Сочетание рано появляющейся гипертонии с высоким систолическим и диастолическим давлением, холестеринемией, повышением сахара в крови, глюкозурией и нарушением электролитного обмена также характерно для болезни Иценко — Кушинга. В то же время многие считают, что при данной болезни чаще наблюдается остеопороз и меньше выражена маскулинизация, чем при синдроме Кушинга.

Кроме того, при рентгенографии черепа в случае болезни Иценко — Кушинга обнаруживаются изменения турецкого седла, а в условиях ретропневмоперитонеума можно выявить не только опухоль надпочечника, но и гиперплазию его коры [Перепуст Л. Н. и др.].
Гиперплазия надпочечников распознается на основании интенсивности тени нормальных надпочечников, которая всегда меньше, чем тень верхнего полюса почки; усиление интенсивности тени надпочечника происходит только при гиперплазии.
Таким образом, при сочетании указанных клинических и гормональных данных можно диагностировать болезнь Иценко—Кушинга в ранней стадии. При дальнейшем развитии заболевания тень надпочечников становится негомогенной, с неровными и нечеткими контурами вследствие скопления большого количества жира в надпочечнике и в околонадпочечниковой клетчатке [Перепуст Л. Н. и др.].
Эти рентгенологические данные позволяют клиницисту распознать гиперкортицизм даже при наличии лишь одного патологического симптома и незначительной его выраженности. Имеются сообщения, что гиперфункция коры надпочечника может проявляться только гипертонией, остеопорозом или нарушением углеводного обмена.
Применение современных методов диагностики дает возможность клиницисту своевременно выявлять различные виды патологии надпочечников. При этом следует особенно осторожно диагностировать конституциональный гирсутизм, так как нередко за ним можно просмотреть ранние симптомы вирильного синдрома, который иногда проявляется только в гирсутизме. Хотя конституциональный гирсутизм может встречаться у совершенно здоровых женщин без каких-либо отклонений в выделении мочевых стероидов, тем не менее для уточнения диагноза в сомнительных случаях нужно производить гормональное обследование больной.
Имеются данные, что у больных с гирсутизмом повышено соотношение ЛГ/ФСГ и в 87% случаев наблюдается повышение андростендиона и тестостерона в плазме.
– Также рекомендуем “Лечение вирильного синдрома и аномалий наружных половых органов”
Оглавление темы “Вирильный синдром. Поликистоз яичников”:
- Дифференциация болезни и синдрома Иценко-Кушинга
- Лечение вирильного синдрома и аномалий наружных половых органов
- Эффекты длительного лечения глюкокортикоидами. Терапия адреногенитального синдрома
- Синдром склерокистозных яичников (Штейна — Левенталя)
- Теория надпочечникового генеза поликистозных яичников
- Теория морфологических и функциональных нарушений яичников при поликистозе
- Клиника и проявления синдрома Штейна—Левенталя
- Диагностика синдрома Штейна—Левенталя. Гормональные нарушения при поликистозе яичников
- Лечение синдрома Штейна—Левенталя. Операция при поликистозе яичников
- Маскулинизирующие опухоли яичников. Арренобластома
Источник
Все мы сталкиваемся с различными стрессовыми ситуациями в нашей повседневной жизни. Кортизол – это гормон, который отвечает за регулирование реакции на стресс. Гормон АКТГ, вырабатываемый нашей гипоф
Основное отличие – болезнь Кушинга от синдрома Кушинга
Все мы сталкиваемся с различными стрессовыми ситуациями в нашей повседневной жизни. Кортизол – это гормон, который отвечает за регулирование реакции на стресс. Гормон АКТГ, вырабатываемый нашей гипофизом, стимулирует выработку, а также высвобождение кортизола, и когда правильная регуляция этого процесса выходит из-под контроля, это приводит к избыточной выработке гормона. Болезнь Кушинга и синдром Кушинга являются двумя эндокринными состояниями, которые возникают из-за чрезмерного производства вышеупомянутого кортизола. Болезнь Кушинга вызывается опухолью или чрезмерным ростом гипофиза, и эта болезнь является основной причиной синдрома Кушинга. В этом главное отличие болезни Кушинга от синдрома Кушинга.
Здесь мы будем обсуждать,
1. Что такое болезнь Кушинга?
– Причина, Признаки и симптомы, Диагностика, Лечение и последующее наблюдение
2. Что такое синдром Кушинга?
– Причина, Признаки и симптомы, Диагностика, Лечение и последующее наблюдение
3. В чем разница между болезнью Кушинга и синдромом Кушинга?
Что такое болезнь Кушинга?
Болезнь Кушинга характеризуется избыточной выработкой гормона АКТГ из гипофиза и, как известно, является одной из основных причин синдрома Кушинга. Будучи очень редким заболеванием, поражающим лишь 10-15 человек на миллион, оно имеет значительное женское преобладание и чаще всего наблюдается у людей в возрасте от 20 до 50 лет.
Это заболевание обычно вызывается опухолью или чрезмерным ростом гипофиза, и известно, что аденома, доброкачественная опухоль железы, является одним из основных инициативных факторов. Эта опухоль начнет высвобождать чрезмерное количество АКТГ, которое, в свою очередь, высвободит кортизол и приведет к усиленному метаболизму углеводов, жиров и белков и уменьшит возможное воспаление.
Признаки и симптомы болезни Кушинга
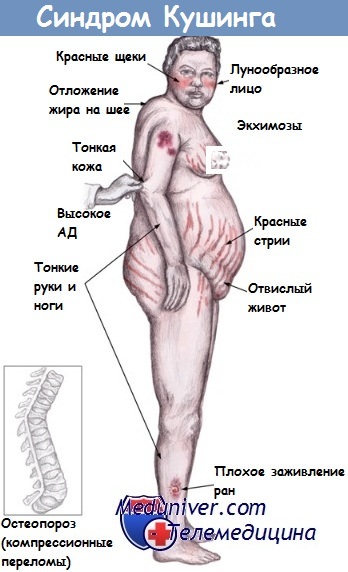
- Ожирение выше талии (верхней части тела) с тонкими верхними и нижними конечностями.
- Луноподобное лицо – полное, круглое и красное
- Задержка роста у детей
- Прыщи
- Кожные инфекции
- Фиолетовые стрии (следы) на коже живота, бедра и груди
- Легко синяки особенно на коже рук и кистей
- Боли в спине при нагрузке
- Буффало горб – отложение жира между плеч
- Мышечная слабость
- Боль в костях и нежность
- Чрезмерный рост волос на теле
- Нерегулярные периоды
- Снижение либидо
- импотенция
- Необъяснимая головная боль
- Увеличение частоты мочеиспускания
Диагностика, лечение и последующее наблюдение
Диагноз болезни Кушинга может быть поставлен на основании полной истории болезни вместе с тщательным физическим обследованием, чтобы увидеть наличие вышеупомянутых признаков и симптомов.
Тем не менее, дальнейшие исследования могут быть проведены для подтверждения чрезмерного уровня кортизола в организме:
- 24 часа – анализ мочи на кортизол
- Тест на подавление дексаметазона в низкой дозе
- Анализ слюны на кортизол (образцы поздней ночи и раннего утра)
Чтобы определить причину:
- Уровни АКТГ в крови
- МРТ головного мозга для исключения опухолей гипофиза
- Тест на кортикотрофин-рилизинг-гормон
- Тест на подавление высокой дозы дексаметазона
- Выборка нижнего синуса Петросала (IPSS)
Чтобы исключить любые связанные заболевания:
- Уровень сахара в крови натощак и HBA1c
- Уровни липидов и холестерина
- Минеральная плотность кости для исключения остеопороза
Что касается лечения болезни Кушинга, хирургическое удаление опухоли гипофиза является выбором выбора. Однако это может быть отложено в зависимости от тяжести состояния. После операции, гипофиз медленно начнет работать здоровым образом, как требуется.
Во время выздоровления пациентам будет назначена заместительная терапия кортизолом, так как железе потребуется достаточно много времени, чтобы начать вырабатывать АКТГ.
В случае, если опухоль не удалена полностью по определенной причине, показана лучевая терапия для медленного подавления усиленной активности.
Если опухоль не реагирует на хирургическую или лучевую терапию, пациенты должны будут использовать лекарства против кортизола, чтобы остановить выработку кортизола в организме.
Необработанная болезнь Кушинга может привести к различным другим осложнениям, таким как,
- Компрессионные переломы
- повышенное кровяное давление
- Сахарный диабет
- Камни в почках
- Инфекции
- Психиатрические состояния
Что такое синдром Кушинга
Это эндокринное заболевание, при котором организм вырабатывает повышенное количество кортизола из-за нескольких нарушений здоровья, таких как:
- Синдром экзогенного кушинга в результате чрезмерного потребления глюкокортикостероидов (преднизолон, дексаметазон) для лечения таких заболеваний, как астма, воспалительные заболевания кишечника, злокачественные новообразования, боли в суставах и т. Д.
- Болезнь Кушинга
- Опухоль надпочечника
- Опухоль, продуцирующая кортикотрофин – высвобождающий гормон (CRH)
- Эктопический синдром Кушинга – высвобождение чрезмерного АКТГ
Признаки и симптомы синдрома Кушинга схожи с синдромом Кушинга, и их диагностируют таким же образом, чтобы выявить избыточное присутствие кортизола в организме и возможные осложнения.
лечение Модальность синдрома Кушинга в основном зависит от этиологии.
- Пациентам, у которых это развивается после чрезмерного употребления кортикостероидов, рекомендуется медленно уменьшать лекарственную дозу и прекращать ее. В тех случаях, когда невозможно остановить дозировку из-за хронических заболеваний (диабет, гипертония), уровень кортизола следует тщательно контролировать для выявления любых возможных побочных эффектов.
- Если диагностирован опухоль гипофиза, удалите его хирургическим путем или проведите лучевую терапию с последующей заменой кортизола.
- Препараты, высвобождающие кортизол, для пациентов, опухоль которых не может быть удалена.
Разница между болезнью Кушинга и синдромом Кушинга
И болезнь Кушинга, и синдром Кушинга возникают из-за эндокринных нарушений в организме, особенно из-за чрезмерной секреции гормона кортизола.
Болезнь Кушинга является одной из основных причин синдрома Кушинга и предрасположен к опухоли гипофиза или аденоме головного мозга.
С другой стороны, синдром Кушинга может иметь множество причин, включая болезнь Кушинга, а также длительное потребление кортикостероидов, эктопические опухоли, высвобождающие ЦРБ и т. д.
Оба состояния диагностируются одинаково; лечение болезни Кушинга включает хирургическое удаление или лучевую терапию опухоли, а синдром Кушинга управляется в соответствии с первопричиной, как описано выше.
Изображение предоставлено:
«Синдром Кушинга» Микаэль Хэггстрем – собственная работа
Источник
Среди других поражений надпочечников нужно выделить симптомокомплекс эндогенного гиперкортицизма. Он объединяет различные по патогенезу, но сходные по клиническим проявлениям заболевания. Сходная клиническая картина обусловлена гиперпродукцией глюкокортикоидных гормонов, прежде всего кортизола.
Различают синдром Иценко—Кушинга и болезнь Иценко—Кушинга (безопухолевая форма). Синдром Иценко—Кушинга вызывается опухолью, развивающейся из пучковой зоны коры надпочечника (доброкачественная опухоль — кортикостерома, злокачественная — кортикобластома). Эндогенный гиперкортицизм встречается у 0,1% населения.
Установлено, что примерно у 60% больных имеет место гиперплазия коркового вещества надпочечников, у 30% — опухоль этого вещества, у 7—10% больных причиной заболевания служит аденома гипофиза.
В 2—3% обнаруживается наличие паранеопластического гиперкортицизма (Зографски С, 1977) или так называемого эктопического АКТГ-синдрома (Калинин А.П. и соавт., 2000), вызванного злокачественной опухолью, секретирующей кортикотропинподобную субстанцию и локализованной вне надпочечников (в бронхах, вилочковой железе, поджелудочной железе, яичках, яичниках и др.).
Болезнь Иценко—Кушинга является полиэтиологическим заболеванием, среди причин которой называют черепно-мозговую травму, инфекционные заболевания, психоэмоциональные нагрузки; отмечена связь заболевания с беременностью, родами, абортом и т.д.
Среди различных классификаций гиперкортицизма наиболее полной представляется классификация Маровой Е.И. (1999), в которой различают:
I. Эндогенный гиперкортицизм.
1. АКТГ-зависимая форма.
1.1. Болезнь Иценко—Кушинга, вызываемая опухолью гипофиза или гиперплазией кортикотрофов аденогипофиза.
1.2. АКТГ-эктопированный синдром, вызываемый опухолями эндокринной и неэндокринной системы, которые секретируют кортикотропин-рилизинг-гормон (КРГ) и/или АКТГ.
2. АКТГ — независимая форма.
2.1. Синдром Иценко—Кушинга, вызываемый опухолью коры надпочечника (кортикостерома, кортикобластома).
2.2. Синдром Иценко—Кушинга — микроузелковая дисплазия коры надпочечников юношеского возраста.
2.3. Синдром Иценко—Кушинга — макроузелковая форма заболевания надпочечников первично-надпочечникового генеза у взрослых.
2.4. Субклинический синдром Кушинга. Неполный синдром гиперкортицизма, наблюдающийся при «неактивных» опухолях надпочечников.
II. Экзогенный гиперкортицизм — ятрогенный синдром Иценко—Кушинга, связанный с длительным применением синтетических кортикостероидов.
III. Функциональный гиперкортицизм.
Наблюдается при ожирении, гипоталамическом синдроме, пубертатно-юношеском диспитуитаризме, сахарном диабете, алкоголизме, заболевании печени, беременности, депрессии.
А.П. Калинин с соавт. (2000) считают, что для хирурга-эндокринолога важно иметь представление о следующих наиболее часто встречающихся клинических формах гиперкортицизма:
• болезнь Иценко—Кушинга гипофизарного генеза;
• синдром Иценко—Кушинга, связанный с автономно секретирующими опухолями коркового вещества надпочечников;
• синдром Иценко—Кушинга, обусловленный кортикотропин-продуцирующими опухолями внегипофизарной локализации.
При гиперплазии надпочечники, не изменяя своей формы, диффузно увеличиваются. Вес и размеры гиперплазированных надпочечников обычно в 2—3 раза превышают нормальные.
Гиперплазия охватывает преимущественно светлые спонгиоциты пучковой зоны, где синтезируются глюкокортикоиды. Опухолевые новообразования коры обычно локализуются в одном надпочечнике.
Для гормональноактивных новообразований в надпочечниках характерно то, что они сочетаются с неактивной атрофией противоположной железы. В 50% случаев, особенно улиц молодого возраста, опухоли надпочечников подвергаются злокачественному перерождению.
Клиническая картина синдрома Иценко—Кушинга обусловливается гиперпродукцией глюкокортикоидных и, в меньшей степени, андрогенных и эстрогенных гормонов корой надпочечников. Количественное соотношение этих гормонов сильно варьирует, и этим объясняется большое изобилие и разнообразие симптомов данного синдрома.
Начало заболевания больных с гиперплазией коры надпочечников неопределенное. У большинства женщин оно начинается после аборта или родов. У больных с опухолевой формой синдрома, особенно при злокачественных опухолях коры, заболевание обычно начинается более остро и развивается быстрее.
Одним из наиболее характерных симптомов синдрома Иценко—Кушинга является ожирение. Оно обычно бывает андроидного типа с характерным перераспределением жирового депо, охватывает лицо и преимущественно верхнюю часть туловища, а конечности остаются тонкими в противовес полноте тела.
Лицо становится полным, круглым, с багрово-красными щеками, так называемое лунообразное лицо — fades tunata. Полнокровие обусловлено сосудорасширяющим влиянием продуцируемых в избытке глюкокортикоидных гормонов на сосуды кожи. Короткая шея с выраженным кифозом шейных позвонков и отложением жировой ткани у основания шеи позволяет называть такую шею «шеей бизона». Живот очень больших размеров, иногда свисает перед лобком как «передник».
Ожирение обычно нарастает медленно в течение нескольких лет.
Другим специфичным симптомом синдрома Иценко—Кушинга служит появление на коже живота, поясницы, молочных желез, бедер синюшно-багровых полос — striae rubrae. Рубцовые полосы при синдроме Иценко—Кушинга отличаются от полос при беременности и при обычном ожирении по своему характерному сизо-багровому цвету.
В длину они достигают 15—20 см, а в ширину — 1—3 см. Кожа по своему виду напоминает мрамор и склонна к пигментации. Последняя вызывается подкожными точечными кровоизлияниями и экхимозами, являющимися следствием повышенной ломкости кровеносных сосудов.
Другим характерным симптомом является обилие угрей локализующихся преимущественно на лице, спине и груди. Угри появляются у 50% больных и более выражены при опухолевых формах синдрома.
Очень часто при гиперглюкокортицизме наблюдаются гирсутизм — в 75% случаев. У женщин гирсутизм выражается увеличением оволосения подбородка, верхней губы, лобка и в подмышечных ямках, вокруг соска и конечностей. Это обусловлено повышенной секрецией андрогенов. У мужчин, наоборот, оволосение лица и груди незначительное.
Гирсутизм при опухолевых формах синдрома более выражен, особенно обильное оволосение наблюдается при злокачественных кортикоандростеромах.
Артериальная гипертензия наряду с ожирением и изменениями кожи является наиболее частым признаком болезни и синдрома Иценко—Кушинга. Она встречается у 90% больных и характеризуется высоким систолическим и диастолическим артериальным давлением, отсутствием кризов и устойчивостью к гипотензивной терапии.
Гипертензия обусловлена избыточной продукцией глюкокортикоидов, вызывающих задержку натрия и воды в организме с последующим увеличением объема циркулирующей крови.
У женщин часто отмечаются расстройства менструального цикла, выражающиеся дисменореей, гипоменореей и аменореей. Они вызваны пониженной гонадотропной стимуляцией гипофизом вследствие угнетения его гидрокортизоном. Половое влечение у таких больных резко понижается.
У мужчин наблюдается снижение полового влечения, достигающее в некоторых случаях полной импотенции. Развивается атрофия яичек с нарушением спермогенеза.
Изменения костей встречаются более чем у 2/3 больных. Они выражаются генерализованным остеопорозом скелета, наиболее сильно охватывающим позвоночник, ребра и кости черепа. Остеопороз обусловлен катаболическим действием глюкокортикоидов на белковую матрицу скелета, вследствие чего наступает повышенное извлечение солей кальция из костей.
При далеко зашедшем остеопорозе могут наступать патологические переломы ребер, костей таза и сдавление тел позвонков, которые приобретают вид «рыбьих позвонков» (Зографски С, 1977).
Это приводит к платиспондилии и кифозному искривлению позвоночника, особенно в шейно-грудной области, что часто вызывает радикулитные боли. У молодых больных наступает задержка роста вследствие усиленного катаболизма белкового субстрата костей.
Повышенная продукция глюкокортикоидов подавляет секрецию соматотропного гормона роста. Вследствие этого рост больных синдромом Иценко—Кушинга, если заболевание наступило в молодом возрасте, остается низким.
Нейро-мышечные симптомы — мышечная слабость и быстрая утомляемость — отмечаются в 70% случаев. Мышечная сила значительно понижается вследствие наступившей амиотрофии и уменьшения уровня калия в клетках.
При тяжелых формах заболевания наблюдаются изменения функций почек. В осадке мочи находят эритроциты и гиалиновые цилиндры. Часто обнаруживают изостенурию, олигурию и никтурию. В 1/3 случаев отмечается снижение клубочковой фильтрации.
Отсутствие параллелизма между тяжестью артериальной гипертензии и нарушениями функций почек объясняют дистрофическими изменениями паренхимы почек в результате нарушенных процессов обмена.
Ввиду обильного выведения солей кальция с мочой нередко развиваются нефролитиаз и нефрокальциноз. Длительная артериальная гипертензия может привести к развитию тяжелого нефроангиосклероза и хронической почечной недостаточности.
Особо нужно указать на нарушения обмена веществ, среди которых значительно изменен углеводный обмен. Чаще всего наблюдается гипергликемия и гликозурия, которые обусловлены гиперпродукцией глюкокортикоидов, стимулирующих белковый неоглюкогенез и обусловливающих развитие гипергликемии у этих больных.
Высокий уровень сахара в крови вызывает компенсаторную гиперинсулинемию. Вследствие анти-инсулинового эффекта кортизола наступает истощение бета-клеток инсулярного аппарата поджелудочной железы и развивается стероидный диабет. Он отличается резистентностью к инсулину, но редко вызывает ацидоз, и больные его хорошо переносят.
Вследствие нарушений процессов обмена в организме больных синдромом Иценко—Кушинга наступают тяжелые дистрофические изменения внутренних органов и пониженная устойчивость к инфекциям, в результате чего наблюдается склонность инфекций к генерализации.
Процессы регенерации у таких больных очень замедлены, поэтому при нагноении может наступить полное расхождение операционной раны.
Большое значение в диагностике болезни и синдрома Иценко—Кушинга, определения вида и характера патологических изменений имеют гормональные исследования. Они выявляют повышение концентрации кортизола плазмы. Повышенный уровень АКТГ указывает на гипофизарную этиологию синдрома.
При дифференциальной диагностике болезни и синдрома Иценко—Кушинга основное значение имеет компьютерная томография, позволяющая выявить гиперплазию или опухоль коры надпочечников (рис. 1,2).

Рис. 1. Компьютерная томограмма при кортикостероме правого надпочечника
Рис. 2. Компьютерная томограмма при гиперплазии левого надпочечника
Лечение. Ввиду полиэтиологичности синдрома для правильного выбора метода лечения абсолютно необходима постановка точного диагноза. При синдроме Иценко—Кушинга единственным методом лечения является адреналэктомия — удаление надпочечника вместе с гормонально-активной опухолью.
Хирургическое удаление опухоли следует проводить как можно раньше и максимально радикально, т.к. она нередко претерпевает злокачественное перерождение. Быстрое прогрессирующее развитие заболевания — доказательство злокачественности опухоли.
Обсуждаются показания к оперативному лечению болезни Иценко—Кушинга. Гиперплазия коры надпочечников встречается в 2—5 раз чаще опухолей ее. Авторы, по мнению которых синдром имеет гипоталамо-гипофизарное происхождение, считают, что для лечения заболевания показана рентгенотерапия (гамматерапия, протонное облучение) гипофизарной области или хирургическое вмешательство на самом гипофизе.
Однако гипофизэктомию нужно проводить по строгим показаниям, т.к. она сопровождается многочисленными осложнениями, наиболее частым из которых является синдром гипофизарной недостаточности. Большинство хирургов рекомендуют выполнять адреналэктомию, которая прекращает дальнейшее развитие синдрома, останавливая гиперсекрецию глюкокортикоидов.
В настоящее время адреналэктомию считают патогенетически обоснованной хирургической операцией, которая не приводит к нарушению функции других эндокринных желез, как это бывает после гипофизэктомии.
Развитие рентгеноэндоваскулярной хирургии привело к появлению щадящих, альтернативных хирургическим, методов лечения эндогенного гиперкортицизма. Так, И.В. Комиссаренко с соавт. (1984) разработали методику рентгеноэндоваскулярной гидродеструкции надпочечников и на опыте лечения многих больных показали ее эффективность.
В 1988 г. Ф.И. Тодуа внедрил в клиническую практику способ пункционной деструкции надпочечника под контролем КТ для лечения болезни Иценко—Кушинга.
В нашей клинике (1989) разработан метод рентгеноэндоваскулярной деструкции надпочечника путем эмболизации его венозного русла 3% раствором тромбовара.
При тяжелых и быстро развивающихся формах синдрома Иценко—Кушинга рентгеноэндоваскулярную деструкцию левого надпочечника дополняем контрлатеральной адреналэктомией, вместо антифизиологичной тотальной билатеральной адреналэктомии.
Ш.И. Каримов, Б.З. Турсунов, Р.Д. Суннатов
Опубликовал Константин Моканов
Источник
