Цитокины и острый коронарный синдром

Содержание | Следующая статья | Предыдущая статья
Оригинальные статьи | Номер 2’2014 |
М.А. Гордеева, А.Р. Бабаева, А.Л. Емельянова, С.И. Давыдов
Цель: Оценить уровень провоспалительных цитокинов: фактора некроза опухоли альфа (ФНО-α ), интерлейкина 1 β (ИЛ-1) и интерлейкина-6 (ИЛ-6) и их динамику в процессе лечения у пациентов с различными вариантами острого коронарного синдрома(ОКС) и хроническими формами ИБС(ХИБС). Материалы и методы: В исследование было включено 164 больных с ИБС: группа больных с инфарктом миокарда (ИМ) с подъемом сегмента ST(ИМспST) – 40 человек, больные с ИМ без подъема сегмента ST(ИМбпST)- 36 человек, пациенты с нестабильной стенокардией (НС) -33 человека и 55 человек с ХИБС. Результаты: Концентрация ФНО-α, ИЛ-1 и ИЛ-6 была достоверно выше во всех трех точках измерения у пациентов с ОКС по сравнению с контролем. Степень повышения медиаторов зависела от формы ОКС.Максимальные значения цитокинов выявлены у лиц с ИМспST. На фоне терапии к моменту выписки отмечена тенденция к снижению исследуемых медиаторов. Заключение: Исследованные маркеры воспаления способны повысить качество ранней диагностики, объективизировать риск сердечно-сосудистых осложнений, улучшить контроль за эффективностью лечения. (Цитокины и воспаление. 2014. Т. 13. № 2. С. 27–33.)
Ключевые слова: острый коронарный синдром, воспаление, цитокины.
На сегодняшний день ишемическая болезнь сердца (ИБС) – главная причина инвалидизации и смертности населения развитых стран, что заставляет искать новые возможности диагностики, профилактики и лечения заболевания, а также возможности прогнозирования и оценки риска сердечно-сосудистой смерти. Наиболее опасным является период обострения ИБС, клинические варианты которого объединяются термином острого коронарного синдрома (ОКС) [6, 7].
В основе различных клинических вариантов ОКС лежит единый патоморфологический процесс, заключающийся в эрозировании или разрыве атеросклеротической бляшки с последующим формированием тромба в месте дефекта интимы и окклюзией коронарной артерии [1, 6]. Данные многочисленных исследований свидетельствуют о том, что большинство опасных клинических проявлений ИБС, таких как ОКС, являются результатом непосредственного участия локального и системного иммунного воспаления, которое приводит к образованию атеросклеротической бляшки, ее разрыву и в конечном итоге к ишемии и потенциальному некрозу миокарда [9, 14] . Воспалительные реакции включают адгезию лейкоцитов к эндотелию, миграцию внутрь сосудистой стенки с последующей их активацией и превращением в пенистые клетки, которые в свою очередь стимулируют миграцию и пролиферацию гладкомышечных клеток и формирование атеросклеротической бляшки. Большое количество медиаторов воспаления было изучено в качестве индикаторов атеросклероза или предикторов его осложнений. Особый интерес представляет изучение специфических маркеров воспаления – цитокинов, которые могут быть прогностически более значимыми в определении процессов, связанных с дестабилизацией течения атеросклероза сосудов. Установлено, что нарушение баланса цитокинов в основном про- и противовоспалительного ряда, таких как интерлейкины: ИЛ-6, ИЛ-8, ИЛ-1β, ФНО -α играет важную роль в патогенезе сердечно-сосудистых заболеваний. Согласно современным представлениям, эти медиаторы участвуют в формировании и прогрессировании атеросклеротических поражений сосудов и связаны с дестабилизацией коронарной болезни сердца [2, 8].В настоящее время известно достаточное количество исследований по изучению уровней цитокинов у больных с ОКС, результаты которых указывают на гиперэкспрессию ФНО -α, ИЛ-1, ИЛ-6, ИЛ-10 при НС и ИМ [9]. Однако не все исследования подтверждают эту точку зрения. При исследовании цитокинового статуса в динамике острого коронарного синдрома отмечены различные варианты изменений уровней цитокинов: как закономерное постепенное снижение по мере стабилизации соcтояния пациента [10, 13], так и тенденция к повышению на 3-7 сутки заболевания [5]. Некоторые авторы отмечают значимое снижение на 3-7-й день, с последующим повышением к 21-му дню наблюдения ОКС [7]. Однако все еще нет четкого представления о взаимосвязи воспаления и развития острого коронарного синдрома (ОКС), о том, какие маркеры и на какой стадии заболевания лучше отражают его активность или затихание. В современной литературе, посвященной этому вопросу, данные часто носят весьма противоречивый характер [7] . В связи с этим мы решили оценить выраженность и динамику системного воспаления путем определения уровней провоспалительных цитокинов крови: ФНО-α, ИЛ-1β и ИЛ-6 у пациентов с различными вариантами ОКС и ХИБС.
Материалы и методы: В исследование было включено 164 больных с ИБС (86 мужчин и 78 женщин в возрасте от 39 до 87 лет.) Пациенты были разделены на 4 группы: группа больных с ИМспST – 40 человек, группа больных с ИМбпST-36 человек, пациенты с НС -33 человека и 55 человек с ХИБС. В зависимости от проводимой терапии больные с диагнозом ИМспST были распределены на две подгруппы: 1-я подгруппа (19 человек) — пациенты, которым проводили тромболитическую терапию, и 2-я подгруппа (21 человек) — пациенты без тромболизиса. Отсутствие тромболитической терапии было обусловлено поздним обращением больных, либо наличием противопоказаний. Группу ХИБС составили пациенты с диагнозом стабильной стенокардии напряжения (ССН) и постинфарктного кардиосклероза (ПК). В контрольную группу вошло 37 пациентов с артериальной гипертензией без признаков ИБС, сопоставимых с основной группой по полу и возрасту.Все пациенты подписывали информированное согласие на участие в исследовании.
Инструментальное исследование включало в себя электрокардиографию (ЭКГ), эхокардиографию (ЭхоКГ), определение толщины комплекса интима-медиа (ТИМ) сонных артерий, рентгенографию органов грудной клетки. Для лиц с ХИБС с целью верификации ишемии Холтер-ЭКГ или нагрузочные пробы. Лабораторное обследование включало в себя общий анализ крови, общий анализ мочи, анализ мочи на МАУ, биохимические исследования, включая билирубин с фракциями, трансаминазы, уровень креатинина, мочевины, биологические маркеры некроза миокарда (креатинфосфокиназа, МВ-фракция, количественное определение тропонина I), определение коагулограммы, С-реактивного белка, общего холестерина и липидного спектра, уровеня гликемии, гликированного гемоглобина (для лиц страдающих сахарным диабетом), электролиты плазмы крови; мочевую кислоту. Перечисленные параметры определяли у всех больных в 1-й день, 10- сутки и на 21-й день пребывания в стационаре.
Наличие ОКС, ССН устанавливали согласно критериям ВНОК. Диагноз ИМспST был выставлен на основании клинической картины (жалобы больных на боли за грудиной длительностью более 20 минут, в большинстве случаев не купирующихся полностью многократным приёмом нитроглицерина), стойкого подъема сегмента ST на ЭКГ, как минимум в двух последовательных отведениях или новой (впервые возникшей или предположительно впервые возникшей) блокадой левой ножки пучка Гиса (БЛНПГ); повышения в крови биологических маркеров некроза миокарда (КФК-МВ и уровня сердечных тропонинов) и выявления локальных нарушений сократимости миокарда [4]. ДиагнозИМбпST устанавливали у пациентов на основании клинической картины: после затяжного ангинозного приступа в покое, длящегося более 15 минут, не купирующегося приёмом нитроглицерина, данных ЭКГ( отсутствие элевации сегмента ST; депрессия сегмента ST 1 мм в двух и более смежных отведениях или инверсия зубца Т 1мм в отведениях с преобладающим зубцом R; данныхЭхоКГ (нарушение локальной сократимости миокарда); повышение в крови биологических маркеров повреждения миокарда [3] .Диагнознестабильной стенокардии устанавливали у пациентов на основании клинической картины: после затяжного ангинозного приступа в покое, длящегося более 15 минут, не купирующегося приёмом нитроглицерина; у пациентов с впервые возникшей в предшествовавшие 28-30 дней тяжелой стенокардией и у лиц, у которых произошла дестабилизация ранее существовавшей СС с появлением характеристик, присущих по крайней мере III ФК по классификации Канадской ассоциации кардиологов и/или приступов боли в покое, данных ЭКГ( депрессия сегмента ST 1 мм в двух и более смежных отведениях или инверсия зубца Т 1мм в отведениях с преобладающим зубцом R, а также сглаженность или псевдонормализация зубцов Т; данныхЭХО-КГ (транзиторное нарушение локальной сократимости миокарда);отсутствия повышения в крови биологических маркеров некроза миокарда[3] .Диагноз ССН устанавливался на основании клинической картины (загрудинная боль или дискомфорт характерного качества и продолжительности, возникающий при физической нагрузке или психоэмоциональном стрессе, проходящая в покое и/или после приема нитроглицерина), регистрации ЭКГ (значимость имела ЭКГ, зарегистрированная на фоне болевого синдрома – выявление ишемии), нагрузочных тестов или суточного мониторирования ЭКГ (верификация ишемии при физической нагрузке).Диагноз ПК был установлен на основании анамнеза (перенесённый в прошлом инфаркт миокарда), ЭКГ-данных (рубцовые изменения, признаки аневризмы левого желудочка), ЭХОКГ (зоны гипо-, акинеза, наличие аневризмы в зоне рубцов).
Всем пациентам с ИМ проводилось определение уровня цитокинов ФНО-α, ИЛ-1, ИЛ-6 в первые, 10-е, 21-е сутки пребывания в стационаре. У пациентов с НС уровень цитокинов определяли дважды: в первые и на 10-е сутки. Пациентам с ХИБС уровень цитокинов определяли однократно при поступлении. Количественный анализ ФНО-α и ИЛ-1, ИЛ-6 в сыворотке крови обследуемых лиц проводили методом твердофазного иммуноферментного анализа с помощью наборов реагентов ЗАО «Вектор-Бест» (г. Новосибирск). Всем больным проводили стандартную терапию в соответствии с рекомендациями ВНОК по лечению ОКС, ССН и ПК. В нашем исследовании и основная и контрольная группа получала статины, таким образом, их роль в воздействии на иммуновоспалительный процесс была равнозначна в сравниваемых группах.
Для статистической обработки результатов использовались пакеты статистических программ «Statistica 6.0» и «Microsoft Excel» – статистика». При сравнении двух независимых групп больных по основным показателям использовали непарный t-критерий Стьюдента. При проведении парных сравнений уровней показателей внутри групп в первые сутки и последующие (10-и и 21-е) сутки применяли t-критерий Стьюдента для зависимых групп. Корреляционный анализ количественных величин проводили вычислением коэффициента корреляции Пирсона. Различия принимали как статистически значимые при р <0,05.
Результаты и обсуждение
Содержание | Следующая статья | Предыдущая статья
Источник
Цитокиновый шторм при коронавирусе можно рассматривать как позднюю стадию инфекции. Он ведет к развитию респираторного дистресс-синдрома, полиорганной недостаточности и может спровоцировать смерть.
Цитокиновый шторм — это ситуация, когда вырабатывается большое количество цитокинов, что ведет к излишне бурной активации воспаления и иммунным сбоям. При ковиде именно вирус запускает этот процесс. Основным корабликом, который перемалывает шторм, становятся легкие. Но попутно могут страдать и близлежащие острова: сердце, почки, кишечник, селезенка, центральная нервная система.
Простыми словами, вирус вводит организм в заблуждение и провоцирует чрезмерную защиту, направленную телом против самого себя. Передозировка защиты приводит к поражению легких.
Цитокины — биологически активные вещества, выделяющиеся в организме лейкоцитами (макрофагами, лимфоцитами), клетками внутренней сосудистой выстилки, фибробластами. Разные их виды могут:
- усиливать воспаление,
- подавлять его,
- регулировать иммунитет.
Начало
В раннем периоде пневмонии, связанной с коронавирусом, идет местное легочное воспаление, усиливающее тромбоз мелких сосудов и небольшие кровоизлияния в ткань органа. У больного имеет место:
- повышение температуры (см. особенности температуры при ковиде),
- заложенность грудной клетки, дискомфорт в ней,
- сухой кашель или с небольшим количеством мокроты (прозрачной или гнойной при присоединении бактерий, см. какой может быть кашель при ковиде),
- одышка (при ковиде).
Все эти признаки укладываются в клинику вирусной или вирусно-бактериальной пневмонии с дыхательной недостаточностью (частота дыханий >22, сатурация <95%) или без нее.
Чаще всего такое положение развивается к 6-8 суткам от начала лихорадки.
На КТ легких можно увидеть характерные для коронавирусного поражения изменения.
В анализах крови фибриноген остается нормальным, D-димер повышен.
Течение
Излишняя агрессия иммунного ответа приводит к развитию бурного воспаления со стороны паренхимы и альвеол легких, прилегающих бронхов. Нарушается нормальное состояние внутренней выстилки сосудов, что совместно с расстройствами свертывания приводит к тромбообразованию.
К фосфолипидам клеточных мембран формируются антитела, развивается подобие антифосфолипидного синдрома. Клинические симптомы цитокинового шторма похожи на массированный тромбоз при ДВС-синдроме. Множественные тромбы в легких превращают их в «фарш», не способный поддерживать газообмен и насыщать кровь кислородом.
Респираторный дистресс-синдром может протекать в несколько фаз:
- Острая занимает от 2 до 5 суток и может благополучно разрешиться на кислородотерапии или ИВЛ.
- При неблагоприятном течении может развиваться подострая фаза воспаления. Она затягивает сроки респираторной поддержки или ведет к неблагоприятному исходу.
- Хронический вариант — это фиброзирующий альвеолит — причина образования рубцов в легких и выключение из работы их части. Это ведет к хронической дыхательной недостаточности (одышке в нагрузке или в покое, см. фиброз легких после ковида).
В финале легкие больше не функционируют и не могут освоить даже аппаратно подаваемый (респираторной маской из баллона или аппаратом искусственной вентиляции) кислород. Дополнительно тромбозы могут приводить к инфарктам внутренних органов (миокарда, селезенки). Больной может погибнуть и без присоединения бактериальной инфекции (см. Реальная статистика смертности от ковид по данным Росстата).
Симптомы
Как проявляется цитокиновый шторм? По сути это — клиника острой дыхательной недостаточности. На какой день она разовьется от начала ковидной пневмонии и разовьется ли вообще, зависит от индивидуальных особенностей организма, сопутствующих патологий, принимаемых препаратов.
Чаще это 8-14 сутки от начала клиники. У больных бронхиальной астмой на поддерживающей терапии ингаляционными глюкокортикоидами такой вариант ковида встречается статистически реже. Молодые здоровые мужчины страдают от него чаще.
Характерные проявления:
- учащение дыхания >30-40,
- ощущение нехватки воздуха, невозможности полноценного вдоха,
- шумное дыхание с участием вспомогательных мышц грудной клетки,
- вынужденное положение сидя с опорой на руки,
- синюшность кожи,
- возбуждение, сменяющееся затем заторможенностью или потерей сознания.
У детей аналогом цитокинового шторма взрослых является мультисистемный воспалительный синдром (см. симптомы ковида у ребенка).
Лабораторные показатели
В анализах крови цитокиновому шторму будут соответствовать:
- лейкоциты ниже 3*10 9 г/л,
- лимфоциты < 1*10 9 г/л,
- снижение базофилов, эозинофилов, моноцитов,
- интерлейкин-6 >40 пг/мл,
- С-реактивный белок > 75 мг/мл,
- увеличение D-димера в 4 и более раз,
- увеличение ферритина > 500 нг/мл,
- укорочение АЧТВ,
- значительное увеличение фибриногена,
- нарастание АлАТ, АсАТ, ЛДГ.
Сколько длится такой сбой, зависит от успешности терапии. При развитии острого респираторного дистрес-синдрома каждые 2-3 суток до получения стойких стабильных уровней необходимо контролировать D-димер, ферритин, фибриноген, СРБ, ЛДГ.
Терапия
- Лечение гидроксихлорахином не оправдано при тяжелых и крайне тяжелых формах ковида (в том числе при цитокиновом шторме), так как его вред для сердца в высоких дозах сведет на нет всю пользу от подавления излишнего иммунитета.
- Возможно использование антиковидной плазмы в первую неделю от развития симптомов респираторного дистресс-синдрома.
- Препарат выбора для подавления высокой реактивности иммунной системы — глюкококртикоид. Метилпреднизолон или дексаметазон внутривенно позволяют вести лечение цитокинового шторма. В дальнейшем переходят на поддерживающие дозы в таблетках. Глюкокортикоиды сочетают с непрямыми антикоагулянтами.
- Профилактика полиорганной недостаточности на фоне цитокинового шторма ведется ингибиторами интерлейкинов (тоцилизумабом, сарилумабом или канакинумабом).
- Для быстрого купирования цитокинового шторма тоцилзумаб назначается внутривенно совместно с глюкокортикоидом.
- Инфузионная терапия (10-15 мл/кг в сутки) в ОРИТ, кислородотерапия в прон-позиции (лежа на животе) по 12-16 часов в сутки, ИВЛ по показаниям (два любых признака из трех: нарушение сознания; сатурация<92%, частота дыханий>35 в минуту).
Как избежать цитокинового шторма? Не заниматься самолечением на дому, при подозрении на ковид или его симптомах, обратиться за квалифицированной медицинской помощью, выполнять рекомендации лечащего врача (см. последствия ковида для организма после болезни и реабилитация после ковида).
Видео: Главврач Коммунарки Денис Проценко о второй волне / ЭПИДЕМИЯ с Антоном Красовским. Новый сезон
- 20-00 Критерии для госпитализации
- 20-14 Шкала, по которой оценивают нужна ли госпитализация
- 21-25 Чем пониженная сатурация при свином гриппе отличается от сатурации при коронавирусе
- 24-37 Что такое цитокиновый шторм
- 30-41 О выживаемости на ИВЛ
- 31-35 Проценко: «Для нас перевод на ИВЛ — это крайняя точка, когда другие меры невозможны»
- 35-58 Чем отличается неинвазивная вентиляция легких от инвазивной
Источник
Острый коронарный синдром — это группа клинических и лабораторно-инструментальных признаков, указывающих на наличие нестабильной стенокардии или инфаркта миокарда. Состояние проявляется загрудинной болью длительностью более 20 минут, которая сопровождается потливостью, одышкой, бледностью кожи. У 15-20% больных наблюдается атипичное клиническое течение синдрома. Для диагностики проводят анализ кардиоспецифических ферментов, регистрируют ЭКГ. Медикаментозное лечение предполагает использование тромболитиков, антиагрегантов и антикоагулянтов, антиангинальных препаратов. В тяжелых случаях показана хирургическая реваскуляризация.
Общие сведения
Острый коронарный синдром (ОКС) является предварительным диагнозом, который устанавливается во время первого обследования пациента врачом-терапевтом. Термин возник в связи с необходимостью выбора лечебной тактики при ургентных состояниях, не дожидаясь постановки окончательного диагноза. ОКС и его осложнения занимают первое место (около 48%) среди всех причин смертности взрослого населения. Неотложное состояние у мужчин в возрасте до 60 лет определяется в 3-4 раза чаще, чем у женщин. В группе пациентов 60-летнего возраста и старше соотношение мужчин и женщин составляет 1:1.
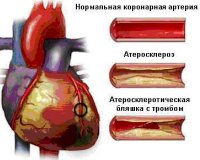
Острый коронарный синдром
Причины
Все нозологические единицы, входящие в состав острого коронарного синдрома имеют общие этиологические факторы. Основной причиной заболевания служит тромбоз коронарного сосуда, возникающий при эрозии или разрыве атеросклеротической бляшки (атеротромбоз). Окклюзия венечной артерии тромбом встречается у 98% больных с выявленной клинической картиной ОКС. При тромбозе развитие коронарного синдрома связано как с механической закупоркой артерии, так и с выделением специфических вазоконстрикторных факторов.
Другая этиология острого процесса определяется крайне редко (около 2% случаев). Появление ОКС возможно при тромбоэмболии либо жировой эмболии коронарной артерии. Еще реже диагностируется переходящий спазм коронарных артерий — вариантная стенокардия Принцметала.
Факторы риска
Поскольку большинство эпизодов связано с атеросклеротическими осложнениями, факторы риска коронарного синдрома идентичны таковым для атеросклероза. Различают:
- Немодифицируемые факторы: мужской пол, пожилой возраст, наследственная предрасположенность;
- Корригируемые факторы: избыточная масса тела, вредные привычки, гиподинамия.
Наибольшую опасность из предпосылок представляет артериальная гипертензия. Повышенное артериальное давление способствует более раннему началу и быстрому прогрессированию атеросклероза.
Патогенез
Патофизиологической основной болезни служит острое снижение кровотока в одном из венечных сосудов. В результате этого нарушается баланс между потребностью мышечных волокон в кислороде и притоком артериальной крови. При остром коронарном синдроме возникает переходящая или стойкая ишемия, которая при прогрессировании вызывает органические изменения миокарда (некрозы, дистрофию).
При разрыве фиброзного покрова атеросклеротической бляшки происходит отложение тромбоцитов и фибриновых нитей — образуется тромб, перекрывающий просвет сосуда. В патогенезе синдрома существенную роль играют гемостатические нарушения, которые обуславливают формирование микротромбов в сосудах, питающих миокард. Выраженная клиническая симптоматика наблюдается при сужении просвета коронарной артерии не менее, чем на 50-70%.
Классификация
В современной кардиологии используется классификация, которая учитывает ЭКГ-проявления коронарного синдрома. Такое разделение патологии наиболее удобно в неотложной ситуации, когда врачу необходимо принимать решение о назначении лекарственной терапии для лечения острого состояния. Согласно этой классификации выделяют 2 формы коронарного синдрома:
- ОКС с подъемом ST (ОКСП ST). При данной форме отмечается стойкая ишемия и полная окклюзия (закрытие просвета) одной из венечных артерий. Состояние соответствует окончательному диагнозу «инфаркт миокарда». Подъем ST выше изолинии на ЭКГ — прогностически неблагоприятный признак.
- ОКС без подъема ST (ОКСБП ST). У таких пациентов начинаются ишемические процессы в миокарде при сохраненном кровотоке в коронарных сосудах. На ЭКГ зачастую определяются патологические изменения зубца T. Такой диагноз соответствует нестабильной стенокардии либо мелкоочаговому инфаркту миокарда без зубца Q.
Симптомы ОКС
Основное проявление острого коронарного синдрома — характерный приступ загрудинной боли. Болевые ощущения локализуются по центру либо с левой стороны грудной клетки. Боль возникает при физической нагрузке (быстрая ходьба, подъем по ступенькам) либо после эмоциональных стрессов. Боли могут быть жгучими, давящими, сжимающими. Типична иррадиация в левую руку, межлопаточную область, шею. Длительность приступа от 20 минут до получаса и более.
На развитие острого кислородного голодания сердечной мышцы указывает учащение и увеличение продолжительности сердечных болей при стабильной стенокардии. При этом снижается эффективность нитроглицерина для купирования острого болевого приступа. Кроме загрудинных болей типична бледность кожных покровов, иногда появляется холодный пот. Беспокоят одышка, резкая слабость и головокружение.
Для молодых (до 40 лет) и пожилых пациентов (старше 75 лет), а также больных сахарным диабетом характерно атипичное течение острого коронарного синдрома. В таких случаях возможны сильные боли в эпигастрии, которые сочетаются с расстройством пищеварения. Реже начинается односторонняя пульсирующая боль в грудной клетке. На фоне острого ухудшения состояния может наступить обморок.
Осложнения
В остром периоде данного состояния существует высокий риск внезапной сердечной смерти: около 7% при ОКС с элевацией сегмента ST, 3-3,5% при коронарном синдроме с нормальным ST. Ранние осложнения выявляются в среднем у 22% пациентов. Наиболее распространенное последствие заболевания — кардиогенный шок, который вдвое чаще диагностируется у мужчин. У больных старше 50 лет, как правило, развиваются тяжелые нарушения ритма и проводимости.
При успешном купировании острого сердечного приступа у 6-10% пациентов сохраняется риск поздних осложнений, которые развиваются спустя 2-3 недели после манифестации синдрома. Вследствие замещения участка мышечных волокон соединительной тканью есть вероятность развития хронической сердечной недостаточности, аневризмы сердца. При сенсибилизации организма продуктами аутолиза возникает синдром Дресслера.
Диагностика
С учетом типичных проявлений острого ангинозного приступа врач-кардиолог может поставить предварительный диагноз. Физикальное обследование необходимо для исключения внесердечных причин боли и кардиальных патологий неишемического происхождения. Для дифференцировки разных вариантов коронарного синдрома и выбора лечебной тактики проводятся три основных исследования:
- Электрокардиография. «Золотым стандартом» диагностики считается регистрация ЭКГ в течение 10 минут от начала острого приступа. Для коронарного синдрома характерна элевация ST более 0,2-0,25 мВ либо его депрессия в грудных отведениях. Первый признак ишемии миокарда — остроконечный высокий зубец Т.
- Биохимические маркеры. Чтобы исключить инфаркт, анализируется содержание кардиоспецифических энзимов — тропонинов I и Т, креатинфосфокиназы-МВ. Наиболее ранним маркером является миоглобин, который повышается уже в первые часы заболевания.
- Коронарная ангиография. Инвазивный метод исследования венечных сосудов используется после выявления подъема сегмента ST на кардиограмме. Коронарография применяется на этапе подготовки к реваскуляризации пораженной тромбом артерии.
После стабилизации состояния и ликвидации острого коронарного синдрома специалист назначает дополнительные методы диагностики. Для оценки риска пациентам с установленным диагнозом ИБС рекомендуют неинвазивные стресс-тесты, которые показывают функциональные возможности сердца. ЭхоКГ выполняют для измерения фракции выброса левого желудочка и визуализации магистральных сосудов.
Лечение острого коронарного синдрома
Консервативная терапия
Лечение больных с ОКС проводится только в специализированных кардиологических стационарах, пациентов в тяжелом состоянии госпитализируют в реанимационные отделения. Терапевтическая тактика зависит от варианта коронарного синдрома. При наличии на кардиограмме подъема ST устанавливают диагноз острого инфаркта миокарда. В таком случае показана интенсивная и тромболитическая терапия по стандартной схеме.
Пациентам, у которых не обнаружено стойкой элевации ST, назначают комбинированную медикаментозную терапию без тромболитиков. Чтобы купировать приступ, используют нитраты. Дальнейшее лечение направлено на ликвидацию ишемических процессов в миокарде, нормализацию реологических свойств крови и коррекцию артериального давления. В этих целях рекомендуется несколько групп лекарственных средств:
- Антиагреганты. Для профилактики тромбообразования принимают препараты на основе ацетилсалициловой кислоты или тиенопиридиновые производные. После начальных нагрузочных доз переходят на длительный прием медикаментов в средних терапевтических дозировках. В первые 2-5 дней схему дополняют антикоагулянтами.
- Антиишемические средства. Для улучшения кровоснабжения сердца и снижения потребности сердечной мышцы в кислороде применяют ряд препаратов: блокаторы кальциевых каналов, нитраты, бета-адреноблокаторы. Некоторые из этих лекарств обладают гипотензивным действием.
- Гиполипидемические препараты. Всем пациентам назначаются статины, которые снижают уровень общего холестерина и атерогенных ЛПНП в крови. Терапия уменьшает риск повторного развития острого коронарного синдрома, значительно улучшает прогноз, продлевает жизнь больных.
Хирургическое лечение
Реваскуляризация миокарда эффективна при инфаркте и рецидивирующей ишемии, рефрактерной к медикаментозной терапии. Методом выбора является малоинвазивная эндоваскулярная ангиопластика, которая быстро восстанавливает кровоток в пораженном сосуде, имеет короткий восстановительный период. При невозможности ее проведения показано коронарное шунтирование.
Прогноз и профилактика
Своевременное начало интенсивной терапии значительно сокращает риск ранних и поздних осложнений, снижает показатель летальности. Прогноз определяется клиническим вариантом острого коронарного синдрома, наличием сопутствующих кардиологических болезней. У 70-80% больных перед выпиской устанавливают низкую или среднюю степень риска, что соответствует сохраненной функции левого желудочка.
Неспецифическая профилактика заболевания включает модификацию факторов риска — нормализацию массы тела, отказ от вредных привычек и жирной пищи. Медикаментозная профилактика повторных эпизодов ОКС включает длительную (более 12 месяцев) антитромбоцитарную терапию и прием липидоснижающих препаратов. Пациенты, перенесшие острый коронарный синдром, находятся на диспансерном учете кардиолога.
Источник
