Делеция длинного плеча хромосомы 18 синдромы
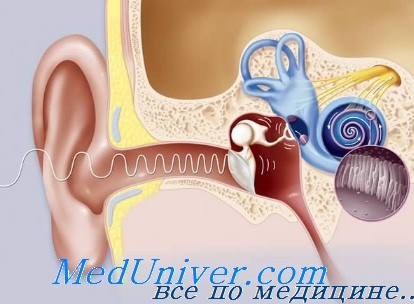
Синдром делеции 18-й хромосомы. Синдром кошачьих глаз – синдром Шмида—ФраккароСимптомокомплекс, обусловленный нехваткой генов, локализованных в длинном плече 18-й хромосомы, описан в 1964 г. I. De Grouchy и др. Частота в популяции не установлена. Синдром включает задержку психического развития, микроцефалию, низкорослость, снижение слуха, деформацию ушных раковин и наружных слуховых проходов, микрофтальмию, гипертелоризм, колобомы радужной оболочки, нистагм, ретракцию средней части лица, плоское переносье, «карпий рот», высокое или расщепленное нёбо, аномалии стопы и бедер, клинодактилию, пороки сердца, почек, половых органов. Синдром верифицируется кариологическим исследованием, при котором обнаруживают простую или замаскированную фрагментом делецию.
Синдром кольцевой 18-й хромосомыСимптомокомилекс, обусловленный частичной нехваткой генов, локализованных в теломерных участках 18-й хромосомы, описан в 1964 г. I. De Grouchy и др. Частота в популяции не установлена, однако известно, что она не зависит от возраста матерей. Дети рождаются с низкой массой, в дальнейшем резко отстают в физическом и психомоторном развитии. Характерна микроцефалия, описывают гипертелоризм, уплощенный затылок, эпикант, деформацию ушей и глухоту, косолапость, синдактилию, аномалии бедер. Синдром «кошачьих глаз» (синдром Шмида—Фраккаро)Симптомокомилекс обусловлен избытком гепов, локализованных, повидимому, в 22-й хромосоме. Частота его в популяции не установлена. При кариологическом исследовании, по крайней мере в части клеток, обнаруживают маленькую добавочную хромосому. – Также рекомендуем “Синдром делеции хромосом группы G. Синдромы дупликации-делеции с частичной трисомией 9-й хромосомы” Оглавление темы “Наследственные синдромы в неврологии”: |
Источник
Трисомия 18 и делеция длинного плеча хромосомы 18 с глухотой. Серповидноклеточная болезнь с глухотой
Дети с трисомией 18 умирают в течение первых нескольких недель жизни. Клиническая характеристика синдрома включает мышечную гипертонию, глубокую умственную отсталость, деформацию ушной раковины, микрогнатию, косолапость, заходящие друг на друга согнутые пальцы, короткую грудину и сердечную патологию.
Гистопатологическое исследование было произведено только в нескольких случаях (Kelemen, Kos et al., Sando ct al., Gacek, Miglets et al.). Были обнаружены различные аномалии среднего уха: неправильная форма слуховых косточек, неправильное направление лицевого нерва и chorda tympany. Аномалии внутреннего уха включали отсутствие полукружных каналов и гребешка, недоразвитие стержня, дефект улиткового отдела и уменьшение или отсутствие клеток спирального узла. Miglets с соавт. отметили полную атрезию костной части наружного слухового прохода, изменение мышцы, натягивающей барабанную перепонку, широкие и короткие утрикулярный и саккулярный ходы, а также широкий открытый водопровод улитки.
Wolf с сотр. не нашли значительных изменений во внутреннем ухе у 4 больных с трисомией 18.
Делеция длинного плеча хромосомы 18 с глухотой
Делеция длинного плеча хромосомы 18 сопровождается низким ростом, психической и моторной отсталостью, мышечной гипотонией, микроцефалией, гипоплазией средней части лица, гипертелоризмом, эпикантусом, веретенообразной формой пальцев, врожденным пороком сердца и увеличением числа спиралей на кожном рисунке пальцев.
Часто отмечается диспластичная ушная раковина с выступающими противозавитком и противокозелком. Выражены стеноз наружного слухового прохода и нарушения слуха. Kunze с соавт. при исследовании собственных 38 наблюдений кольцевой хромосомы 18 (18r) и 52 наблюдений делеции длинного плеча хромосомы 18 (18 q-) обнаружил более чем у 50% больных атрезию или стеноз наружного слухового прохода и примерно у 65% детей глухоту. Bergstrom с соавт. у 3 из 4 больных с синдромами 18 q- или 18 г описали проводящую глухоту, возникшую в связи с атрезией или гипоплазией наружного слухового прохода.
Политомография каменистой части пирамиды височной кости показала атрезию пластинок в области барабанной перепонки. Авторы рассмотрели патологию органа слуха, выявленную в других случаях: рудиментарная барабанная перепонка, отсутствие кольцевого желобка и синостозирование и/или деформация слуховых косточек.

Серповидноклеточная болезнь с глухотой
Серповидноклеточная болезнь является относительно частой гемоглобинопатией у негров. Установлено, что около 7—9% американских негров гетерозиготы по гемоглобину S. Таким образом, гомозиготы встречаются с частотой 1:400.
У гомозигот вначале может появиться только анемия с небольшой спленомегалией или даже с нормальной селезенкой. Но у них наблюдаются экстрамсдуллярное кроветворение и гиперплазия костного мозга. У больных могут возникнуть повторные приступы слабости, утомляемости, болей в животе, отсутствия аппетита с желтухой и бледностью. С возрастом у них могут развиться расширение сердца, изъязвления ног, асептический некроз бедренной кости и гематурия.
Morgenstein и Маnасе описали у больных с серповидноклеточной анемией двусторонний умеренный дефект слуха, выраженный резче на высоких частотах. Исследования височной кости показали дегенеративные изменения в кортиевом органе и сосудистой полоске, совместимые с ишемией. Костный мозг внутри слуховых косточек был гиперплазированным и эрозивным. Todd с соавт. обнаружили у 22% больных с серповидноклеточной болезнью на Ямайке, по сравнению с 4% в контроле, нейросенсорный дефект слуха, достигающий по крайней мерс уровня 25 дБ.
Мужчины и женщины были поражены одинаково часто. Нарушения слуха выявлялись постепенно, первично нарушалось восприятие высоких тонов. Авторы считают, что дефект слуха развился в результате тромбоэмболического процесса. Serjeant с соавт. исключили сужение внутреннего слухового прохода как этиологический фактор потери слуха при серповидноклеточной болезни.
– Также рекомендуем “Актуальность изучения зрительного восприятия устной речи. Чтение с губ”
Оглавление темы “Генетические болезни с глухотой”:
- Синдром Жервелла и Ланге-Нильсена. Кардиоаудиторный или сурдокардиальный синдром
- Ушная-зубная или отодентальная дисплазия. Липодистрофия лица, плеч и кисты костей с глухотой
- Семейная отогенная интоксикация стрептомицином. Синдром Тернера с глухотой
- ХХ-дисгенезия гонад с врожденной глухотой. Трисомия 21 и 13 с глухотой
- Трисомия 18 и делеция длинного плеча хромосомы 18 с глухотой. Серповидноклеточная болезнь с глухотой
- Актуальность изучения зрительного восприятия устной речи. Чтение с губ
- Возможности развития навыка чтения с губ у глухого. Изучение процесса чтения с губ
- Видимые признаки артикуляции русских фонем. Группы артикуляции букв
- Особенности артикуляции согласных. Артикуляция гласных букв
- Чтение с губ неударных гласных букв. Артикуляция губ при произношении
Источник
Õàðàêòåðèñòèêà ïðèçíàêîâ äåëåöèè äèñòàëüíîãî îòäåëà äëèííîãî ïëå÷à õðîìîñîìû 11. Îïèñàíèå çàáîëåâàíèé è íàðóøåíèé ðàçâèòèÿ, ñâÿçàííûõ ñ äåëåöèåé äëèííîãî ïëå÷à õðîìîñîìû 18. Àíàëèç ôåíîòèïè÷åñêèõ âàðèàíòîâ ïîðîêà ïðè óòðàòå êîðîòêîãî ïëå÷à õðîìîñîìû 18.
Ñòóäåíòû, àñïèðàíòû, ìîëîäûå ó÷åíûå, èñïîëüçóþùèå áàçó çíàíèé â ñâîåé ó÷åáå è ðàáîòå, áóäóò âàì î÷åíü áëàãîäàðíû.
Ðàçìåùåíî íà https://www.allbest.ru/
Äåëåöèÿ äèñòàëüíîãî îòäåëà äëèííîãî ïëå÷à õðîìîñîìû 11
Äåëåöèÿ äèñòàëüíîãî îòäåëà äëèííîãî ïëå÷à õðîìîñîìû 11 âïåðâûå îïèñàíà P. Jacobsen, ñïóñòÿ 2 ãîäà ñòàëè ãîâîðèòü î êëèíè÷åñêîì ñèíäðîìå, ñîïðîâîæäàþùåì òàêóþ äåëåöèþ.
×àùå âñåãî ïîëîìêè ïðîèñõîäÿò â çîíå llq23, â îòäåëüíûõ ñëó÷àÿõ òî÷êè ïîëîìîê ëîêàëèçîâàíû ëèáî íåñêîëüêî ïðîêñèìàëüíåå, ëèáî áîëåå äèñòàëüíî. Èíòåðñòèöèàëüíûå äåëåöèè äëèííîãî ïëå÷à õðîìîñîìû 11 âåäóò ê ñîâåðøåííî èíîé êëèíè÷åñêîé êàðòèíå, ïîýòîìó ïîä ñèíäðîìîì äåëåíèè llq ïîíèìàþò êîìïëåêñ àíîìàëèé, ñâÿçàííûõ ñ òåðìèíàëüíîé äåëåöèåé.
Ïîäàâëÿþùåå áîëüøèíñòâî èç ïðèìåðíî 50 îïèñàííûõ â ëèòåðàòóðå íàáëþäåíèé – ñëåäñòâèå ñïîðàäè÷åñêèõ ìóòàöèé, õîòÿ â ðÿäå ñëó÷àåâ ó îäíîãî èç ðîäèòåëåé îáíàðóæåíû òå èëè èíûå òðàíñëîêàöèé ñ ó÷àñòèåì õðîìîñîìû 11. Èçâåñòíû è íàáëþäåíèÿ äåëåöèè â ðåçóëüòàòå ñïîðàäè÷åñêèõ òðàíñëîêàöèé. äåëåöèÿ õðîìîñîìà ïîðîê
Îáà ïîëà ïîðàæàþòñÿ ñ îäèíàêîâîé ÷àñòîòîé. Õîòÿ â ñðåäíåì ìàññà íîâîðîæäåííûõ ñ llq – ìåíüøå íîðìû, ìèíèìóì â 40% îíè ðîæäàþòñÿ ñ ìàññîé âûøå 3000 ã.
Ïîñòîÿííûì ïðèçíàêîì ÿâëÿåòñÿ çàäåðæêà ïñèõîìîòîðíîãî ðàçâèòèÿ, íî ôèçè÷åñêîå ðàçâèòèå ó áîëüøèíñòâà áîëüíûõ íîðìàëüíîå: ñóùåñòâåííàÿ çàäåðæêà ìàññû è ðîñòà îòìå÷åíà ëèøü ó òðåòè ïàöèåíòîâ.  îòëè÷èå îò áîëüøèíñòâà õðîìîñîìíûõ ñèíäðîìîâ äëÿ llq – íå õàðàêòåðíà ìèêðîöåôàëèÿ, îòìå÷åííàÿ ëèøü ó 2 áîëüíûõ. Ñàìûé ïîñòîÿííûé è ñàìûé òèïè÷íûé ïðèçíàê – òðèãîíîöåôàëèÿ, îòìå÷àåìàÿ ó 80% áîëüíûõ. Ñòåïåíü âûðàæåííîñòè òðèãîíîöåôàëèè âàðüèðóåò â øèðîêèõ ïðåäåëàõ. Òàêèå ÷åðåïíî-ëèöåâûå äèçìîðôèé, êàê ïëîñêàÿ øèðîêàÿ ñïèíêà íîñà, «ðîò êàðïà», ãèïåðòåëîðèçì, íèçêî ðàñïîëîæåííûå óøíûå ðàêîâèíû, ìèêðîðåòðîãíàòèÿ, âûñîêîå íåáî, âñòðå÷àþòñÿ â 70-80% íàáëþäåíèé. Ó 40% áîëüíûõ îòìå÷åí ìîíãîëîèäíûé ðàçðåç ãëàçíûõ ùåëåé, ó òàêîãî æå ÷èñëà – àíòèìîíãîëîèäíûé. Äîâîëüíî ÷àñòî âñòðå÷àþòñÿ ïîðîêè ãëàçíîãî ÿáëîêà: ó 20% áîëüíûõ îòìå÷åíû êîëîáîìû ðàäóæêè, åñòü ðÿä íàáëþäåíèé ìèêðîôòàëüìà, ãëàóêîìû, ïîìóòíåíèÿ ðîãîâèöû.
Äëÿ äåëåöèè llq- õàðàêòåðíû àíîìàëèè ñòðîåíèÿ ïàëüöåâ – áðàõèäàêòèëèÿ, îñîáåííî óêîðî÷åíèå äèñòàëüíûõ ôàëàíã V ïàëüöåâ (âïëîòü äî îòñóòñòâèÿ äèñòàëüíûõ ôàëàíã), êëèíî-äàêòèëèÿ, íåîáû÷íîå ïîëîæåíèå ïàëüöåâ, êîãäà II-IV ïàëüöû ïåðåêðûòû I è V.
Ó 53% áîëüíûõ îòìå÷àþòñÿ âðîæäåííûå ïîðîêè ñåðäöà: îáû÷íî â âèäå ñî÷åòàíèÿ äåôåêòà ìåææåëóäî÷êîâîé ïåðåãîðîäêè ñ äðóãèìè àíîìàëèÿìè. Ïîðîêè äðóãèõ âíóòðåííèõ îðãàíîâ íåõàðàêòåðíû, õîòÿ îòìå÷åíû êîëüöåâèäíàÿ ïîäæåëóäî÷íàÿ æåëåçà, ïèëîðîñòåíîç, êèñòû ïî÷åê, óäâîåíèå ëîõàíîê è ìî÷åòî÷íèêîâ è äð.
Èññëåäîâàíèÿìè ïîêàçàíî, ÷òî «êðèòè÷åñêèì» ñåãìåíòîì, îòâåòñòâåííûì çà âîçíèêíîâåíèå ñèíäðîìà, ÿâëÿåòñÿ ñóá-äèñê llq24.1. Óòðàòà ýòîãî ó÷àñòêà âûçûâàåò òèïè÷íóþ êëèíè÷åñêóþ êàðòèíó çàáîëåâàíèÿ.
Äåëåöèÿ äëèííîãî ïëå÷à õðîìîñîìû 18
Äëÿ áîëüíûõ ñ äåëåöèåé äëèííûõ ïëå÷ I8q- õàðàêòåðíû ìèêðîöåôàëèÿ, ãèïåðòåëîðèçì, äèçìîðôèÿ ëèöà (óïëîùåíèå ñïèíêè ìàëåíüêîãî ïî ðàçìåðàì íîñà, ãëóáîêî ïîñàæåííûå ãëàçíûå ÿáëîêè, òîíêàÿ âåðõíÿÿ ãóáà, ðîò «êàðïà» ñ îïóùåííûìè âíèç óãëàìè), ïëîñêèé ïðîôèëü, âûñîêîå íåáî (èëè ðàñùåëèíà), ñóæåíèå (èëè äàæå àòðåçèÿ) íàðóæíûõ ñëóõîâûõ ïðîõîäîâ, àíîìàëèè ãëàç (ïðåæäå âñåãî àòðîôèÿ çðèòåëüíûõ íåðâîâ). Óøè îáû÷íî óäëèíåíû â ïåðåäíåçàäíåì íàïðàâëåíèè, çàâèòîê íåïðàâèëüíîé ôîðìû, ãëóáîêàÿ ëàäüåâèäíàÿ ÿìêà, âûñòóïàþùèå ïðîòèâîçàâèòîê è ïðîòèâîêîçåëîê (òàê íàçûâàåìûå «óøè ñàòèðà»). Òèïè÷íàÿ îñîáåííîñòü äåðìàòîãëèôèêè – áîëüøîå ÷èñëî çàâèòêîâ íà ïàëüöàõ ðóê.
Äëÿ ìàëü÷èêîâ õàðàêòåðíà ãèïîïëàçèÿ ïîëîâîãî ÷ëåíà è ìîøîíêè, êðèïòîðõèçì, ãèïîñïàäèÿ.
Ïðèìåðíî ó òðåòè äåòåé èìåþòñÿ âðîæäåííûå ïîðîêè ñåðäöà, ÷àùå âñåãî íå ñîïðîâîæäàþùèåñÿ ñåðäå÷íîé íåäîñòàòî÷íîñòüþ.
Ïîðîêè ÖÍÑ, æåëóäî÷íî-êèøå÷íîãî òðàêòà è ïî÷åê – íåñïåöèôè÷íû, õîòÿ è îïèñàíû íåîäíîêðàòíî.
Ïðîäîëæèòåëüíîñòü æèçèè áîëüíûõ ñ 18q- îïðåäåëÿåòñÿ â îñíîâíîì íàëè÷èåì ïîðîêîâ âíóòðåííèõ îðãàíîâ è, õîòÿ â ðàííåì âîçðàñòå ýòè äåòè îáû÷íî èå ïîãèáàþò, îáùèé ïðîãíîç õóæå, ÷åì äëÿ 18ð-. Ñàìîìó ñòàðøåìó èç îïèñàííûõ áîëüíûõ 42 ãîäà.  êà÷åñòâå ïðèìåðà ïðèâîäèì îäíó èç íàáëþäàâøèõñÿ íàìè ñåìåé ñ ýòèì ñèíäðîìîì.
Ãåíåòè÷åñêèé ïðîãíîç ïðè ëþáîé ôîðìå ÷àñòè÷íîé ìîíîñîìèè 18 îïðåäåëÿåòñÿ öèòîãåíåòè÷åñêîé ñèòóàöèåé â ñåìüå.
Äåëåöèÿ êîðîòêîãî ïëå÷à õðîìîñîìû 18
 íàñòîÿùåå âðåìÿ äëÿ ôåíîòèïè÷åñêîãî àíàëèçà äîñòóïíî áîëåå 110 îïèñàíèé áîëüíûõ ñ äåëåöèåé 18ð-. Âïðî÷åì, êîãäà ÷èñëî íàáëþäåíèé òîãî èëè èíîãî ñèíäðîìà ïðåâûøàåò 70-80, ïðåèìóùåñòâåííî ïóáëèêóþò ñëó÷àè, íåîáû÷íûå â êëèíè÷åñêîì èëè öèòîãåíåòí÷åñêîì ïëàíå. Êàæäàÿ êðóïíàÿ ãåíåòè÷åñêàÿ ëàáîðàòîðèÿ ðàñïîëàãàåò ñîáñòâåííûìè íàáëþäåíèÿìè ýòîãî ñèíäðîìà. Ñóùåñòâóåò 2 îñíîâíûõ ôåíîòèïè÷åñêèõ âàðèàíòà ñèíäðîìà 18ð-. Ïðè ïåðâîì (áîëåå ðåäêîì) äîìèíèðóþò ãðóáûå ïîðîêè àðèíýíöåôàëí÷åñêîé ñåðèè: îò öèêë îïèè äî àðèíýíöåôàëèï. Íåñêîëüêî ñõîäíûõ ïîðîêîâ îòìå÷åíî è ïðè 18 ã. Ìîðôîëîãè÷åñêèå èçìåíåíèÿ ìîçãà â ýòèõ ñëó÷àÿõ ñîîòâåòñòâóþò èçìåíåíèÿì ïðè ïîðîêàõ àðèíýíöåôàëí÷åñêîé ñåðèè.
Âûñêàçàííî ïðåäïîëîæåíèå, ÷òî ïîðîêè àðèíýíöåôàëí÷åñêîé ñåðèè ïðè óòðàòå êîðîòêîãî ïëå÷à õðîìîñîìû 18 âûçâàíû ãåìèçèãîòèçàöèåé ðåöåññèâíîãî ãåíà, íàõîäÿùåãîñÿ ïà èíòàêòíîì ãîìîëîãå. Îäíàêî ÷èñëî ïîðîêîâ ýòîé ãðóïïû ñëèøêîì âåëèêî, ÷òîáû â ñâåòå ñîâðåìåííûõ äàííûõ î ãåíåòèêå ïîðîêîâ àðèíýíöåôàëè÷åñêîé ñåðèè ñ÷èòàòü ýòó ãèïîòåçó ñïðàâåäëèâîé. Ðàçóìååòñÿ, ñèíäðîì 18ð- ÷àùå ðàñïîçíàåòñÿ èìåííî ó äåòåé ñ ïîðîêàìè òàêîãî òèïà, è òàêèå ñëó÷àè ÷àùå ïóáëèêóþòñÿ. Ïðàêòè÷åñêè âñå äåòè ñ ïîðîêàìè àðèíýíöåôàëí÷åñêîé ñåðèè ïîãèáàþò â ïåðâûå ìåñÿöû æèçíè.
Ïðè îòñóòñòâèè ïîðîêîâ ìîçãà ñèíäðîì 18ð- ïðîÿâëÿåòñÿ çàäåðæêîé ïñèõè÷åñêîãî ðàçâèòèÿ, èèçêîðîñëîñòûî, ïòîçîì, ýïèêàíòîì, ìèêðîðåòðîãåíèåé, êîðîòêîé ñêëàä÷àòîé øååé è êëèêî äàêòèëèåé. Ïîðîêè âíóòðåííèõ îðãàíîâ ìàëîõàðàêòåðíû, õîòÿ ïî÷òè ó êàæäîãî øåñòîãî ðåáåíêà îáíàðóæèâàåòñÿ ïîðîê ñåðäöà. Ïîðîêè äðóãèõ îðãàíîâ âñòðå÷àþòñÿ ðåäêî.
Ñðàâíèòåëüíî ðåäêèé, íî íåîáû÷íûé ïðèçíàê ñèíäðîìà- àëîïåöèÿ – îòìå÷åíà ó 4 áîëüíûõ ñ 18ð- í ó îäíîãî ñ 18ã.  òðåõ ñëó÷àÿõ àëîïåöèÿ áûëà òîòàëüíîé. Î÷åâèäíî, ãåí àëîïåöèè ëîêàëèçîâàí íà êîðîòêîì ïëå÷å õðîìîñîìû 18, è ãåìèçèãîòèçàöèÿ ðåöåññèâíîãî ãåíà ñïîñîáñòâóåò ïðîÿâëåíèþ ïðèçíàêà.
 îòñóòñòâèå àëîïåöèè è ïîðîêîâ àðèíýíöåôàëí÷åñêîé ñåðèè êëèíè÷åñêè ñèíäðîì 18ð- äëÿ äèàãíîñòèêè òðóäåí.
Âèòàëüíûé ïðîãíîç îïðåäåëÿåòñÿ ïðàêòè÷åñêè íàëè÷èåì ïîðîêîâ àðèèýèöåôàëè÷åñêîé ñåðèè. Äåòè ñ òàêèìè ïîðîêàìè ïîãèáàþò â ïåðâûå äíè èëè ìåñÿöû æèçíè. Åñëè ãðóáûõ ïîðîêîâ ìîçãà èåò, ïðîäîëæèòåëüíîñòü æèçíè îáû÷íàÿ: èçâåñòíû áîëüíûå ñ äåëåöèåé 18ð- â âîçðàñòå ñâûøå 60 ëåò.
Ðàçìåùåíî íà Allbest.ru
…
Источник
оперативного лечение крипторхизма; планируется предварительное проведение полисомнографии с целью выявления ночных апноэ, свидетельствующих о риске развития внезапной смерти; тщательный мониторинг функции дыхательной системы во время операции и в раннем послеоперационном периоде;
4) решение вопроса о проведении повторного курса соматотропина в дошкольном и школьном возрасте с целью обеспечения адекватной окончательной длины тела.
Таким образом, ранняя, в 1-й фазе развития клини-
©
Хромосомная патология занимает одно из ведущих мест в структуре причин формирования множественных пороков развития, неврологических расстройств, злокачественных новообразований, а также смертности в раннем периоде жизни. По данным цитогенетических исследований, распространенность хромосомного дисбаланса в материале ранних спонтанных абортусов достигает 70% [1]. В популяции новорожденных у 0,6—1,0% ежегодно диагностируется хромосомная патология, причиной которой нередко являются структурные перестройки в результате разрывов глицерофосфатных связей в одной или нескольких хромосомах [2].
Синдром терминальной делеции длинного плеча хромосомы 18, впервые описанный в 1964 г. de Grouchy, обусловлен подобными структурными поломками. Клинический фенотип, ассоциированный с хромосомной аномалией 18q-, описан Lejeune в 1966 г. [3]. Он характеризуется широким варьированием диагностических признаков в зависимости от генного состава утраченного фрагмента хромосомы [4]. Возможная совокупность симптомов включает множественные стигмы дизэмбриогене-за, краниофациальный дисморфизм, задержку физического развития, аномалии зрительного анализатора, половых органов, а также разнообразную психоневрологическую патологию, эпилептоидные проявления и глубокую умственную отсталость [3, 5—9]. В связи с недостатком аутопсийного материала характеристика поражения ЦНС при синдроме de Grouchy длительное время базировалась на клинических данных. Впоследствии ряд авторов продемонстрировали результаты магнитно-резонансной томографии головного мозга при обследовании пациентов с синдромом 18q-. Наиболее специфичными чертами для данной патологии оказались признаки де-
ческой картины диагностика СПВ весьма актуальна. Возможности ее возрастают при использовании балльной шкалы M. Gunay-Aygun, S. Schwartz, S. Heeger et al. Ранняя терапия соматотропином позволяет существенно корректировать фенотип больных СПВ, повторный курс на последующих этапах развития обеспечивает адекватные окончательные размеры тела. Диагноз СПВ требует абсолютно специфической верификации, которая осуществляется генетическими методами исследования образца крови.
миелинизации и дефектного синтеза основного миели-нового белка белого вещества ЦНС, а также недифферен-цированность границы между белым и серым веществом паренхимы головного мозга [5, 10—11]. В настоящее время не установлен ген, делеция которого вызывает нарушения миелинизации, однако обсуждается роль расположенного в дистальном участке 18q- и экспрессирую-щегося в олигодендроцитах ЦНС гена-кандидата MBP (myelin basic protein) [3].
Настоящая публикация иллюстрирует клинический случай синдрома de Grouchy у ребенка 2 месяцев.
Пациент К. госпитализирован в отделение клинической иммунологии и аллергологии областной детской больницы г. Томск с диагнозом: перинатальное пораже-
Рис. 1. Родословная семьи пробанда.
^ лицо можского пола, £ лицо женского пола, самопроизвольный аборт, мертворождение; стрелкой обозначен пробанд.
ЛИТЕРАТУРА
См. опИпе-версию журнала https://www.pediatriajournal.ru ц 6/2006, приложение ц 16. Коллектив авторов, 2006
Е.М. Камалтьтова1, О.А. Салюкова2, О.С. Федорова1, С.Л. Вовк2, Е.Л. Тимошина1, Л.М. Огородова1
СЛУЧАЙ ДЕЛЕЦИИ ДЛИННОГО ПЛЕЧА ХРОМОСОМЫ 18
У РЕБЕНКА 2 МЕСЯЦЕВ
1 ГОУ ВПО СибГМУ Росздрава, 2 ГУ НИИ медицинской генетики ТНЦ СО РАМН, г. Томск, РФ
Е.М. Камалтынова, О.А. Садюкова, О.С. Федорова и др.
121
ние ЦНС смешанного генеза, гипертензионно-гидроце-фальный синдром, бульбарный синдром, тетрапарез, кровоизлияние в правый боковой желудочек; множественные врожденные пороки развития.
Из анамнеза: ребенок родился от V беременности, II родов. Родители мальчика фенотипически здоровы: матери 28 лет, отцу 25 лет. I беременность от первого брака матери завершилась рождением здорового ребенка, две последующие от настоящего брака — самопроизвольными абортами, III — рождением пробанда, IV — замершая беременность. Ребенок от первого брака отца пробанда умер в периоде новорожденности в связи с множественными врожденными пороками развития (рис. 1). Данная беременность протекала на фоне токсикоза I и II половины. Роды срочные путем кесарева сечения, осложненные преждевременным излитием околоплодных вод и вставлением головки плода. Масса тела при рождении 3500 г, длина 53 см. Ребенок родился в асфиксии (оценка по шкале Апгар 4 балла на 1-й минуте, 7 баллов на 5-й минуте), в 1-е сутки переведен на зондовое питание и ИВЛ. Больной находился в отделении патологии новорожденных центральной районной больницы с диагнозом: респираторный дистресс-синдром новорожденного, отечно-геморрагический синдром. Нейросонографи-ческое обследование выявило признаки гидроцефалии, кровоизлияние в правый боковой желудочек. В связи с прогрессирующим ухудшением состояния и неэффективностью проводимой терапии пациент был направлен для дальнейшего обследования и лечения в областную детскую больницу.
Возраст пациента на момент госпитализации 2 месяца. При поступлении в стационар состояние пациента оценивалось как тяжелое преимущественно за счет неврологической симптоматики. Обращало на себя внимание вынужденное положение ребенка: лежа на боку с запрокинутой головой. Больной отставал в физическом развитии, масса тела 3250 г, длина 53 см. Выявлены множественные стигмы дисэмбриогенеза: микроцефалия, гипоплазия средней части лица, рот «карпа», готическое небо, деформированные ушные раковины, сужение наружных слуховых каналов, страбизм, пупочная грыжа и гипоспадия типа хорды. Размеры большого родничка 5×7 см. Наблюдались бульбарные нарушения, вертикальный нистагм, асимметрия глазных щелей, сходящееся косоглазие, тремор конечностей при беспокойстве, двусторонняя пирамидная недостаточность и асимметричная мышечная дистония. Сухожильные рефлексы переменные, с рук — оживлены, периодически возникали тонические судороги. Отмечалась тенденция к тахикардии и тахипноэ, рецидивировали немотивированные эпизоды фебрилитета, лихорадка не купировалась приемом нестероидных противовоспалительных средств и ликвидировалась самостоятельно.
Общий анализ крови: Hb 140 г/л, эр. 4,2-1012/л, л. 12,4-109/л, п. 5%, с. 40%, баз. 1%, э. 3%, лимф. 12%, мон. 10%, СОЭ 2 мм/ч.
Общий анализ мочи без патологических особенностей.
Биохимический анализ крови: общий белок 54,7 г/л, глюкоза 3,9 ммоль/л, тимоловая проба 2,2 ЕД, общий билирубин 64 мкмоль/л, прямой билирубин 47,3 мкмоль/л, АЛТ 51,3 МЕ, АСТ 41,8 МЕ, кальций 2,3 ммоль/л, фосфор 1,65 ммоль/л, натрий 142 ммоль/л, калий 3,4 ммоль/л.
Эхографическое исследование структур головного мозга выявило поликистоз в лобно-височной области, тромб в правом боковом желудочке и аплазию мозолис-
*! fj , » v-
tl n 11 St h
~t f k’ ! • у , | J – f
ii г» ft « * * SI – tt i»
* * i * ■ * ( ¡j {
Рис. 2. Кариотип пробанда: 46, XYgh+, del (18) (21).
того тела. При осмотре глазного дна наблюдалась ангио-патия сосудов сетчатки по гипертензионному типу.
За время нахождения в стационаре ребенку назначались антиконвульсанты, дегидратационные, метаболические, антибактериальные препараты, а также симптоматическая гипотермическая терапия.
Несмотря на проведенное лечение, тяжесть состояния пациента сохранялась. Гипертермический синдром приобрел стойкий характер, присоединился геморрагический синдром — желудочно-кишечное кровотечение. С диагнозом ДВС-синдром ребенок был переведен в реанимационное отделение детской хирургической больницы ц 4. На фоне проведенной интенсивной терапии отмечалась слабая положительная динамика и по достижении стабилизации гемостаза и появления сосательного и глотательного рефлексов пациент вновь госпитализирован в областную детскую больницу. Однако судорожный синдром и признаки грубой задержки психомоторного развития сохранялись.
В связи с клинической картиной, представленной множественными врожденными пороками развития, а также отягощенным семейным анамнезом, проведено медико-генетическое консультирование с последующим цитогенетическим обследованием пробанда и его родителей для исключения хромосомной патологии. После культивирования клеток крови в течение 72 ч, фиксации, приготовления препаратов и окрашивания по G-ме-тоду выполнен цитогенетический анализ. В кариоти-пе больного обнаружена делеция длинного плеча хромосомы 18 и увеличенная Y-хромосома, что указывает на наличие транслокации между хромосомами 18 и Y. В последующем проведена дополнительная C-окраска, которая позволила выявить увеличение гетерохроматинового блока на половой хромосоме, фенотипически не проявлявшегося, и подтвердила наличие делеции в хромосоме 18 (рис. 2).
В кариотипе отца пробанда была обнаружена пери-центрическая инверсия хромосомы 18 и увеличение гетерохроматинового блока на хромосоме Y. При постановке данного цитогенетического диагноза также проводилось G- и C-окрашивание препаратов (рис. 3). Исследование кариотипа матери ребенка патологических особенностей не выявило.
По достижении стабилизации соматического и неврологического статуса пациент был выписан из стационара для дальнейшего амбулаторного наблюдения и лечения. Родителям ребенка было рекомендовано в случае наступления последующей беременности медико-генети-
В возрасте 3 месяцев больной умер, причиной смерти явились некупируемые судорожный и гипертермический синдромы.
Таким образом, представленный клинический случай демонстрирует раннее и тяжелое течение синдрома 18q- у пациента с отягощенным наследственным анамнезом, повлекшее летальный исход в раннем возрасте. Своевременное цитогенетическое обследование позволило правильно поставить диагноз, выявить хромосомную перестройку у отца пробанда и оценить риск повторных случаев патологии у потомства.
Следует отметить недостаточную освещенность данной проблемы и отсутствие публикаций с подобными клиническими примерами в российской педиатрической периодике, что указывает на низкую выявляемость синдрома 18q- в раннем возрасте. Сочетание симптомов поражения ЦНС с множественными стигмами дизэмб-риогенеза является показанием для проведения цитоге-нетического обследования и медико-генетического консультирования.
ЛИТЕРАТУРА
См. опИпе-версию журнала https://www.pediatriajournal.ru ц 6/2006, приложение ц 17. © Коллектив авторов, 2006
Н.М. Судакова, В.Ф. Гаплевская, Н.И. Гревцева, Р.Б. Трунова СИНДРОМ АЙЕРСА У РЕБЕНКА ПЕРВОГО ГОДА ЖИЗНИ
Кафедра акушерства, гинекологии и педиатрии медицинского факультета Белгородского государственного университета, детская городская больница, г. Белгород, РФ
Рис. 3. Кариотип отца пробанда: 46, XYgh+, inv (18) (p11:q21).
ческое консультирование с обязательной цитогенетичес-кой пренатальной диагностикой кариотипа плода.
Синдром Айерса (первичная легочная гипертензия — ПЛГ, идиопатическая гипертрофия правого желудочка сердца, болезнь Ayerza—Arrilaga) — редкое заболевание, характеризующееся совокупностью клинических признаков склероза системы легочной артерии (ЛА) (резкий диффузный цианоз, полицитемия, одышка и высокая легочная гипертензия со значительной гипертрофией правой половины сердца) [1]. Впервые синдром описан в 1901 г. аргентинскими терапевтами Ayerza Abel и F.C. Arrilaga [2].
Заболевание встречается крайне редко — примерно у 1—2 на 1 млн популяции [3, 4]. Оно может начаться в любом возрасте, в том числе и в грудном. Этиология заболевания до настоящего времени неизвестна. Существующие предположения говорят о том, что ПЛГ на сегодняшний день не является болезнью с единой этиологией [5]. Среди возможных причин развития выделяют ВИЧ-инфекцию, портальную гипертензию, коллагенозы, врожденные системно-легочные шунты, заболевания щитовидной железы, врожденные пороки сердца, сопровождающиеся увеличением легочного кровотока, лекарственные препараты (амфетамины, L-триптофан и др.) [5, 6]. В последние годы обсуждается роль генетических факторов. Примерно в 7% случаев ПЛГ — это семейное заболевание, которое наследуется по аутосомно-доминантному типу
с неполной пенетрантностью. Риск развития семейной патологии выше у лиц женского пола [7].
Патогенез заболевания также недостаточно изучен. Известно два типа ПЛГ. Первый тип, встречающийся в большинстве случаев, обусловлен резкой гипертрофией, фиброзом, фиброэластозом мышечного слоя легочных артериол. При втором типе, более редком, отмечается рыхлый базофильный клеточный фиброз, приводящий к сужению и облитерации легочных венул [8].
Ранние стадии заболевания, как правило, не распознаются. Основной симптом — одышка. В течение долгого времени она остается единственным проявлением заболевания, поэтому зачастую диагноз ставят поздно, когда появляется выраженное поражение сосудов легких — тогда присоединяются цианоз, полицитемия, расширение, правосторонняя гипертрофия и недостаточность правого сердца (синдром «легочного» сердца) с повышенным венозным давлением, при аускультации акцентуация и усиление II тона над ЛА, хлопающий I тон; на ЭКГ — правосторонний тип, правосторонняя гипертрофия сердца вследствие перегрузки, нарушение внутрижелудоч-ковой проводимости, на обзорной рентгенограмме — усиление легочного рисунка в прикорневой зоне, выбухание дуги ЛА [5, 6, 8].
Е. М. Камалтынова, О. А. Салюкова, О. С. Федорова, С. Л. Вовк, Е. Л. Тимошина, Л. М. Огородова
ЛИТЕРАТУРА
1. Медицинская генетика / Под ред. Н.П. Бочкова. – М., Мастерство, 2003. – 192 с.
2. Назаренко С.А., Яковлева Ю.С. Цитогенетика человека и хромосомные болезни. -Томск, 2001. – 84 с.
3. Loevner L.A., Shapiro R.M., Grossman R.I. et al. // Am. J. Neuroradiol. – 1996. – Vol. 17, № 10. – P. 1843 – 1848.
4. Brkanac Z., Cody J.D., Leach R.J. et al. // Am. J. Hum. Genet. – 1998. – Vol. 62, № 6. -P.1500 – 1506.
5. Linnankvi T.T., Autty Т.Н., Pihko S.H. et al. // J. Magn. Reson. Imaging. – 2003. -Vol. 18, № 4. – P. 414 – 419.
6. Verotti A., Trotta D., Salladini C. et al. // Childs Nerv. Syst. – 2004. – Vol. 20, № 5. -P. 362
– 365.
7. Grosso S., Pussy L., Di Bartolo R.M. et al. // Am. J. Med. Genet. – 2005. – Vol. 134, № 1. -P. 88 – 94.
8. Vogel H., Urich H., Horoupian D.S. et al. // Dev. Med. Child Neurol. – 1990. – Vol. 32, № 8.
– P. 732 – 737.
9. Nuijten I., Admiraal R., Buggenhout G. et al. // Otol. Neurotol. – 2003. – Vol. 24, № 6. -P. 900 – 906.
10. Becker L.E. // Am. J. Neuroradiol. – 1998. – Vol. 19, № 2. – P. 399.
11. Hausler M., Anhuf D., Schuler H. et al. // Neurroradiology. – 2005. – Vol. 47, № 1. -P. 83 – 86.
Источник

