Диссертации на тему синдром диабетической стопы
 Для цитирования. Кисляков В.А., Оболенский В.Н., Юсупов И.А. Синдром диабетической стопы: комплексный подход к лечению // РМЖ. 2015. No 12. С. 768–770.
Для цитирования. Кисляков В.А., Оболенский В.Н., Юсупов И.А. Синдром диабетической стопы: комплексный подход к лечению // РМЖ. 2015. No 12. С. 768–770.
Распространенность и экономические аспекты
В XXI в. сахарный диабет (СД) стал ведущим неинфекционным заболеванием. Каждые 10 с в мире становится на 2 больных СД больше – это 7 млн в год. По мнению экспертов Всемирной организации здравоохранения, СД занимает 1-е место среди заболеваний, приводящих к инвалидности, и 3-е – по смертности [1–4].
Согласно исследованиям Эндокринологического научного центра (ЭНЦ), в России распространенность СД достигает 10–12 млн человек (7–8% населения страны). Наиболее высокая распространенность СД среди взрослого населения крупных городов. При этом соотношение мужчин и женщин – 1:3. В половине случаев СД 2-го типа выявляется на 5–7-м году от начала заболевания, и у 20–30% выявляются специфические осложнения: катаракта, ретинопатия, нефропатия, нейропатия, синдром диабетической стопы (СДС), ишемическая болезнь сердца, артериальная гипертония и др. [5–8].
СДС приводит к гнойно-некротическим поражениям стоп с последующей потерей нижних конечностей – к самой высокой инвалидизации. Окончательные цифры распространенности СДС в настоящее время неизвестны. Тем не менее установлено, что у 15% больных СД развиваются патологические изменения в стопах или голеностопном суставе [9–13].
В последние годы широко обсуждаются не только клинические, но и экономические, социальные аспекты профилактики и лечения СДС, методы клинико-экономического анализа и, прежде всего, учет всех затрат, связанных с лечением СДС [1, 14].
На 18-м конгрессе Международной федерации диабета (МФД) были представлены, в частности, данные о распространенности язвенных дефектов при СДС в странах Балканского региона – 7,5%. Диагноз СД впервые ставится во время хирургического вмешательства у 15–19% больных, подвергающихся ампутации. Специалисты МФД считают, что вероятная частота ампутаций при СД составляет 5–24 на 100 000 населения в год, или 6–8 на 1000 больных в год, а в эпидемиологически неблагоприятных регионах достигает 24 на 1000 больных в год. В России, согласно данным государственного регистра, эти показатели колеблются от 0,76 до 18,2 и в среднем составляют 6,4 случая на 1000 больных [3, 4, 11, 15].
Расходы на лечение СДС в развитых странах составляют около 12–15% от всех затрат на лечение СД, в развивающихся странах они могут составлять до 40% от общего объема финансовых ресурсов, выделяемых на СД. Подсчитано, что на проведение одной ампутации в зарубежных странах тратится более 10 000 долл. Общие затраты на лечение СДС в среднем составляют 13 179 долл. и меняются в зависимости от степени тяжести по классификации Wagner в пределах от 1892 долл. при I степени до 27 721 долл. при IV–V степени тяжести. Лечение СДС на фоне хронической артериальной недостаточности нижних конечностей обходится в 4,5 раза дороже, чем при сохранном периферическом кровотоке. Ежегодная стоимость лечения язвенных поражений стоп при СДС в США составляет 5 млрд долл. прямых медицинских затрат и 400 млн долл. косвенных медицинских затрат. Кроме того, в США зафиксировали, что 77% людей старше 75 лет после ампутации не способны вернуться в собственный дом и им нужна дополнительная помощь и поддержка социальных групп [8, 16–18].
Анализ работы отделения диабетической стопы ЭНЦ показал, что при своевременно начатой адекватной терапии СДС понижается риск хирургических вмешательств и тяжелых осложнений: у 98% больных с нейропатической инфицированной формой СДС можно избежать хирургического вмешательства; у 60% с нейроишемической формой – проведения ампутаций на уровне голени и бедра; у 25% с критической ишемией – предотвратить высокие ампутации на уровне бедра; на 50% уменьшить частоту образования язв стоп в группе высокого риска [4, 5, 13].
Летальность среди больных СД, перенесших высокую ампутацию конечности по поводу гангрены, в течение последующих 5 лет достигает 68%, в ближайшие 3 нед. – 22%, в течение года – 11–41%, через 3 года – 20–50%, через 5 лет – от 39–68%. Частота ипсилатеральных ампутаций через год после первой ампутации – до 24%, через 2 года – 30%, через 5 лет – 49% и контралатеральных ампутаций через год после первой ампутации – до 12%, через 2 года – 23%, через 5 лет – 28-51%. Рецидивы язв на стопах через 1, 3, 5 лет составили 44, 61, 70% соответственно. Рецидивирующие деструктивные поражения ухудшают проблемы лечения, реабилитации, социальной помощи, увеличивая экономические затраты [19–23].
Если распространенность СД, а соответственно и СДС будет увеличиваться с той же скоростью, что и сейчас, то к 2025 г. экономический ущерб составит от 213 до 396 млрд долл. в год. 75% прироста заболевания придутся на развивающиеся страны. По данным немецких исследователей, общая стоимость лечения больных СД в Германии составляет приблизительно 5 млрд. евро, а средняя стоимость лечения 1 пациента – 5000 евро в год. Ежегодные общие затраты в России на лечение нейроишемической формы СДС составляют 56,2 млн долл., при этом затраты на ампутации достигают 14,4 млн долл. [2, 5, 17].
По оценке главного экономиста Morgan Stanley Эльги Бартш, сочетание двух факторов – СД и ожирения – снизит среднегодовые темпы роста валового внутреннего продукта (ВВП) в странах Организации экономического сотрудничества и развития (ОЭСР) в 2015–2035 гг. с 2,3 до 1,8%, в странах БРИКС (Бразилия, Россия, Индия, Китай, Южно-Африканская Республика) – с 4,5 до 4,2%. Согласно прогнозам ОЭСР, среднегодовые темпы роста ВВП России составят 2,8%. При сохранении нынешнего уровня потребления сахара гражданами страны этот показатель снизится до 2%. Согласно результатам исследования, проведенного фармацевтической компанией «Ново Нордиск», «Инвестиции в лечение сахарного диабета в России», ежегодные прямые затраты, связанные с СД в России, составляют 12,5 млрд долл. США. При этом 42% объема этих средств расходуется на лечение осложнений, которые выявляются у 40–50% людей в момент постановки диагноза. Соответственно диагностика заболевания на ранних стадиях позволит российскому обществу сэкономить более 1,5 млрд долл. США из средств, выделяемых на здравоохранение [13].
Принципы терапии
По мнению большинства авторов, в лечении пациентов с синдромом диабетической стопы должны участвовать квалифицированные эндокринолог, гнойный хирург, сосудистый хирург, ортопед, специально обученный средний медицинский персонал, а комплексное лечение должно включать общие и местные методы (рис. 1) [24–26].
Тактика комплексного лечения зависит от формы заболевания [14, 15, 18, 19, 21, 27]. Мы, как и ряд специалистов, выделяем следующие клинические формы СДС.
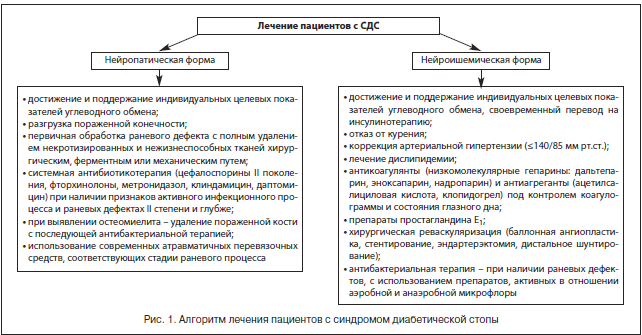
1. Нейропатическая форма:
– без остеоартропатии;
– с остеоартропатией – «сустав Шарко».
2. Нейроишемическая форма с учетом других характеристик.
К общим принципам терапии пациентов с СДС относятся коррекция факторов риска, компенсация углеводного обмена и поддержание целевых показателей углеводного обмена, компенсация сопутствующих заболеваний, системная антибактериальная, антитромботическая, вазопротекторная терапия в сочетании с адекватным обезболиванием.
К местным принципам лечения относятся: обеспечение полной разгрузки пораженной области с помощью разгрузочного полубашмака, индивидуальной разгрузочной повязки, костыля, сложной ортопедической обуви, кресла-каталки; контроль раневой инфекции, заключающийся в первичной обработке раны и местном лечении раны с правильным выбором повязки в зависимости от фазы течения раневого процесса; хирургическое лечение гнойно-некротического очага стопы с закрытием ран и/или формированием культи пораженной стопы при помощи реконструктивных и пластических операций; восстановление магистрального артериального кровотока в сосудах нижних конечностей.
Перспективным является применение L-лизина эсцината в комплексном лечении язвенных и гнойно-некротических поражений при СДС. Эффективность препарата объясняется его противоотечным действием, связанным со снижением проницаемости сосудистой стенки и улучшением венозного оттока. L-лизина эсцинат обладает стабилизирующим действием на мембраны клеток, снижает активность лизосомальных ферментов, принимающих непосредственное участие в воспалительном процессе. Кроме того, препарат блокирует эффекты фосфолипазы А2, которая является ключевым веществом в развитии воспалительной реакции, связанной с повреждением мембран клеток различными факторами при ишемии, инфекции и травме. Стабилизация фосфолипазы А2 способствует снижению активности простагландинов, что также приводит к уменьшению воспалительного ответа. Доказано также влияние L-лизина эсцината на такие медиаторы воспаления, как гистамин, серотонин, которые выделяются из тромбоцитов, тучных клеток и создают основу для классической воспалительной реакции. Комплексный эффект препарата L-лизина эсцината апробирован в нейрохирургической, неврологической, травматологической практике, ангиологии и флебологии [26–31].
Мы регулярно применяем L-лизина эсцинат по 10 мл в разведении на 50 мл физиологического (0,9%) раствора внутривенно капельно в течение 10 дней у пациентов с нейропатической формой СДС в послеоперационном периоде, с трофическими язвами на фоне нейропатических отеков и у больных с язвами на фоне венозной недостаточности (СЕАР 2-3). Отмечаем благоприятное течение послеоперационного периода, более раннее уменьшение отеков, снижение болевого синдрома, нейропатических болей, заживление язв. Рекомендуем применение L-лизина эсцината для лечения язвенных и гнойно-некротических поражений при СДС в амбулаторной и стационарной практике.
Заключение
СД является серьезным заболеванием, способным привести к тяжелым социально-экономическим и демографическим последствиям. Вопрос о влиянии СДС на качество жизни остается малоизученным. Неизвестны долговременные затраты, связанные с лечением рецидивов язв, проведением повторных ампутаций и увеличением расходов на социальное обслуживание. Кроме того, неучтенными остаются непрямые затраты вследствие утраты человеком из-за болезни профессиональных и социальных функций, что наносит обществу материальный и духовный ущерб.
Опыт других стран, например США, показал, что мультидисциплинарный подход, ранняя диагностика и обучение больных позволяют снизить количество язв стопы и ампутаций на 49–85% и существенно уменьшить расходы государства. Использование программ по профилактике осложнений и обучению больных СД приводит к уменьшению количества ампутаций почти в 2 раза, а экономический эффект от внедрения программ обучения составил 10 млн долл. [2, 5, 9, 11, 13, 21].
Учитывая вышеизложенное, 20 апреля 2015 г. в Кремле Президент РФ Владимир Путин подписал Закон о ратификации соглашения о сотрудничестве стран СНГ в борьбе с ростом заболеваемости сахарным диабетом [18], что в сочетании с грамотным ведением пациентов с СДС может улучшить прогноз как для этих пациентов, так и для больных СД в целом.
Источник
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ Федеральное агентство по здравоохранению и социальному развитию ГОУ ВПО Челябинская государственная медицинская академия Кафедра хирургических болезней и урологии
Н. М. Грекова, В. Н. Бордуновский, И. В. Гурьева
ДИАГНОСТИКА И ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ СИНДРОМА ДИАБЕТИЧЕСКОЙ СТОПЫ
Учебное пособие для системы послевузовского профессионального образования врачей
(специальность: хирургия)
Рекомендовано учебно-методическим объединением по медицинскому и фармацевтическому образованию ВУЗов России
в качестве учебного пособия для системы послевузовского профессионального образования врачей
Гриф УМО –17—29/146 от 13.04.2009
Челябинск
2010
УДК 616.379–008.64–06:617.58 ББК 54.15
Г 80
Рецензенты:
Профессор кафедры хирургических болезней и клинической ангиологии Московского государственного Медико-стоматологического университета, Заслуженный деятель науки РФ, доктор медицинских наук Б. С. Брискин
Ведущий научный сотрудник отдела эндокринологии ФГУ «Федеральный центр сердца, крови, и эндокринологии им. В. А. Алмазова ФА по оказанию высокотехнологичной медицинской помощи», доктор медицинских наук В. Б. Бреговский
Профессор кафедры торакальной хирургии Российской Медицинской академии последипломного образования, доктор медицинских наук
С. М. Чудных
Авторы:
Грекова Н. М. – ассистент кафедры хирургических болезней и урологии ЧелГМА, кандидат медицинских наук;
Бордуновский В. Н. – заведующий кафедрой хирургических болезней и урологии ЧелГМА, доктор медицинских наук, профессор.
Гурьева И. В. — директор центра «Диабетическая стопа» ФБМСЭ, доктор медицинских наук, профессор каф. эндокринологии РМАПО, Представитель России в Международной рабочей группе по Диабетической стопе – консультативной секции Международной Федерации Диабета.
Учебное пособие отражает современные взгляды на этиологию, патогенез, классификацию, диагностику синдрома диабетической стопы. Представленная лечебная тактика соответствует принципам доказательной медицины. Подробно освещена хирургическая тактика и техника, наиболее часто производимых хирургических вмешательств на нижней конечности. Рассматриваются вопросы, касающиеся органосохраняющих вмешательств на стопе. Приведен список литературы для углубленного изучения темы. Пособие предназначено врачам, обучающимся в системе последипломного образования, – хирургам, эндокринологам, ортопедам. Учебное пособие соответствует типовой учебной программе дополнительного профессионального образования врачей по специальности 040126 – «Хирургия», утвержденной МЗ РФ, Москва, 2002 г.
Учебное пособие утверждено на заседании Ученого Совета ГОУ ВПО «ЧелГМА» (протокол № 3 от 24 октября 2008)
ISBN 978-5-94507-110-0
Оглавление | |
Список сокращений……………………………………………………………………………………….. | 4 |
Введение……………………………………………………………………………………………………….. | 5 |
1. Определение, патогенез, классификация синдрома диабетической | |
стопы…………………………………………………………………………………………………………….. | 8 |
1.1. Определение синдрома диабетической стопы ……………………………………….. | 8 |
1.2. Хирургическая анатомия стопы…………………………………………………………….. | 8 |
1.3. Патогенез синдрома диабетической стопы…………………………………………… | 12 |
1.4. Классификация синдрома диабетической стопы………………………………….. | 16 |
2. Клиника, диагностика гнойно-некротических поражений стопы | |
у больных сахарным диабетом …………………………………………………………………….. | 21 |
2.1. Диагностика диабетической нейропатии……………………………………………… | 23 |
2.2. Диагностика диабетической макроангиопатии…………………………………….. | 26 |
2.2.1. Физикальные методы обследования артерий нижних конечностей…………… | 26 |
2.2.2. Ультразвуковые методы обследования артерий нижних конечностей………. | 28 |
2.2.3. Другие неинвазивные методы визуализации артерий нижних | |
конечностей…………………………………………………………………………………………………….. | 33 |
2.2.4. Рентгенконтрастная ангиография нижних конечностей…………………………… | 34 |
3. Лечение гнойно-некротических поражений стопы при сахарном | |
диабете………………………………………………………………………………………………………… | 36 |
3.1. Реваскуляризация конечности при критической ишемии на фоне | |
синдрома диабетической стопы…………………………………………………………………. | 36 |
3.2. Тактика хирурга при лечении гнойно-некротических поражений | |
стопы больных сахарным диабетом…………………………………………………………… | 42 |
3.3. Оперативные вмешательства при синдроме диабетической стопы……….. | 51 |
3.4. Вакуумная терапия гнойных ран при синдроме диабетической | |
стопы………………………………………………………………………………………………………… | 80 |
3.5. Пластическое закрытие ран при синдроме диабетической стопы…………. | 85 |
3.6. Медикаментозная терапия гнойно-некротических поражений стопы | |
при сахарном диабете………………………………………………………………………………… | 87 |
4. Принципы профилактики гнойно-некротических поражений при | |
синдроме диабетической стопы………………………………………………………………….. | 100 |
Список рекомендуемой литературы:…………………………………………………………… | 103 |
Ситуационные задачи………………………………………………………………………………… | 104 |
Тестовый контроль…………………………………………………………………………………….. | 108 |
Список сокращений
ГБО – гипербарическая оксигенация ДАП – диабетическая ангиопатия ДНП – диабетическая нейропатия ДОАП – диабетическая остеоартропатия КИ – критическая ишемия
КИН – контраст-индуцированная нефропатия КТА – компьютерно-томографическая ангиография ЛПИ – лодыжечно-плечевой индекс МРА – магнитно-резонансная ангиография
МСКТА – мультиспиральная компьютерно-томографическая ангиография ОПН – острая почечная недостаточность ОРИТ – отделение реанимации и интенсивной терапии
ПСП – пероральные сахароснижающие препараты ПТФЭ – политетрафторэтилен
РАСХИ – российская ассоциация специалистов по хирургическим инфекциям СД – сахарный диабет СДС – синдром диабетической стопы
УЗДГ – ультразвуковая допплерография ХОЗАНК – хроническое облитерирующее заболевание артерий нижних
конечностей ЦДК – цветовое доплеровское картирование
ЦДКЭ – цветовое доплеровское картирование по энергии DFSG – рабочая группа по изучению диабетической стопы EASD – Европейская ассоциация сахарного диабета MRSAМетициллин резистентный золотистый стафилококк
ТсрО2 – Чрескожное парциальное напряжение кислорода в тканях
Введение
Качество жизни пациента, страдающего сахарным диабетом, и сама его жизнь нередко подвергаются серьезной опасности. Вместе с поражением сердца, головного мозга, почек и глаз заметную роль в этом играет синдром диабетической стопы.
История изучения гнойно-некротических поражений стопы у больных сахарным диабетом в России, имеющая отражение в фундаментальных трудах, имеет чуть более чем 20летнюю историю. В отечественной литературе понятие «Диабетическая стопа» и первое определение этой патологии появилось в 1987 году в переводе с английского, в докладе исследовательской группы ВОЗ по сахарному диабету.
Особенностям течения раневого процесса при сахарном диабете посвящен раздел капитального труда «Раны и раневая инфекция» под редакцией М. И. Кузина, Б. М. Костюченок, (1990). Здесь впервые было отвергнуто господствующее в то время негативное отношение к радикальному иссечению гнойно-некротического очага у больных сахарным диабетом. В работе подверглось критике общепринятое положение о том, что при сахарном диабете после иссечения очага инфекции нецелесообразно ушивание раны и ее пластическое закрытие. Были сформулированы основы активной хирургической тактики при гнойно-некротических процессах у больных сахарным диабетом (СД).
В 1991 году вышла в свет монография Б. М. Газетова и А. П. Калинина «Хирургические заболевания у больных сахарным диабетом». Здесь было раскрыто понятие «диабетическая стопа» и несколько разделов посвящены патологии стопы при сахарном диабете.
Е. В. Кулешов, и С. Е. Кулешов (1996) в монографии «Сахарный диабет и хирургические заболевания» опубликовали, в частности, результаты изучения заживления ушитых и гнойных ран при СД. Авторы, измеряя парциальное напряжение кислорода в тканях, составили «оксиметрическую карту гнойного очага и инфильтрата». Здесь же представлено подробное описание клинических форм диабетической стопы и, что особенно
5
важно, диабетической остеоартропатии с известными в то время теориями патогенеза этого проявления Синдрома диабетической стопы (СДС).
Первая классическая отечественная монография «Синдром диабетической стопы» (Дедов И. И., Анциферов М. Б., Галстян Г. Р., Токмакова А. Ю.) вышла в 1998 году. В этом труде впервые подробно рассмотрены все без исключения аспекты этой сложнейшей патологии. До сих пор — это единственная книга, где освещены вопросы хирургической тактики при СДС.
Переломным моментом в организации помощи больным синдромом диабетической стопы в России является выход в свет русского перевода «Международного соглашения по диабетической стопе», составленного Международной рабочей группой по диабетической стопе (перевод И. В. Гурьевой, 2000). С этого времени междисциплинарная помощь больным синдромом диабетической стопы в России стала подчиняться требованиям мировых стандартов.
Высока практическая и теоретическая значимость двух последних монографий, посвященных синдрому диабетической стопы. Это «Поражение нижних конечностей при сахарном диабете» (В. Б. Бреговский, А. А. Зайцев, А. Г. Залевская, О. И. Карпов, И. А. Карпова, Т. Л. Цветкова, 2004) и «Диабетическая стопа» (И. И. Дедов, О. В. Удовиченко, Г. Р. Галстян, 2005). Эти книги являются настольными и служат «руководством к действию» эндокринологов, терапевтов, клинических фармакологов, ортопедов, лучевых диагностов и других специалистов, занимающихся этой сложной патологией.
Основными клиническими проявлениями синдрома диабетической стопы являются хронические язвы, критическая ишемия и неинфекционная деструкция костей и суставов – диабетическая нейроостеоартропатия или стопа Шарко. Именно язвы являются наиболее распространенным и угрожающим потере конечности состоянием диабетической стопы вследствие присоединения вторичной инфекции и развития гнойнонекротического процесса, гангрены, сепсиса.
Гнойный процесс любой локализации в условиях гипергликемии и абсолютной или относительной инсулиновой недостаточности сопровожда-
6
ется прогрессирующим некрозом тканей. В гнойной ране, на фоне синдрома диабетической стопы, деструкция развивается быстрее, чем где–либо и сопровождается распространением гноя в глубокие ткани и в проксимальные отделы стопы и голени. Именно поэтому в мире каждый час происходит 55 ампутаций нижних конечностей у больных сахарным диабетом.
В настоящее время специальности подиатр (от английского слова podiatrist), не существует в нашей стране, и проблемами этого, весьма распространенного синдрома, занимаются хирурги и эндокринологи.
К сожалению, тиражи специальных и общих руководств для хирургов, монографий, справочников, учебников, в которых отражены практические рекомендации по диагностике и лечению гнойно-некротических поражений стопы у больных сахарным диабетом, недостаточны. Эти книги не имеют должного распространения в научно-медицинских библиотеках и розничной книжной сети.
В предлагаемом пособии отражены этиология, патогенез и наиболее распространенные классификации синдрома диабетической стопы, которые имеются в отечественной и зарубежной литературе последних лет. Освещены вопросы диагностики и дифференциальной диагностики форм синдрома диабетической стопы.
Значительная часть пособия посвящена хирургической тактике, оперативному лечению и медикаментозной терапии гнойно-некротических поражений стопы у больных сахарным диабетом.
В пособии имеются ситуационные задачи и тест-контроль.
Пособие предназначено хирургам системы послевузовского профессионального образования врачей, а также может быть полезно интернам и клиническим ординаторам хирургических специальностей, может заинтересовать эндокринологов, врачей кабинета «Диабетическая стопа».
7
1. Определение, патогенез, классификация синдрома диабетической стопы
Нижняя конечность представляет собой сложный аппарат для опоры и движения. При нагрузке вся тяжесть тела через голень передается на своды стопы, сформированные костями, суставами, мышцами и фиброзными образованиями. Поэтому при сочетании патологии нервов, сосудов, костей, суставов, вызванных сахарным диабетом, стопа особенно подвержена различным деформациям и поражениям.
1.1. Определение синдрома диабетической стопы
Согласно ВОЗ, понятие «Синдром диабетической стопы» определяется, как самостоятельное осложнение СД, наряду с диабетическим поражением глаз, почек, нервной и сердечно-сосудистой систем. Это «комплекс анато- мо-функциональных изменений стопы, связанный с диабетической нейропатией, микро- и/или макроангиопатией, на фоне которых развиваются тяжелые гнойно-некротические процессы». Любой из этих факторов может играть ведущую роль, хотя, обычно, все они присутствуют в той или иной степени.
На основе этого определения ВОЗ Международное соглашение по диабетической стопе дает следующее определение этого синдрома:
«Инфекция, язва и/или деструкция глубоких тканей, связанная с неврологическими нарушениями и снижением магистрального кровотока в артериях нижних конечностей различной степени тяжести».
Целью практического хирурга в лечении синдрома диабетической стопы является сохранение опорной и рессорной функции стопы в условиях острой хирургической патологии, которая чаще всего является гнойным и/или некротическим поражением различной локализации, распространенности, глубины.
1.2. Хирургическая анатомия стопы
Стопа – это дистальный отдел нижней конечности, которая служит опорным и пружинящим аппаратом при стоянии, ходьбе, беге.
На тыльной поверхности стопы под кожей расположена поверхностная фасция. Далее — тонкий слой подкожной жировой клетчатки и собствен-
8
ная фасция стопы, под которой лежат сухожилия длинных разгибателей. Непосредственно под ними – a. dorsalis pedis (проекционная линия – от середины расстояния между лодыжками до первого межпальцевого проме-
жутка), a. arcuata с ветвями и n. peroneus profundus.
Еще глубже расположены короткие разгибатели пальцев, которые начинаются от пяточной кости. Фасциальный мешок для сухожилий длинных разгибателей с их синовиальными влагалищами и коротких мышц стопы образуется из собственной фасции тыла и из глубокой фасции, покрывающей кости предплюсны, плюсны и межкостные мышцы. На подошве собственная фасция сильно утолщена и образует в средней своей части сухожильно-блестящий подошвенный апоневроз, натягивающийся от пяточного бугра до основания пальцев.
На уровне головок плюсневых костей, при помощи поперечных волокон, образуется 3 комиссуральных отверстия, через которые глубокое ложе подошвы сообщается с клетчаткой межпальцевых промежутков. От апоневроза вглубь, к длинной связке подошвы и к глубокой подошвенной фасции идут фиброзные перегородки, разделяющие подапоневротическое пространство на четыре ложа. Медиальное, латеральное ложе и среднее.
При синдроме диабетической стопы особое значение имеет выделение задних ее отделов – пяточной и надпяточной областей.
Пяточная область содержит бугор пяточной кости, покрытый надкостницей. От его нижней передней поверхности начинается мощная подошвенная связка, являющаяся верхней стенкой подошвенного канала. Более поверхностно, от его надкостницы берут начало короткие мышцы подошвы. И, ближе всего к коже, от пяточного бугра начинается подошвенный апоневроз.
К задней поверхности пяточного бугра прикрепляется ахиллово сухожилие. Пяточный бугор окружен подкожной клетчаткой, пронизанной мощными фиброзными пучками, соединяющими надкостницу и кожу. Эти тяжи разделяют жировую ткань на дольки. Всвязи с этим, гнойнонекротический процесс в мягких тканях пяточной области быстро распространяется вглубь, и поражает надкостницу и кость. Надпяточная область
9
содержит в себе ахиллово сухожилие с окружающим его влагалищем, сухожилие подошвенной мышцы и синовиальную сумку.
Под ахилловым сухожилием, между его передней поверхностью и глубоким листком собственной фасции голени, покрывающим заднюю поверхность большеберцовой кости, расположен слой жировой клетчатки (рис. 1-А, 1-Б). В это пространство гной может попадать при флегмоне пяточной области, из клетчатки, окружающей пяточный бугор. Причина таких флегмон у больных СД – ссадины, мозоли, трещины, трофические язвы в местах повышенного давления при нарушенной статикодинамической функции стопы, связанной с диабетической остеоартропатией и нейропатией.
Среди дистальных отделов стопы выделяют межпальцевые промежутки. При СДС их строение имеет особое значение, т. к. именно здесь расположены начальные отделы собственных пальцевых артерий, просвет которых часто оказывается сужен или полностью облитерирован при диабетической макроангиопатии. С развитием изолированной межпальцевой флегмоны или при распространении гноя в эту область из других отделов стопы, кровоснабжение пальца резко нарушается. Возможно развитие вторичной гангрены пальца.
Практическое значение в гнойной хирургии стопы имеет сообщение клетчаточных пространств подошвы и тыла друг с другом и возможные пути распространения гноя. Срединное клетчаточное пространство, в котором находится подошвенная артериальная дуга, вдоль клетчатки, окружающей этот сосуд, а также по сухожилиям сгибателей пальцев сообщается с лодыжечным каналом и с глубоким ложем голени. Сухожилие длинного сгибателя 1 пальца на своем пути через лодыжечный канал тесно прилежит к задним отделам капсулы голеностопного сустава, которая здесь особенно тонка. Гной, распространяющийся по сухожилию, может вызвать деструкцию капсулы сустава и попасть в его полость, вызвав гнойный артрит. Срединное ложе подошвы через комиссуральные отверстия в подошвенном апоневрозе имеет связь с подкожной клетчаткой подошвы, межпальцевыми промежутками, боковыми и тыльными сторонами пальцев. Вдоль глубокой подошвенной ветви тыльной артерии стопы и по
10
Источник
