Если нет порока сердца это может быть синдром дауна

Хорошо известно, что врожденные аномалии сердца встречаются почти у половины детей с синдромом Дауна и оказывают большое влияние на младенческую выживаемость. С середины прошлого столетия проводилось множество исследований по выявлению частоты, специфичности и характера пороков сердца у этих детей. Так, в период 1970–1980-х гг. отмечалось повышение распространенности врожденных аномалий сердечнососудистой системы у пациентов с синдромом Дауна. Связано это было в основном с улучшением диагностики открытого артериального протока и дефекта межпредсердной перегородки (M. J. Khoury, J. D. Erickson, 1992). По данным зарубежных авторов, при синдроме Дауна наиболее часто встречаются дефект межжелудочковой перегородки, дефект межпредсердной перегородки, общий открытый атриовентрикулярный канал, тетрада Фалло и другие пороки, составляющие менее 1 %.
За годы научных наблюдений стало очевидным, что для выявления врожденного порока сердца у новорожденного с синдромом Дауна физическое обследование, включающее осмотр и аускультацию, является обязательным, но недостаточным. Так, McElhinney и др. установили, что информативность физического обследования для выявления сердечных аномалий у детей с синдромом Дауна не превышает 80 %. Оказалось, что 15 из 114 исследуемых детей при осмотре не имели признаков врожденных пороков сердца, но при ультразвуковом исследовании у них были диагностированы сердечные аномалии, а девяти из них в дальнейшем потребовалось оперативное лечение.
Материалы и методы
Нами проведено исследование частоты встречаемости и особенностей клинической картины врожденных пороков сердца и персистирующих фетальных коммуникаций у 522 детей с синдромом Дауна в возрасте от 0 до 8 лет, воспитывающихся в домашних условиях. Дети получали медико-психолого-педагогическую помощь в Центре ранней помощи Благотворительного фонда «Даунсайд Ап», где наблюдались с момента обращения (возраст при первом посещении варьировал от 0 до 7 лет) до 8 лет. При первичном обращении проводился сбор анамнеза, клиническое обследование, анализ медицинской документации. Все дети, даже в случае отсутствия клинически выраженных симптомов порока сердца, направлялись на электрокардиографическое и эхокардиографическое обследования и, при необходимости, на лечение в соответствующие профильные кардиологические стационары и диспансеры.
Результаты
У всех пациентов синдром Дауна был подтвержден хромосомным исследованием. Регулярная трисомия 21-й хромосомы была выявлена у 499 детей (499/522), что составило 90,4 %, транслокационная форма – у 24 (4,3 %), мозаицизм – у 28 (5,1 %), у одного ребенка трисомии 21-й и Х хромосом (кариотип 48,ХХХ,+21) – 0,2 %.
Получены результаты эхокардиографического исследования 428 детей (см. рис.). Врожденные пороки сердца диагностированы у 195 (195/428), что составило 45,6 %. В структуре этих аномалий у детей с синдромом Дауна чаще отмечался дефект межпредсердной перегородки (ДМПП), а именно в 30,2 % (59/195) случаев. Общий атриовентрикулярный канал (ОАВК) составил 24,1 % (47/195), дефект межжелудочковой перегородки (ДМЖП) – 23,1 % (45/195), сочетание дефектов межпредсердной и межжелудочковой перегородок (ДМПП+ДМЖП) – 10,8 %. Другие пороки, такие как тетрада Фалло, стеноз легочной артерии и др., в сумме составили 11,8 % (23/195). Персистенция гемодинамически значимого открытого артериального протока (ОАП), потребовавшего оперативного вмешательства, была выявлена в 2,8 % (12/428).
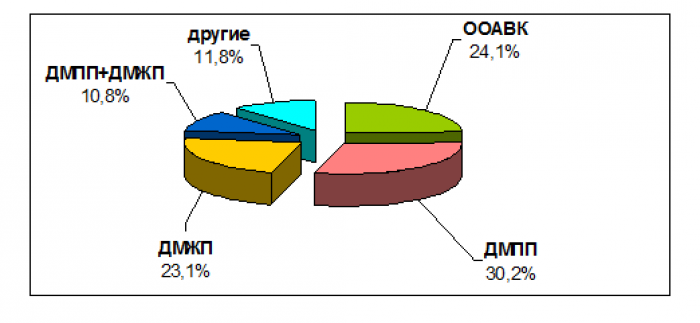 Структура сердечных аномалий у детей с синдромом Дауна
Структура сердечных аномалий у детей с синдромом Дауна
Почти все исследуемые нами дети родились доношенными. Срок родов составил 38,2 ± 1,3 недель. Однако при оценке антропометрических данных новорожденных с синдромом Дауна и врожденными пороками сердца оказалось, что их физическое развитие страдает еще внутриутробно. Задержка физического развития (ЗВУР) – масса тела при рождении ниже 10 перцентилей в соответствии со сроком гестации в сравнении с показателями физического развития Г. М. Дементьевой, Е. В. Короткой – отмечалась у 18,7% детей. У всех новорожденных с сердечными аномалиями наблюдалась асимметричная форма ЗВУР (Pounderal Index, PI>25). Вероятно, задержка физического развития формировалась под влиянием, в основном, не генетического фактора.
Известно, что у новорожденных с синдромом Дауна нередко отмечается морфофункциональная незрелость (по нашим данным, она встречается в 17,9 % случаев). У детей с морфофункциональной незрелостью часто недооцениваются размеры дефекта межпредсердной перегородки, который рассматривают как открытое овальное окно даже при гемодинамической его значимости, и артериального протока, в то время как имеет место недостаточность кровообращения. Застойная легочная гипертензия приводит к развитию пневмонии. Возникновение и затяжное течение пневмонии у детей с синдромом Дауна объясняется характерными для них иммунологическими нарушениями.
Хорошо известно, что манифестация сердечной недостаточности у детей раннего возраста, в отличие от детей старшего возраста, может протекать под маской других состояний. Помимо классических симптомов, таких как тахикардия (учащение сердцебиения), тахипноэ (увеличение частоты дыхания), цианоз кожи и слизистых, типичны вялое сосание, снижение темпов физического и психомоторного развития. В подобных случаях у педиатров возникают определенные затруднения в проведении дифференциальной диагностики при наличии у ребенка синдрома Дауна. У таких детей клинические симптомы недостаточности кровообращения могут расцениваться как проявления особенностей психомоторного развития, типичных для синдрома Дауна. Так, если возникают трудности вскармливания: ребенок вялый, неохотно берет грудь или соску, вяло сосет, не может высосать необходимый объем питания, вплоть до полного отказа от кормлений, такие проблемы часто объясняются мышечной гипотонией, общей вялостью, характерной для детей с синдромом Дауна, с последующим назначением общеукрепляющего массажа, что ухудшает состояние ребенка. В дальнейшем отмечается плохая прибавка в весе. Она направляет клиницистов на выявление патологии со стороны желудочно-кишечного тракта, гипогалактии у матери, исследования качества молока, его инфицированности. В борьбе с прогрессирующей гипотрофией младенца нередко переводят на искусственные смеси. Важно отметить, что гипотрофия может стать причиной отсрочки оперативного лечения порока сердца и/или неблагоприятно повлиять на его исход.
Таким образом, слабая нацеленность педиатров на выявление симптомов недостаточности кровообращения у ребенка с синдромом Дауна затрудняет ее своевременную диагностику, а следовательно, и адекватное лечение врожденного порока сердца.
Наглядным примером будет анализ истории болезни.
Андрей Б., от первой, физиологично протекавшей беременности. Роды в срок. Вес мальчика при рождении – 3000 г., рост – 51см, оценка по шкале АПГАР 88б. Состояние ребенка после рождения удовлетворительное. Отмечались признаки морфофункциональной незрелости, фенотипические признаки синдрома Дауна. С целью подтверждения хромосомной патологии была взята кровь для определения кариотипа. Выявлена регулярная трисомия 21-й хромосомы. С первых суток жизни отмечался систолический шум при аускультации грудной клетки. Для исключения аномалий развития сердца проведено ЭХОКГ и обнаружено открытое овальное окно размером 4 мм. Ребенок был выписан домой под наблюдение участкового педиатра и кардиолога по месту жительства. В дальнейшем мальчик стал вялым, неохотно брал грудь, отмечались частые срыгивания, редкий стул. За месяц ребенок прибавил в весе 210 г. При осмотре обращали на себя внимание признаки недостаточности кровообращения: одышка в покое, умеренная тахикардия. Мальчик был направлен в НЦССХ им. Бакулева, где диагностирован порок развития сердца – дефект межпредсердной перегородки размером 6 мм со значительным нарушением сердечной гемодинамики. Рентгенограмма грудной клетки показала расширение корней легких, КТИ = 57 %. По данным ЭКГ: отклонение электрической оси сердца вправо. В возрасте 4 месяцев проведено оперативное лечение дефекта межпредсердной перегородки.
Успехи в области кардиохирургии за последние десятилетия позволили повысить выживаемость младенцев с синдромом Дауна и патологией сердечнососудистой системы с 78 % в 1985 г до 90 % к 2004 г. (Claire Irving и др., 2008).
Hijii Т. и др. (1997) сообщили, что до 24-летнего возраста доживают 87,8 % пациентов с синдромом Дауна, перенесших оперативное лечение врожденного порока сердца.
При сравнении течения и исходов оперативного лечения полной формы атривентрикулярного канала у младенцев с синдромом Дауна и без синдрома, в работе, проведенной на базе НЦССХ им. Бакулева, Т. И. Задко отмечает, что у детей с синдромом Дауна быстрее развивается легочная гипертензия, важным механизмом в развитии которой, очевидно, является окислительный стресс. Генетически обусловленные особенности антиоксидантной системы, в том числе изначально низкий уровень глутатиона и более высокая антиоксидантная активность сыворотки у детей с синдромом Дауна (Н. П. Котлукова, О. И. Артеменко и др., 2008), свидетельствуют о более высоком окислительном стрессе при развитии легочной гипертензии при пороках сердца с легочной гиперволемией.
Из ранних осложнений хирургической коррекции атриовентрикулярного канала у детей с синдромом Дауна чаще встречаются инфекционно-септические осложнения, тогда как у детей без синдрома – острая сердечная недостаточность (Т. И. Задко, 2005). Это обстоятельство объясняется анатомическими особенностями порока и имеющимися иммунологическими нарушениями у младенцев с трисомией 21-й хромосомы.
Выводы
Полученные нами данные частоты сердечных аномалий не противоречат уже известным в литературе. Около половины детей с синдромом Дауна имеют патологию сердечнососудистой системы: 45,5 % – врожденные пороки сердца, 2,8 % – гемодинамически значимый открытый артериальный проток.
Анализ данных проведенных исследований, а также собственные полученные результаты делают очевидной необходимость раннего кардиологического обследования всех новорожденных с синдромом Дауна, включающего помимо осмотра и аускультации проведение эхокардиологического и электрокардиологического исследований. Внимательный подход и оценка клинических симптомов, а также знание генетически обусловленных особенностей детей с синдромом Дауна помогут своевременно диагностировать недостаточность кровообращения и начать адекватную терапию. Все дети с выявленными пороками сердца должны быть консультированы кардиохирургом для определения необходимости и сроков оперативного лечения.
Литература
- Задко Т. И. Синдром Дауна в сочетании с полной формой атриовентрикулярной коммуникации: актуальность, диагностика, сопутствующая патология, анатомия, особенности естественного течения, результаты хирургического лечения // Детские болезни сердца и сосудов. – 2005. – № 6. – С. 10–18.
- Роль окислительного стресса и антиоксидантной системы в патогенезе врожденных пороков сердца / Н. П. Котлукова, О. И. Артеменко, М. П. Давыдова, О. Н. Ильина, Л. А. Курбатова // Педиатрия. – 2009. – Т. 87, № 1. – С. 24–28.
- Cassidy S. B., Allanson J. E. Management of Genetic Syndromes. 2-nd ed. – P. 191–210. URL: https://www.wiley.com/en-us/Management+of+Genetic+Syndromes%2C+3rd+Edition-p-9780470191415
- Correlation between abnormal cardiac physical examination and echocardiographic findings in neonates with Down syndrome / D. B. McElhinney, M. Straka, E. Goldmuntz, E. H. Zackai // American Journal of Medical Genetics. – 2002. – Part A. – P. 238–241.
- Khory M. J., Erickson J. D. Improved ascertainment of cardiovascular malformation in infants with Down syndrome, Atlanta, 1968 through 1989 // Epidemiology. – 1992. – Vol. 136. – P. 1457–1464.
- Life expectancy and social adaptation in individuals with Down syndrome and without surgery for congenital heart disease / T. Hijii, J. Fukushige, H. Igarashi et al. // Clinical Pediatrics. – 1997. –Vol. 36. – P. 327–332.
- Twenty-year trends in prevalence and survival of Down syndrome / C. Irving, A. Basu, S. Richmond et al. // European Journal of Human Genetics. – 2008. – Vol. 16. – P. 1336–1340.
Источник
Синдром Дауна (трисомия 21-й пары): причины, клиника
Синдром Дауна самая частая трисомия аутосом и самая частая генетическая причина тяжёлой умственной отсталости. Частота встречаемости (в том числе при антенатальном скрининге) у живых новорождённых составляет около 1:650.
Клинические проявления синдрома Дауна. Синдром Дауна обычно определяют сразу после рождения ребёнка по характерному виду его лица. У большинства отмечают гипотонию, другие диагностически важные клинические симптомы включают уплощённый затылок, единственную ладонную борозду, изогнутый мизинец и широкий промежуток между большим и вторым пальцем на стопе («сандалевидная стопа»). Диагностика может быть затруднительна, если основана только на клинических проявлениях, поэтому предварительный диагноз должен быть подтверждён более опытным педиатром. До взятия крови на анализ следует предупредить родителей, что будет проведён тест на синдром Дауна. На получение результатов с применением метода быстрой флуоресцентной гибридизации in-situ (FISH) может потребоваться 1-2 дня. Родителей следует информировать о предварительном и окончательном диагнозе. Они захотят понять, как и почему развилось такое заболевание, каков риск повторного рождения такого ребёнка и есть ли возможность антенатальной диагностики при будущих беременностях.
Характерные клинические проявления синдрома Дауна
I. Типичные краниофациальные проявления синдрома Дауна:
• Округлое лицо и плоская переносица.
• Монголоидный разрез глаз.
• Эпикант (кожная складка вокруг внутреннего угла глаза).
• Уплощённый затылок и малый родничок.
• Открытый маленький рот и высунутый язык.
• Маленькие уши.
• Пигментные пятна на радужной оболочке.
II. Другие аномалии при синдроме Дауна:
• Короткая шея.
• Единственная ладонная складка, изогнутый кнутри мизинец и сандалевидная стопа (широкий промежуток между первым и вторым пальцами).
• Гипотония.
• Болезнь Гиршпрунга.
• Атрезия двенадцатиперстной кишки.
• Врождённые пороки сердца (40%).
III. Поздние медицинские осложнения синдрома Дауна:
• Задержка моторного развития.
• Умеренная или тяжёлая умственная отсталость.
• Маленький рост.
• Повышенная восприимчивость к инфекциям.
• Нарушение слуха, обусловленное катаральным средним отитом.
• Нарушение зрения на фоне катаракты, косоглазия, миопии.
• Повышенный риск лейкемии и одиночных опухолей.
• Болезнь Альцгеймера.
• Гипотиреоз и целиакия.
• Эпилепсия.
• Риск нестабильности атланто-аксиального сочленения.

В период новорождённости трудно дать точный долгосрочный прогноз, поскольку существуют индивидуальные колебания степени умственной отсталости и развития осложнений. Более 85% грудных детей с трисомией 21-й пары хромосом доживают до года. Основной причиной смерти в раннем возрасте является тяжёлый врождённый порок сердца (особенно дефект межжелудочковой перегородки — ДМЖП).
Как минимум 50% пациентов живут дольше 50 лет. Родители также захотят узнать, доступна ли какая-нибудь помощь специалистов и групп самопомощи (социальная и профессиональная адаптация). Для них будет полезна печатная информация, поскольку они смогут дать её другим членам семьи.
Семье может потребоваться психологическое консультирование для преодоления чувства подавленности, страха или вины. Важно заметить, что родителям легче принять ситуацию, когда к ребёнку относятся не как к диагностической категории («ребёнок-даун»), а как к индивидуальности («ребёнок с синдромом Дауна»).
Цитогенетические причины синдрома Дауна. Дополнительная хромосома 21 может возникнуть в результате нерасхождения, транслокации или мозаицизма.
Нерасхождение хромосом (94%) при синдроме Дауна. При нерасхождении:
• большинство случаев возникает из-за ошибки при мейозе;
• 21-я пара хромосом не расходится, поэтому в одной гамете содержится две хромосомы 21, а в другой — ни одной;
• оплодотворение гаметы с двумя хромосомами 21 вызывает образование зиготы с трисомией 21-й пары;
• при этом отсутствует необходимость анализа родительских хромосом.
Встречаемость трисомии 21-й пары, развившейся в результате нерасхождения, связана с возрастом матери. Тем не менее доля беременных женщин старшего возраста мала и большинство больных детей рождается у более молодых мам. В настоящее время всем беременным женщинам предлагают скрининговый тест, измеряющий биохимические маркёры в образцах крови и изменения при УЗИ (утолщение подкожно-жировой клетчатки на задней поверхности шеи) для определения повышенного риска синдрома Дауна у плода. При обнаружении этого признака возможен амниоцентез для оценки структуры хромосом плода.
Хотя в большинстве случаев выявляется нормальная структура хромосом, следует заранее обсудить возможность положительного результата и прерывания беременности. Должны быть доступны психологическая поддержка и консультирование. После рождения одного ребёнка с трисомией 21-й пары в результате нерасхождения риск повторного рождения ребёнка с синдромом Дауна составляет 1:200 среди матерей младше 35 лет, но остается сходным с возрастным риском в популяции для женщин старше 35 лет.
Транслокация (5%) при синдроме Дауна. Феномен, при котором дополнительная хромосома 21 присоединяется к другой хромосоме (обычно к хромосоме 14, но иногда — 15, 22 или 21), известен под названием «несбалансированная транслокация Робертсона». У больного ребёнка 46 хромосом, среди которых три копии хромосомного материала хромосомы 21. В такой ситуации хромосомный анализ родителей необходим, поскольку в 25% случаев один из них — носитель сбалансированной транслокации.
У носителя транслокации 45 хромосом, одна из которых состоит из двух соединенных хромосом. При синдроме Дауна, вызванном транслокацией:
• если мать является носителем транслокации, риск повторного рождения больного ребёнка равен 10-15%, если отец — 2,5%;
• если родитель является носителем редкой транслокации 21:21, все потомство будет иметь синдром Дауна;
• если ни у одного родителя нет транслокации (75% случаев), риск развития синдрома у потомства менее 1%.
Мозаицизм (1%) при синдроме Дауна. При мозаицизме часть клеток нормальные, а в остальных обнаруживают трисомию 21-й пары. Обычно такое случается после образования зиготы, при нерасхождении хромосом во время митоза. При мозаицизме фенотип может быть менее ярким.
Синдром Дауна (трисомия 21-й пары):
• Частота встречаемости в популяции — 1,5% на 1000 живых новорождённых.
• Цитогенетическая основа — нерасхождение хромосом (самая частая, зависит от возраста матери), транслокация (родители могут быть носителями сбалансированной транслокации) или мозаицизм (редко).
• Диагностика — УЗИ во время беременности или клинически. Для подтверждения диагноза — хромосомный анализ.
• Ближайшие осложнения — повышенный риск атрезии двенадцатиперстной кишки, врождённый порок сердца.
– Также рекомендуем “Синдром Эдвардса и синдром Патау: причины, клиника”
Оглавление темы “Детские болезни”:
- Хроническое отравление детей. Отравление свинцом, курение
- Жесткое обращение с детьми. Варианты
- Признаки жесткого обращения с детьми. Диагностика
- Пренебрежительное отношение с детьми. Эмоциональное насилие детей
- Ложные и вызванные заболевания у детей родителями. Особенности
- Тактика врача при подозрении на жестокое обращение с ребёнком. Рекомендации
- Сексуальное насилие над детьми. Варианты, диагностика, тактика
- Генетические заболевания у детей и их влияние на ребенка
- Синдром Дауна (трисомия 21-й пары): причины, клиника
- Синдром Эдвардса и синдром Патау: причины, клиника
Источник
