Геморрагические лихорадки с почечным синдромом литература
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Хунафина Д.Х.
1
Валишин Д.А.
1
Шайхуллина Л.Р.
1
Галиева А.Т.
1
1 ГБОУ ВПО «Башкирский Государственный медицинский университет МЗ РФ»
Геморрагическая лихорадка с почечным синдромом – острое вирусное заболевание, характеризующееся системным поражением мелких сосудов с возникновением иммунокомплексного васкулита с полиорганным поражением и развитием опасных для жизни осложнений: инфекционно-токсическим шоком (ИТШ), острой почечной недостаточностью (ОПН), ДВС-синдромом. Отсутствие на сегодня эффективных специфических средств лечения и профилактики определяет крайнюю важность рассмотрения вопросов ранней клинической диагностики для своевременной госпитализации и назначения на догоспитальном этапе противовирусных препаратов.
геморрагическая лихорадка с почечным синдромом
ранняя клиническая диагностика
противовирусная терапия
1. Бурганова А.Н. Сравнительная оценка некоторых видов этиотропной терапии геморрагической лихорадки с почечным синдромом / А.Н. Бурганова // Автореф. дис… на соиск. уч. ст. канд. мед. наук. – Уфа, 2001. – 22 с.
2. Мавзютова Г.А. Клинико-иммунологические аспекты применения α1-интерферона в комплексной терапии геморрагической лихорадки с почечным синдромом: Автореф. дисс…канд.мед.наук. – Уфа, 1996.
3. Мирсаева Г.Х., Фазлыева Р.М., Камилов Ф.Х., Хунафина Д.Х. Патогенез и лечение геморрагической лихорадки с почечным синдромом.- Уфа, 2000.- 236 с.
4. Мурзабаева Р.Т. Система интерферона и иммунный статус больных геморрагической лихорадкой с почечным синдромом, разработка новых способов терапии: Автореф. дисс… д-ра мед. наук. – М., 2003. – 47 с.
5. Сиротин Б.З. Геморрагическая лихорадка с почечным синдромом. – Хабаровск. 1994. – 300с.
6. Хунафина Д.Х. Геморрагическая лихорадка с почечным синдромом (клинико-патогенетические аспекты): Автореф. дисс… д-ра мед. наук. – СПб., 1995. – 31с.
7. Шайхуллина Л.Р. Состояние процессов пероксидации у больных геморрагической лихорадкой с почечным синдромом на фоне терапии с применением йодантипирина: Автореф. дис… канд. мед. наук. – Уфа, 2004. – 21с.
8. Interferon enhances macrophage transcription of the tumor necrosis fac-tor/cachectin, interleukin-1, and urokinase genes, which are controlled by short-lived repressors/M.A.Collort, D. Belin, J. D. Vassali // J. Exp. Med. -1986-Vol.l64.-P. 2113-2118.
9. Interferon-induced Mx A Protein mediates resistance to Hantaviruses / M. Frese, G. Kochs, H. Feldman, H. D. Klenk and 0. Haller // 3-rd Intern. Conf. on HFRS and Hantaviruses. – Helsinki,-1995.- P.25.
Геморрагическая лихорадка с почечным синдромом (ГЛПС) – острое вирусное заболевание, характеризующееся системным поражением мелких сосудов, геморрагическим диатезом, гемодинамическими расстройствами и своеобразным поражением почек по типу острого интерстициального нефрита с развитием острой почечной недостаточности. Заболевание нередко протекает с опасными для жизни осложнениями – инфекционно-токсическим шоком (ИТШ), острой почечной недостаточностью (ОПН), кровоизлияниями в жизненно-важные органы, ДВС-синдромом, спонтанными разрывами капсулы почек и др. Один из активных очагов ГЛПС ежегодно регистрируется в Республике Башкортостан, поддерживая заболеваемость в Российской Федерации на высоком уровне. Существует прямая зависимость заболеваемости человека от численности грызунов, прежде всего, основного источника инфекции – рыжей полевки. Заражение чаще всего происходит при кратковременном посещении лесных территорий (туризм, охота, рыбная ловля, сбор грибов, ягод, ночевки в лесу, сенокос) с выраженным сезонным характером – с мая по ноябрь. Наблюдается высокий тропизм возбудителей к эндотелию сосудов. Из мест внедрения вирус проникает в кровь, затем в эндотелий сосудов с развитием геморрагического капилляротоксикоза, с возникновением имунокомплексного васкулита с полиорганным поражением.
Широкая распространенность ГЛПС требует дифференцированного отношения к больным, пребывавших в эндемичных районах, для своевременного оказания специфического и патогенетического лечения и профилактики грозных осложнений. Отсутствие на сегодня эффективных лабораторных диагностикумов на ранних этапах развития болезни, стандартных схем этиотропного лечения и профилактики определяет крайнюю актуальность рассмотрения вопросов ранней клинической диагностики и своевременного раннего назначения противовирусных препаратов в лихорадочный период до наступления разгара заболевания, когда данные препараты неэффективны.
Начальный (лихорадочный) период соответствует вирусемии, токсинемии и гематогенной диссеминации и длится первые 5 дней от начала болезни. За время многолетнего наблюдения за больными ГЛПС в клинике инфекционной больницы № 4 мы выделяем следующие характерные признаки начального периода болезни, на которые врачи первичного звена должны обратить внимание.
Заболевание начинается, как правило, остро с повышения температуры тела до 38-39º С в течение 3 – 7 дней. У больных с тяжелой формой заболевания лихорадка может продолжаться до 2-х недель. Лихорадке сопутствуют головные боли, боль в глазных яблоках, слабость, боли в мышцах, суставах, выраженная сухость во рту. К 3 – 4-му дню болезни состояние ухудшается. Интоксикация усиливается. Больной вялый, заторможенный; возможен бред, многократная рвота, диарея. Выраженность симптомов интоксикации находится в прямой зависимости от степени тяжести заболевания. Признаков воспаления верхних дыхательных путей не отмечается, хотя в начале заболевания иногда отмечается першение в горле, кратковременное покашливание. Характерными являются жалобы на боли в глазных яблоках и снижение остроты зрения («туман», «мушки» перед глазами), которые бывают кратковременными и бесследно исчезают через 1-5 дней. Возможны образование геморрагических «корочек» в носовых ходах, скудные кровянистые выделения из носа. У больных с тяжелой формой уже в начальном периоде присоединяются боли в области поясницы и животе, рвота, жидкий стул, уменьшение объема диуреза.
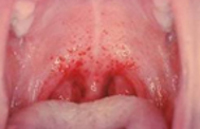
При осмотре больных отмечается гиперемия кожи лица, шеи, верхних отделов живота. Слизистая оболочка зева гиперемирована, сосуды склер инъецированы, на фоне гиперемированных конъюнктив иногда можно заметить петехиальную сыпь. Со 2 – 3-го дня болезни у большинства больных обнаруживается на слизистой оболочке мягкого неба геморрагическая энантема, а с 3 – 5-го дня у части больных – линейная петехиальная сыпь в подмышечных впадинах, на груди, в области ключиц, иногда на шее, лице. Со стороны внутренних органов в начальном периоде особых изменений выявить не удается. Возможна умеренная брадикардия, у некоторых больных тупые боли в пояснице, положительный симптом поколачивания по поясничной области с двух сторон. Относительно редко при тяжелых формах могут быть явления менингизма. На 4 – 6 день болезни, особенно при нарушении лечебно-охранительного режима (физический труд, посещение бани, злоупотребление алкоголем) возрастает риск развития ИТШ.
Дифференцировать в начальном периоде ГЛПС необходимо чаще всего с острой респираторной вирусной инфекцией, острой кишечной инфекцией, крупозной пневмонией, острым или обострением хронического пиелонефрита, острой хирургической патологией. Заподозрить ГЛПС позволяет в первую очередь сезонность и подробный эпидемиологический анамнез.
В гемограмме в этот период выявляется нормоцитоз или лейкопения с нейтрофильным сдвигом влево (в олиганурический период – лейкоцитоз), умеренная тромбоцитопения, повышение числа эритроцитов и уровня гемоглобина. Увеличение эритроцитов и гемоглобина в первые дни болезни является результатом сгущения крови в связи интенсивной плазморреи в ткани. В общем анализе мочи можно обнаружить небольшое количество свежих эритроцитов, клетки почечного эпителия. Белок в этот период может отсутствовать или определяется в небольшом количестве. В начальном периоде заболевания суточный диурез существенно не меняется.
Необходима наиболее ранняя госпитализация – в начале лихорадочного периода, в первые три дня болезни. Транспортировка пациентов должна быть максимально щадящей, с обязательным сопровождением медицинского персонала. Нужно стараться избегать тряской езды с целью предупреждения усиления болевого синдрома, нарушения гемодинамики, развития спонтанных субкапсульных разрывов коркового вещества почки и кровоизлияния в околопочечную клетчатку. Так, по данным ИКБ №4 г. Уфы, основная масса больных госпитализируется в первые пять дней болезни. Недопустимо амбулаторное наблюдение больного с подозрением на ГЛПС. В начальном лихорадочном периоде болезни основными принципами лечения являются: противовирусная терапия, дезинтоксикационная, профилактика ДВС-синдрома, ИТШ.
Этиотропное лечение может проводиться с использованием двух основных подходов: иммунобиологическими средствами и химиопрепаратами. Известно, что формирование различных клинических форм и исходов любого инфекционного заболевания во многом зависят от силы и продолжительности иммунного ответа организма. Положительное влияние на иммунологическое звено патогенеза оказывают препараты иммуноглобулина. Доказана эффективность применения донорского специфического иммуноглобулина против ГЛПС с высоким титром антител 1:1024 – 1:2048, изготовленного ГУП «Иммунопрепарат» [3,6], к сожалению, широкого применения в практике лечения ГЛПС не имеет.
Система интерферона (ИФН) значительно опережает ответ иммунной системы в отличие от антител, способных нейтрализовать лишь гомологичный вирус. Интерфероны активно подавляют продукцию большинства известных вирусов, формируя защитный барьер, активируют систему естественной цитотоксичности, функцией которой является лизис пораженных вирусом клеток, благодаря чему создается антивирусный эффект. Была доказана эффективность применения лейкоцитарного интерферона в свечах по 30.000 МЕ 3-4 раза в течение 4-5 дней [2, 9].
В литературе имеются данные эффективного применения рибавирина при лечении ГЛПС, который вводится инфузионно по 700-750 мг/сут в течение 3 дней, что приводит к более раннему снижению лихорадки и исчезновению клинических и лабораторных сдвигов [6, 8]. Нами был апробирован отечественный аналог рибавирина – рибамидил, который назначается в таблетках по 0,2 г 4-5 раз в сутки в течение 5 дней. Терапия рибамидилом приводил к сокращению продолжительности лихорадки (4,43±0,40 и 7,21±0,44 дня), достоверно меньшей интоксикации, значительно снижался геморрагический синдром, показатели мочевины и креатинина в олигоанурическом периоде были достоверно ниже (p < 0,001). Препарат оказывал положительное действие на тромбоцитарно-сосудистый гемостаз [6].
Проводилось изучение лечебной эффективности отечественного препарата рекомбинантного интерферона альфа 2в в свечах – виферона [4]. Препарат назначается до 5-го дня болезни по 500 тыс. МЕ и 1 млн. МЕ 2 раза в сутки с интервалом 12 часов в течение 5 дней, затем на 7, 9, 11, 13, 15 дни от начала интерферонотерапии. Результаты исследования показали, что включение виферона в комплексную терапию больных среднетяжелой и тяжелой формы ГЛПС до 5-го дня болезни стимулировало α- и γ-интерфероногенез, клеточные факторы иммунитета, фагоцитоз, что сопровождалось укорочением длительности и выраженности основных клинических симптомов болезни [4].
Современным направлением в клинической иммунопатологии является разработка иммуномодуляторов нового класса – индукторов синтеза интерферона. Применение индукторов ИФН имеет ряд преимуществ перед введением экзогенных ИФН. Индукторы стимулируют выработку собственных интерферонов, которые не обладают антигенностью.
В целях поиска альтернативных путей коррекции иммунного интерферонового статуса было проведено изучение терапевтической эффективности нового препарата – йодантипирина (1-фенил-2,3-диметил-4 йодпиразолон-5). Йодантипирин является активным индуктором альфа- и бета- интерферонов, существенно повышает активность фибробластов и индуцирует их антивирусную резистентность, задерживает проникновение вируса в клетку за счет стабилизирующего действия на биологические мембраны, значительно стимулирует продукцию антител. Препарат назначается по 0,2 г 3 раза в день в течение первых 4-х дней, затем 0,1 г 3 раза в день в течение следующих 5 дней. Курсовая доза составляет 4,5 г (45 таблеток). Исследование клинической эффективности применения йодантипирина при ГЛПС показало положительное влияние на течение болезни, сокращение продолжительности интоксикационного и болевого синдрома, ускоренное восстановление параметров клеточного иммунитета, повышение способности лейкоцитов продуцировать альфа-интерферон [7]. Нами в настоящее время апробируется новый современный препарат интерферона α-2β – лайфферон. У этого препарата высокая степень очистки, из состава исключен альбумин, применяемый для стабилизации, вместо которого применен твин-80 и ЭДТА, в связи с этим производители гарантируют меньшую токсичность препарата и высокую иммуномодулирующую активность. По предварительным данным препарат эффективен в первые 3 дня заболевания, с 5-го дня болезни назначение данного препарата не влияло на течение ГЛПС. Для окончательных выводов необходимо продолжить клиническую апробацию препарата.
Выводы. Эффективность лечения больных ГЛПС в первую очередь зависит от правильной первичной диагностики и ранней госпитализации. Этиотропная терапия до настоящего времени окончательно не разработана и широко не применяется. Учитывая ведущее значение в патогенезе иммунных нарушений, перспективной является иммунокорригирующая терапия. Ускоренная элиминация вируса отмечена при лечении препаратами α-интерферона и специфического иммуноглобулина. Доказана лечебно-профилактическая эффективность индукторов интерферона – амиксина, йодантипирина, виферона.
Библиографическая ссылка
Хунафина Д.Х., Валишин Д.А., Шайхуллина Л.Р., Галиева А.Т. ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА С ПОЧЕЧНЫМ СИНДРОМОМ (ОБЗОР ЛИТЕРАТУРЫ) // Международный журнал экспериментального образования. – 2014. – № 8-1. – С. 14-17;
URL: https://expeducation.ru/ru/article/view?id=5781 (дата обращения: 26.11.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
Геморрагическая лихорадка с почечным синдромом – зоонозная хантавирусная инфекция, характеризующаяся тромбогеморрагическим синдромом и преимущественным поражением почек. Клинические проявления включают острую лихорадку, геморрагическую сыпь, кровотечения, интерстициальный нефрит, в тяжелых случаях – острую почечную недостаточность. К специфическим лабораторным методам диагностики геморрагической лихорадки с почечным синдромом принадлежат РИФ, ИФА, РИА, ПЦР. Лечение заключается во введении специфического иммуноглобулина, препаратов интерферона, проведении дезинтоксикационной и симптоматической терапии, гемодиализа.
Общие сведения
Геморрагическая лихорадка с почечным синдромом (ГЛПС) – природно-очаговое вирусное заболевание, характерными признаками которого являются лихорадка, интоксикация, повышенная кровоточивость и поражение почек (нефрозонефрит). На территории нашей страны эндемичными районами являются Дальний Восток, Восточная Сибирь, Забайкалье, Казахстан, европейская территория, поэтому ГЛПС известна под различными названиями: корейская, дальневосточная, уральская, ярославская, тульская, закарпатская геморрагическая лихорадка и др. Ежегодно в России регистрируется от 5 до 20 тыс. случаев заболеваний геморрагической лихорадкой с почечным синдромом. Пик заболеваемости ГЛПС приходится на июнь-октябрь; основной контингент заболевших (70-90%) составляют мужчины в возрасте 16-50 лет.

Геморрагическая лихорадка с почечным синдромом
Причины ГЛПС
Возбудителями болезни являются РНК-содержащие вирусные агенты рода Hantavirus (хантавирусы), относящиеся к семейству Bunyaviridae. Для человека патогенны 4 серотипа хантавирусов: Hantaan, Dubrava, Puumala, Seoul. Во внешней среде вирусы относительно долго сохраняют стабильность при отрицательной температуре и малоустойчивы при температуре 37°C. Вирусы имеют сферическую или спиральную форму, диаметр 80-120 нм; содержат одноцепочечную РНК. Хантавирусы обладают тропностью к моноцитам, клеткам почек, легких, печени, слюнных желез и размножаются в цитоплазме инфицированных клеток.
Переносчиками возбудителей геморрагической лихорадки с почечным синдромом служат грызуны: полевые и лесные мыши, полевки, домовые крысы, которые инфицируются друг от друга через укусы клещей и блох. Грызуны переносят инфекцию в форме латентного вирусоносительства, выделяя возбудителей во внешнюю среду со слюной, фекалиями и мочой. Попадание инфицированного выделениями грызунов материала в организм человека может происходить аспирационным (при вдыхании), контактным (при попадании на кожу) или алиментарным (при употреблении пищи) путем. К группе повышенного риска по заболеваемости геморрагической лихорадкой с почечным синдромом относятся сельскохозяйственные и промышленные рабочие, трактористы, водители, активно контактирующие с объектами внешней среды. Заболеваемость человека напрямую зависит от численности инфицированных грызунов на данной территории. ГЛПС регистрируется преимущественно в виде спорадических случаев; реже – в виде локальных эпидемических вспышек. После перенесенной инфекции остается стойкий пожизненный иммунитет; случаи повторной заболеваемости единичны.
Патогенетическую сущность геморрагической лихорадки с почечным синдромом составляют некротизирующий панваскулит, ДВС-синдром и острая почечная недостаточность. После заражения первичная репликация вируса происходит в эндотелии сосудов и эпителиальных клетках внутренних органов. Вслед за накоплением вирусов наступает вирусемия и генерализация инфекции, которые клинически проявляются общетоксическими симптомами. В патогенезе геморрагической лихорадки с почечным синдромом большую роль играют образующиеся аутоантитела, аутоантигены, ЦИК, оказывающие капилляротоксическое действие, вызывающие повреждение стенок сосудов, нарушение свертываемости крови, развитие тромбогеморрагического синдрома с повреждением почек и других паренхиматозных органов (печени, поджелудочной железы, надпочечников, миокарда), ЦНС. Почечный синдром характеризуется массивной протеинурией, олигоанурией, азотемией, нарушением КОС.
Симптомы ГЛПС
Геморрагическая лихорадка с почечным синдромом характеризуется циклическим течением с последовательной сменой нескольких периодов:
- инкубационного (от 2-5 дней до 50 суток – в среднем 2-3 недели)
- продромального (2-3 дня)
- лихорадочного (3-6 дней)
- олигоурического (с 3-6-го по 8-14-й день ГЛПС)
- полиурического (с 9-13 дня ГЛПС)
- реконвалесцентного (раннего – от 3-х недель до 2 месяцев, позднего – до 2-3-х лет).
В зависимости от выраженности симптомов, тяжести инфекционно-токсического, геморрагического и почечного синдромов различают типичные, стертые и субклинические варианты; легкие, среднетяжелые и тяжелые формы геморрагической лихорадки с почечным синдромом.
По истечении инкубационного периода наступает короткий продромальный период, во время которого отмечаются утомляемость, недомогание, головные боли, миалгии, субфебрилитет. Лихорадочный период развивается остро, с повышения температуры тела до 39-41°С, озноба и общетоксических симптомов (слабости, головной боли, тошноты, рвоты, расстройства сна, артралгии, ломоты в теле). Характерны боли в глазных яблоках, затуманенное зрение, мелькание «мушек», видение предметов в красном цвете. В разгар лихорадочного периода появляются геморрагические высыпания на слизистых оболочках полости рта, коже грудной клетки, подмышечных областей, шеи. При объективном осмотре выявляется гиперемия и одутловатость лица, инъекция сосудов конъюнктив и склер, брадикардия и артериальная гипотония вплоть до коллапса.
В олигоурический период геморрагической лихорадки с почечным синдромом температура тела снижается до нормы или субфебрильных цифр, однако это не приводит к улучшению состояния пациента. В эту стадию еще более усиливаются симптомы интоксикации и возникают признаки поражения почек: нарастают боли в пояснице, резко снижается диурез, развивается артериальная гипертензия. В моче выявляется гематурия, протеинурия, цилиндрурия. При нарастании азотемии развивается ОПН; в тяжелых случаях – уремическая кома. У большинства больных отмечается неукротимая рвота и диарея. Геморрагический синдром может быть выражен в различной степени и включать в себя макрогематурию, кровотечения из мест инъекций, носовые, маточные, желудочно-кишечные кровотечения. В олигоурический период могут развиваться тяжелые осложнения (кровоизлияния в головной мозг, гипофиз, надпочечники), служащие причиной летального исхода.
Переход геморрагической лихорадки с почечным синдромом в полиурическую стадию знаменуется субъективными и объективными улучшениями: нормализацией сна и аппетита, прекращением рвоты, исчезновением боле в пояснице и т. д. Характерными признаками данного периода служит увеличение суточного диуреза до 3-5 л и изогипостенурия. В период полиурии сохраняется сухость во рту и жажда.
Период реконвалесценции при геморрагической лихорадке с почечным синдромом может затягиваться на несколько месяцев и даже лет. У больных долго сохраняется постинфекционная астения, характеризующаяся общей слабостью, снижением работоспособности, быстрой утомляемостью, эмоциональной лабильностью. Синдром вегетативной дистонии выражается гипотонией, инсомнией, одышкой при минимальной нагрузке, повышенной потливостью.
Специфическими осложнениями тяжелых клинических вариантов ГЛПС могут являться инфекционно-токсический шок, кровоизлияния в паренхиматозные органы, отек легких и головного мозга, кровотечения, миокардит, менингоэнцефалит, уремия и др. При присоединении бактериальной инфекции возможно развитие пневмонии, пиелонефрита, гнойных отитов, абсцессов, флегмон, сепсиса.
Диагностика ГЛПС
Клиническая диагностика ГЛПС основывается на цикличности течения инфекции и характерной смене периодов. При сборе эпидемиологического анамнеза обращается внимание на пребывание пациента в эндемичной местности, возможный прямой или косвенный контакт с грызунами. При проведении неспецифического обследования учитывается динамика изменения показателей общего и биохимического анализа мочи, электролитов, биохимических проб крови, КОС, коагулограммы и др. С целью оценки тяжести течения и прогноза заболевания выполняется УЗИ почек, ФГДС, рентгенография органов грудной клетки, ЭКГ и др.
Специфическая лабораторная диагностика геморрагической лихорадки с почечным синдромом проводится с помощью серологических методов (ИФА, РНИФ, РИА) в динамике. Антитела в сыворотке крови появляются в конце 1-ой недели болезни, к концу 2-й недели достигают максимальной концентрации и сохраняются в крови 5–7 лет. РНК вируса может быть выделена с помощью ПЦР-исследования. ГЛПС дифференцируют с лептоспирозом, острым гломерулонефритом, пиелонефритом и энтеровирусной инфекцией, прочими геморрагическими лихорадками.
Лечение ГЛПС
Больные геморрагической лихорадкой с почечным синдромом госпитализируются в инфекционный стационар. Им назначается строгий постельный режим и диета №4; проводится контроль водного баланса, гемодинамики, показателей функционирования сердечно-сосудистой системы и почек. Этиотропная терапия геморрагической лихорадки с почечным синдромом наиболее эффективна в первые 3-5 суток от начала заболевания и включает введение донорского специфического иммуноглобулина против ГЛПС, назначение препаратов интерферона, противовирусных химиопрепаратов (рибавирина).
В лихорадочном периоде проводится инфузионная дезинтоксикационная терапия (внутривенные вливания глюкозы и солевых растворов); профилактика ДВС-синдрома (введение препаратов-дезагрегантов и ангиопротекторов); в тяжелых случаях применяются глюкокортикостероиды. В олигурическом периоде осуществляется стимуляция диуреза (введение ударных доз фуросемида), коррекция ацидоза и гиперкалиемии, профилактика кровотечений. При нарастающей ОПН показано переведение пациента на экстракорпоральный гемодиализ. При наличии бактериальных осложнений назначается антибиотикотерапия. В полиурическую стадию основной задачей является проведение оральной и парентеральной регидратации. В период реконвалесценции проводится общеукрепляющая и метаболическая терапия; рекомендуется полноценное питание, физиотерапия (диатермия, электрофорез), массаж и ЛФК.
Прогноз и профилактика ГЛПС
Легкие и среднетяжелые формы геморрагической лихорадки с почечным синдромом в большинстве случаев заканчиваются выздоровлением. Резидуальные явления (постинфекционная астения, боли в пояснице, кардиомиопатия, моно- и полиневриты) длительно наблюдаются у половины переболевших. Реконвалесценты нуждаются в ежеквартальном диспансерном наблюдении инфекциониста, нефролога и окулиста на протяжении года. Тяжелое течение сопряжено с высоким риском осложнений; смертность от ГЛПС колеблется в пределах 7-10%.
Профилактика геморрагической лихорадки с почечным синдромом заключается в уничтожении мышевидных грызунов в природных очагах инфекции, предупреждении загрязнения жилищ, водоисточников и продуктов питания выделениями грызунов, дератизации жилых и производственных помещений. Специфической вакцинации против ГЛПС не разработано.
Источник
