Инфаркт миокарда резорбционно некротический синдром

Диагностика инфаркта миокарда. Резорбционно-некротический синдром инфаркта миокарда.
Приведенные выше основные клинические варианты инфаркта миокарда, несмотря на их разнообразие, характеризуются достаточно четкими изменениями лабораторно-биохимических показателей в связи с некробиотическими изменениями, обусловленными распадом мышечных волокон сердца и всасыванием продуктов аутолитического расщепления белковых веществ. Некробиотический синдром нередко запаздывает по сравнению с клиникой ИМ, но в то же время он является достоверным признаком этой патологии. Поэтому в плане обследования больного врач должен предусмотреть и выявление этих признаков.
К резорбционно-некротическому синдрому относятся клинические, электрокардиографические признаки и данные ферментной диагностики.
– Клинические данные: субфебрильная лихорадка (редко до 38,5°С) в течение 5-7 дней, обычно со второго дня болезни. Это важный и легкообнаруживаемый симптом, часто позволяет отличить инфаркт миокарда от приступа грудной жабы.
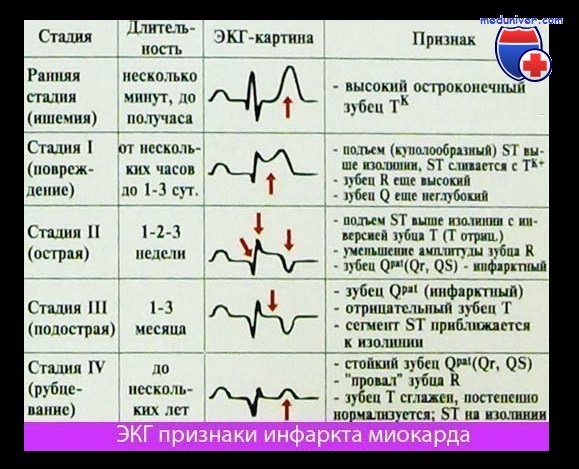
– Электрокардиографическая диагностика ИМ
– Главные ЭКГ признаки ОИМ:
1. Появление новых зубцов Q шириной более 30 мсек и глубиной более 2 мм по крайней мере в 2-х отведениях:
• II, III или avF;
• V1-V6 отведениях;
• 1 и avL отведениях.
2. Новые подъемы или депрессия сегмента ST-T более 1 мм через 20 мсек после точки J в двух смежных отведениях.
3. Появление полной блокады левой ножки пучка Гиса при наличии соответствующей клиники.
Так, при помощи ЭКГ можно, как правило, диагностировать ИМ в первые часы его развития (более чем в 90% случаев).
Отсутствие на ЭКГ признаков инфаркта миокарда не является основанием отвергать этот диагноз или отказывать в госпитализации, если у больного имеются соответствующие клинические проявления заболевания. Иногда ЭКГ признаки ИМ появляются не сразу – ЭКГ-картина инфаркта миокарда может запаздывать во времени – лишь через несколько и даже через 10-20 дней (был интрамуральный инфаркт миокарда затем трансформировался в трансмуральный) или ЭКГ не дает полного комплекса изменений – наблюдается только инвертированный зубец Т или смещение ST при отсутствии зубца Q или ЭКГ при ИМ, на которых проявляются блокады ножки, нарушения атриовентрикулярной проводимости без типичных ЭКГ признаков ИМ.
– Лабораторная диагностика инфаркта миокарда
асептического воспаления (лейкоцитоз, с нейтрофильным сдвигом – в течение 5-7 дней), повышение СОЭ – через 1-2 дня после повышения температуры и количества лейкоцитов; С-реактивный белок.
– Ферментная диагностика инфаркта миокарда
МБ-КФК и тропонины являются наиболее информативными биохимическими критериями инфаркта миокарда. Через сутки после болевого синдрома их информативность значительно снижается.
– Тропонины.У больных инфарктом миокарда уровень тропонинов повышается через 3-6 часов от начала болевого приступа и сохраняется повышенным в течение 7-10 дней (на протяжении этого периода продолжаются процессы дезинтеграции миокарда и поступление тропонинов в кровь). Тропонины обладают высокой специфичностью и чувствительностью. Можно использовать для диагностики ИМ в течение 2 недель от начала болевого приступа. Низкая чувствительность в течение первых 6 часов от начала приступа. В случае отрицательного ответа теста в первые сутки необходимо повторное проведение исследования. Они имеют большое значение для диагностики ИМ без подъема сегмента ST. Нельзя использовать для диагностики рецидива ИМ.
– КФК-МВ – нельзя использовать в периоды до 6 часов и спустя 36 часов от начала болевого приступа. Можно применять для выявления рецидивов инфаркта.
– Миоглобин является наиболее ранним признаком повреждения миокарда – его уровень повышается в крови через 1-2 часа от начала болевого приступа и остается повышенным в течение 24 часов. Отрицательный тест через 4-8 часов от начала болевого приступа позволяет исключить ИМ. Можно применять для выявления рецидивов инфаркта миокарда.
– Лактатдегидрогеназа повышается через 8-10 часов после приступа и достигает максимума через 24-48 часов.
– Аспартат-аминотрансфераза – максимальная активность наблюдается в конце первых и на вторые сутки заболевания.
Как следует из приведенных сведений, диагностическая значимость этих показателей различна.
Учитывая запаздывание (отставание от клинической картины) некробиотического синдрома, тактика врача заключается в обязательной госпитализации больного для подтверждения или исключения ИМ. В противном случае возможны непоправимые диагностические ошибки, ведущие к неблагоприятному исходу. В таких случаях должен срабатывать предписываемый нами принцип лечебно-диагностической тактики: думать и исключать более тяжелую патологию.
По течению можно выделить инфаркт миокарда неосложненный и осложненный.
– Также рекомендуем “Осложнения инфаркта миокарда в остром периоде. Отек легких при инфаркте миокарда.”
Оглавление темы “Неотложная помощь в при инфаркте миокарда.”:
1. Купирование ангинозного приступа. Неотложная помощь при болях в сердце.
2. Инфаркт миокарда. Пути развития инфаркта миокарда.
3. Клинические варианты инфаркта миокарда. Клиника инфаркта миокарда.
4. Церебральный вариант инфаркта миокарда. Безболевой вариант инфаркта миокарда. Аритмический, отечный вариант инфаркта миокарда.
5. Диагностика инфаркта миокарда. Резорбционно-некротический синдром инфаркта миокарда.
6. Осложнения инфаркта миокарда в остром периоде. Отек легких при инфаркте миокарда.
7. Кардиогенный шок. Гиповолемия при инфаркте миокарда.
8. Нарушения ритма и проводимости при инфаркте миокарда. Желудочковая экстрасистолия при инфаркте миокарда.
9. Нарушение проводимости при инфаркте миокарда. Тромбоэмболии при инфаркте миокарда. Синдром Дресслера.
10. Лечение инфаркта миокарда. Лечение болей при инфаркте миокарда.
Источник
Инфаркт миокарда
Резорбционно-некротический синдром является одним из основных проявлений острого периода инфаркта миокарда. Он обусловлен резорбцией некротических масс и развитием асептического воспаления в зоне некроза.
Важнейшие признаки резорбционно-некротического синдрома: повышение температуры тела; лейкоцитоз; увеличение СОЭ; появление «биохимических признаков воспаления»; появление в крови биохимических маркеров гибели кардиомиоцитов.
Подъем температуры тела обычно отмечается на 2—3-й день, она достигает величины 37,1—37,9 °С, иногда превышает 38°С. Длительность повышения температуры тела около 3—7 дней, при обширном трансмуральном инфаркте миокарда лихорадка может продолжаться до 10 дней. Более продолжительный субфебрилитет может свидетельствовать о развитии осложнений — тромбэндокардита, пневмонии, перикардита, или о затяжном течении инфаркта миокарда. Величина температуры тела и длительность ее повышения в определенной мере зависят от обширности некроза и возраста больных. При распространенном инфаркте миокарда и более молодом возрасте повышение температуры тела более значительное и продолжительное, чем при мелкоочаговом инфаркте и у лиц пожилого возраста. При осложнении инфаркта кардиогенным шоком температура тела может оказаться даже сниженной.
Повышение количества лейкоцитов в крови при данном заболевании обусловлено развитием асептического воспаления в зоне некроза и повышением глюкокортикоидной функции надпочечников. Лейкоцитоз развивается уже через 3—4 ч, достигает максимума на 2—4-й день и сохраняется около 3—7 дней. Более длительное сохранение лейкоцитоза свидетельствует о затяжном течении инфаркта, появлении новых очагов некроза, развитии осложнений, присоединении пневмонии. Обычно количество лейкоцитов повышается до 10—12 х 109/л, при распространенном и трансмуральном инфаркте — до 15 х 109/л и даже выше. Лейкоцитоз более 20 х 109/л обычно является неблагоприятным прогностическим фактором. Лейкоцитоз сопровождается сдвигом лейкоцитарной формулы влево. В первые дни болезни можно отметить полное исчезновение из крови эозинофилов, в дальнейшем, по мере улучшения состояния больного, количество эозинофилов в крови нормализуется.
Основным фактором, определяющим увеличение СОЭ, является белковый состав крови. Увеличение в крови количества белковых молекул снижает отрицательный заряд, способствующий отталкиванию эритроцитов и поддержанию их во взвешенном состоянии. Наибольшее влияние на увеличение СОЭ оказывают фибриноген, иммуноглобулины, гаптоглобин. Увеличение СОЭ отмечается со 2— 3-го дня, достигает максимума между 8—12-м днем, затем постепенно снижается, и чёрез 3—4 недели СОЭ нормализуется. Характерным при инфаркте миокарда считается феномен «ножниц» между лейкоцитозом и СОЭ: в конце 1-й—начале 2-й недели лейкоцитоз начинает снижаться, а СОЭ возрастает.
При инфаркте миокарда в крови возрастает уровень неспецифических показателей некроза и асептического воспаления, получивших образное название «биохимических маркеров воспаления». Речь идет о повышении содержания в крови фибриногена, серомукоида, гаптоглобина.
Появление в крови биохимических маркеров гибели кардиомиоцитов. При инфаркте миокарда из кардиомиоцитов выходят различные ферменты, белковые молекулы — компоненты мышечных волокон. Они поступают в межклеточную жидкость, оттекают от сердца по лимфатическим путям и далее поступают в кровь, являясь, таким образом, маркерами некроза миокарда. К маркерам гибели кардиомиоцитов относятся ферменты АсТ, ЛДГ, креатинфосфокиназа (КФК), гликогенфосфорилаза (ГФ), а также миоглобин, миозин, кардиотропонины. Указанные вещества поступают в кровь при некрозе не только миокарда, но и скелетной мускулатуры. От момента гибели кардиомиоцитов до появления маркеров в крови проходит определенный период, характерный для каждого маркера. Длительность данного периода зависит от величины белковых молекул-маркеров, обширности и продолжительности некроза миокарда. Вначале повышается концентрация в крови миоглобина, тропонина Т, далее — КФК, ее изофермента КФК-МВ, АсТ; позже увеличивается уровень в крови ЛДГ и ее изофермента ЛДГ-1.
Другой характерной особенностью маркеров гибели кардиомиоцитов является характерная для каждого маркера динамика повышения и снижения его концентрации. Объясняется это тем, что миокард постоянно сокращается — это приводит к быстрой элиминации белков-маркеров из участка некроза, а затем и к полному вымыванию этих белков в кровь.
Определение содержания в крови миоглобина. Миоглобин — гемсодержащий хромопротеид, представляющий собой легкую цепь миозина. Миоглобин транспортирует кислород в скелетной мускулатуре и миокарде, он идентичен в миоцитах скелетных мышц и кардиомиоцитах, Миоглобин постоянно присутствует в плазме крови в связанном с белками состоянии. Содержание миоглобина в крови в норме составляет: у мужчин — 22— 66 мкг/л, у женщин — 21—49 мкг/л или 50—85 нг/мл. При повреждении миокарда или скелетной мускулатуры миоглобин поступает в кровь и затем выделяется с мочой.
Кинетика миоглобина при инфаркте миокарда
1) Повышение содержания миоглобина в крови начинается через 2—3 ч;
2) максимальный уровень миоглобина в крови наблюдается через 6—10 ч от начала инфаркта;
3) длительность повышения содержания миоглобина в крови составляет 24—32 ч.
Чувствительность миоглобинового теста колеблется от 50 до 100%. Уровень миоглобина в крови может повышаться при инфаркте в 10—20 раз. Повторное повышение уровня миоглобина в крови на фоне уже наступающей нормализации может указывать на расширение зоны некроза или образование новых некротических очагов.
Определение содержания в крови легких и тяжелых цепей миозина. В миофибриллах содержатся белки миозин, актин, актомиозин, тропомиозин, тропонин, а— и в-актинин. Все перечисленные белки связаны с сократительной функцией мышц.
Определение активности общей КФК в сыворотке крови. КФК катализирует обратимое фосфорилирование креатина с участием АДФ. Наибольшее количество КФК содержится в сердечной мышце, скелетной мускулатуре, менее богаты этим ферментом головной мозг, щитовидная железа, матка, легкие.
Содержание в сыворотке крови общей КФК в норме составляет 10-195 МЕ/л.
Окончание >>>
Источник
Общие сведения
Трансмуральный инфаркт миокарда — одна из самых тяжелых, жизнеугрожающих патологий сердца, уже многие годы остающаяся ведущей причиной смерти больных с сердечно-сосудистыми заболеваниями. Госпитальная смертность достигает 10%, а в некоторых регионах России 15%. В течение года после интенсивной терапии умирает еще около 10%. Половина больных с тяжелой формой кардиального некроза погибает на догоспитальном этапе. Мужчины 40-60 лет болеют чаще женщин, пик заболеваемости отмечается после 50 лет. Основная группа пациентов — люди с сопутствующим сахарным диабетом, гиперлипидемией, отягощенным семейным анамнезом.

Трансмуральный инфаркт миокарда
Причины
Подавляющее большинство случаев инфаркта миокарда является следствием окклюзии главного ствола или ветви коронарной артерии. Процесс сопровождается значительным ухудшением снабжения кровью сердечной мышцы. При увеличении нагрузки на кардиальную мышцу она начинает испытывать гипоксию, ее функции снижаются, что приводит к последующему некрозу. В рамках современной медицины выделяют несколько причин сужения просвета венечных сосудов:
- Атеросклероз. Ведущий фактор развития инфаркта, обнаруживаемый у 95% людей, умерших от крупноочаговых процессов. Частый признак — высокий уровень липидов крови. Перекрытие диаметра артерии более чем на 75% вызывает отмирание тканей.
- Тромбоз. Флотирующие образования в кровотоке могут попадать в коронарные сосуды двумя путями: из левого желудочка, в котором образуются в результате фибрилляции предсердий и клапанных патологий, либо при незакрытом овальном окне.
К факторам риска развития инфаркта относят отягощенную наследственность (сердечно-сосудистые заболевания у ближайших родственников), возраст старше 50 лет, многолетний стаж курения. Провоцировать отложение липидов в стенках сосудов может ожирение, недостаточная физическая активность. Группу риска составляют пациенты с установленной артериальной гипертензией, сахарным диабетом, системными заболеваниями (особенно васкулитами).
Патогенез
Трансмуральный инфаркт развивается вследствие нарушения кровоснабжения сердечной мышцы. Адекватность коронарного кровотока запросам миокарда определяется наполненностью венечных артерий, которое зависит от аортального давления и сосудистого сопротивления, насыщенности кислородом, колеблющейся в зависимости от нагрузки на сердце и частоты его сокращений, а также составом плазмы и форменных элементов, меняющемся при гипогидратации, анемиях, токсических отравлениях. Любое нарушение баланса приводит сначала к ишемии, затем к омертвлению кардиальных клеток.
Крупноочаговый характер патологии практически всегда находит отражение в интенсивном болевом синдроме. Это связано с массивным поражением кардиальной мышцы, активацией большого количества болевых рецепторов, значительным снижением ее функции. Массивный очаг некроза может стать причиной попадания в кровь большого количества продуктов распада (миоглобин, тропонины) с развитием системного воспалительного ответа — резорбционно-некротического синдрома.
Симптомы
Трансмуральный инфаркт миокарда обычно имеет выраженную клиническую картину. Наиболее характерным симптомом является интенсивная боль, способная иррадиировать в левую сторону тела — руку, шею, спину, челюсть. Кардиалгия при данной патологии напоминает хорошо знакомый пациентам с заболеваниями сердечно-сосудистой системы приступ стенокардии, но, в отличие от него, крайне сложно купируется, длится более 20 минут.
Применение нитроглицерина, оправданное в большинстве случаев, не дает должного эффекта даже после трех таблеток. Также малоэффективно изменение положения тела, подача свежего воздуха, холодное питье. Помимо боли пациенты могут ощущать головокружение, тошноту вплоть до рвоты. При выраженной сердечной недостаточности на фоне инфаркта появляется одышка, особенно выраженная у женщин. Поражение массивного участка миокарда приводит к нарушению проведения импульса, тахикардии, экстрасистолии, различным блокадам. К общим признакам относят холодный пот, угнетение сознания или эмоциональное возбуждение, выраженную слабость.
Ретроспективно диагностируется около 50% случаев патологии, особенно у пожилых людей или больных сахарным диабетом на фоне развившейся нейропатии, в состоянии после трансплантации сердца. В подобных случаях инфаркт начинается без боли в грудной клетке, поэтому второстепенные признаки приобретают ведущую роль. Нетипичная манифестация может включать в себя инсульт, острый психоз, расстройства пищеварения, периферические эмболии.
Если к общему состоянию присоединяется резорбционно-некротический синдром, к прочим симптомам добавляется повышение температуры тела до 38-39° С на протяжении более 5-7 дней, лейкоцитоз до 15х109/л с преобладанием нейтрофильной фракции. В анализе крови обнаруживается высокая скорость оседания эритроцитов в течение нескольких недель, анэозинофилия. Больные отмечают озноб, сменяющийся жаром, потливость, выраженную слабость.
Осложнения
Трансмуральный инфаркт миокарда способен привести к целому ряду жизнеугрожающих состояний. Самое частое осложнение — нарушения ритма сердца вплоть до фибрилляции желудочков. Нередко наблюдается сердечная недостаточность, обычно – левожелудочковая, сопровождающаяся хрипами, сердечной астмой, отеком легких. Специфическим именно для массивного некроза сердечной мышцы является кардиогенный шок, для которого характерно критическое уменьшение сердечного выброса, падение давления.
К менее частым последствиям относят эмболии в системе легочной артерии, аневризму и разрыв стенки сердца с тампонадой. При затрагивании инфарктом сосочковых мышц может возникнуть недостаточность митрального клапана с острой кардиальной недостаточностью. Описаны случаи так называемого постинфарктного синдрома, появляющегося через одну или несколько недель после болезни как иммунологическая реакция на некротическую ткань. Протекает как перикардит или плеврит с выраженной эозинофилией.
Диагностика
Физикальное обследование не позволяет выявить каких-то надежных диагностических признаков, подтверждающих либо опровергающих инфаркт миокарда, однако имеет большое значение в процессе оценки тяжести состояния больного. Визуально пациент обычно беспокоен, бледен, кожа покрыта холодным потом. Артериальное давление может повышаться на пике болевого приступа, сочетаться с тахикардией. Нередко нарастают признаки левожелудочковой недостаточности. Из инструментальных методик врачи-кардиологи используют:
- Электрокардиографию. Базовый метод диагностики. Изменения на ЭКГ появляются уже во время стенокардии и проходят ряд характерных стадий. Трансмуральный инфаркт характеризуется глубоким и широким зубцом Q, снижением амплитуды R, сегмент ST поднимается над изолинией. Через несколько дней формируется отрицательный зубец Т, сегмент ST снижается. Локализацию процесса определяют по грудным отведениям.
- Лабораторные методы. Массивный некроз мышечной ткани находит свое отражение в общем анализе крови. У пациентов обнаруживается выраженный лейкоцитоз на фоне лихорадки, лейкоцитарный сдвиг влево, увеличение СОЭ. В биохимическом анализе повышается значение внутриклеточных ферментов (АЛТ, АСТ, ЛДГ), отмечается высокий уровень креатининфосфокиназы, тропонинов.
- Коронарная ангиография. Рентгенологический метод, помогающий установить окклюзию коронарной артерии тромбом, оценить функцию желудочков, риск аневризм или разрыва стенок. Является обязательным компонентом предоперационной подготовки перед аортокоронарным шунтированием, ангиопластикой.
Лечение трансмурального инфаркта миокарда
Все больные с подозрением на данную патологию подлежат скорейшей госпитализации в специализированные отделения — реанимации, неотложной кардиологии, сосудистые центры. Терапию начинают на этапе до госпитализации, особенно при активном вызове скорой медицинской помощи, и продолжают стационарно. Больному прописывается строгий постельный режим, психический и эмоциональный покой, диета.
Консервативная терапия
Важнейшей начальной целью лечения является адекватное обезболивание, предотвращение шоковых состояний, жизнеугрожающих аритмий. Применяют сильные обезболивающие средства (морфин, промедол, трамадол), комбинируемые с атропином, кордароном. Назначают ингаляции кислорода, при угрозе фибрилляции желудочков используют дефибрилляцию либо внутривенное введение лидокаина. При подозрении на тромбоз показаны антикоагулянты прямого действия, преимущественно гепарин или стрептокиназа в больших дозировках.
Хирургическое лечение
Непосредственная цель инвазивных методов — восстановление адекватного кровоснабжения миокарда (реваскуляризация). Своевременно сделанная операция может значительно уменьшить зону некроза, снизить риск осложнений, предупредить рецидивы патологии. В настоящее время хирургическое лечение является приоритетным методом в терапии ишемической болезни сердца и инфаркта миокарда, позволяет добиться тех результатов, которые недоступны при медикаментозном воздействии. Применяются:
- Чрескожная коронаропластика. Расширение просвета сосуда достигается путем введения в него сетчатой металлической трубочки. Манипуляция провидится под рентген-контролем, чаще с доступом из бедренной или подключичной артерии. Результат вмешательства по многом зависит от материала, из которого изготовлен стент. В последующем от пациента требуется долгосрочный прием лекарственных средств (гиполипидемических, антитромбоцитарных).
- Аортокоронарное шунтирование. Суть операции заключается в создании обходного пути для тока крови в обход склерозированного или тромбированного участка сосуда. Это более серьезная манипуляция, приводимая на открытом сердце с использованием аппарата искусственного кровообращения. В качестве шунта может применяться как эндогенный материал (части дистальных артерий), так и искусственные импланты.
- Трансмиокардиальная лазерная реваскуляризация. Перспективный хирургический метод лечения, появившийся в последние годы. С помощью специальной лазерной установки в миокарде проделывается несколько десятков тонких сквозных ходов глубиной плоть до желудочковых полостей. По этим ходам кровь поступает непосредственно из камер к мышечным клеткам, минуя коронарные сосуды.
Прогноз и профилактика
Трансмуральный инфаркт наиболее неблагоприятен по прогнозу вследствие высокой вероятности летального исхода еще до момента оказания медицинской помощи, 20% вероятности гибели в первый месяц после приступа. Полноценная своевременная помощь минимизирует эти риски. Профилактика состояния, главным образом, сводится к предупреждению или коррекции атеросклероза. Важна нормализация массы тела, уровня липидов крови, контроль артериального давления, отказ от вредных привычек. Эти мероприятия особенно необходимы лицам с неблагоприятным семейным анамнезом.
Источник
