Эксфолиативный синдром что это такое

Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Эксфолиативный синдром – системное заболевание, которое приводит к развитию вторичной открытоугольной глаукомы.
Специфическое хлопьевидное белое вещество, видимое при обследовании переднего сегмента глаза, может вызвать обструкцию трабекулярной сети. Хлопьевидное белое вещество встречают и в других тканях организма.
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Эпидемиология эксфолиативного синдрома
Распространённость эксфолиативного синдрома варьирует практически от нуля у эскимосов до 30% у жителей Скандинавии. Заболеваемость увеличивается с возрастом и с течением времени. Также увеличивается частота бинокулярного поражения по сравнению с монокулярным. Пациенты с ЭС-связанной глаукомой могут составлять лишь небольшую часть всех пациентов с глаукомой или же представлять большинство в зависимости от исследуемой популяции. Несмотря на повышенный риск развития глаукомы у пациентов с эксфолиативным синдромом (по данным Blue Mountains Eye Study, в 5 раз больше), у большинства из них глаукома не развивается.
[11], [12], [13], [14], [15], [16], [17], [18], [19]
Патофизиология эксфолиативного синдрома
Вещество, образующее эксфолиации, было выделено из радужки, хрусталика, ресничного тела, трабекулярной сети, эндотелия роговицы и эндотелиальных клеток сосудов глаза и орбиты, а также из кожи, миокарда, лёгких, печени, жёлчного пузыря, почек и оболочек головного мозга. Однако его природа до конца не изучена. Вещество закупоривает трабекулярную сеть, что приводит к развитию вторичной открытоугольной глаукомы. Развивается также ишемия перипупиллярной части радужки, формируются задние синехии. В результате пигмент вымывается, увеличиваются зрачковый блок и нагрузка на трабекулярную сеть, что способствует закрытию угла передней камеры.
Анамнез
Несмотря на редкое развитие явного повышения внутриглазного давления, у большинства пациентов не удается выявить какие-то значимые анамнестические данные. Иногда наблюдают семейные случаи заболевания, для которых характерно хирургическое лечение осложнённой катаракты в семье. Точные механизмы наследования не выявлены.
Диагностика эксфолиативного синдрома
Биомикроскопия
Признак эксфолиативного синдрома – хлопьевидное белое вещество, обнаруживаемое чаще при расширении зрачка у его края, в виде концентрических кругов на поверхности передней капсулы хрусталика. Такие же отложения обнаруживают на радужке, структурах угла передней камеры, эндотелии, интраокулярной линзе и передней пограничной мембране стекловидного тела при афакии. При проведении трансиллюминации часто выявляют перипупиллярные дефекты и атрофию пигментного листка. Наблюдают также вымывание пигмента из перипупиллярной зоны. Зрачок на поражённом глазу обычно меньшего размера и слабее расширяется по сравнению со здоровым глазом, что связано с синисиями и ишемией радужки. Высвобождение пигмента, связанное с дилатацией зрачка, может вызвать скачок внутриглазного давления. В поражённых глазах также чаще формируется катаракта.
Гониоскопия
Угол передней камеры глаза при эксфолиативном синдроме часто сужен, особенно в нижних отделах. Из-за риска развития острого приступа закрытоугольной глаукомы необходим постоянный контроль состояния угла передней камеры. При гониоскопии выявляют неравномерную пигментацию трабекулярной сети с крупными тёмными гранулами пигмента. Отложение пигмента кпереди от линии Швальбе приводит к характерной волнистости линии Сампаолези.
Задний полюс
Характерную глаукомную атрофию зрительного нерва наблюдают при продолжительном подъёме или периодических скачках внутриглазного давления.
[20], [21], [22], [23], [24]
Лечение эксфолиативного синдрома
При глаукоме, связанной с эксфолиативным синдромом, наблюдают более высокие значения внутриглазного давления и более выраженные его суточные колебания. Возможно назначение капель, снижающих вутриглазное давление, но было показано, что такой метод лечения малоэффективен. Несмотря на послеоперационное повышение внутриглазного давления при аргон-лазерной трабекулопластике, метод эффективен. Для воздействия на интенсивно пигментированную трабекулярную сеть можно использовать меньшую энергию лазерного излучения, что позволит снизить послеоперационные скачки внутриглазного давления. Результаты операций, направленных на повышение фильтрации, такие же, как при первичной открытоугольной глаукоме. При проведении экстракции катаракты следует проявлять особую осторожность, принимая во внимание слабость капсулы и связочного аппарата.
Источник
Псевдоэксфолиативный синдром – достаточно распространенная причина возникновения хронической открытоугольной глаукомы. Он обусловлен отложением псевдоэксфолиативного вещества на структурах переднего сегмента глазного яблока, в местах, где они могут соприкасаться с внутриглазной жидкостью.
Синдром характеризуется дегенеративными изменениями радужной оболочки и цилиарного тела, снижением прочности цинновой связки, нарушением гидродинамики глаза, усиленной пигментацией угла передней камеры, а на поздних стадиях процесса и помутнением хрусталика.
На задней поверхности роговицы, псевдоэксфолиативные отложения имеют вид светловато-серых комочков, которые по структуре своей напоминают пепел либо войлок. На радужке (передней и задней ее поверхности) они обнаруживаются в виде серых комочков, хлопьев или щеточек, а на поверхности цилиарного тела – кустиками, высота которых достигает 90 мкм. В проекции угла передней камеры, серые комочки псевдоэксфолиативных отложений, а также отложения пигментного эпителия становятся одним из проявлений деструктивных изменений трабекулярной ткани и причиной сужения межтрабекулярных щелей. При этом, в шлеммовом канале подобные отложения не образуются. На поверхности передней капсулы хрусталика в зоне зрачка и в преэкваториальной зоне, псевдоэксфолиативные отложения чаще представляют собой серые пленки, края которых нередко отслаиваются и закручиваются в сторону хрусталиковой периферии. Из-за пленчатого характера таких образований некоторые специалисты принимали их за отслойку дегенеративно измененной хрусталиковой капсулы и называли эксфолиациями.
При выполнении электронно-микроскопического исследования псевдоэксфолиации предстают в виде нежных фибрилл, с гранулярной структурой. Гистохимическое исследование этих отложений показывает, что они представляют собой нейтральные мукополисахариды.
По мнению некоторых исследователей, причинами возникновения таких отложений могут быть: дистрофии сосудистой оболочки глаза; нарушения процессов полимеризации с выпадением гиалуроновой кислоты, перенасыщающей влагу глаза; патологические изменения межуточной ткани; патологии биохимических процессов, вызывающие денатурацию особого типа мукополисахаридов; нарушения функций ЦНС, ведущие к расстройству кровоснабжения цилиарного тела. Некоторые авторы утверждают, что псевдоэксфолиативный материал образуется в эпителии герминативной зоны хрусталика.
Подтверждается это и тем фактом, что экстракция катаракты снижает количество псевдоэксфолиаций или они исчезают вовсе, кроме того, существует сходство мукополисахаридов капсулы хрусталика и псевдоэксфолиативных отложений.
По данным большинства исследований псевдоэксфолиации присутствуют практически у половины больных глаукомой. Однако, единого мнения о влияния отложений на возникновение глаукомы нет. Большинство специалистов полагают, что псевдоэксфолиации могут блокировать пути оттока внутриглазной влаги, создавая условия для повышения ВГД. Они предлагают глаукому с псевдоэксфолиациями называть «капсульной глаукомой». Правда существует и другое мнение, утверждающее, что это параллельные проявления первичной фазы дегенерации хориоидеи. По мнению третьих, и псевдоэксфолиации, и глаукома являются процессами совершенно самостоятельными, не зависящими друг от друга.
Помутнения хрусталика, развиваются при псевдоэксфолиациях чаще, причем, в этом случае, преобладают корковые катаракты. Покрытые псевдоэксфолиативными отложениями волокна цинновой связки имеют деструктивные изменения. Это может становится причиной спонтанных подвывихов хрусталика.
Крайне редко псевдоэксфолиативный синдром встречается у людей не достигших 50 лет, его частота увеличивается с возрастом и достигает максимума к 70-80 годам. Как правило, поражение имеет двусторонний характер, хотя процесс может проходить не одновременно, а с промежутком в несколько лет.
В медицинском центре «Московская Глазная Клиника» все желающие могут пройти обследование на самой современной диагностической аппаратуре, а по результатам – получить консультацию высококлассного специалиста. Клиника открыта семь дней в неделю и работает ежедневно с 9 ч до 21 ч. Наши специалисты помогут выявить причину снижения зрения, и проведут грамотное лечение выявленных патологий.
Уточнить стоимость той или иной процедуры, записаться на прием в “Московскую Глазную Клинику” Вы можете по телефонам в Москве 8 (800) 777-38-81 и 8 (499) 322-36-36 (ежедневно с 9:00 до 21:00) или воспользовавшись формой онлайн-записи.
Источник
Псевдоэксфолиативный синдром относится к дистрофическим заболеваниям и редко диагностируется у пациентов в возрасте до 45 лет. При этом недуге на передних отделах глазного яблока, соприкасающихся с внутриглазной жидкостью, начинает откладываться экстрацеллюлярное вещество. Псевдоэксфолиативный синдром глаза нередко ведёт к дистрофии радужной оболочки, возникновению катаракты и глаукомы хронической формы. Именно поэтому при его диагностировании требуется срочно приступить к лечению.
Характеристика заболевания
Псевдоэксфолиативный синдром – офтальмологическая патология, спровоцированная обменно-дистрофическими изменениями в глазном яблоке и дегенеративными процессами в радужной оболочке. При этом поражении на хрусталике образуется тончайшая плёнка из отложений, которая подворачивается под хрусталик. Опасность недуга заключается в том, что при отсутствии лечения он может стать причиной развития глаукомы и катаракты, а также спровоцировать помутнение хрусталика. Как показывает медицинская практика, избежать необратимых последствий можно только при своевременном обращении к специалисту. Если болезнь будет диагностирована в запущенном состоянии, предотвратить осложнения будет фактически невозможно.
В ходе многочисленных клинических исследований было выявлено, что развитие болезни связано с возрастом пациента. В группу риска попадают люди старше 50. После этого возраста вероятность развития недуга составляет около 30%.
Причины развития
Несмотря на многочисленные клинические исследования, этиология заболевания до сих пор не изучена до конца. Считается, что спровоцировать отложение белково-фиблярных и пигментных структур на хрусталике могут следующие факторы:
- разрушение и дисфункция капилляров глаза вследствие дистрофических процессов;
- структурные изменения тканей глаза;
- травмирование глазных органов;
- внутриглазные инфекционные заболевания;
- ослабление защитных сил местного иммунитета;
- негативное воздействие на органы зрения ультрафиолета;
- расстройства ЦНС, ведущие к ухудшению кровотока в капиллярах цилиарного тела;
- патологические биохимические процессы;
- генетическая предрасположенность.
В группы риска по развитию этого недуга попадают люди, злоупотребляющие курением, а также пациенты, страдающие от сердечно-сосудистых заболеваний, гипертонии и атеросклероза.
Симптомы
Опасность псевдоэксфолиативного синдрома заключается в том, что на начальных этапах он протекает практически бессимптомно, из-за чего болезнь обычно диагностируется в запущенном состоянии. Симптоматика становится заметной ближе к третьей стадии, на которой начинается разрушение связочного аппарата хрусталика. Большинство пациентов при этом жалуются на появление отложений в переднем углу глаза и ухудшение зрительной функции. Если не обратиться в клинику, болезнь будет прогрессировать и станет причиной развития глаукомы.
На этом этапе могут наблюдаться следующие симптомы:
- ухудшение зрения одного глаза (более чем в 75% случаев болезнь поражает сначала левый глаз, и только через несколько лет возникают двусторонние изменения);
- расплывчатость и раздвоение предметов;
- появление черных точек перед глазами;
- сложности во время чтения.
При ПЭС во время проведения комплексной диагностики офтальмолог заметит помутнение хрусталика, появление отложений в углу глаза и пигментирование трабекулярных клеток.
Способы диагностики
Выявить заболевание на начальном этапе практически невозможно. Единственное обследование, в ходе которого можно заподозрить развитие ПЭС, – ультразвуковая биомикроскопия.
На более поздних этапах диагностирование псевдоэксфолиативного синдрома проводится при помощи:
- глазная биомикроскопия. Позволяет рассмотреть отложения на поверхностных оболочках переднего отдела глазного яблока;
- гониоскопия. Визуальное исследование передней камеры глаза;
- ультразвуковое исследование. УЗИ позволяет обнаружить деструктивные нарушения и изменение размеров переднего и заднего сегмента глаза;
- ультразвуковая биомикроскопия. При помощи этого обследования можно обнаружить даже микроскопические точечные включения на оболочке глаза;
- визометрия. Методика, использующаяся для определения качества зрения.
При подозрении на ПЭС для выявления общей клинической картины пациенту могут назначить дополнительные консультации невропатолога, ревматолога и других узкопрофильных специалистов.
Методы лечения
Цель лечения при псевдоэксфолиативном синдроме – минимизировать риск развития дальнейших осложнений. На ранних стадиях пациентам выписывают медикаменты следующих фармкатегорий:
- антиоксиданты. Подобные препараты разрушают активные формы кислорода, которые негативно влияют на ткани глазного яблока;
- антигипоксанты. Улучшают обменные процессы и регенерацию клеток;
- гипотензивные средства. Выписываются при повышенном внутриглазном давлении и признаках офтальмогипертензии;
- поливитаминные комплексы. При глазных заболеваниях особенно полезен ретинол, токоферол и витамин B6. Чаще всего витамины назначаются в форме глазных капель.
Если болезнь обнаружена в запущенном состоянии и сопровождается множественными осложнениями, медикаментозная терапия не принесёт эффекта. В этом случае единственный шанс сохранить зрение – проведение лазерного или хирургического вмешательства. Наиболее эффективным методом лечения псевдоэксфолиативного синдрома является лазерная трабекулопластика. Однако необходимо понимать, что через 3–4 года болезнь может вновь дать о себе знать.
Специалисты предупреждают, что даже замена хрусталика не поможет полностью устранить проблему. Именно поэтому пациенту придётся постоянно принимать лекарственные средства, помогающие поддержать зрительную функцию.
Прогноз и профилактика
При ПЭС прогноз для пациента зависит от того, на каком этапе была выявлена болезнь, а также от степени поражения структур глаза. При своевременной диагностике и грамотно подобранном лечении вероятность сохранения зрительной функции и предотвращения осложнения достаточно высока. Но если недуг будет обнаружен в запущенном состоянии, предотвратить развитие глаукомы и катаракты будет невозможно.
Что касается профилактических мер, то они до сих пор не разработаны. Именно поэтому всем людям, вне зависимости от состояния здоровья и возраста, рекомендуется каждые 6 месяцев посещать офтальмолога, который сможет своевременно заметить деструктивные изменения и назначить подходящую схему лечения.
Псевдоэксфолиативный синдром – опаснейшая офтальмологическая патология, которая нередко приводит к серьёзным осложнениям. Поскольку недуг крайне сложно поддаётся лечению, намного разумнее постараться предотвратить его развитие. Всё, что для этого требуется, – регулярно посещать офтальмолога и своевременно лечить заболевания глаз.
Источник
Статья посвящена псевдоэксфолиативному синдрому как фактору риска развития синдрома «сухого глаза»
Введение
В последние годы вопросы диагностики, профилактики и лечения синдрома «сухого глаза» (ССГ) приобретают все большую актуальность. В настоящее время это состояние вышло за рамки отдельной нозологической формы, распространенность ССГ составляет среди общей популяции 35% [1], а среди пациентов офтальмологического профиля – 45%, увеличиваясь с возрастом [2]. Определен спектр основных заболеваний глаз, имеющих тесную патогенетическую связь с ССГ, не ослабевает значимость общих расстройств организма, нередко сопровождающихся его развитием. Однако наряду с общеизвестными нозологическими формами ССГ осложняется еще целый ряд заболеваний органа зрения, традиционно не учитывающихся практикующими офтальмологами.
Псевдоэксфолиативный синдром (ПЭС), представляющий собой системную патологию с преимущественным поражением органа зрения, характеризуется избыточной продукцией и накоплением в различных структурах глаза патологического экстрацеллюлярного материала [3]. Псевдоэксфолиативные отложения обнаружены и в поверхностных тканях глаз, изменения которых нередко ассоциированы с развитием ССГ [4]. Опубликован ряд исследований, касающихся изменений функциональных и морфологических показателей прероговичной слезной пленки у пациентов с ПЭС [5–7], однако их единичный характер, наряду с высокой распространенностью ПЭС в Центральной России [8] и клинической значимостью ПЭС и ССГ, обусловливают необходимость дальнейшего углубленного изучения этого вопроса.
Цель исследования
Оценить влияние ПЭС на развитие и клиническое течение ССГ.
Материал и методы
В рамках поперечного исследования «случай – контроль» обследовано 120 пациентов (240 глаз) с ПЭС различной степени выраженности, составивших основную группу, и 120 лиц (240 глаз) без признаков ПЭС (контрольная группа). Основная и контрольная группы были сопоставимы по возрастно-половой структуре (табл. 1).
Выборка формировалась сплошным методом по мере госпитализации больных для планового хирургического лечения катаракты в профильные отделения. Критериями исключения являлись: глаукома, любые операции и травмы глаз в анамнезе, патологические процессы органа зрения, затрудняющие диагностику ПЭС (воспалительные заболевания сосудистого тракта, изменения роговицы и т. п.), общие заболевания (аутоиммунные, сахарный диабет), а также местное и общее использование медикаментозных средств, способных вызвать снижение стабильности слезной пленки и угнетение слезопродукции.
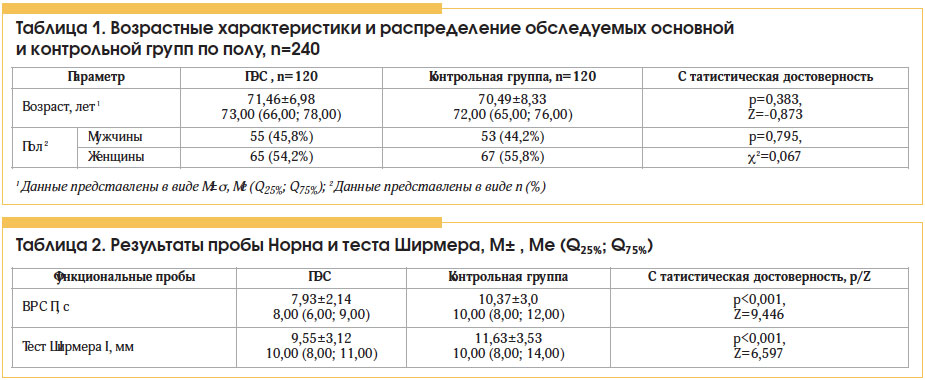
Всем пациентам проводилось стандартное офтальмологическое обследование, включавшее визометрию, биомикроскопию, тонометрию по Маклакову, офтальмоскопию. Диагноз ПЭС устанавливался при наличии псевдоэксфолиативных отложений по зрачковому краю радужки и/или на передней капсуле хрусталика (в условиях максимально достижимого медикаментозного мидриаза). Степень выраженности ПЭС оценивали по классификации Е.Б. Ерошевской (1997). Функциональные методы диагностики ССГ включали определение времени разрыва слезной пленки (ВРСП) (проба Норна) и величины суммарной слезопродукции (тест Ширмера I с использованием тест-полосок фирмы Bausсh & Lomb, Германия).
Статистическая обработка данных осуществлялась с использованием пакета прикладных программ Statistica 8.0 (StatSoftInc., США). Анализ выборок на соответствие закону нормального распределения проверяли критерием Колмогорова – Смирнова. Результаты представлены в таблицах в виде медианы (Me), верхнего и нижнего квартилей (Q25%; Q75%), а также в формате М±σ (где М – среднее значение, σ – стандартное отклонение среднего значения), что позволило сопоставить полученные данные с данными ранее опубликованных исследований. Выборки не подчинялись закону нормального распределения на уровне значимости p<0,05, в связи с чем достоверность различий групп оценивали с помощью Z-аппроксимации непараметрического U-критерия Манна – Уитни. Сравнение групп по качественным признакам проводилось с использованием критерия χ2 (метод Пирсона), при анализе взаимосвязи между признаками использовали непараметрический ранговый r-коэффициент корреляции Спирмена. Критический уровень значимости при проверке статистических гипотез принимался равным <0,05.
Результаты
Результаты функциональных проб в основной группе статистически значимо отличались от показателей контрольной группы. ВРСП и показатель суммарной слезопродукции (тест Ширмера I) у пациентов с ПЭС были снижены в сравнении с таковыми у лиц без признаков заболевания (табл. 2). Различия сохранялись как среди мужчин, так и среди женщин после стратификации исследуемых групп по полу (p<0,001 для обоих тестов). Доля глаз с клинически значимым снижением ВРСП (менее 10 с) в основной группе почти в 2 раза превысила аналогичные данные в контрольной группе (78,3% и 42,1% соответственно). Значение пробы Ширмера I менее 15 мм имело место в 92,1% глаз с ПЭС и 82,9% глаз в группе сравнения, менее 5 мм – в 7,1% и 2,9% соответственно.
При биомикроскопии частота обнаружения параллельных нижнему веку конъюнктивальных складок (конъюнктивохалазис, LIPCOF) при ПЭС значительно превышала показатель в группе сравнения. Данный признак определялся в 73,8% глаз с ПЭС против 52,9% глаз в контрольной группе (p=0,000002, χ2=22,428) (рис. 1).

С увеличением возраста исследуемых наблюдалась тенденция к уменьшению ВРСП как в основной, так и в контрольной группе (коэффициент корреляции r=0,557 и r=0,502 соответственно; p<0,001). Статистически значимые различия показателей у пациентов с наличием ПЭС и без ПЭС сохранялись в каждой возрастной группе (p<0,001) (рис. 2). Аналогичная тенденция наблюдалась при использовании пробы Ширмера I (рис. 3) (коэффициент корреляции между результатами теста и возрастом обследуемых r=0,456 и r=0,461 соответственно; p<0,001).
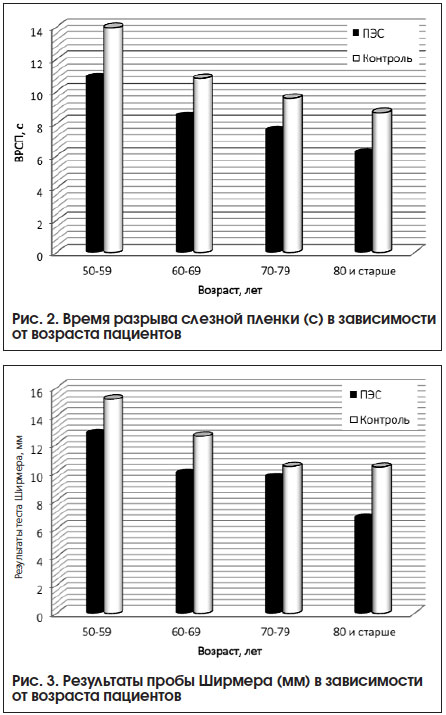
Исследована зависимость стабильности прероговичной слезной пленки от степени выраженности псевдоэксфолиативного процесса. С возрастанием интенсивности псевдоэксфолиативных отложений, сопровождающихся более выраженными дистрофическими изменениями переднего отдела глаза, ВРСП сокращается. При ПЭС I степени этот показатель составил 9,0±1,74 с; 9,00 (8,00; 10,00), при II степени – 7,77±1,79 с; 8,00 (7,00; 9,00), при III стадии заболевания – 6,76±2,09 с; 6,50 (5,00; 7,00) (p1,2=0,002, Z=3,309; р2,3=0,0004, Z=3,515).
Результаты пробы Ширмера I также находились в обратной зависимости от стадии ПЭС, снижаясь с 10,81±2,59; 10,00 (9,00; 12,00) при ПЭС I степени до 9,43±2,51; 9,00 (8,00; 10,00) при II степени и 8,65±3,26; 9,00 (7,00; 11,00) при III степени выраженности синдрома (p1,2=0,025, Z=2,236; р2,3=0,106, Z=1,619).
Данные литературы свидетельствуют о том, что при электронно-микроскопических исследованиях конъюнктивы парных глаз, клинически не вовлеченных в процесс, признаки ПЭС выявляются в 100% случаев. Следовательно, термины «односторонний» или «двусторонний» ПЭС не совсем верны, и речь надо всегда вести об ассиметричном поражении [9, 10]. В случаях, когда клинически ПЭС определялся только с одной стороны, показатель ВРСП на пораженном глазу был статистически значимо меньше. Значение пробы Норна составило 8,5±2,1 с; 8,0 (7,0; 10,0) на глазу с клинической манифестацией ПЭС и 9,9±1,7 с; 10,0 (9,0; 10,0) – на парном (p=0,001; Z=3,335). Средние значения теста Ширмера I на глазах с клинически определяемым заболеванием также оказались несколько ниже – 10,7±2,42 мм; 10,0 (9,0; 12,0) в сравнении с 11,6±2,42 мм; 11,0 (9,0; 10,0) на парном глазу, впрочем, не достигая статистически достоверных различий (p=0,139; Z=1,481). Следует отметить, что показатели ВРСП и теста Ширмера I в основной группе на глазах без клинической манифестации ПЭС хотя и были ниже, чем в контрольной группе, также не достигали статистически значимых различий (p=0,403; Z=-0,836 и p=0,924; Z=0,010 соответственно).
Обсуждение
К настоящему времени установлено, что псевдоэксфолиативный процесс может поражать большинство тканей глаза. ПЭС ассоциирован со значительным количеством заболеваний и патологических состояний органа зрения, в т. ч. с глаукомой, катарактой, нарушением гематоофтальмического барьера, дистрофическими изменениями переднего отдела глаза [3]. Использование электронной микроскопии позволило обнаружить псевдоэксфолиативный материал в конъюнктиве век и глазного яблока [10]. В ряде опубликованных ранее работ показано, что наличие ПЭС может коррелировать с изменениями функциональных показателей слезы, характерных для ССГ. Обоснованием этого факта можно считать данные, касающиеся изменения морфологии бокаловидных клеток конъюнктивы на фоне ПЭС, что, в свою очередь, может оказать влияние на муциновый слой прероговичной слезной пленки [6].
В данном исследовании установлено снижение показателей ВРСП и суммарной слезопродукции в группе пациентов с ПЭС в сравнении с контрольной группой, что позволяет отнести псевдоэксфолиативный процесс к факторам риска развития ССГ. Полученные данные говорят об ухудшении функциональных показателей слезы с увеличением возраста обследуемых, что соответствует физиологическим особенностям организма пожилого человека, однако в каждой возрастной группе сохранялись статистически значимые различия между больными с ПЭС и группой сравнения.
Результаты исследования свидетельствуют о прямой зависимости между степенью выраженности ПЭС и характером угнетения ВРСП и результатами теста Ширмера I. Это подтверждается снижением изучаемых показателей по мере увеличения стадии заболевания, а также их значимым ухудшением в глазах с наличием ПЭС в сравнении с парными глазами без признаков отложения псевдоэксфолиативного материала при клинически одностороннем процессе.
ПЭС – фактор, значительно увеличивающий риск развития и прогрессирования катаракты и глаукомы. Хирургия катаракты сама по себе может вызвать развитие ССГ либо усугубить течение уже имеющегося процесса. Глаукома требует длительного использования местной гипотензивной терапии, способной вызвать развитие ССГ [11–15]. В этой связи необходимо учитывать предрасположенность к ССГ у лиц с ПЭС при выборе препарата для медикаментозной терапии и тактики хирургического лечения данных групп больных [16, 17].
Заключение
Полученные данные свидетельствуют об изменениях функциональных показателей суммарной слезопродукции и стабильности прероговичной слезной пленки у пациентов с ПЭС. Это может рассматриваться как факт предрасположенности данной категории больных к развитию ССГ. Установлена зависимость изменений слезопродукции и ВРСП от степени выраженности ПЭС. С учетом частоты возникновения у таких больных глаукомы и, соответственно, перспективы использования местных гипотензивных средств, способных вызвать либо усугубить течение ССГ, очевидны необходимость дополнительного обследования этой категории пациентов и адекватный выбор терапии, а также своевременное назначение препаратов «искусственной слезы».
Источник
