Катамениальный синдром что это такое

Катамениальная эпилепсия у женщин: причина, клиника и лечение
Термин «катамениальная» происходит от греческого слова katamenios, что означает «ежемесячно», так как в прежние времена цикличность эпилептических приступов связывали с лунным циклом. По разным данным, 10-70% женщин, больных эпилепсией, страдают катамениальной эпилепсией. Как и в случае с менструальной мигренью, отсутствие общепринятого определения приводит к широкому разнообразию описаний проявлений этого заболевания. Строго говоря, катамениальная эпилепсия — эпилепсия, возникающая или обостряющаяся в период менструаций.
По крайней мере, в 75% случаев приступы регистрируют в течение 10 дней, начиная за 4 дня до менструации; при этом ежедневная частота приступов возрастает в 6 раз. Несмотря на то что до 70% женщин, страдающих эпилепсией, утверждают, что их заболевание обостряется во время менструаций, лишь приблизительно у 12% можно объективно диагностировать истинную катамениальную эпилепсию.
Менструальные обострения проявляются при всех типах приступов, хотя у женщин с фокальными формами эпилепсии это происходит чаще, чем с генерализованными приступами. Описано три различных типа катамениальной эпилепсии у женщин с овуляторным менструальным циклом: перименструальный, периовуляторный и лютеиновый.
• В большинстве случаев встречают перименструальный тип — частота приступов наибольшая в период менструаций (от -3 до +3 дней).
• Периовуляторный тип характеризуется возрастанием частоты приступов в овуляторную фазу (в середине цикла) по сравнению с фолликулярной и лютеиновой фазами.
• При лютеиновом типе частота приступов наибольшая в овуляторную, лютеиновую и менструальную фазы по сравнению с фолликулярной.

У женщин с ановуляторными циклами чаще отмечают общее увеличение частоты приступов в течение всего цикла по сравнению с овулирующими женщинами. Вполне вероятно, что это связано с общим понижением количества прогестерона, характерным для ановуляции. В противоположность этим типам, наблюдаемым у овулирующих женщин, при ановуляции количество приступов во время менструаций по сравнению с остальной частью цикла значительно меньше.
Некоторые женщины, страдающие эпилепсией, входят в группу повышенного риска по овуляторной дисфункции. Одно из исследований показало, что среди женщин, больных эпилепсией с очагом в височной доле, ановуляторные циклы встречаются в 35% по сравнению с 8% в контрольной группе. Другие эндокринные нарушения репродуктивной системы, включая СПКЯ, гиперпролактинемию и ПЯН, также часто встречают у женщин с эпилепсией.
Патофизиология катамениальной эпилепсии
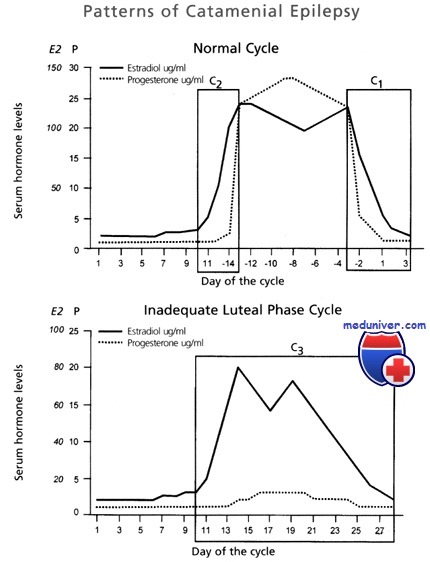
Считают, что катамениальиая эпилепсия — результат циклических изменений количества яичниковых гормонов и метаболизма лекарственных средств. Судорожный порог повышается под воздействием прогестерона, а понижается при увеличении количества эстрогенов. Снижение концентрации прогестерона или отношения прогестерона к эстрогенам коррелирует с возрастанием частоты приступов. Было замечено, что частота приступов увеличивается в течение двух особых периодов менструального цикла. Первый связан с быстрым понижением количества прогестерона непосредственно перед менструацией, а второй — с повышением концентрации эстрогенов перед овуляцией.
Есть также свидетельства о возрастании частоты приступов во время ановуляторных циклов при относительно низком содержании прогестерона.
Доказано, что метаболизм противосудорожных средств различен в разные периоды цикла. Снижение количества эстрогенов и прогестерона во время менструации стимулирует образование монооксигеназных ферментов печени, ускоряющих метаболизм противосудорожных препаратов, и повышает риск возникновения припадков. Лечение катамениальной эпилепсии должно включать определение содержания противосудорожных препаратов в сыворотке крови в период обострения приступов. Увеличение дозы препаратов в период обострения может предупредить приступы.
Лечение катамениальной эпилепсии
Для постановки диагноза и подбора специфической терапии очень важно подробное проспективное документирование приступов относительно менструальных периодов. По данным многих исследователей, отмечен хороший эффект прогестероновой терапии. Лучше всего было изучено применение медроксипрогестерона внутрь (10-40 мг в день) или в/м (150 мг в течение 6-12 нед). В дополнение к противосудорожным свойствам прогестерон, принимаемый в такой дозе, может также снижать частоту приступов, подавляя выделение гонадотропина, что в свою очередь понижает количество эстрогенов.
Недавно появилось подтверждение эффективности лечения некоторых женщин натуральным микронизированным прогестероном. В одном из исследований восемь женщин С эпилептическим очагом в височной доле применяли вагинальные суппозитории с прогестероном 50-100 мг каждые 12 ч во время фазы наибольшей частоты приступов. Средняя месячная частота приступов снизилась на 68%, и у 75% женщин количество приступов уменьшилось за 3 мес исследования. При другом широком исследовании 36 женщин получали прогестерон сублингвально, при этом локальные и генерализованные приступы снизились на 68 и 57% соответственно, а у 4 пациенток приступы вообще прекратились.
Влияние комбинированных пероральных контрацептивов на частоту приступов непостоянно, по некоторым данным в дни перерыва между приемом лекарств могут отмечаться обострения. Для больных эпилепсией предпочтителен непрерывный прием комбинированных пероральных контрацептивов или препаратов, содержащих только прогестерон, так как в данном случае обеспечивается постоянное поступление прогестерона.
Было проведено несколько исследований эффективности агонистов люлиберина в лечении катамениальной эпилепсии, устойчивой к другим методам терапии. Хотя обычно эти препараты эффективно снижают частоту приступов, их долговременное применение может вызвать деминерализацию костной ткани.
– Вернуться в оглавление раздела “гинекология”
Оглавление темы “Предменструальный синдром – ПМС”:
- Предменструальный синдром (ПМС). Молимина и предменструальные дисфорические расстройства
- Распространенность предменструального синдрома. Критерии ПМС
- Диагностика предменструального синдрома. Сбор анамнеза и осмотр
- Причины предменструального синдрома. Этиология ПМС
- Лечение предменструального синдрома (ПМС). Изменение образа жизни и диета
- Лекарства в терапии предменструального синдрома (ПМС). Медикаменты
- Лечение болей молочных желез при месячных. Хирургическое лечение ПМС
- Менструальная мигрень: частота, причины и лечение
- Лечение менструальной мигрени. Лекарства от головной боли при месячных
- Катамениальная эпилепсия у женщин: причина, клиника и лечение
Источник
Катамениальный (менструальный) пневмоторакс является крайне редким и потенциально опасным состоянием у женщин. Пневмоторакс – медицинский термин, им описывают коллапс легкого, состояние, при котором воздух или другие газы попадают в ловушку в пространстве, окружающем легкие, тем самым вызывая разрушение легкого. Женщины с менструальным пневмотораксом имеют периодические эпизоды пневмоторакса, которые происходят в течение 72 часов до или после начала менструации. Точная причина развития менструального пневмоторакса неизвестна (хотя было высказано несколько теорий). Некоторые случаи были связаны с ненормально развитым эндометрием ткани вне матки (эндометриоз).
Катамениальный (менструальный) пневмоторакс. Эпидемиология
Чаще всего, менструальный пневмоторакс развивается у женщин в детородном возрасте (в возрасте 30-40 лет). Точная распространенность этого расстройства неизвестна. Многие исследователи считают, что менструальный пневмоторакс часто упускается женщинами и врачами или неправильно диагностируется. Термин «менструальной пневмоторакс» был впервые использован в медицинской литературе в 1972 году.
Катамениальный (менструальный) пневмоторакс. Причины
Точная причина развития менструального пневмоторакса неизвестна. Исследователями было выведено несколько различных теорий затрагивающих метастатические, гормональные и анатомические аномалии.
Интраоперационная находка диафрагмального эндометрия
В метастатическим модели, менструальной пневмоторакс вызывается ненормальной миграцией ткани эндометрия из матки (эндометрий) к другим областям тела, к таким как диафрагма или пространство между мембранами, выстилающих полость грудной стенки и легких (плевральная полость). Когда ткани эндометрия находятся вне матки, врачи описывают это событие термином «эндометриоз». Многие женщины с менструальным пневмотораксом имеют эндометриоз. Эндометриоз может вызвать небольшие отверстия в мембране, которые позволили бы воздуху и жидкости проходить через них в плевральную полость. У многих женщин, с менструальным пневмотораксом, в легких имеются ткани эндометрия, это то состояние, которое называется грудным эндометриозом. Тем не менее, некоторые женщины не имеют таких диафрагмальных отверстий и тканей эндометрия в легких, это наталкивает врачей на идею, что другие факторы также могут играть определенную роль в развитии этого состояния.
В гормональной модели, исследователи полагают, что гормон, известный как простагландин F2, который вырабатывается во время овуляции, вызывает сужение трубочек в легких (бронхиолы). Сужение бронхиол может привести к разрыву альвеол в легких с последующим высвобождением воздуха в плевральную полость.
Согласно анатомической модели, исследователи считают, что отсутствие слизистой пробки в шейке матки, что является вполне нормальным явление во время менструального цикла, позволяет воздуху проходить из половых путей в плевральную полость через маленькие отверстия в диафрагме.
И согласно последней теории, исследователи полагают, что это состояние может быть вызвано спонтанным разрывов пузырьков (заполненных жидкостью или воздухом), которые могут развиться на поверхности легких у некоторых женщин. Некоторые исследователи предполагают, что гормональные изменения во время менструального цикла могут привести к разрыву этих пузырьков, что в свою очередь может привести к пневмотораксу.
Катамениальный (менструальный) пневмоторакс. Похожие расстройства
Спонтанный пневмоторакс – состояние, при котором воздух попадает в ловушку в плевральной полости. Спонтанный пневмоторакс также приводит к коллапсу легкого. У лиц с этим состоянием может развиться внезапная боль в груди, затрудненное дыхание, одышка и кашель. Многим женщинам, с менструальным пневмотораксом, часто первоначально ставят диагноз спонтанного пневмоторакса, пока врачи не обнаружат корреляцию между пневмотораксом и менструальными циклами.
Катамениальный (менструальный) пневмоторакс. Симптомы и проявления
Симптомы / проявления и тяжесть менструального пневмоторакса могут варьироваться от одного эпизода к другому и от одного человека к другому. В большинстве случаев, пневмоторакс затрагивает правое легкое.
Симптомы и проявления, которые могут возникнуть у женщин с менструальным пневмотораксом, включают: ежемесячные эпизоды боли в груди (эта боль может отдавать в лопатки), одышка, головокружение, усталость, сухой кашель. Некоторые женщины могут сообщить о появлении звука «потрескивания» при вдохе. Тяжелые боли в груди, связанные с повреждением легкого, часто требуют срочной медицинской помощи.
Катамениальный (менструальный) пневмоторакс. Диагностика
Постановка диагноза менструального пневмоторакса проводится на основе подробного изучения истории болезни, тщательного клинического обследования и на основе определения характерных клинических особенностей этого состояния (т.е. повторные эпизоды пневмоторакса в сочетании с наступлением менструации). Также, врачи могут назначить некоторые диагностические тесты, например торакоскопию, по ходу которой, хирурги пропускают трубку-стетоскоп с маленькой, волоконно-оптической камерой в конце, через небольшой разрез в грудной клетке. Это позволит врачам детально исследовать легкие, грудную полость и диафрагму.
Катамениальный (менструальный) пневмоторакс. Лечение
Серьезные эпизоды пневмоторакса могут потребовать введения специальной трубки в грудную область, с помощью которой можно будет выпустить накопившейся воздух. Это позволит легким нормально расширяться.
Как хирургия так и гормональная терапия, либо отдельно, либо вместе, также часто используются в лечении женщин с менструальным пневмотораксом. В одних случаях может быть выполнена хирургическая операция по удалению всех областей эндометрия в легких и в плевральной полости, а в других случаях, хирургическая операция может быть необходима для удаления апикальных пузырьков в верхней части легких.
Кроме того, некоторым женщинам, с менструальным пневмотораксом, может потребоваться проведение плевродеза. Это та операция, при которой хирурги будут внутриплеврально вводить некоторые препараты, искусственно вызывающие воспаление двух слоев плевры. Этим воспалением можно уменьшить или совсем устранить плевральную полость (сращение листков плевры), в которой может находиться лишняя жидкость или воздух.
Что касается гормональной терапии, то она чаще всего используется в качестве дополнения к хирургическим методам лечения. Одними из самых часто используемых препаратов являются агонисты гонадотропин-рилизинг гормона, ими можно подавлять овуляцию и высвобождение других гормонов, включая эстроген или прогестерон. Эти препараты широко применяются в лечении женщин с эндометриозом.
Источник
Катамениальный (менструальный) пневмоторакс (КП) – рецидивирующий спонтанный пневмоторакс (СП) у женщин 30-40 лет, возникающий в период за 24 ч до начала и через 72 ч после начала менструации [4, 5, 11, 16, 18]. Впервые КП был описан в 1958 г. E. Maurer и соавт. [15]. Причиной возникновения КП является торакальный эндометриоз (ТЭ) [9, 11], который, являясь редкой разновидностью экстрагенитального эндометриоза, приводит к развитию торакального катамениального синдрома, включающего боли в груди во время менструации, пневмоторакс, гемоптизис и гемоторакс [6, 7, 21]. Частота рецидивов КП достигает 71% [4], что делает эту проблему крайне актуальной.
В НИИ скорой помощи им. Н.В. Склифосовского за 2005-2013 гг. были оперированы 17 женщин с СП, что составило 20,7% всех оперированных больных с СП. Рецидивный СП был у 7 из них. Средний возраст больных с рецидивным СП составил 32±11 лет. Правосторонний СП был у 6 больных, левосторонний – у 1 больной. Буллезные изменения легкого имели место у 2 больных, причина пневмоторакса не выявлена у 3 больных, ТЭ был диагностирован у 2 (11,8%) из 17 больных.
1. Больная Б., 38 лет (в анамнезе: роды – 3, генитальным эндометриозом не страдала). Не курит. Поступила 23.05.11 с жалобами на боль в правой половине груди при дыхании, сухой кашель, чувство нехватки воздуха. Заболела за 24 ч до поступления. При обращении в НИИСП состояние относительно удовлетворительное. ЧДД 18 в 1 мин. Дыхание справа ослаблено, слева проводится во все отделы, хрипов нет. ЧСС 82 в 1 мин. Живот мягкий, безболезненный. При рентгенографии груди был диагностирован СП в верхнелатеральных отделах правого гемоторакса. Корни легких структурны, диафрагма четкая. Гидроторакс не выявлен. Плевральная полость была дренирована во втором межреберье по среднеключичной линии, эвакуирован воздух. Проводилась аспирация по дренажу в течение 3 сут. На контрольной рентгенограмме, выполненной на 4-е сутки, пневмоторакс не выявлен, поэтому после контрольного периода дренажная трубка из плевральной полости была удалена. С целью установления причины пневмоторакса была произведена компьютерная томография груди, при которой справа был выявлен пневмоторакс объемом 175 см3. Буллезных изменений легких не обнаружено. При контрольной рентгенографии груди был выявлен паракостальный пневмоторакс (шириной до 3 см), в связи с чем произведено повторное дренирование правой плевральной полости во втором межреберье по среднеключичной линии. На 5-е сутки дренажная трубка была удалена. При контрольной рентгенографии пневмоторакс не обнаружен. На 15-е сутки с момента поступления больная была выписана в удовлетворительном состоянии.
Обратилась повторно 20.06.11 с прежними жалобами. Заболела за 16 ч до поступления. При рентгенографии груди выявлен правосторонний паракостальный пневмоторакс (шириной 3 см). В связи с рецидивом СП была выполнена срочная видеоторакоскопия (ВТС) справа. При ревизии легкого буллезных изменений не выявлено. На сухожильном центре диафрагмы было обнаружено 5 округлых отверстий диаметром около 5 мм и округлое, выступающее над поверхностью образование синего цвета диаметром 5 мм (рис. 1). Рисунок 1. Интраоперационная фотография (больная Б.). Очаг эндометриоза на диафрагме (черная стрелка). В белом круге – множественные фенестрации сухожильного центра диафрагмы. Были произведены биопсия внешне неизмененного CIII легкого, париетальная плеврэктомия от III до VIII ребра. Купол плевральной полости обработан 5% спиртовым раствором йода. На контрольных рентгенограммах, выполненных на 3-и и 8-е сутки после операции, сохранялся верхушечный пневмоторакс шириной 0,5 см. Дренажные трубки удалены. При гистологическом исследовании выявлен умеренный фиброз париетальной плевры с невыраженными очаговыми лимфоплазмоцитарными воспалительными инфильтратами. Висцеральная плевра с фиброзом, очаговыми субплевральными кровоизлияниями, дистелектазами и буллезной эмфиземой, невыраженными перибронхиальными воспалительными инфильтратами.
Рисунок 1. Интраоперационная фотография (больная Б.). Очаг эндометриоза на диафрагме (черная стрелка). В белом круге – множественные фенестрации сухожильного центра диафрагмы. Были произведены биопсия внешне неизмененного CIII легкого, париетальная плеврэктомия от III до VIII ребра. Купол плевральной полости обработан 5% спиртовым раствором йода. На контрольных рентгенограммах, выполненных на 3-и и 8-е сутки после операции, сохранялся верхушечный пневмоторакс шириной 0,5 см. Дренажные трубки удалены. При гистологическом исследовании выявлен умеренный фиброз париетальной плевры с невыраженными очаговыми лимфоплазмоцитарными воспалительными инфильтратами. Висцеральная плевра с фиброзом, очаговыми субплевральными кровоизлияниями, дистелектазами и буллезной эмфиземой, невыраженными перибронхиальными воспалительными инфильтратами.
Больная была выписана в удовлетворительном состоянии на 12-е сутки после операции. В дальнейшем ее по-прежнему периодически беспокоили боли в груди во время менструации. Во время болей при рентгенографии легких неоднократно выявляли пневмоторакс над диафрагмой и в области купола плевральной полости. Ретроспективная оценка клинического течения заболевания и макроскопических изменений позволила установить диагноз ТЭ и КП, однако от повторного хирургического лечения больная воздерживается. Неоднократно была осмотрена акушером-гинекологом, генитального эндометриоза не установлено. Гормональную терапию не назначали в связи с отсутствием морфологической верификации эндометриоза.
Ретроспективный анализ этого клинического наблюдения показал, что у больной имеется сочетание микроскопических признаков эмфиземы легких и макроскопических признаков ТЭ с поражением правого купола диафрагмы. Неустраненный ТЭ, недостаточная по объему плеврэктомия, отсутствие гистологической верификации характерных изменений диафрагмы при отсутствии признаков генитального эндометриоза не позволили назначить гормональную терапию, что привело к дальнейшим рецидивам КП.
2. Больная Ч., 44 лет (роды – 1, аденомиоз, эндометриоз яичников с 1980 г.), курила до операции умеренно. С 80-х годов наблюдается у врача акушера-гинеколога по поводу аденомиоза и эндометриоза яичников. В 1991 г. были самопроизвольные роды. В 2010 г. дважды были выполнены диагностические выскабливания полости матки под гистероскопическим контролем в связи с гиперпластическим процессом эндометрия. В 2011 г. было произведено лапароскопическое удаление эндометриоидной кисты левого яичника. После операции в течение трех менструальных циклов получала препараты, являющиеся агонистами гонадотропин-рилизинг-гормона. В настоящее время клинических проявлений генитального эндометриоза нет. В апреле 2013 г. при флюорографии был выявлен клинически не проявлявшийся правосторонний СП. К хирургу не обращалась. В июле того же года при повторном рентгенологическом обследовании вновь был выявлен правосторонний СП небольшого объема, не потребовавший дренирования плевральной полости. Больная была осмотрена фтизиатром, признаков туберкулеза нет. В связи с рецидивным СП госпитализирована в НИИСП, где была предложена операция, от которой больная воздержалась. С целью определения причины СП была выполнена компьютерная томография груди (томограф ZXi, General Eleсtric), эмфизематозных, очаговых, инфильтративных изменений в легких не обнаружено.
С июля 2013 г. в течение 3 мес для исключения КП ежемесячно больной выполняли рентгенологическое исследование груди, по результатам которого был выявлен быстро регрессировавший пневмоторакс (в августе и в октябре 2013 г.), по срокам не связанный с менструацией. В октябре 2013 г. больной повторно была произведена компьютерная томография груди в высоком разрешении (томограф Aquilion Prime, Thoshiba), при которой на фоне пневмоторакса большого объема в верхушечном сегменте верхней доли правого легкого был выявлен фиброз. Под диафрагмой были визуализированы пузырьки газа (рис. 2).
 Рисунок 2. Компьютерная томограмма. а – аксиальный срез. В черном овале – газ под правой половиной диафрагмы; б – фронтальный срез. В белом овале – газ под правой половиной диафрагмы. Всего за период с апреля по ноябрь 2013 г. было зафиксировано 4 эпизода СП без клинических проявлений. Рецидивирующий СП и подозрение на эндометриоз диафрагмы явились показанием к оперативному лечению. 28.10.13 была выполнена ВТС. При ревизии выявлены изменения, характерные для эндометриоза диафрагмы и париетальной плевры (рис. 3, а, б).
Рисунок 2. Компьютерная томограмма. а – аксиальный срез. В черном овале – газ под правой половиной диафрагмы; б – фронтальный срез. В белом овале – газ под правой половиной диафрагмы. Всего за период с апреля по ноябрь 2013 г. было зафиксировано 4 эпизода СП без клинических проявлений. Рецидивирующий СП и подозрение на эндометриоз диафрагмы явились показанием к оперативному лечению. 28.10.13 была выполнена ВТС. При ревизии выявлены изменения, характерные для эндометриоза диафрагмы и париетальной плевры (рис. 3, а, б).
 Рисунок 3. Интраоперационные фотографии (больная Ч.). а – в белом круге множественные фенестрации сухожильного центра диафрагмы; б – очаг эндометриоза на париетальной плевре (черная стрелка). Произведены иссечение очага эндометриоза на париетальной плевре, резекция измененной сухожильной части диафрагмы. С целью плевродеза выполнена тотальная париетальная плевроабразия (рис. 3, в, г).
Рисунок 3. Интраоперационные фотографии (больная Ч.). а – в белом круге множественные фенестрации сухожильного центра диафрагмы; б – очаг эндометриоза на париетальной плевре (черная стрелка). Произведены иссечение очага эндометриоза на париетальной плевре, резекция измененной сухожильной части диафрагмы. С целью плевродеза выполнена тотальная париетальная плевроабразия (рис. 3, в, г).
 Рисунок 3. Интраоперационные фотографии (больная Ч.). в – выполнена резекция и плевроабразия диафрагмы; г – выполнена тотальная костальная плевроабразия. При гистологическом исследовании ткань была представлена железистым и стромальным компонентами с различными признаками функциональной активности (рис. 4).
Рисунок 3. Интраоперационные фотографии (больная Ч.). в – выполнена резекция и плевроабразия диафрагмы; г – выполнена тотальная костальная плевроабразия. При гистологическом исследовании ткань была представлена железистым и стромальным компонентами с различными признаками функциональной активности (рис. 4).
 Рисунок 4. Микрофотографии. а – эндометриоидная киста (стрелки) в фиброзной ткани диафрагмы. Окраска гематоксилином и эозином. Ув. 100; б – деталь рис. 4, а (квадрат). Кисту выстилает эндометриальный эпителий (ЭЭ стрелки), расположенный на эндометриальной строме (ЭС). Окраска гематоксилином и эозином. Ув. 400. Послеоперационный период протекал без осложнений.
Рисунок 4. Микрофотографии. а – эндометриоидная киста (стрелки) в фиброзной ткани диафрагмы. Окраска гематоксилином и эозином. Ув. 100; б – деталь рис. 4, а (квадрат). Кисту выстилает эндометриальный эпителий (ЭЭ стрелки), расположенный на эндометриальной строме (ЭС). Окраска гематоксилином и эозином. Ув. 400. Послеоперационный период протекал без осложнений.
После операции с целью системной терапии эндометриоза больной был назначен аналог гонадотропин-рилизинг-гормона (депо-форма).
В базе PubMed нами найдено 238 рефератов статей, посвященных ТЭ, и 234 реферата, посвященных КП, при этом часть из них относится к одним и те же источникам. В целом это примерно в 70 раз меньше, чем ссылок на статьи о СП – 21 120 ссылок. Это косвенно свидетельствует не только о незначительной распространенности этого заболевания, но и о недостаточной осведомленности о нем врачей.
Данные об эпидемиологии ТЭ и КП значительно различаются у разных авторов. Так, исследования, проведенные H. Nakamura и соавт. [16], показали, что из всех наблюдений вторичного пневмоторакса КП был у 2,8% женщин, оперированных по поводу рецидивного СП. T. Haga и соавт. [10] выявили ТЭ у 13,7% женщин с СП. A. Visouli и соавт. [22] считают, что у 25-30% женщин, нуждающихся в хирургическом лечении в связи с рецидивирующим СП, он связан с экстрагенитальным эндометриозом. С. Rousset-Jablonski и соавт. [20] проанализировали причины СП у 156 больных, у 68,6% из них он был некатамениальный. КП без выявленных признаков ТЭ имел место у 8,3% женщин. КП с выявленным ТЭ был отмечен у 15,4% больных. Некатамениальный пневмоторакс при наличии ТЭ был диагностирован у 7,7% больных. Та же группа исследователей, но во главе с M. Alifano [4] показала, что КП имел место у 24,6% женщин, а с учетом различных вариантов рецидивного некатамениального пневмоторакса, но связанного с ТЭ, его доля была значительно большей.
В основе патогенеза ТЭ лежит маточно-перитонеальный рефлюкс менструальной крови с последующей имплантацией клеток эндометрия по брюшной полости, в том числе в поддиафрагмальное пространство [1]. Особенности циркуляции жидкости в брюшной полости приводят к тому, что ТЭ справа встречают в 91,7% наблюдений, слева – в 4,8%, а билатеральное поражение наблюдали у 3,5% больных [4, 12, 13, 22]. При этом тазовый эндометриоз имел место у 58,8% больных с КП [20].
Основным путем распространения воздуха и развития СП во время менструации считают трансгенитальный – трансабдоминальный – трансдиафрагмальный путь [9]. Поражение диафрагмы эндометриозом и ее перфорация в результате циклических гормонально-зависимых процессов приводят к развитию КП [17, 19]. Поскольку описаны случаи рецидива КП у больных с плотным сращением диафрагмы и легкого, рассматриваются и другие механизмы развития КП [10, 19]. Так, еще в 50-60-е годы XX века в литературе были описаны наблюдения, свидетельствующие о выявлении децидуальной ткани в сосудах легких у женщин, умерших во время родов или ранее перенесших операции на матке, что подтверждает возможность гематогенного пути диссеминации клеток эндометрия [1, 7, 17].
Для диагностики вторичного характера пневмоторакса и профилактики рецидивов заболевания необходим алгоритм, позволяющий не только своевременно установить правильный клинический диагноз, но и выполнить оптимальный объем лечебных мероприятий.
Важным этапом дооперационного обследования больных является сбор анамнестических данных, позволяющий выяснить гинекологический анамнез: количество беременностей, родов, наличие болей внизу живота во время менструации, перенесенные хирургические вмешательства на органах женской половой сферы. Обязательным этапом обследования должен быть осмотр акушером-гинекологом, нацеленный на выявление генитального эндометриоза или его исключение. Другими важными симптомами, позволяющими выявить ТЭ, могут быть боли в груди в период менструации, катамениальный гемоптизис. Клинические наблюдения показали, что ТЭ проявляется пневмотораксом у 73% женщин, гемотораксом у 14%, гемоптизисом у 7%, рентгенологическими признаками новообразования в легком у 6% женщин [11]. Инструментальная диагностика ТЭ основана на выявлении характерных признаков этого заболевания. По сводным данным литературы с 1958 по 2004 г., из 195 больных с КП (85,2%) ТЭ был диагностирован у 52,1%, фенестрация диафрагмы – у 38,8% [12]. Исследования, проведенные D. Foster и соавт. [9], T. Roth и соавт. [19], A. Visouli и соавт. [22], выявили специфические рентгенологические симптомы как при обзорной рентгенографии, так и при компьютерной томографии, знание которых позволило нам в одном наблюдении заподозрить эндометриоз диафрагмы еще до операции.
Компьютерная томография является принципиально важным методом дооперационной диагностики ТЭ. Для выявления специфических для ТЭ изменений компьютерно-томографическое исследование необходимо проводить с коллимацией слоя не более 2 мм и интервалом реконструкции не более 2 мм. Из этого следует, что оптимального результата можно добиться, выполняя исследование на современных мультиспиральных томографах либо прицельно исследуя ограниченные области с указанными параметрами разрешения на односпиральных аппаратах. Анализируя изображение, необходимо прицельно оценить контуры диафрагмы. Высокое разрешение позволяет визуализировать в ней очаги эндометриоза. Кроме того, признаки пневмоторакса в сочетании с выявленными пузырьками газа под диафрагмой свидетельствуют о ее фенестрации (клиническое наблюдение 2) [19, 22]. При исследовании необходимо обратить внимание на выявление очаговых изменений легкого и на симптом «матового стекла», возникающий вследствие геморрагического пропитывания легочной ткани [6].
Наиболее достоверным методом диагностики ТЭ является ревизия плевральной полости в ходе ВТС. Применение современных миниинвазивных хирургических технологий способствовало увеличению частоты выявления специфических изменений диафрагмы до 78,6% [4]. Накопленный опыт лечения этого заболевания позволил выделить характерные изменения, возникающие при ТЭ. К ним относят округлые отверстия диаметром 3-5 мм и более в сухожильном центре диафрагмы [3, 5, 9, 12, 13, 18-20, 22], участки геморрагического пропитывания легкого при наличии или отсутствии воздушных пузырьков – блебов [17, 19, 22], бурые, белесые или синюшные узловые образования [3, 20, 22], геморрагический выпот [21]. Как следует из перечисленного, наиболее частым признаком ТЭ являются округлые или овальные отверстия в диафрагме, которые при далеко зашедшем заболевании могут сливаться между собой и приводить к частичному перемещению печени в плевральную полость [22]. Выявление при ВТС каких-либо изменений диафрагмы, легкого или париетальной плевры служит показанием к проведению биопсии этих участков с последующим их морфологическим исследованием. Подтверждение диагноза ТЭ необходимо для назначения патогенетически обоснованной терапии, которая способствует значительному улучшению отдаленных результатов хирургического вмешательства.
Среди гормональных препаратов наиболее часто используют агонисты гонадотропин-рилизинг-гормона (бусерелин лонг, диферелин, декапептил депо, золадекс и др.). Проведение такого лечения возможно лишь при морфологически подтвержденном ТЭ, поскольку это лечение связано со значительным количеством противопоказаний и побочных эффектов, что нередко приводит к необходимости досрочного прекращения терапии. Проведение курса гормонотерапии без хирургического устранения поражения легкого или диафрагмы практически во всех наблюдениях заканчивается рецидивом КП или другими проявлениями ТЭ [2, 14, 17]. Это объясняют более сложными условиями лечения экстрагенитального эндометриоза [2].
На основании патогенеза КП его лечение должно состоять из трех компонентов.
Первый компонент – устранение трансдиафрагмального (через дефекты диафрагмы) пути развития пневмоторакса. С этой целью необходимо выполнять резекцию диафрагмы сшивающими аппаратами или пластику методом диафрагмопликации, или с применением синтетических сетчатых имплантов. При наличии единичных мелких дефектов диафрагмы возможно их ушивание. Выявленные очаги эндометриоза нужно удалять с последующей гистологической верификацией. При наличии буллезных изменений показана атипичная резекция легкого с гистологическим исследованием удаленного препарата [8, 12, 13, 22].
Второй компонент – создание надежного плевродеза. С этой целью следует применять костальную париетальную плеврэктомию, механическую плевроабразию, плевродез тальком. Тем не менее применение только хирургических методов приводит к рецидиву КП у 14-50% больных [4, 5, 10, 11].
Третий компонент – гормональная терапия сроком не менее 6 мес после операции. Необходимость этого компонента лечения доказана наблюдениями рецидивов КП после преждевременного прекращения лечения и значительным числом безрецидивных результатов после проведения полного рекомендуемого курса [2, 6, 9, 12, 13, 18].
Таким образом, проблема торакального эндометриоза и катамениального пневмоторакса лежит в зоне ответственности как торакальных хирургов, так и акушеров-гинекологов. Тщательный сбор информации о больной при поступлении, детальная оценка данных лучевых методов исследования, ревизия плевральной полости с адекватной оценкой и гистологической верификацией всех выявленных изменений позволяют своевременно поставить диагноз и выбрать правильную тактику в отношении такого заболевания.
Источник
