Код мкб функциональный систолический шум

Рубрика МКБ-10: R01.0
МКБ-10 / R00-R99 КЛАСС XVIII Симптомы, признаки и отклонения от нормы, выявленные при клинических и лабораторных исследованиях, не классифицированные в других рубриках / R00-R09 Симптомы и признаки, относящиеся к системам кровообращения и дыхания / R01 Сердечные шумы и другие сердечные звуки
Определение и общие сведения[править]
Помимо тонов при аускультации над областью сердца и крупных сосудов можно услышать дополнительные звуки большей продолжительности – шумы. Шумы часто выслушивают у детей (даже у совершенно здоровых).
Выделяют две группы шумов: внутрисердечные и внесердечные.
Внутрисердечные шумы делят на органические, обусловленные наличием анатомических особенностей клапанов, отверстий или перегородок сердца, и функциональные, имеющие в основе нарушение функции клапанов, ускорение движения крови через неизменённые отверстия или снижение вязкости крови.
Этиология и патогенез[править]
Появление функциональных шумов может быть обусловлено различными причинами.
– Функциональные шумы характерны для детского возраста. Обычно функциональные шумы бывают систолическими, они непродолжительны, редко занимают всю систолу, обычно слышны в середине систолы. По звучанию функциональные шумы чаще мягкие, нежные, могут иметь «музыкальный» тембр; слышны на ограниченном участке и не проводятся далеко от места максимального выслушивания. Они непостоянны, изменяются в зависимости от положения тела (лучше выслушиваются в положении лёжа), фазы дыхания, физической нагрузки (меняют интенсивность и тембр), не сопровождаются изменениями I и II тонов, появлением дополнительных тонов, расширением границ сердца и признаками недостаточности кровообращения.
– В основе возникновения динамических шумов лежит значительное увеличение скорости кровотока, что отмечают при лихорадочных состояниях, тиреотоксикозе, неврозах, физическом и психическом напряжении и т.д. Появление шумов при анемии вызвано уменьшением вязкости крови в сочетании с некоторым ускорением кровотока и тахикардией.
– Появление функциональных шумов может быть обусловлено изменениями тонуса сосочковых мышц или всего миокарда, а также сосудистого тонуса, что приводит к неполному смыканию клапанов сердца и регургитации крови (дистрофия миокарда, СВД).
– Преходящие шумы могут быть связаны с продолжающимся формированием сердца, а также быть следствием неполного соответствия темпов развития различных сердечных структур, что обусловливает несоответствие размеров камер и отверстий сердца и кровеносных сосудов. Кроме того, возможна неравномерность роста отдельных створок клапанов и хорд, что приводит не только к временной несостоятельности запирающей функции клапанов, но и к изменению их резонансных свойств.
– Шумы возникают при наличии «малых аномалий» сердца и сосудов, когда отсутствуют гемодинамические расстройства, изменения размеров сердца и сократительной способности миокарда. Чаще всего это дополнительные хорды, аномальное расположение хорд, особенности строения сосочковых мышц и др.
Из внесердечных шумов наиболее часто выявляют шум трения перикарда (обычно слышен на определённом участке, не проводится в другие точки, усиливается при надавливании фонендоскопом на грудную клетку) и плевроперикардиальный шум (выслушивают по левому краю относительной тупости сердца, усиливается на высоте вдоха, исчезает при задержке дыхания).
Клинические проявления[править]
“Доброкачественные” и не причиняющие беспокойства сердечные шумы: Диагностика[править]
Дифференциальный диагноз[править]
“Доброкачественные” и не причиняющие беспокойства сердечные шумы: Лечение[править]
Профилактика[править]
Прочее[править]
Источники (ссылки)[править]
Детские болезни [Электронный ресурс] : учебник / Под ред. А.А. Баранова. – 2-е изд., испр. и доп. – М. : ГЭОТАР-Медиа, 2009. – https://www.rosmedlib.ru/book/ISBN9785970411162.html
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
Аритмия — нарушение частоты и ритма сердечных сокращений. Чаще наблюдается у пожилых людей. Факторы риска зависят от формы аритмии. Пол значения не имеет.
У здорового человека частота сердечных сокращений составляет 60-80 ударов в минуту. При аритмии нарушаются как частота, так и ритм сокращений желудочков и предсердий. Существует две формы аритмии: тахикардия (повышенная частота сердечных сокращении) и брадикардия (пониженная частота сердечных сокращений). Тахикардия может начинаться в желудочках или предсердиях и бывает как регулярной, так и хаотической. Самая тяжелая форма желудочковой аритмии – желудочковая фибрилляция, которая может закончиться остановкой сердца. Причиной брадикардии может быть синдром слабости синусового узла; наиболее опасное его проявление – полная блокада сердца. Большинство форм аритмии вызвано болезнями сердца и его сосудов. Повышенная частота сердечных сокращений не всегда является причиной для беспокойства.
При большой физической нагрузке или во время беременности частота сердечных сокращений повышается, а у людей в хорошей физической форме она, наоборот, ниже нормальной. Аритмия нарушает работу сердца, вызывая прилив крови к головному мозгу. Вне зависимости от тревожных ощущений, таких как тяжелые удары сердца, тяжесть состояния зависит от формы аритмии.
Причины большинства форм аритмии – болезни сердца и его сосудов, в основном ишемическая болезнь сердца. При этом ухудшается кровоснабжение сердца, в том числе и его проводящей системы, которая контролирует частоту сокращений сердца. Реже аритмию вызывают различные нарушения сердечных клапанов и воспаление сердечной мышцы. Некоторые формы аритмии вызваны врожденными пороками сердца, такими как нарушение проводимости между предсердиями и желудочками. Но эти нарушения развиваются только с возрастом.
Внесердечные причины аритмии – нарушение работы щитовидной железы или изменение биохимического состава крови (избыток калия). Некоторые лекарства – бронходилататоры, препараты дигиталиса также могут вызывать аритмию, как и табак или кофе.
Не всегда аритмия сопровождается симптомами, но их появление всегда внезапно. В их составе:
– неровное сердцебиение;
– головокружение, которое может закончиться потерей сознания;
– одышка;
– боль в груди и шее.
Возможными осложнениями являются инсульт и сердечная недостаточность.
При развитии аритмии следует обратиться к врачу. На приеме будет проверен пульс и выслушаны жалобы пациента. Для установления диагноза будет снята ЭКГ, которая покажет электрическую активность сердца. Поскольку некоторые формы аритмии проявляются периодически, пациента направят на непрерывную ЭКГ в течение 24 часов или он будет носить портативный кардиомонитор. Кроме того, необходимо провести исследование электрической проводимости сердца.
В некоторых случаях для лечения используют антиаритмические лекарства. Иногда назначают электрическую дефибрилляцию для восстановления нормальной работы сердца. Патологические источники возбуждения в сердце могут быть разрушены с помощью радиочастотной абляции, которую проводят параллельно с физиологическими исследованиями. При сниженной частоте сердечных сокращений вживляют искусственный водитель ритма, который восстанавливает нормальный сердечный ритм.
Прогноз зависит от формы аримии: наджелудочковая аритмия – не тяжелое заболевание, которое вряд ли повлияет на продолжительность жизни, но желудочковая фибрилляция – опасное для жизни состояние, при котором требуется срочная медицинская помощь.
Источник
Функциональный систолический шум у детей. Происхождение функционального систолического шума
Функциональный систолический шум детского типа может определяться в возрасте 20—25 и даже 30 лет, при этом, как правило, у лиц с тонкой грудной клеткой и астенической конституцией.
По вопросу о происхождении его у детей большинство авторов сходятся на той точке зрения, что он обусловлен так называемым функциональным (относительным) стенозом легочной артерии и ускоренным кровотоком через ее устье. По удивительным законам природы в сердце человека, несмотря на быстрое движение крови через атрио-вентрикулярные отверстия и устья крупных сосудов, не возникает шумов.
Это обусловлено соотношением величины отверстий, скоростью кровотока и физическими свойствами крови. Исключение, очевидно, составляет детский функциональный систолический шум. По данным Кубат (1965), у детей имеется несоответствие между темпом развития правого желудочка и легочной артерии, в результате чего возникает ее относительная узость. При наличии частого ритма и ускоренного кровотока создаются акустические условия для возникновения шума.
Эти же условия, очевидно, отмечаются и у лиц с астенической конституцией, а тонкая грудная стенка способствует хорошему проведению шума к поверхности грудной клетки.
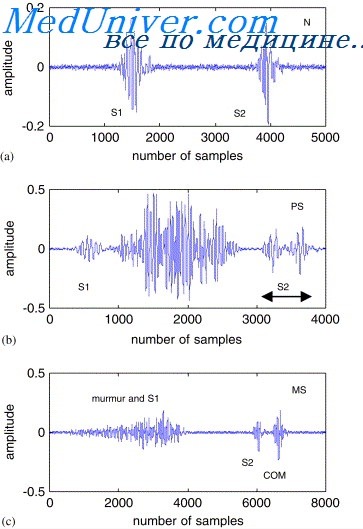
Первым подтверждением того, что этот шум связан с легочной артерией, является тот факт, что он оптимально определяется во II—III межреберье слева от грудины. Шум может усиливаться при физической нагрузке в связи с усилением кровотока через устье легочной артерии. Он также слышен и лучше записывается в положении лежа, что объясняется большим притоком крови к правому сердцу.
Окончательным доказательством генеза функционального систолического шума явилась запись внутрисердечной фонокардиограммы. Американские исследователи применили катетеризацию сердца в ряде сомнительных случаев с целью дифференциации функционального характера шума или его связи с врожденным пороком. При этом записывалась и внутрисердечная фонокардиограмма. Данные катетеризации показали отсутствие порока, а на внутрисердечной фонокардиограмме систолический шум записывался при положении микрофона у устья легочной артерии. При этом шум имел ту же характеристику, что и на обычной наружной фонокардиограмме.
В настоящее время наш опыт и опыт других исследователей позволяет дать довольно точную характеристику функционального систолического шума на легочной артерии, что помогает правильно его распознавать у большинства больных. При этом, конечно, следует учитывать анамнез, клинику, данные электрокардиограммы и рентгенологического исследования. В сомнительных случаях целесообразно использовать динамическое наблюдение на протяжении нескольких лет.
– Также рекомендуем “Признаки функционального систолического шума сердца. ФКГ при врожденных пороках сердца”
Оглавление темы “Фонокардиография в норме и при открытом артериальном протоке”:
1. Нормальная фонокардиограмма. Характеристика и состав I (первого) тона сердца
2. II тон сердца. Зависимость второго тона сердца от фаз дыхания
3. Нормальные изменения II тона сердца. Характеристика III (третьего) тона сердца
4. Характеристика IV и V тонов сердца. Фазы систолы и диастолы сердца
5. Функциональный систолический шум у детей. Происхождение функционального систолического шума
6. Признаки функционального систолического шума сердца. ФКГ при врожденных пороках сердца
7. Тоны сердца при открытом артериальном протоке. Шумы сердца при ОАП
8. Систолический шум при открытом артериальном протоке. Дифференциация шумов сердца при ОАП
9. Варианты открытого артериального протока. Шум Грехэм-Стила
10. Частота шума Грехэм Стила при открытом артериальном протоке. Шумовые признаки легочной гипертензии
Источник
Рубрика МКБ-10: I42.1
Содержание
Определение и общие сведения [ править ]
Гипертрофический субаортальный стеноз
Этиология и патогенез [ править ]
Хотя этиология подклапанного стеноза неизвестна, но, вероятно, анатомические или физиологические предпосылки к его развитию существуют с рождения. Дискретный тип обструкции под кольцом аортального клапана формируется с течением времени в результате аномальных сокращений либо аномального роста и гипертрофии. Предполагается мультифакториальная этиология субаортального стеноза, и в число возможных факторов входят такие морфологические особенности, как слишком крутой аортосептальный угол, удлиненный и узкий выводной тракт ЛЖ, избыточная степень изгиба корня аорты, генетическая предрасположенность. Указанные врожденные морфологические особенности строения выводного тракта ЛЖ повышают ге-модинамический стресс на участок межжелудочковой перегородки под аортальным клапаном, в результате чего возникает аномальная клеточная пролиферация с постепенным формированием фибромускулярного гребня.
Поэтому дискретная субаортальная мембрана не является врожденным образованием в истинном смысле этого слова. Она развивается в течение жизни постепенно из-за воздействия турбулентного кровотока на аномально сформированный выводной тракт ЛЖ. У этих пациентов с помощью двухмерной эхокардиографии показано, что угол между длинной осью ЛЖ и аортой является более острым, чем обычно. Турбулентный кровоток в выводном тракте ЛЖ вызывает гемодина-мическую травму эндокарда, а затем последующую пролиферацию и фиброз. Образующаяся фибромускулярная мембрана, в свою очередь, усиливает степень турбулентности потока крови, выходящего из ЛЖ, и вследствие постоянной гемодинамической травмы фиброз прогрессирует. Турбулентный поток также травмирует аортальные створки. Их последующее утолщение может привести к невозможности полного смыкания в диастоле либо к откровенному пролапсу, что приводит к аортальной недостаточности. В некоторых случаях фиброзная мембрана распространяется непосредственно под створки аортального клапана, вызывая их деформацию и усиливая регургитацию. Туннельный тип субаортального стеноза часто развивается вторично после предшествовавшей резекции простой субаортальной мембраны. Образование рубца в участке первичного иссечения фиброзного гребня в месте соединения с аномально сформированным выводным трактом ЛЖ может привести к прогрессирующей фибромышечной пролиферации с формированием туннеля в его выводном тракте. Митральный клапан тоже принимает участие в развитии этого туннельного повреждения благодаря расположению фиброзного тяжа, распространяющегося от перегородки к обращенной к ней поверхности передней створки МК.
К редким причинам субаортального стеноза относится септальное прикрепление створки МК либо избыточное развитие ткани эндокарда, прикрепленной к передней створке МК и выталкивающей ее в выводной тракт ЛЖ во время систолы. Обе эти формы обструкции обычно наблюдаются в сочетании с другими пороками, такими как неполный атриовентрикулярный канал либо L-транспозиция ТМС (кТМС).
Аортальная регургитация возникает приблизительно у 65% больных с подклапанным стенозом аорты и часто сохраняется после устранения субаортального стеноза. Она создает дополнительную нагрузку объемом на ЛЖ, уже страдающий от перегрузки давлением. Из-за аортальной регургитации снижается коронарный кровоток, что приводит к усилению ишемического повреждения миокарда. Нарастающая аортальная регургитация может потребовать протезирования аортального клапана после иссечения субаортальной мембраны.
Клинические проявления [ править ]
Для субаортального стеноза характерно его прогрессирование с постепенным нарастанием степени обструкции и присоединением аортальной недостаточности. Субаортальный стеноз редко проявляется клиническими симптомами до времени, пока он не становится достаточно выраженным. При аускультации слышен систолический шум изгнания на основании сердца, типичный для обструктивных пороков выводного тракта ЛЖ, и может быть усилен II тон. При значительной обструкции появляются интолерантность к нагрузке и ангинозные боли.
Хотя диагноз может быть поставлен в младенческом возрасте, клинически значимые симптомы субаортального стеноза редко требуют оперативного лечения до 3-6 лет, чаще всего это происходит в подростковом возрасте. К явным клиническим симптомам порока относятся левожелудочковая дисфункция и интолерантность к нагрузке, а боли за грудиной и синкопе встречаются реже.
В противоположность дискретной форме субаортального стеноза диффузный туннельный тип субаортальной обструкции часто является составным компонентом сложных наследственных синдромов.
Обструктивная гипертрофическая кардиомиопатия: Диагностика [ править ]
На прямой рентгенограмме грудной клетки при резко выраженном стенозе появляются кардиомегалия и признаки венозного застоя в легких. Однако даже у больных с выраженной подаортальной обструкцией размеры сердечной тени иногда бывают нормальными.
На электрокардиограмме признаки гипертрофии ЛЖ встречаются у 85% больных (в первую очередь в случаях с выраженной обструкцией).
Допплерэхокардиография уточняет локализацию и разновидность стеноза, градиент обструкции на участке сужения и степень гипертрофии стенок ЛЖ. Обычно визуализируются признаки дискретного стеноза (мембраны) под створками аортального клапана. Очень важна оценка компетентности аортального клапана, поскольку появление аортальной регургитации обычно является показанием к хирургическому вмешательству.
Катетеризация сердца помогает оценить градиент на участке сужения и его уровень, но при достаточной эхокардиографической информации она обычно не требуется для принятия решения по виду и срокам оперативного лечения. Правое и левое зондирование рекомендуется выполнять в случаях ассоциированных с субаортальным стенозом пороков сердца.
Дифференциальный диагноз [ править ]
Обструктивная гипертрофическая кардиомиопатия: Лечение [ править ]
До операции показан прием β-блокаторов либо блокаторов кальциевых каналов и по показаниям — двухкамерная стимуляция желудочков. Хирургическое лечение редко применяется в детстве при этом заболевании, однако септальная миоэктомия является безопасной и эффективной процедурой для уменьшения обструкции выводного тракта ЛЖ.
Хирургическое лечение показано при симптомах, возникших вследствие стеноза, либо при очевидных признаках прогрессирования стеноза по данным динамических исследований. Не следует дожидаться, пока при субаортальной обструкции появится застой в легких в результате повышения давления в ЛП.
У бессимптомных пациентов градиент в участке обструкции более 30 мм рт.ст. является показанием к операции при дискретном типе стеноза и более 50 мм рт.ст. — при туннельном типе субаортальной обструкции. Появление аортальной недостаточности даже при небольших значениях градиента тоже обычно свидетельствует о необходимости хирургического вмешательства. Некоторые хирурги оперируют таких больных сразу после установления диагноза с учетом прогрессирующего характера болезни и опасности дальнейшего гемодинамического повреждения аортального клапана.
Виды оперативного лечения
1. Лечение субаортального фибромускулярного стеноза
Резекция подклапанной фибромускулярной обструкции и септальная миоэктомия являются стандартными методами хирургического лечения этой формы болезни.
2. Лечение диффузных форм субаортального стеноза
Метод операции определяется состоянием кольца аортального клапана. Если оно хорошо развито, то выполняют септальную вентрику-лопластику, так называемую операцию Конно-Растана [Tabatabaie M. et al., 2006]. Если кольцо аортального клапана исходно гипоплазировано либо повреждено из-за гемодинамической травмы при субаортальном стенозе, то проводится аортовентрикулопластика, т.е. иссечение обструкции выводного тракта обоих желудочков (классическая процедура Konno-Rastan). При этом разрез по межжелудочковой перегородке распространяется вверх через аортальное кольцо и дополнительно протезируется аортальный клапан механическим протезом либо выполняется процедура Росса-Конно [Brown J. et al., 2006].
Профилактика [ править ]
Прочее [ править ]
Ранняя хирургическая летальность менее 3% в большинстве кардиохирургических центров. Выживаемость после оперативного лечения составляет 85-95% через 15 лет. Поздняя летальность обычно связана с резидуальной (повторной) подклапанной обструкцией и повторными операциями. Высокая частота рецидивов субаортальной обструкции (10-50% при 10-летнем наблюдении) ассоциирована с высоким предоперационным градиентом (>50 мм рт.ст.), туннельным типом обструкции, неполным удалением подаортальной мембраны, возрастом менее 10 лет на момент первой операции. Есть данные, что операция Росса-Конно снижает частоту послеоперационных рецидивов стеноза при туннельном типе обструкции.
Кардиомиопатии
142.0 Дилатационная кардиомиопатия
142.1 Обструктивная гипертрофическая кардиомиопа тия (гипертрофический субаортальный стеноз)
142.2 Другая гипертрофическая кардиомиопатия
142.3 Эндомиокардиальная (эозинофильная) болезнь (эндомиокардиальный тропический фиброз, эндо кардит Леффлера)
142.4 Эндокардиальный фиброэластоз (врожденная кар диомиопатия)
142.5 Другая рестриктивная кардиомиопатия
142.6 Алкогольная кардиомиопатия
142.7 Кардиомиопатия, обусловленная воздействием ле карственных средств и других внешних факторов
142.8 Другие кардиомиопатии
142.9 Кардиомиопатия неуточненная
143* Кардиомиопатия при болезнях, классифицированных в других рубриках
143.0* Кардиомиопатия при инфекционных и паразитарных болезнях, классифицированных в других рубриках
143.1 * Кардиомиопатия при метаболических нарушениях
143.2* Кардиомиопатия при расстройствах питания
143* Кардиомиопатия при болезнях, классифицированных в других рубриках.
Классификация кардиомиопатии (ВОЗ, 1996)
1. Дилатационная кардиомиопатия
2. Гипертрофическая кардиомиопатия
3. Рестриктивная кардиомиопатия (табл. 31)
4. Аритмогенная правожелудочковая дисплазия
5. Не классифицируемая кардиомиопатия Специфические:
Кардиомиопатия при клапанных заболеваниях сердца
Кардиомиопатия при воспалительных заболеваниях сердца
Кардиомиопатия при системных заболеваниях
Кардиомиопатия при мышечных дистрофиях
Кардиомиопатия при нейромышечных заболеваниях
Кардиомиопатия при гиперчувствительности и токсических реакциях
Дилатационную кардиомиопатию диагностируют при наличии дилатации и снижения систолической сократительной функции левого или обоих желудочков, симптомов застойной сердечной недостаточности в отсутствие данных о специфической причине, вызывавшей эти изменения (алкоголь, инфаркт миокарда, порок сердца, миокардит и др.).
Не классифицируемая кардиомиопатия отличается от дилатационной тем, что размеры желудочков сердца нормальные или незначительно расширены; при этом выявляются снижение систолической сократительной функции сердца, симптомы застойной сердечной недостаточности и отсутствие данных о специфической причине.
Гипертрофическую кардиомиопатию диагностируют при наличии выраженной гипертрофии миокарда в отсутствие специфической причины, вызывающей эти изменения (артериальная гипертензия, порок сердца и др.).
Клинико-морфологические формы гипертрофической кардиомиопатии
Симметричные (симметрическая концентрическая гипертрофия миокарда).
2. Асимметричные (гипертрофия межжелудочковой перегородки или верхушки).
3. Диффузные и локальные формы (диффузная — гипертрофия переднебоковой стенки левого желудочка и передневерхней части межжелудочковой перегородки — это идиопатический гипертрофический субаортальный стеноз: локальная — гипертрофия межжелудочковой перегородки).
Патофизиологические формы гипертрофической кардиомиопатии
Первичная рестриктивная кардиомиопатия характеризуется выраженной ригидностью желудочка(ов), следствием чего является нарушение диастолической функции, при отсутствии других инфильтративных заболеваний миокарда, вызывающих рестриктивные изменения.
Заболевания сердца, вызывающие рестриктивные изменения
(Wynne J., Braunwald Е., 2005)

Аритмогенная правожелубочковая дисплазия. Диагноз ставится при наличии дилатации и снижения систолической сократительной функции правого желудочка (редко — обоих желудочков) и желудочковых тахиаритмий, исходящих из правого желудочка.
Примеры формулировки диагноза
Основное заболевание: Дилатационная кардиомиопатия. Осложнения: Полная блокада левой ножки пучка Гиса. ХСН ПА (ФК III).
Код по МКБ-10 142.0.
Основное заболевание: Гипертрофическая кардиомиопатия, обструктивная форма. Осложнения: Пароксизмальная желудочковая тахикардия. ХСН І (ФК I).
Код по МКБ-10 142.1.
Основное заболевание: Гипертрофическая верхушечная кардиомиопатия.
Кодируется 142.2 как другая гипертрофическая кардиомиопатия
Обратим внимание: Термины «эндокринная кардиопатия», «тонзиллогенная кардиопатия» и т.п. в клиническом диагнозе не используют. Обычно в подобных случаях изменения сердца обусловлены специфическими заболеваниями, что требует уточнения диагноза. В этом случае код будет определяться в соответствии с основной болезнью.
Кардиомиопатия: что означает диагноз, как расшифровывается код по МКБ 10
 Кардиомиопатия – патология сердечной мышцы, имеющая в своей основе различные причины.
Кардиомиопатия – патология сердечной мышцы, имеющая в своей основе различные причины.
Заболевание может развиваться вследствие генетических нарушений, гормональных изменений, токсического воздействия лекарств, алкоголя, а также иных патологических состояний.
Кардиомиопатия как отдельная нозология имеет общий код по МКБ 10, обозначенный графой I42.
Виды и проявления
 Классификация изменений миокарда базируется на выделении патогенетических механизмов формирования кардиальных нарушений.
Классификация изменений миокарда базируется на выделении патогенетических механизмов формирования кардиальных нарушений.
Существуют семейные кардиомиопатии, причина которых кроется в наследственных факторах. Нередкостью становится гипертрофия с последующим изнашиванием сердечной мышцы у спортсменов.
Вопреки частому бессимптомному течению заболевания, кардиопатия может стать причиной внезапной смерти среди полного «здоровья» человека.
Обычно патология диагностируется при обращении пациентов с характерными кардиальными жалобами на сердцебиение, загрудинные боли, общее ухудшение состояния, слабость, головокружение, обмороки.
Какие изменения происходят
Существует несколько ответных процессов со стороны миокарда при воздействии повреждающего этиологического фактора:
- сердечная мышца может гипертрофироваться;
- полости желудочков и предсердий перерастягиваются и расширяются;
- непосредственно вследствие воспаления возникает перестройка миокарда.
Морфологически измененные ткани сердца не способны адекватно обеспечивать кровообращение. На первый план выходит сердечная недостаточность и/или аритмия.
Диагностика и лечение
 Кардиомиопатию диагностируют на основании анамнеза пациента с проведением дополнительных исследований. Одними из скрининговых методов являются ЭКГ (при необходимости с суточным мониторированием) и эхокардиография (посредством УЗИ). Для установления причины заболевания изучают лабораторные показатели крови и мочи.
Кардиомиопатию диагностируют на основании анамнеза пациента с проведением дополнительных исследований. Одними из скрининговых методов являются ЭКГ (при необходимости с суточным мониторированием) и эхокардиография (посредством УЗИ). Для установления причины заболевания изучают лабораторные показатели крови и мочи.
Терапия кардиопатии заключается в симптоматическом лечении основных проявлений. С этой целью назначаются таблетированные формы антиаритмиков, диуретиков, сердечных гликозидов. Для улучшения питания миокарда прописывают витамины, антиоксиданты, метаболические средства.
Чтобы облегчить работу сердца применяют препараты, уменьшающие сосудистое сопротивление (антагонисты кальция и бета-блокаторы).
При необходимости производят хирургическое вмешательство по установке водителя ритма.
Шифр в списке заболеваний
Среди болезней системы кровообращения (статья IX, I00-I99) диагноз «Кардиомиопатия» МКБ выделен в отдельную подстатью других заболеваний сердца наряду с крупными нозологическими группами.
Подразделение на кардиопатии в зависимости от проявлений и этиологии отражается в международном перечне болезней через точку после основного шифра.
 Так кардиомиопатия, развившаяся на основе длительного приема лекарственных препаратов, кодируется по МКБ 10 в виде I42.7.
Так кардиомиопатия, развившаяся на основе длительного приема лекарственных препаратов, кодируется по МКБ 10 в виде I42.7.
Патология миокарда часто выявляется в составе симптомокомплекса различных заболеваний.
Если сердечные нарушения становятся частью отдельной нозологии, то в МКБ 10 кардиомиопатия может шифроваться под рубрикой I43.
Источники:
https://wikimed.pro/index.php?title=%D0%9C%D0%9A%D0%91-10:I421
https://xn--80ahc0abogjs.com/kardiologiya_730/kardiomiopatii-46946.html
https://vseoserdce.ru/disease/cardiomyopathy/kardiomiopatiya-kod-po-mkb.html
Источник
