Код по мкб тиреотоксический зоб
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Симптомы
- Диагностика
- Причины
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Другие названия и синонимы
ДТЗ, Тиреотоксикоз, Базедова болезнь.
Названия
Диффузный токсический зоб.

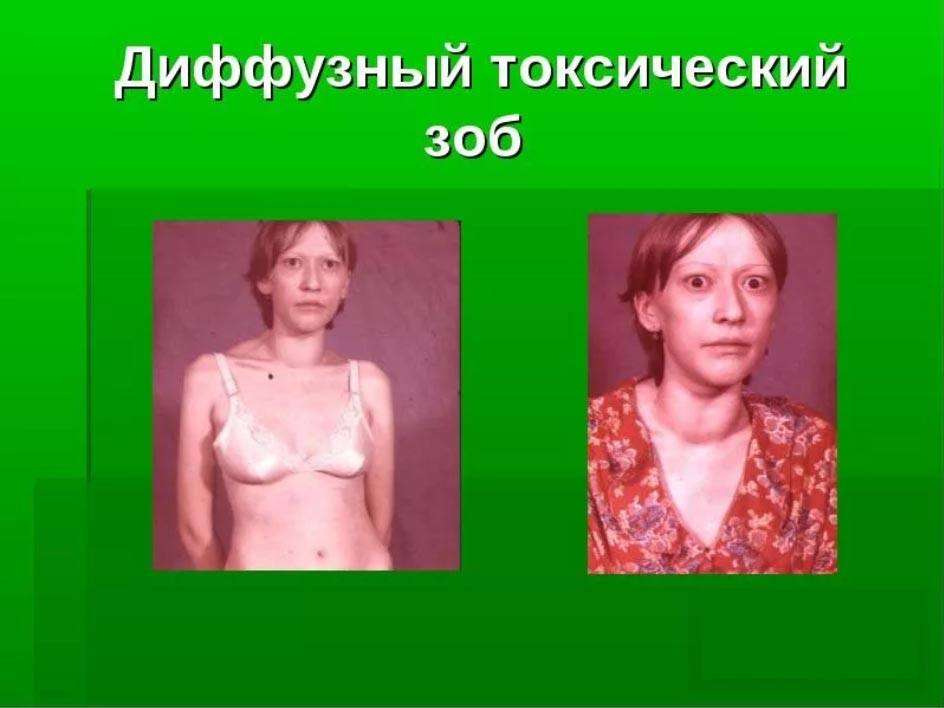
Диффузный токсический зоб
Описание
Болезнь Грейвса (болезнь Базедова, диффузный токсический зоб)- системное аутоиммунное заболевание, развивающееся вследствие выработки антител к рецептору тиреоторопного гормона, клинически проявляющееся поражением щитовидной железы с развитием синдрома тиреотоксикоза в сочетании с экстратиреоидной патологией: эндокринной офтальмопатией, претибиальной микседемой, акропатией. Впервые заболевание было описано в 1825 г. Калебом Парри, в 1835 г. – Робертом Грейвсом, а в 1840 г. – Карлом фон Базедовым.
Симптомы
Для диффузного токсического зоба, в большинстве случаев, характерен относительно короткий анамнез: первые симптомы обычно появляются за 4-6 месяцев до обращения к доктору и постановки диагноза. Как правило, ключевые жалобы связаны с изменениями со стороны сердечно-сосудистой системы, так называемым катаболическим синдромом и эндокринной офтальмопатией.
Основным симптомом со стороны сердечно-сосудистой системы является тахикардия и достаточно выраженные ощущения сердцебиений. Пациенты могут ощущать сердцебиения не только в грудной клетке, но и голове, руках, животе. ЧСС в покое при синусовой тахикардии, обусловленной тиреотоксикозом, может достигать 120-130 ударов в минуту.
При длительно существующем тиреотоксикозе, особенно у пожилых пациентов, развиваются выраженные дистрофические изменения в миокарде, частым проявлением которых являются суправентрикулярные нарушения ритма, а именно фибрилляция (мерцание) предсердий. Это осложнение тиреотоксикоза достаточно редко развивается у пациентов моложе 50 лет. Дальнейшее прогрессирование миокардиодистрофии приводит к развитию изменений миокарда желудочков и застойной сердечной недостаточности.
Как правило, выражен катаболический синдром, проявляющийся прогрессирующим похудением (порой на 10-15 кг и более, особенно у лиц с исходным избытком веса) на фоне нарастающей слабости и повышенного аппетита. Кожа больных горячая, иногда имеется выраженный гипергидроз. Характерно чувство жара, пациенты не мерзнут при достаточно низкой температуре в помещении. У некоторых пациентов (особенно в пожилом возрасте) может быть выявлен вечерний субфебрилитет.
Изменения со стороны нервной системы характеризуются психической лабильностью: эпизоды агрессивности, возбуждения, хаотичной непродуктивной деятельности сменяются плаксивостью, астенией (раздражительная слабость). Многие пациенты некритичны к своему состоянию и пытаются сохранить активный образ жизни на фоне достаточно тяжелого соматического состояния. Длительно существующий тиреотоксикоз сопровождается стойкими изменениями психики и личности пациента. Частым, но неспецифичным симптомом тиреотоксикоза является мелкий тремор: мелкая дрожь пальцев вытянутых рук выявляется у большинства пациентов. При тяжелом тиретоксикозе тремор может определяться во всем теле и даже затруднять речь пациента.
Для тиреотоксикоза характерны мышечная слабость и уменьшение объема мускулатуры, особенно проксимальных мышц рук и ног. Иногда развивается достаточно выраженная миопатия. Весьма редким осложнением является тиреотоксический гипокалиемический периодический паралич, который проявляется периодически возникающими резкими приступами мышечной слабости. При лабораторном исследовании выявляется гипокалиемия, повышение уровня КФК. Чаще встречается у представителей азиатской расы.
Интенсификация костной резорбции приводит к развитию синдрома остеопении, а сам тиреотоксикоз рассматривается как один из наиболее важных факторов риска остеопороза. Частыми жалобами пациентов являются выпадение волос, ломкость ногтей.
Изменения со стороны желудочно-кишечного тракта развиваются достаточно редко. У пожилых пациентов в ряде случаев может быть диарея. При длительно существующем тяжелом тиреотоксикозе могут развиваться дистрофические изменения в печени (тиреотоксический гепатоз).
Нарушения менструального цикла встречаются достаточно редко. В отличие от гипотиреоза, тиреотоксикоз умеренной выраженности может не сопровождаться снижением фертильности и не исключает возможности наступления беременности. Антитела к рецептору ТТГ проникают через плаценту, в связи с чем у детей, рожденных (1 %) от женщин с диффузным токсическим зобом (иногда спустя годы после проведенного радикального лечения), может развиться транзиторный неонатальный тиреотоксикоз. У мужчин тиреотоксикоз достаточно часто сопровождается эректильной дисфункцией.
При тяжелом тиреотоксикозе уряда пациентов выражены симптомы тиреогенной (относительной) надпочечниковой недостаточности, которую необходимо дифференцировать от истинной. К уже перечисленным симптомам добавляются гиперпигментация кожи, открытых частей тела (симптом Еллинека), артериальная гипотензия.
В большинстве случаев при диффузном токсическом зобе происходит увеличение размеров щитовидной железы, которое, как правило, имеет диффузный характер. Нередко железа увеличена значительно. В ряде случаев над щитовидной железой можно выслушать систолический шум. Тем не менее зоб не является облигатным симптомом диффузного токсического зоба, поскольку он отсутствует не менее чем у 25-30 % пациентов.
Ключевое значение в диагностике диффузного токсического зоба имеют изменения со стороны глаз ( выпучивание ), которые являются своеобразной «визитной карточкой» диффузного токсическогго зоба, т. Е. Их обнаружение у пациента с тиреотоксикозом практически однозначно свидетельствует именно о диффузном токсическом зобе, а не о другом заболевании. Очень часто благодаря наличию выраженной офтальмопатии в сочетании с симптомами тиреотоксикоза диагноз диффузный токсический зоб очевиден уже при осмотре пациента.
Клиническая картина тиреотоксикоза может иметь отклонения от классического варианта. Так, если у молодых диффузным токсическим зобом характеризуется развернутой клинической картиной, у пожилых пациентов ее течение зачастую олиго- или даже моносимптомное (нарушение ритма сердца, субфебрилитет). При «апатическом» варианте течения диффузного токсического зоба, который встречается у пожилых пациентов, клинические проявления включают потерю аппетита, депрессию, гиподинамию.
Весьма редким осложнением диффузного токсического зоба является тиреотоксический криз, патогенез которго не вполне понятен, так как криз может развиваться и без запредельного повышения уровня тиреоидных гормонов в крови. Причиной тиреотоксического криза могут оказаться сопутствующие диффузному токсическому зобу острые инфекционные заболевания, проведение оперативного вмешательства или терапии радиоактивным йодом на фоне выраженного тиреотоксикоза, отмена тиреостатической терапии, введение пациенту контрастного йодсодержащего препарата.
Клинические проявления тиреотоксического криза включают резкое утяжеление симптомов тиреотоксикоза, гипертермию, спутанность сознания, тошноту, рвоту, иногда диарею. Регистрируется синусовая тахикардия свыше 120 уд/мин. Нередко отмечается мерцательная аритмия, высокое пульсовое давление с последующей выраженной гипотонией. В клинической картине может доминировать сердечная недостаточность, респираторный дистресс-синдром. Нередко выражены проявления относительной надпочечниковой недостаточности в виде гиперпигментации кожи. Кожные покровы могут быть желтушны вследствие развития токсического гепатоза. При лабораторном исследовании может выявляться лейкоцитоз (даже при отсутствии сопутствующей инфекции), умеренная гиперкальциемия, повышение уровня щелочной фосфатазы. Смертность при тиреотоксическом кризе достигает 30-50 %.
Ассоциированные симптомы: Агрессивность. Боль в шее. Боль в шее спереди. Жажда. Жар во всем теле без температуры. Ломота в суставах. Лихорадка. Обострение обоняния. Общая потливость. Одышка. Опухание шеи. Осиплость голоса. Плаксивость. Повышенный аппетит. Понос (диарея). Потеря веса. Потливость. Раздражительность. Рвота. Тошнота. Тремор.
Диагностика
В анализе крови на гормвоны щитовидной железы наблюдается следующая картина:
• ТТГ снижен.
• Т3 и Т4 повышены.
• Тиреоглобулин и тироксинсвязывающий глобулин повышены или в норме.
• Достаточно часто повышаются антитела к ТТГ.
Причины
Диффузный токсический зоб является мультифакторным заболеванием, при котором генетические особенности иммунного реагирования реализуются на фоне действия факторов окружающей среды. Наряду с этнически ассоциированной генетической предрасположенностью (носительство гаплотипов HLA-B8, -DR3 и -DQA1*0501 у европейцев), в патогенезе диффузного токсического зоба определенное значение придается психосоциальным передовым факторам. Эмоциональные стрессорные и экзогенные факторы, такие как курение, могут способствовать реализации генетической предрасположенности к диффузному токсическому зобу. Курение повышает риск развития диффузного токсического зоба в 1,9 раза. Диффузный токсический зоб в ряде случаев сочетается с другими аутоиммунными эндокринными заболеваниями (сахарный диабет 1 типа, первичный гипокортицизм).
В результате нарушения иммунологической толерантности, аутореактивные лимфоциты (CD4+ и CD8+ Т-лимфоциты, В-лимфоциты) при участии адгезивных молекул (ICAM-1, ICAM-2, Е-селектин, VCAM-1, LFA-1, LFA-3, CD44) инфильтрируют паренхиму щитовидной железы, где распознают ряд антигенов, которые презентируются дендридными клетками, макрофагами и В-лимфоцитами. В дальнейшем цитокины и сигнальные молекулы инициируют антигенспецифическую стимуляцию В-лимфоцитов, в результате чего начинается продукция специфических иммуноглобулинов против различных компонентов тироцитов. В патогенезе диффузного токсического зоба основное значение придается образованию стимулирующих антител к рецептору ТТГ (АТ-рТТГ).
В отличие от других аутоиммунных заболеваний при диффузном токсическом зобе происходит не разрушение, а стимуляция органа-мишени. В данном случае аутоантитела вырабатываются к фрагменту рецептора ТТГ, который находится на мембране тироцитов. В результате взаимодействия с антителом этот рецептор приходит в активное состояние, запуская пострецепторный каскад синтеза тиреоидных гормонов (тиреотоксикоз) и, кроме того, стимулируя гипертрофию тироцитов (увеличение щитовидной железы). По не вполне понятным причинам сенсибилизированные к антигенам щитовидной железы Т-лимфоциты инфильтрируют и вызывают иммунное воспаление в ряде других структур, таких как ретробульбарная клетчатка (эндокринная офтальмопатия), клетчатка передней поверхности голени (претибиальная микседема).
Лечение
Существует три метода лечения диффузного токсического зоба (консервативное лечение тиреостатическими препаратами, хирургическое лечение и терапия 131I), при этом ни один из них не является этиотропным. В разных странах удельный вес использования указанных методов лечения традиционно отличается. Так, в Европейских странах в качестве первичного метода лечения наиболее принята консервативная терапия тиреостатиками, в США подавляющее большинство пациентов получает терапию 131I.
Консервативная терапия осуществляется при помощи препаратов тиомочевины, к которым относится тиамазол (мерказолил, тирозол, метизол) и пропилтиоурацила (ПТУ, пропицил). Механизм действия обоих препаратов заключается в том, что они активно накапливаются в щитовидной железе и блокируют синтез тиреоидных гормонов благодаря ингибированию тиреоидной пероксидазы, которая осуществляет присоединение йода к остаткам тирозина в тиреоглобулине.
Целью оперативного лечения, равно как и терапии 131I является удаление практически всей щитовидной железы, с одной стороны обеспечивающее развитие послеоперационного гипотиреоза (который достаточно легко компенсируется), а с другой – исключающее любую возможность рецидива тиреотоксикоза.
В большинстве стран мира основная часть пациентов с диффузним токсическим зобом, равно как и с другими формами токсического зоба, в качестве основного метода радикального лечения получает терапию радиоактивным 131I. Это связано с тем, что метод эффективен, неинвазивен, относительно недорог, лишен тех осложнений, которые могут развиться во время операции на щитовидной железе. Единственными противопоказаниями к лечению 131I являются беременность и грудное вскармливание. В значимых количествах 131I накапливается только в щитовидной железе; после попадания в нее он начинает распадаться с выделением бета-частиц, которые имеют длину пробега около 1-1,5 мм, что обеспечивает локальную лучевую деструкцию тироцитов. Существенное преимущество заключается в том, что лечение 131I можно проводить без предварительной подготовки тиреостатиками. При диффузном токсическом зобе, когда целью лечения является разрушение щитовидной железы, терапевтическая активность с учетом объема щитовидной железы, максимального захвата и времени полувыведения 131I из щитовидной железы рассчитывается исходя из предполагаемой поглощенной дозы в 200-300 Грей. При эмпирическом подходе пациенту без предварительных дозиметрических исследований при зобе небольшого размера назначается около 10 мКи, при зобе большего размера – 15-30 мКи. Гипотиреоз обычно развивается в течение 4-6 месяцев после введения 131I.
Особенность лечения диффузного токсического зобо во время беременности заключается в том, что тиреостатик (предпочтение отдается ПТУ, который хуже проникает через плаценту) назначается в минимально необходимой дозе (только по схеме «блокируй), которая необходима для поддержания уровня свободного Т4 на верхней границе нормы или несколько выше нее. Обычно по мере увеличения сроков беременности потребность втиреостатике уменьшается и большинство женщин после 25-30 недели препарат вообще не принимает. Тем не менее у большинства из них после родов (обычно через 3-6 месяцев) развивается рецидив заболевания.
Лечение тиреотоксического криза подразумевает интенсивные мероприятия с назначение больших доз тиреостатиков. Предпочтение отдается ПТУ в дозе 200-300 мг каждые 6 часов, при невозможности самостоятельного приема пациентом – через назогастральный зонд. Кроме того, назначаются ß-адреноблокаторы (пропранолол: 160-480 мг вдень per os или в в/в из расчета 2-5 м г/час), глюкокортикоиды (гидрокортизон: 50-100 мг каждые 4 часа или преднизолон (60 мг/сут), дезинтоксикационную терапию (физиологический раствор, 10 % раствор глюкозы) под контролем гемодинамики. Эффективным методом лечения тиреотоксического криза является плазмаферез.
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Также:
Тиреотоксическая аденома, болезнь Пламмера, мононодозный токсический зоб, автономная аденома щитовидной железы
Версия: Справочник заболеваний MedElement
Категории МКБ:
Тиреотоксикоз с токсическим одноузловым зобом (E05.1)
Разделы медицины:
Эндокринология
Общая информация
Краткое описание
Примечание. В большинстве литературных источников тиреотоксикоз с токсическим одноузловым зобом описывается под названием “тиреотоксическая аденома”, поэтому именно этот термин будет использоваться при дальнейшем описании заболевания.
Тиреотоксическая аденома – это гипертиреоидное состояние, сопровождающееся высоким уровнем
тиреоидных гормонов
в крови вследствие их повышенной секреции автономно функционирующей аденомой (узлом) щитовидной железы (ЩЖ).
Повышенное содержание
Т3
и
Т4
в крови приводит к ингибированию секреции
ТТГ
гипофизом, что сопровождается сниженной его концентрацией в сыворотке крови.
Как правило, тиреотоксическая аденома имеет небольшой размер (около 2,5-3 см в диаметре), тогда как солитарный эутиреоидный узел всегда обладает большими размерами (4-5 см в диаметре).
Особенность функциональной активности тиреотоксической аденомы заключается в том, что она избыточно секретирует тиреоидные гормоны автономно, независимо от секреции TТГ.
Облачная МИС “МедЭлемент”
Облачная МИС “МедЭлемент”
Классификация
По течению (по отсутствию или наличию тиреотоксикоза):
1. Компенсированная токсическая аденома – ткань ЩЖ продолжает функционировать нормально, продукция гормонов гипофизом относительно сохранна и признаки гипертиреоза проявляются незначительно.
2. Декомпенсированная форма токсической аденомы ЩЖ – характеризуется выраженными проявлениями
тиреотоксикоза
и значительным снижением продукции тиротропина гипоталамусом.
По результатам сцинтиграфии ЩЖ выделяют 3 варианта функциональной автономии:
1. Унифокальная – характрена для тиреотоксической аденомы.
2. Мультифокальная – характрена для многоузлового токсического зоба.
3. Диссеменированная – диффузное распределение автономно функционирующих тиреоцитов в виде мелкоузловых ареалов.
Первый и второй варианты отличаются числом “горячих” узлов. В последнем варианте, который встречается относительно редко, клинически значимые узлы ЩЖ отсутствуют либо зона насыщения 99mТс не соответствует узловым образованиям, выявляемым при УЗИ ЩЖ.
Этиология и патогенез
Механизм, посредством которого аденома приобретает автономность, не изучен полностью. Исследования, проводившиеся в последние годы, показывают, что способность аденом к повышенной автономной функциональной активности связана с мутацией гена рецептора к ТТГ или гена альфа-субъединицы белка G, что приводит к активации каскада
цАМФ
, а следовательно, усилению ответа на стимуляцию ТТГ.
Эти мутации вызывают рост и увеличение функциональной активности пораженных клеток, что в свою очередь приводит к формированию автономного узла, подавлению секреции ТТГ и снижению функции остальной части железы.
Способность отдельных участков ЩЖ приобретать автономную функцию связана с негенетическими и наследственными механизмами, включая паракринные и аутокринные регуляторные процессы. Процесс образования функциональной автономии занимает многие годы, а чаще десятилетия, в связи с чем она манифестирует у лиц пожилого возраста (чаще у женщин в возрасте 60 лет).
Патогенетическая особенность тиреотоксической аденомы (в отличие от тиреотоксикоза при диффузном токсическом зобе) – длительное субклиническое течение, предшествующее постепенной моносимптомной манифестации явного тиреотоксикоза.
Гистологически удаленная аденома состоит из скопления дифференцированных фолликулярных клеток, выстланных гиперплазированным эпителием (фолликулярная аденома).
Тиреотоксическая аденома, как правило, инкапсулирована и доброкачественна. Злокачественное перерождение автономно функционирующих узлов ЩЖ встречается редко. По некоторым данным, такая трансформация аденомы встречается у 2% взрослых (M.Smith и соавт., 1988) и у 11% детей (R.D.Croom и соавт., 1987).
Эпидемиология
Тиреотоксическая аденома в 3-5 раз чаще встречается у женщин в любом возрасте (с небольшим превалированием возраста 40-60 лет), особенно – у проживающих на территориях в условиях дефицита йода (эндемичных по зобу). Нередко встречается у детей.
Факторы и группы риска
Женщины в возрасте 40-60 лет, проживающие в эндемичных по зобу территориях (в условиях дефицита йода).
Клиническая картина
Cимптомы, течение
Клиническая картина тиреотоксической аденомы характеризуется симптомами тиреотоксикоза, сходными по клинике с диффузным токсическим зобом:
– снижение массы тела при отсутствии изменения в питании;
– учащенное сердцебиение, сохраняющееся в покое и во сне;
– мышечная слабость;
– плохая переносимость жары;
– потливость;
– раздражительность.
При тиреотоксической аденоме данные симптомы менее выражены, а само заболевание имеет медленное развитие; долгое время больные наблюдаются у эндокринолога по поводу узлового зоба.
Развитие опухоли происходит медленно. Когда она достигает крупного размера, то может сдавливать органы шеи. Единственными жалобами у пожилых пациентов могут быть учащенное сердцебиение и одышка при физической нагрузке, слабость, сонливость или бессонница.
Постепенно прогрессируют изменения со стороны сердечно-сосудистой системы: появляются
мерцательная аритмия
, тиреотоксическая миокардиодистрофия, которые в конечном итоге приводят к развитию сердечной недостаточности.
По мере течения заболевания у пациентов возникают нарушения со стороны желудочно-кишечного тракта, повышается артериальное давление, иногда появляется постоянное небольшое повышение температуры тела.
У больных отмечается влажная кожа, теплые конечности, изменения цвета кожи обычно отсутствуют.
Глазные симптомы тиреотоксикоза могут выявляться, но офтальмопатия, так же как и дермопатия (
претибиальная микседема
), при этом заболевании никогда не определяется.
Диагностика
Диагноз тиреотоксической аденомы устанавливается на основании следующих результатов исследований:
1. Опрос и осмотр больного. При пальпации щитовидной железы выявляется увеличение одной из ее долей, наличие узла. Узловое образование имеет эластичную консистенцию, округлую форму с отчетливыми краями и гладкой поверхностью, различную плотность; смещается при глотании.
2. Исследование содержания в крови гормонов щитовидной железы:
– наблюдается значительное повышение количества Т3 при умеренно повышенном или нормальном уровне Т4;
– количество ТТГ может быть нормальным или сниженным;
– тиреоидстимулирующие антитела не определяются.
3. Радиоизотопное сканирование щитовидной желез – позволяет обнаружить “горячий” узел, который активно накапливает радиоактивный йод. Поглощение его другими участками ЩЖ может быть резко снижено или полностью отсутствовать в связи с угнетением секреции ТТГ гипофизом.
Наиболее чувствительный метод диагностики функциональной автономии – сцинтиграфия на фоне приема тироксина (супрессионная сцинтиграфия). Подавление тироксином секреции ТТГ обуславливает то, что захват радиофармпрепарата осуществляется преимущественно автономно функционирующими участками.
L-тироксин назначается, как правило, в дозе 200 мкг на протяжении 10 дней, как метод подавить функцию ЩЖ и на этом фоне затем провести сцинтиграфию, чтобы лучше визуализировать автономные участки ткани.
О наличии функциональной автономии и высоком риске развития тиреотоксикоза свидетельствует результат, когда через 10 минут после введения радиофармпрепарата захват 99тТс-пертехнетата превышает 3%. Считается, что критический в отношении развития тиреотоксикоза объем автономной области составляет 15 мл (3 см в диаметре).
4. УЗИ щитовидной железы: обнаруживается узловое образование.
5. Биохимический анализ крови: выявляются признаки нарушения белкового, жирового и углеводного обмена.
Лабораторная диагностика
Лабораторно определяются:
– значительное повышение количества Т3 при умеренно повышенном или нормальном уровне Т4;
– количество в крови ТТГ может быть нормальным или сниженным;
– тиреоидстимулирующие антитела не определяются;
– в биохимическом анализе крови обнаруживают признаки нарушения белкового, жирового и углеводного обмена.
Дифференциальный диагноз
Для дифференциальной диагностики тиреотоксической аденомы используют пробы с угнетением трийодтиронином (Т3) или тиролиберином. Отрицательный результат проб подтверждает автономность функционирующей аденомы ЩЖ. Решающий фактом в пользу тиреотоксической аденомы – сцинтиграфия ЩЖ, где отмечается высокий захват 98mТс узлом (“горячий” узел) при пониженном захвате его остальной тканью ЩЖ.
Тиреотоксическая аденома наиболее часто дифференцируется со следующими заболеваниями:
1. Диффузный токсический зоб. Отличия от тиреотоксичекой аденомы:
– развивается в более молодом возрасте (ранее 50 лет);
– более короткий анамнез;
– диффузное увеличение щитовидной железы;
– равномерное поглощение радиофармпрепарата;
– в 30-50% случаев наблюдается эндокринная офтальмопатия;
– в 70-80% случаев выявляется высокий титр антител к рецепторам ТТГ, кроме того, могут определяться антитела к пероксидазе тиреоцитов и тиреоглобулину;
– на УЗИ отмечаются диффузное снижение эхогенности ткани ЩЖ, отсутствие узловых образований.
2. Многоузловой токсический зоб: при сцинтиграфии выявляются как “горячие”, так и “холодные” узлы.
3. Рак ЩЖ (высокодифференцированная аденокарцинома). Как правило, протекает в эутиреоидном состоянии. Различить цитопатологическую картину, наблюдаемую при токсической аденоме и раке ЩЖ, весьма трудно. Поэтому в данной ситуации тонкоигольная биопсия не помогает проведению дифференциальной диагностики.
В тех случаях, когда имеется “горячий” узел и происходит поглощение радиоизотопа в прилегающих областях при нормальной концентрации ТТГ в сыворотке крови, необходимо провести пробу с назначением Т3 (25 мкг 4 раза в день, в течение 10 дней). При повторном сканировании будет четко видно, что в окружающих “горячий” узел областях поглощения радиоизотопа отсутствуют в связи с ингибированием под влиянием экзогенного Т3 секреции ТТГ.
Осложнения
Вследствие поздней диагностики и длительного субклинического течения, а также неадекватного лечения возможно развитие следующих осложнений:
– фибрилляции предсердий;
– развитие сердечно-сосудистой недостаточности у пожилых пациентов при неадекватном лечении;
–
остеопороз
;
– сдавление окружающих органов и тканей при дальнейшем увеличении узла4
– злокачественное перерождение узла (редко).
Онлайн-консультация врача
Посоветоваться с опытным специалистом, не выходя из дома!
Консультация по вопросам здоровья от 2500 тг / 430 руб
Интерпретация результатов анализов, исследований
Второе мнение относительно диагноза, лечения
Выбрать врача
Лечение
1. Наблюдение (ежегодная сцинтиграфия и исследование уровней ТТГ, Т3, Т4) без активного лечения с запретом на введение препаратов йода показано в следующих случаях:
– при
эутиреозе
или небольшом подавлении ТТГ, при нормальном уровне Т3 и Т4;
– при отсутствии зоба;
– при отсутствии данных о тиреотоксикозе в прошлом;
– при захвате технеция (Тс) менее 2% при проведении супрессионной сцинтиграфии.
2. Тиреостатики (мерказолил, тиразол, пропицил) назначают только в качестве подготовки к операции и терапии радиоактивным йодом.
3. Операция показана при тиреотоксической аденоме с объемом автономной ткани более 3 см в диаметре, узловом, многоузловом токсическом зобе.
4. В остальных случаях (у больных в возрасте старше 40 лет), а также при противопоказаниях к операции проводят терапию радиоактивным йодом (300-400 г).
5. Пациенту необходимо обеспечить психический покой, полноценный сон. Больным нельзя находиться на открытом солнце. Назначается диета с большим содержанием белка в пище, витаминов. Иногда назначаются бета-адреноблокаторы.
Прогноз
Прогноз у большинства больных удовлетворительный.
После радикального лечения (терапия 131I, субтотальная резекция ЩЖ) при условии поддержания стойкого эутиреоза на фоне заместительной терапии препаратами тиреоидных гормонов (левотироксина натрия в индивидуальных дозах) качество жизни пациентов страдает незначительно.
Злокачественное перерождение аденомы после лечения радиоактивным йодом происходит исключительно редко, но при этом возможно дальнейшее увеличение узла.
Госпитализация
Сроки госпитализации зависят от тактики лечения (операция или терапия радиоактивным йодом).
Профилактика
Поскольку тиреотоксическая аденома чаще встречается в эндемичных по йоду областях и обусловлена йододефицитом, необходимо проведение массовой и индивидуальной профилактики йододефицитных заболеваний.
Массовая (популяционная) профилактика должна охватывать все население и обеспечивать минимально адекватный уровень потребления йода (150-200 мкг йода в сутки). Осуществляется путем реализации населению йодированной соли и использования ее в пищевой промышленности и животноводстве.
Индивидуальная (или групповая) профилактика направлена на группы населения, для которых дефицит йода наиболее опасен (беременные и кормящие женщины и дети в возрасте от 7 до 24 месяцев). Наряду с употреблением йодированной соли, рекомендуется прием лекарственных препаратов йода.
Информация
Источники и литература
- Braverman L. Diseases of the thyroid. – Humana Press, 2003
- Балаболкин М.И., Клебанова Е.М., Креминская В.М. Дифференциальная диагностика и лечение эндокринных заболеваний. Руководство, М., 2002
- Боднар П.Н. Эндокринология. Учебное пособие для иностранных учащихся, Киев, 1999
- Валдина Е.А. Заболевания щитовидной железы. Руководство, СПб: Питер, 2006
- Дедов И.И, Мельниченко Г.А. Эндокринология. Национальное руководство, 2012.
- Дедов И.И., Мельниченко Г.А, Герасимов Г.А. и др. Клинические рекомендации Российской ассоциации эндокринологов по диагностике и лечению аутоиммунного тиреоидита у взрослых. Клиническая тиреоидология, 2003
