Лами синдром что это такое

Лимфангиолейомиоматоз (ЛАМ) – это полисистемное заболевание, которое встречается редко и характеризуется прогрессирующей кистозной деструкцией ткани легкого, возникновением новообразований в органах брюшной полости и поражением лимфатической системы.
Как правило, заболеванию подвержены женщины репродуктивного возраста. Лимфангиолейомиоматоз способен развиваться без видимой причины или вследствие наследственной болезни.
Классификация
Существует две формы лимфангиолейомиоматоза:
- диффузная – отличается неуклонно прогрессирующим течением;
- очаговая – протекает более благоприятно, симптомы на ранних стадиях отсутствуют.
Клиническая картина
В начальной стадии заболевания клинические проявления обычно не наблюдаются. Лимфангиолейомиоматоз долго протекает без симптомов и случайно выявляется при рентгенологическом обследовании органов грудной клетки как межузловое или диффузное поражение ткани легкого. К основным клиническим проявлениям болезни относятся следующие симптомы:
- болезненные ощущения в грудной клетке, которые становятся сильнее при дыхании;
- одышка – возникает в результате развития обструкции дыхательных путей (сначала наблюдается при физических нагрузках, затем становится постоянной);
- кровохарканье (непостоянный признак);
- спонтанный рецидивирующий пневморакс (проявляется в виде внезапной боли в грудной клетке, одышки, отсутствия везикулярного дыхания);
- хилоторакс – сосредоточение хиллезной жидкости в плевральной области (совпадает с менструацией);
- хиллезный асцит и хилоперикардит (совпадает с менструацией и развивается в результате прогрессирования болезни);
- развитие легочного сердца (главным признаком является одышка, которая обычно усиливается при физических нагрузках).
Кроме того, у пациентов наблюдаются боли в области сердца, выраженная слабость, постоянные мигрени, бессонница ночью и сонливость днем, снижение аппетита, усиленная потливость.
Диагностика
Основными способами диагностирования при лимфангиолейомиоматозе легких являются:
- компьютерная томография высокого разрешения;
- VEGF-D тест;
- биопсия легкого;
- рентген грудной клетки;
- обследование функции внешнего дыхания.
Компьютерная томография высокого разрешения передает двухмерное изображение грудной клетки и легких. Такой способ диагностики при лимфангиолейомиоматозе является наиболее точным. Он позволяет определить аномальные скопления клеток в легких, кисты, увеличенные лимфатические узлы или коллапс легкого. Также настоятельно рекомендуется проведение компьютерной томографии брюшной полости, так как у 40% женщин обнаруживаются доброкачественные опухоли почек.
VEGF-D тест является первым обследованием, которое позволяет диагностировать лимфангиолейомиоматоз по анализу крови. Полученные результаты используются, чтобы отличить данное заболевание от различных кистозных болезней легких. Иногда, когда показатели VEGF-D теста выше установленного значения, для определения диагноза не требуется проведение хирургической биопсии. Такой способ диагностики на сегодняшний день используется только в США.
Биопсия легкого предусматривает взятие проб ткани органа дыхательной системы для последующего исследования под микроскопом. Таким способом можно выявить аномалии, которые свидетельствует о развитии лимфангиолейомиоматоза. Существует несколько методов проведения биопсии:
- торакоскопия (используется специальный инструмент – торакоскоп, который вводится через маленький разрез в стенке грудной клетки);
- трансбронхиальная биопсия (применяется гибкая длинная трубка – бронхоскоп, которая вставляется через нос в легкие и трахею);
- открытая биопсия (используется только в крайних случаях, взятие легочной ткани осуществляется через разрез между ребрами).
Рентген грудной клетки выдает изображение легких, сердца и окружающих тканей на экран. Такой вид диагностики способен выявить наличие коллапса, скопление жидкости вокруг легких, кисты. Однако рентген не считается оптимальным вариантом для обнаружения лимфангиолейомиоматоза.
При помощи исследования функций внешнего дыхания оценивается правильная работа легких. Для этого проводятся измерения количества и скорости вдыхаемого воздуха. Данный способ исследования предусматривает использование специального аппарата под названием спирометр. В него и дышит через мундштук пациент. Как правило, такой вид исследования используется достаточно редко при определении диагноза лимфангиолейомиоматоз.
Лечение
При лимфангиолейомиоматозе легких больные люди зачастую проходят стандартную терапию. Она заключается в трансплантации легкого. Правда, болезнь способна рецидивировать и в трансплантате. К альтернативным методам лечения относятся гормональная терапия, использование прогестинов, тамоксифенов, овариэктомии, однако они обычно оказываются неэффективными.
Прогноз
В целом, прогноз неблагоприятный. Правда, он до конца не понятен по причине редкости болезни и существенной вариабельности клинического состояния пациентов. Лимфангиолейомиоматоз медленно прогрессирует и, как правило, приводит к дыхательной недостаточности и летальному исходу. Необходимо знать, что развитие заболевания ускоряется во время беременности.
Источник
Лимфангиолейомиоматоз – заболевание, при котором в дыхательных органах разрастается гладкомышечная ткань. Патология редкая, точная этиология ее до сих пор неизвестна. Лечение проводится медикаментозно или хирургическим путем. Рассмотрим, лимфангиолейомиоматоз – что это, как обнаружить и вылечить болезнь.
Общие сведения
Лимфангиолейомиоматоз в МКБ 10 обозначен под кодом J84.8 и относится к болезням легких. Существуют иные наименования патологии: лейомиоматоз легких и диффузная лёгочная лимфангиэктазия.
Патология представляет собой разрастание гладких мышц вдоль бронхов, бронхиол, мелких сосудов в дыхательных органах. Легочная ткань подвергается мелкокистозной трансформации. Последствием изменений становится легочная недостаточность.
Болезнь возникает чаще всего на фоне туберозного склероза. Большинство случаев заболевания приходится на женщин, но встречается оно редко, 1-2 случая на 500 000 человек среднего возраста.
У женщин недуг может сочетаться с опухолями матки, почек, головного мозга. Обострение происходит во время беременности или при приеме препаратов с эстрогенами.

Симптомы заболевания
Признаки заболевания на начальной стадии мало заметны или вовсе отсутствуют. Так может продолжаться долгое время. Патология обнаруживается случайно при плановом рентгене грудной клетки. На снимке проявляются поражение легочной ткани в форме мелких узлов. На более поздних стадиях больных беспокоит одышка. Она появляется в результате обструкции дыхательных путей и ухудшения функционирования легких.
Кроме одышки, развитая форма болезни характеризуется следующими признаками:
- болевые ощущения в груди, особенно заметные;
- время от времени возникающее кровохарканье;
- спонтанный пневмоторакс;
- скопление жидкости в плевральной полости (хилоторакс);
- развитие легочного сердца.
При системном заболевании лейомиомы присутствуют в кишечнике, матке, брюшной полости, почках. Если развивается легочное сердце. Пациентов беспокоят слабость, учащенное сердцебиение, головные боли, бессонница, снижение аппетита.
Причины
Почему у людей, больных лимфангиолейомиоматозом легких, развивается эта патология, ученые ответить не могут. Выявлена косвенная зависимость изменений гормонального фона и болезни, поскольку развивается недуг в основном у женщин детородного возраста. Реже его диагностируют у мужчин.
Предполагается, что аномалию провоцирует избыточный выброс гормонов эстрогенов. Это объясняет, почему болезнь активизируется во время беременности и стихает в период климакса.
Сочетание недуга с лейомиомой также указывает на гормонозависимость заболевания. Врачи не исключают иммунные нарушения как причину патологии. Есть еще несколько версий:
- генетические нарушения в белках;
- патологическое разрастание мышечной ткани в иных органах, в матке;
- как результат удаления фибромиомы.
Лейомиоматозные клетки скапливаются вокруг мелких бронхов, бронхиол, сосудов, в плевре. Бронхиолы сужаются, их проходимость нарушается, образуются мелкие кисты, из-за чего нарушается состав газов.
Сдавление кистами стенок сосудов приводит к увеличению давления и развитию легочного сердца. При разрастании плевры в полости скапливается жидкость. В связи с тем, что именно эстрогены провоцируют размножение мышечных клеток, ученые пришли к выводу о гормонозависимости заболевания.
Как часто указывает википедия, синдром свайера и лимфангиолейомиоматоз нередко сочетаются. Обе болезни связаны с гормональным нарушением. Синдром свайера и лимфангиолейомиоматоз — это патологии, при которых в организме не вырабатываются женские или мужские гормоны. Неудивительно, что заболевания могут провоцировать друг друга.
Загадочный диагноз синдром свайера и лимфангиолейомиоматоз связаны тем, что при синдроме еще во внутриутробном развитии происходят нарушения хромосом. Половые клетки остаются недоразвитыми, не выделяются половые гормоны. При таком течение обстоятельств организм ребенка развивается по женскому типу.
Но даже в этом случае у малыша нет четко выделенных половых признаков. Генетические и гормональные нарушения вполне могут спровоцировать опухоли и разрастание мышечной ткани.
Классификация
Заболевание может развиваться как самостоятельное или как следствие туберозного склероза. Патологические изменения происходят в органах дыхания, но патология затрагивает организм. Болезнетворный процесс затрагивает мозг, брюшную полость, мочеполовую систему. В зависимости от того, насколько патология распространена в организме, она бывает очаговой или диффузной.
Очаговая форма отличается единичными очагами. Симптомы болезни обычно отсутствуют. Диагностируется недуг случайно, при плановом осмотре. При диффузной форме очаги множественные, располагаются в органах дыхания или за их пределами. Заболевание склонно к ускоренному развитию и приводит к нарушению работы сердца и дыхательных органов.
Возможные осложнения
Среди наиболее частых осложнений врачи называют скопление жидкости в плевральной или брюшной полости, в перикарде. Заболевание сочетается с разрастанием опухоли в почках или мозговой оболочке. Прогрессирование недуга проявляется при беременности или гормональных нарушениях.
Если опухоль разрастается, может увеличиться внутричерепное давление. На фоне кист прогрессирует дыхательная и сердечная недостаточность, нарушается кровообращение, возникает нехватка кислорода в крови.
При очаговой форме прогноз лимфангиолейомиоматоза легких может быть благоприятным. Недуг протекает бессимптомно и не влияет на качество жизни. Диффузная форма приводит к инвалидизации.
Диагностика
Первичный диагноз после осмотра ставит врач-пульмонолог. По симптомам он может заподозрить недуг и отправить больного на обследование. Общий анализ крови и мочи нельзя назвать информативным, поскольку особых изменений в показателях не происходит. Биохимический анализ крови показывает увеличение холестерина, глобулинов, ферментов.
К лабораторным анализам также относится исследование плевральной жидкости. Она имеет молочно-белый оттенок, мутная, в ней повышается содержание триглицеридов. В последнее время в качестве маркера при диагностике используется наличие сосудистого эндотелия в сыворотке крови пациентов.
К инструментальным методам диагностики относятся:
- Рентген легких. Показывает увеличенный объем легких, усиление сетчатого рисунка. Для очаговой формы также характерны затемнения диаметром от 0,5 до 1,5 см.
- Компьютерная томография. Метод исследования позволяет выделить множественные мелкие или крупные кисты. Получаемые данные настолько точные, что некоторые врачи для постановки диагноза исключают необходимость биопсии легких.
- Электрокардиография. Метод позволяет выявить развитие легочного сердца и другие изменения в органе.
Наряду с указанными методами диагностики могут проводиться исследование газов крови и вентиляционной способности легких. Для гистологического подтверждения диагноза назначается легочная биопсия.
Лимфангиолейомиоматоз надо дифференцировать с другими заболеваниями органов дыхания, такими как туберкулез, саркоидоз, патологии органов кроветворения. При постановке окончательного диагноза принимают участие медики разных специализаций: пульмонолог, кардиолог, фтизиатр, гинеколог.

Методы лечения
Схема лечения, которая позволила бы избавиться от заболевания, пока не разработана. Лечение лимфангиолейомиоматоза легких сводится к приему ингибиторов ферментов для регуляции клеточного роста, но эти методы пока находятся на экспериментальной стадии. Если патология прогрессирует, назначают медикаменты с прогестероном для коррекции гормонального фона.
В тяжелых стадиях, когда развивается легочная и сердечная недостаточность, принимается ряд мер для устранения осложнений:
- бронхолитики для ингаляций (расширяют бронхи, облегчают дыхание);
- терапия кислородом;
- препараты для улучшения работы сердца.
Если воздух скапливается в плевральной полости, выполняется плеврэктомия. Так называют операцию, при которой удаляются части плевры. Если указанные методы лечения оказываются неэффективными, в тяжелой стадии патологии производится трансплантация легких.
Профилактика болезни
Профилактические меры, которые бы защитили от заболевания, пока не существуют. Если недуг присутствует у женщины в начальной стадии, ей рекомендуется не беременеть и воздержаться от приема эстрогенных препаратов.
Не рекомендуется летать на самолете, чтобы не спровоцировать пневмоторакс. Чтобы избежать скопления жидкости, назначается рацион с низким содержанием жиров. Больным рекомендуют отказаться от вредных привычек. Чтобы предотвратить заболеваемость гриппом и пневмонией, нужно делать прививки.
Лимфангиолейомиоматоз — хоть и редкое, но серьезное заболевание, которое может серьезно ухудшить качество жизни. Своевременные профилактические меры и регулярный осмотр у врача помогут приостановить его на ранней стадии и облегчить состояние больного.

Автор:
Лешенкова Евгения
Терапевт, пульмонолог
Источник
Этиология (причины)
Спорадическим ЛАМ практически всегда болеют женщины. Лишь несколько случаев заболевания было выявлено среди мужчин. Первый из них был обнаружен у мужчины с туберозным склерозом, зарегистрированным в 2000 году в клинике Майо, командой врачей во главе с Генри Тазеларом.
Пролиферации гладких мышц, которые происходят в ЛАМ, часто наблюдаются у пациентов с туберозным склерозом (ТСК-ЛАМ), что показывает наличие клонов гладких мышц при почечной ангиомиолипоме у этих пациентов. Таким образом, считается, что они представляют собой метастаз этой «доброкачественной» опухоли. Отмечается явное преобладание женского пола среди больных ТСК-ЛАМ. ЛАМ болеют практически исключительно женщины. Средний возраст появления первых симптомов 34 года. Первые симптомы болезни могут появиться до изменений на рентгенограмме или функционального исследования лёгких; пока функциональные методы не покажут изменений болезнь сложно диагностировать. Часто существует значительная задержка между появлением первых симптомов и постановкой правильного диагноза.
Первые симптомы ЛАМ, как правило, начинаются с одышки при физической нагрузке и рецидивирующего пневмоторакса. В течении болезни может быть непродуктивный кашель, кровохарканье, лимфатический плевральный выпот или лимфатический асцит. Обструкция лёгочных венул вызывает застой в кровеносных сосудах и кровохарканье, лимфатическая обструкция приводит к хилотораксу и хилёзному асциту. Клиническое течение болезни у пациентов с ЛАМ имеет существенные различия. Болезнь, как полагают, медленно прогрессирует, что приводит к дыхательной недостаточности и смерти. 10-летняя выживаемость от начала болезни и появления первых симптомов составляет 49%, хотя сообщались цифры в диапазоне от 8.5-летней выживаемости вероятностью в 38% до 10-летней – 79%. Различия в выживаемости могут быть связаны с улучшением диагностики, особенно с применением КТ высокого разрешения, и это вовсе не означает, что прогрессирование болезни существенно изменилось.
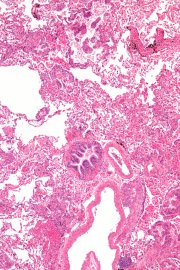
Диагностика лёгких бессимптомных форм также может внести свой вклад в больший процент выживаемости. Спирометрия у пациентов с ЛАМ показала наличие хронической обструкции дыхательных путей с увеличением объёма лёгких и снижением диффузии CO2. Межузловая радиологическая картина по результатам спирометрии у молодой женщины позволяет сузить круг дифференциальной диагностики некоторых форм эмфиземы, гистиоцитоза Лангерганса и саркоидоза. Информация, предоставленная HRCT имеет важное значение для дифференциации ЛАМ от этих заболеваний.
Многочисленные схемы лечения были описаны для лечения ЛАМ. В свете сообщений о клиническом обострении болезни во время беременности и использования экзогенных эстрогенов, многие врачи стали применять терапевтические способы снижения гормонов. Антиэстрогенная терапия, впервые использованная в начале 1980-х годов, состояла из хирургической кастрации или овариэктомии, назначении тамоксифена, прогестерона и гонадотропин-рилизинг гормона или агонистов лютеинизирующего гормона-рилизинг гормона. Некоторые исследования показали благотворное влияние антиэстрогенов в гормональной терапии ЛАМ, но тщательные изучения некоторых из этих исследований показывают, что лечение улучшило исход хилоторакса или хилёзного асцита, в то время как поражение лёгких оставалось прежним и не давало видимой положительной динамики, но в то же время и не прогрессировало. Несмотря на то, что трансплантация лёгких стала доступной для пациентов с плохим ответом на лекарственную терапию, всё же данную операцию необходимо производить с большой осторожностью и по крайней необходимости.
На самом деле, кастрация не даёт явного положительного влияния на течение болезни, а также не демонстрирует отдалённые последствия, особенно в послеоперационном периоде трансплантации легких, а наоборот способствует раннему разрушению костной структуры.
В большинстве случаев хилоторакс должен лечиться консервативно. Хилоторакс обычно появляется на ранних стадиях заболевания, когда общее состояние пациента удовлетворительное. Досрочное использование хирургических вмешательств, таких как плевральная пункция, плевродез или плеврэктомия следует избегать, так как эти процедуры могут снизить возможность дальнейшей трансплантации лёгких. Лечение включает в себя тамоксифен, прогестерон и, в некоторых случаях, диета с низким содержанием жиров.
Когда состояние пациента резко ухудшается, двусторонняя трансплантация лёгких является наилучшим методом лечения. Показаниями для трансплантации являются: прогрессия болезни, несмотря на проводимое лечение, снижение соотношения – объем форсированного выдоха за 1 секунду (ОФВ1) / форсированная жизненная емкость менее 50%. Общей ёмкости лёгких более чем на 130% и ОФВ1 менее 30%. В самой большой публикации по трансплантации лёгких у пациентов с ЛАМ, средний ОФВ1 во время оценки для проведения операции составляла 24%.
Общими послеоперационными осложнениями после проведения трансплантации являются: бактериальные, вирусные и грибковые инфекции; острого и хронического отторжения. Осложнениями специфичными для ЛАМ являются: пневмоторакс своего лёгкого после односторонней трансплантации лёгких, хилоторакс, повторный ЛАМ и осложнения со стороны органов брюшной полости.
Клиническая картина
ЛАМ болеют преимущественно женщины. Средний возраст появления первых симптомов 34 года. Первые симптомы болезни могут появиться до изменений на рентгенограмме или функционального исследования лёгких; пока функциональные методы не покажут изменений болезнь сложно диагностировать. Часто существует значительная задержка между появлением первых симптомов и постановкой правильного диагноза.
Первые симптомы ЛАМ, как правило, начинаются с одышки при физической нагрузке и рецидивирующего пневмоторакса. В течении болезни может быть непродуктивный кашель, кровохарканье, лимфатический плевральный выпот или лимфатический асцит. Обструкция лёгочных венул вызывает застой в кровеносных сосудах и кровохарканье, лимфатическая обструкция приводит к хилотораксу и хилёзному асциту. Клиническое течение болезни у пациентов с ЛАМ имеет существенные различия. Болезнь, как полагают, медленно прогрессирует, что приводит к дыхательной недостаточности и смерти. 10-летняя выживаемость от начала болезни и появления первых симптомов составляет 49%, хотя сообщались цифры в диапазоне от 8.5-летней выживаемости вероятностью в 38% до 10-летней – 79%. Различия в выживаемости могут быть связаны с улучшением диагностики, особенно с применением КТ высокого разрешения, и это вовсе не означает, что прогрессирование болезни существенно изменилось.
Диагностика лёгких бессимптомных форм также может внести свой вклад в больший процент выживаемости. Новые информационные данные рассказывают о некоторых пациентах с ЛАМ, которые прожили 20 лет и более. Исследования по ЛАМ значительно возросли с 1995 года, и каждый год есть улучшения в поиске новых схем лечения болезни.
Спирометрия у пациентов с ЛАМ показала наличие хронической обструкции дыхательных путей с увеличением объёма лёгких и снижением диффузии CO2. Межузловая радиологическая картина по результатам спирометрии у молодой женщины позволяет сузить круг дифференциальной диагностики некоторых форм эмфиземы, гистиоцитоза Лангерганса и саркоидоза. Информация, предоставленная HRCT имеет важное значение для дифференциации ЛАМ от этих заболеваний.
Сосудистый эндотелиальный фактор роста D повышается в сыворотке пациентов с ЛАМ. Типичные кистозные изменения на КТ высокого разрешения и уровень в сыворотке крови сосудистого эндотелиального фактора роста D более 800 пг / мл считаются диагностически значимыми для ЛАМ.
Для постановки диагноза некоторым пациентам может потребоваться биопсия. Видеоассистированная торакоскопическая биопсия является наиболее достоверным и широко используемым методом, но также очень эффективно использование трансбронхиальной биопсии. В некоторых случаях диагноз ЛАМ можно с уверенностью поставить на основании клинической картины (без биопсии) у пациентов с типичными кистозными изменениями на КТ высокого разрешения и обнаружения туберозного склероза, ангиомоилипомы или хилоторакса.
Многочисленные схемы лечения были описаны для лечения ЛАМ. В свете сообщений о клиническом обострении болезни во время беременности и использования экзогенных эстрогенов, многие врачи стали применять терапевтические способы снижения гормонов. Антиэстрогенная терапия, впервые использованная в начале 1980-х годов, состояла из хирургической кастрации или овариэктомии, назначении тамоксифена, прогестерона и гонадотропин-рилизинг гормона или агонистов лютеинизирующего гормона-рилизинг гормона. Некоторые исследования показали благотворное влияние антиэстрогенов в гормональной терапии ЛАМ, но тщательные изучения некоторых из этих исследований показывают, что лечение улучшило исход хилоторакса или хилёзного асцита, в то время как поражение лёгких оставалось прежним и не давало видимой положительной динамики, но в то же время и не прогрессировало. Несмотря на то, что трансплантация лёгких стала доступной для пациентов с плохим ответом на лекарственную терапию, всё же данную операцию необходимо производить с большой осторожностью и по крайней необходимости.
На самом деле, кастрация не даёт явного положительного влияния на течение болезни, а также не демонстрирует отдалённые последствия, особенно в послеоперационном периоде трансплантации легких, а наоборот способствует раннему разрушению костной структуры.
В большинстве случаев хилоторакс должен лечиться консервативно. Хилоторакс обычно появляется на ранних стадиях заболевания, когда общее состояние пациента удовлетворительное. Досрочное использование хирургических вмешательств, таких как плевральная пункция, плевродез или плеврэктомия следует избегать, так как эти процедуры могут снизить возможность дальнейшей трансплантации лёгких. Лечение включает в себя тамоксифен, прогестерон и, в некоторых случаях, диета с низким содержанием жиров.
Когда состояние пациента резко ухудшается, двусторонняя трансплантация лёгких является наилучшим методом лечения. Показаниями для трансплантации являются: прогрессия болезни, несмотря на проводимое лечение, снижение соотношения – объем форсированного выдоха за 1 секунду (ОФВ1) / форсированная жизненная емкость менее 50%. Общей ёмкости лёгких более чем на 130% и ОФВ1 менее 30%. В самой большой публикации по трансплантации лёгких у пациентов с ЛАМ, средний ОФВ1 во время оценки для проведения операции составляла 24%.
Общими послеоперационными осложнениями после проведения трансплантации являются: бактериальные, вирусные и грибковые инфекции; острого и хронического отторжения. Осложнениями специфичными для ЛАМ являются: пневмоторакс своего лёгкого после односторонней трансплантации лёгких, хилоторакс, повторный ЛАМ и осложнения со стороны органов брюшной полости.
Прогноз
Точные данные о выживаемости трудно собрать, так как ЛАМ часто диагностируется как астма или другие более распространенные заболевания и не может быть правильно определён, пока не достигнет развёрнутой клиники. Всесторонние исследования всех известных британских пациентов обнаружили, что из 21 пациента с ЛАМ, наблюдавшихся в течение 15 и более лет, 18 были ещё живы, и 11 из 12 пациентов, течение болезни у которых наблюдались в течение 20 и более лет были живы, однако многие из них вышли на инвалидность по дыхательной недостаточности.
Осложнения
• Ухудшение легочной недостаточности
• Пневмоторакс, вторичный по отношению к разрыву кисты в плевральную полость
• хилезный плевральный выпот
Лечение
Наличие ЛАМ у женщин детородного возраста предполагает, что гормональная стимуляция играет определенную роль в процессе развития болезни, на этой основе разработано несколько подходов к лечению, основанных на уменьшении эффекта эстрогенов.
В той или иной ситуации для лечения назначается:
• прогестерон
• удаление яичников
• тамоксифен
• агонисты гонадотропин-рилизинг гормона (ГнРГ)
• терапия андрогенами
Не один из этих методов не доказал своей 100% эффективности и каждый из них имеет свои побочные эффекты. Существует ряд фактов, которые подтверждают то, что тамоксифен может ухудшить течение ЛАМ у некоторых пациентов.
Когда функция лёгких снижается до состояния, при котором оксигенация становится неадекватной потребностям организма, рассматривается вопрос о трансплантации лёгких. После трансплантации лёгких состояние пациентов с ЛАМ оценивается по таблицам Каплана-Мейера (кривым выживания), как и других больных после трансплантации лёгких. Хотя, как сообщается по некоторым данным, ЛАМ повторяется в пересаженных легких, не было зарегистрировано ни одного случая отторжения трансплантата или смерти из-за рецидива ЛАМ..
Недавно сообщалось об одном случае положительного ответа при лечении доксициклином. Тем не менее, эта терапия не была подтверждена клиническими испытаниями.
Сиролимус недавно был испытан для лечении ЛАМ. Суд Миля (Международный Многоцентровой суд Сиромиля по эффективности в лечении ЛАМ) провёл рандомизированное, двойное слепое и плацебо-контролируемое исследования. Первичным пунктом исследования была скорость изменения функции легких в течение одного года после лечения. В общей сложности в исследовании участвовали 89 пациентов из 13 городов Соединенных Штатов, Японии и Канады. Чтобы участвовать в исследовании, пациенты должны иметь определённую стадию ЛАМ и нарушение функции лёгких. В целом, в исследовании приняли участие пациенты с умеренно тяжёлым течением ЛАМ и функцией лёгких около 50% от должной. Пациенты получали сиролимус или плацебо в течение одного года и эффект от лечения оценивался спустя один год. Анализ данных показал, что сиролимус стабилизирует функцию лёгких, улучшает некоторые показатели качества жизни и трудоспособности и снижает уровень сосудистого эндотелиального фактора роста D (VEGF-D) у пациентов с ЛАМ. Побочные эффекты чаще наблюдались в группе пациентов, принимающих сиролимус, но серьезные побочные эффекты были равномерно распределены между группами. Положительный эффект сиролимуса ослабевал после отмены приёма препарата и снижение функции лёгких возобновлялось. Вывод исследования заключался в том, что сиролимус может рассматриваться как препарат для лечения умеренно тяжёлого ЛАМ. Необходимы дополнительные исследования для определения рисков и преимуществ в лечении пациентов с более лёгкими формами заболевания и тех, кто принимает препарат более одного года.
Источник
