Лечение болевого синдрома клинические рекомендации
В данной статье отражены ключевые положения, определенные в клинических рекомендациях по ведению хронического болевого синдрома при оказании паллиативной медицинской помощи, разработанные и утвержденные в 2016 году несколькими профессиональными сообществами.
Международная организация по изучению боли (IASP) определяет боль, как неприятное сенсорное или эмоциональное переживание, связанное с фактическим или потенциальным повреждением тканей или описываемое в терминах такого повреждения [1]. Боль может быть симптомом различных заболеваний; по данным разных исследований, боль испытывают 41–77% пациентов, имеющих сердечно-сосудистые заболеваниях, 47–50% пациентов, имеющих почечную недостаточность, 67% – ХОБЛ, 63–80% – ВИЧ, 67% – цирроз печени, 43% – рассеянный склероз, 82% – болезнь Паркинсона, 47% – болезнь Альцгеймера и другие деменции, 89% – ревматоидный артрит, 64% – сахарный диабет, 90% – мультирезистентный туберкулез, 84% – онкологические заболевания [2]. Хронический болевой синдром (ХБС) не исполняет защитной функции и не несет никакой биологической целесообразности.
ДИАГНОСТИКА БОЛЕВОГО СИНДРОМА
Любое восприятие боли, которую ощущает пациент, субъективно, поэтому не существует «прибора» для объективного ее измерения. Регулярная оценка интенсивности боли имеет важное значение в терапии болевого синдрома (БС).
Основные принципы оценки БС:
- оценка интенсивности боли должна проводиться медицинским работником при каждом визите и осмотре пациента;
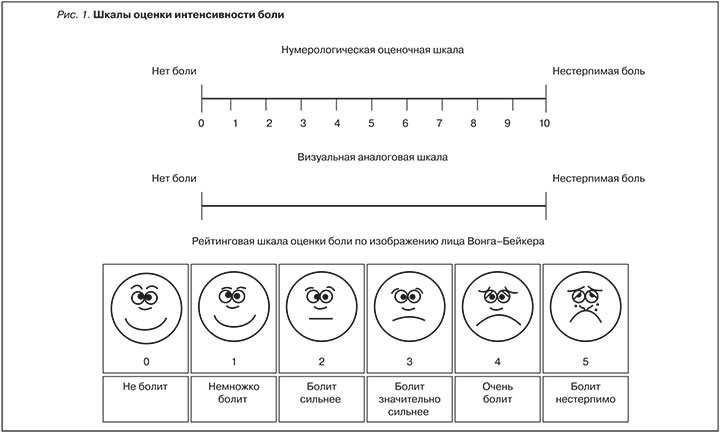
- интенсивность боли оценивается по оценочным шкалам (рис. 1), больному предлагается отметить свое восприятие боли в баллах или процентах;
- для более точного диагноза оценку интенсивности боли у пациента проводят раздельно – при движении и в покое.
Для оценки ХБС используют критерии, отражаемые в дневнике осмотра:
- число, локализация и характер очагов боли;
- длительность предшествующего болевого анамнеза;
- применение анальгетиков;
- эффективность предшествующей терапии (что ослабляет или усиливает боль);
- влияние боли на активность, сон, прием пищи и пр.
Сопоставив полученные сведения с клинической картиной и данными обследования, определяется интенсивность боли (слабая, умеренная, сильная). Оценка боли у лиц с когнитивными нарушениями основана на схожих принципах оценки боли у детей. Основой являются поведенческие реакции и возможность отвлечь или утешить, причем степень выраженности проявлений оценивается в динамике.
ОБЩИЕ ПРИНЦИПЫ ТЕРАПИИ ХРОНИЧЕСКОГО БОЛЕВОГО СИНДРОМА
Лекарственная терапия проводится в соответствии с основными принципами, провозглашенными Всемирной организацией здравоохранения (ВОЗ):
- «Через рот» – означает, что максимально следует исключить все инъекционные формы анальгетиков.
- «По часам» – анальгетики следует назначать регулярно по схеме, в соответствии с длительностью эффекта препарата, не дожидаясь развития боли.
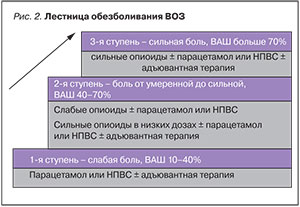
- «По восходящей» – подбор препаратов для обезболивания осуществляется от неопиоидных анальгетиков при слабой боли, слабыми опиоидами при умеренной боли и сильными опиоидными анальгетиками при сильной боли, по мере нарастания интенсивности боли, в соответствии с «лестницей обезболивания ВОЗ» (рис. 2).
- «Индивидуальный подход» – предполагает необходимость «индивидуального» подбора наиболее эффективного анальгетика в нужной дозе с наименьшими побочными эффектами.
- «С вниманием к деталям» – предполагает учет особенностей пациента и проведение мониторинга его состояния.
ТЕРАПИЯ ХРОНИЧЕСКОГО БОЛЕВОГО СИНДРОМА ПРИ ОКАЗАНИИ ПАЛЛИАТИВНОЙ МЕДИЦИНСКОЙ ПОМОЩИ
1-я ступень обезболивания
Интенсивность боли оценивается пациентом, как слабая, в пределах от 0 до 4 баллов по НОШ (ВАШ).
Рекомендация 1. На 1-й ступени фармакотерапии боли следует использовать неопиоидные анальгетики, при необходимости дополнительно назначать адъювантные анальгетики [3, 4].
2-я ступень обезболивания
Интенсивность боли оценивается пациентом, как умеренная, в пределах от 40 до 70% по НОШ (ВАШ), а адекватный ее контроль не достигается регулярным приемом парацетамола, НПВС и адъювантных анальгетиков.
Рекомендация 2. На 2-й ступени фармакотерапии боли использовать слабые опиоиды (трамадол, кодеин), при необходимости дополнительно назначать неопиоидные и адъювантные анальгетики [4, 5].
Рекомендация 3. Для терапии умеренной боли следует применять лекарственный препарат пропионилфенилэтоксиэтилпиперидин в защечных таблетках [6–8].
Рекомендация 4. При умеренно выраженной боли в качестве альтернативы трамадолу и кодеину возможно применять опиоиды 3-й ступени в низких дозах [9, 10].
С учетом зарегистрированных в РФ препаратов на 2-й ступени можно использовать:
- 1. морфин в таблетках или в капсулах продленного действия. Начальная доза составляет 10 мг 1–2 раза/сут (максимально до 30 мг/сут) [11–13];
- 2. оксикодон + налоксон в таблетках продленного действия. Стандартная начальная доза составляет 5/2,5 мг 1–2 раза/сут (максимально до 20 мг/сут). Налоксон, содержащийся в препарате, позволяет нивелировать побочные эффекты оксикодона в отношении риска развития запоров [14];
- 3. фентанил в трансдермальной форме (трансдермальная терапевтическая система – ТТС). Для терапии умеренной боли рекомендуется использовать в дозе до 12,5 мкг/ч [15].
Рекомендация 5. В качестве альтернативы пероральным опиоидам следует применять ТТС фентанила и бупренорфина без предпочтительного применения какого-либо из двух препаратов [9, 15, 16].
Рекомендация 6. В случае невозможности применения пероральных форм препаратов и использования ТТС следует назначать парентеральное введение морфина [4, 9, 17].
В качестве адъювантных анальгетиков на 2-й ступени применяют препараты 1-й ступени, а также кортикостероиды (дексаметазон, преднизолон, триамцинолон), спазмолитики (дротаверин, папаверин), миорелаксанты (толперизон, тизанидин, баклофен), антиконвульсанты (прегабалин, габапентин), антидепрессанты (амитриптилин, дулоксетин, сертралин). К препаратам 2-й ступени необходимо назначить терапию, уменьшающую побочные эффекты применяемых препаратов. В первую очередь это: противорвотные средства (метоклопрамид, домперидон, тиэтилперазин), блокаторы протонной помпы (омепразол, рабепразол, пантопразол), слабительные (лактулоза, макрогол).
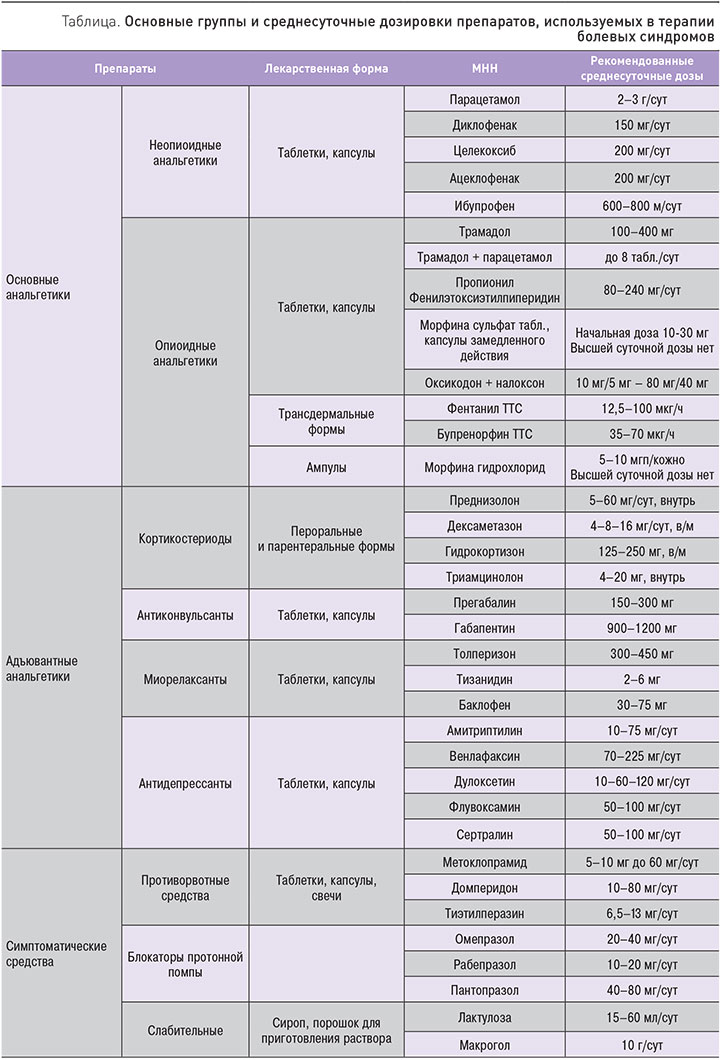
 Основные группы и среднесуточные дозировки используемых препаратов представлены в таблице.
Основные группы и среднесуточные дозировки используемых препаратов представлены в таблице.
3-я ступень обезболивания
Интенсивность боли оценивается пациентом как сильная, в пределах от 70 до 100% по НОШ (ВАШ), а адекватный ее контроль не достигается регулярным приемом препаратов 2-й ступени и адъювантных анальгетиков.
Рекомендация 7. На 3-й ступени фармакотерапии боли следует использовать сильные опиоиды, при необходимости дополнительно назначать неопиоидные и адъювантные анальгетики [9, 18].
К сильным опиоидам, зарегистрированым в РФ для терапии ХБС, относят морфин (в таблетках, капсулах, растворе), оксикодон + налоксон (в таблетках), фентанил (ТТС – пластырь) и бупренорфин (ТТС). У пациентов без нарушения функции глотания и явлений умеренной и выраженной почечной и печеночной недостаточности, с учетом их пожелания, терапию сильной боли начинают с таблетированных форм лекарственных препаратов (морфин и оксикодон + налоксон) [9]. В случае, если прием таблетированных форм невозможен, терапию начинают с ТТС фентанила или бупренорфина.
Рекомендация 8. Как альтернативу пероральным препаратам при нарушении функции глотания, тошноте и рвоте, почечной и печеночной недостаточности, отказе пациента от таблетированных форм, в случае наличия у пациента сильной боли постоянного характера, когда произведен подбор адекватной обезболивающей суточной дозы опиоидными препаратами короткого действия, следует использовать ТТС [19].
Рекомендация 9. Следует с осторожностью применять опиоиды у пациентов с печеночной и почечной недостаточностью [9, 13, 20, 21].
Морфин метаболизируется в печени с образованием активных метаболитов, которые выводятся преимущественно почками – 85%, с желчью – 10%. Из-за особенностей элиминации следует снижать его дозу у пациентов с нарушением кишечного пассажа (при запорах), умеренной почечной и печеночной недостаточностью. Фентанил, в отличие от морфина, имеет неактивные метаболиты и является преимущественным для пациентов со средней и тяжелой степенью выраженности почечной и печеночной недостаточности.
Рекомендация 10. Следует назначать морфин парентерально пациентам, которым невозможно по различным причинам обеспечить адекватное обезболивание неинвазивными анальгетиками [4, 9, 16, 19].
Подкожный путь введения является эффективным в качестве альтернативного метода у пациентов, неспособных принимать опиоиды пероральным или трансдермальным способами. Внутривенные инфузии применяются в том случае, когда подкожное введение препарата противопоказано. Внутримышечный путь введения препаратов следует избегать.
Рекомендация 11. При переходе с одного опиоида на другой, осуществляемом из-за недостаточного обезболивания и/или избыточных побочных эффектов, использовать начальную дозировку нового препарата ниже, чем дозировку, рассчитанную по таблицам соответствия доз опиоидов по анальгезирующему эффекту [4, 16]. При смене опиоидов следует обеспечить безопасность приема препарата в отношении передозировки. Риски, связанные со сменой препаратов, являются управляемыми, если использовать таблицу эквивалентных доз.
Рекомендация 12. Не рекомендуется чередование опиоидов без необходимости [9, 21]. Менять опиоидный анальгетик и/или путь его введения следует только при недостаточном обезболивающем эффекте на фоне высоких доз препарата и/или при развитии непереносимых побочных эффектов.
Рекомендация 13. Не рекомендуется использовать тримеперидин (таблетки, раствор) для длительной терапии боли [22]. Тримеперидин подвергается биотрансформации с образованием нейротоксичного Н-деметилированного метаболита, который стимулирует ЦНС (возможны тремор, подергивания мышц, гиперрефлексия, судороги). Метаболит имеет период полураспада 15–20 ч, поэтому может наблюдаться кумулятивный эффект.
Титрование дозы и терапия «прорывов боли»
Рекомендация 14. При подборе необходимой дозы базового обезболивания с применением препаратов в пролонгированных формах проводить ее титрование препаратами короткого действия [9, 12, 23]. Для титрования дозы возможно использовать раствор морфина для подкожного или внутривенного введения, в эквивалентной дозе 1/12 от пероральной суточной дозы. При подборе необходимой дозы базового обезболивания с применением пероральных препаратов морфина и оксикодон + налоксон следует увеличивать разовую дозу на 5–15% (1/6) от суточной дозы [12].
Рекомендация 15. Для экстренной терапии резкого, спонтанного или эпизодически возникающего приступа боли на фоне приема препаратов в пролонгированных формах («прорыв боли») назначать препараты быстрого действия («препарат спасения») [3, 5, 9, 11, 24]. Для купирования прорывной боли на фоне применения ТТС фентанила не используется трамадол.
Рекомендация 16. Следует использовать для контроля предсказуемых эпизодов прорывной боли, за 20–30 мин до провоцирующего воздействия, опиоиды с немедленным высвобождением и коротким действием [4, 13].
Лечение осложнений опиоидной терапии
Рекомендация 17. Дополнительно к опиоидам назначать слабительные средства как сопроводительную терапию [4, 16].
Рекомендация 18. Применять дофаминергические препараты (например, галоперидол) и препараты с дофаминергическими дополнительными действиями (например, метоклопрамид) для лечения тошноты и рвоты, связанных с приемом опиоидов [4, 19, 25]. Длительность назначения антиэметиков на фоне опиоидной терапии около 2 нед. Если тошнота сохраняется, необходимо назначить или скорректировать дозировку противорвотных средств или сменить опиоид.
Рекомендация 19. Пациентам с умеренными или тяжелыми явлениями со стороны ЦНС (когнитивные расстройства, сонливость), связанными с применением опиоидов, снижать их дозировки, если БС контролируется достаточно, или менять опиоидный препарат, если БС не контролируется [26, 27].
Обезболивание в последние часы жизни
Рекомендация 20. Не рекомендуется снижать подобранную дозу опиоидов из-за пониженного уровня артериального давления или спутанности сознания (если они не являются следствием применения неверно подобранной дозы).
Рекомендация 21. Следует сохранять прием опиоидов даже при отсутствии сознания, применяя титрование дозы до эффективной.
Рекомендация 22. Отменять опиоиды следует путем постепенного снижения дозы препарата [26, 27]. При необходимости снижения дозы анальгетика уменьшать ее следует не более чем на 50% в течение суток, чтобы избежать прорыва БС, для профилактики синдрома отмены и не причинить страдания пациенту.
Рекомендация 23. Оценивать уровень и динамику других тягостных симптомов, которые могут усиливать страдания пациента [26, 27].
Рекомендация 24. При рефрактерности БС решить вопрос возможной медикаментозной седации [26, 27]. Вопрос седации обсуждается с пациентом и/или его законным представителем и решается на заседании врачебной комиссии. В некоторых клинических случаях медикаментозная седация является единственным методом, способным обеспечить адекватное обезболивание и облегчение страданий пациента.
В данной статье отражены ключевые положения, определенные в клинических рекомендациях по ведению ХБС при оказании паллиативной медицинской помощи, разработанные и утвержденные в 2016 г. несколькими профессиональными сообществами. Основными разработчиками рекомендаций явились Ассоциация профессиональных участников хосписной помощи, Ассоциация междисциплинарной медицины, Общество специалистов доказательной медицины и Российское научное медицинское общество терапевтов.
- IASP //www.iasp-pain.org.
- Worldwide palliative care alliance (WPCA); World Health Organization 2015.-https://www.who.int/nmh/Global_Atlas_of_Palliative_Care.pdf
- Jost L., Roila F., ESMO Guidelines Working Group. Management of cancer pain: ESMO Clinical Practice Guidelines. Ann. Oncol. 2010;21(5):257–60.
- Обезболивание при раке и паллиативное лечение: доклад комитета экспертов ВОЗ. Женева, 1992. 76 с. URL: https://www.who.int/iris/handle/10665/89602.
- Caraceni A., Hanks G., Kaasa S., Bennett M.I., Brunelli C., Cherny N., Dale O., De Conno F., Fallon M., Hanna M., Haugen D.F., Juhl G., King S., Klepstad P., Laugsand E.A., Maltoni M., Mercadante S., Nabal M., Pigni A., Radbruch L., Reid C., Sjogren P., Stone P.C., Tassinari D., Zeppetella G. Use of opioid analgesics in the treatment of cancer pain: evidence-based recommendations from the EAPC. Lancet Oncol. 2012;13:58–68.
- Glossary of globalization, trade and health terms of the World Health Organization. https://who.int/trade/glossary/en/.
- Clinical pain management. Cancer pain. Edited by N. Sykes, M.I. Bennett, C. Yuan. 2nd edition. Hodder Arnold, UK London: 2008. 443 p.
- Fisch M.J., Burton A.W. Cancer pain management. The McGraw-Hill C. 2006. 319 p.
- Lussier D., Portenoy R.K. Adjuvant analgesic drugs. In: Bruera E., Higginson I.J., Ripamonti C., von Gunten C., editors. Textbook of palliative medicine. London: Edward Arnold Publishers. 2006:402–14.
- Новиков Г.А. Основы паллиативной помощи онкологическим больным с хронической болью: дис. … д-ра мед. наук. М.: 1994. 224 с.
- Абузарова Г.Р. Просидол в лечении хронического болевого синдрома у онкологических больных: дис. … канд. мед. наук. М.: 2001. 124 с.
- Инструкция к препарату пропионилфенилэтоксиэтилпиперидин на официальном сайте Государственного реестра лекарственных средств https://grls.rosminzdrav.ru/
- Davies A.N., Dickman A., Reid C., Stevens A.M., Zeppetella G. The management of cancer-related breakthrough pain: recommendations of a task group of the Science Committee of the Association for palliative medicine of Great Britain and Ireland. Eur. J. Pain. 2009;13:331–8.
- Hanks G.W., Conno F., Cherny N., Hanna M., Kalso E., McQuay H.J., Mercadante S., Meynadier J., Poulain P., Ripamonti C., Radbruch L., Casas J.R., Sawe J., Twycross R.G., Ventafridda V. Morphine and alternative opioids in cancer pain: The EAPC recommendations. Br. J. Cancer. 2001;84:587–93.
- Инструкция к препарату морфин сульфат на официальном сайте Государственный реестр лекарственных средств https://grls.rosminzdrav.ru/
- Инструкция к препарату таргин (оксикодон+налоксон) на официальном сайте Государственный реестр лекарственных средств https://grls.rosminzdrav.ru/
- Пчелинцев М.В. Проблемы применения сильных опиоидов при хронической боли в России. Возможные пути их решения. Русский врач. 2013;5:19–22.
- National Institute for Health and Clinical Effectiveness (NICE). Guide to the Methods of Technology Appraisal
- Инструкция к препарату ТТС фентанила на официальном сайте Государственный реестр лекарственных средств https://grls.rosminzdrav.ru/
- Caraceni A., Cherny N., Fainsinger R., Kaasa S., Poulain P., Radbruch L., De Conno F. The Steering Committee of the EAPC Research Network. Pain measurement tools and methods in clinical research in palliative care: recommendations of an expert working group of the European Association of Palliative Care. J. Pain Symptom Manage. 2002;3;239–55.
- Moore R.A., Mc. Quay H.J. Prevalence of opioid adverse events in chronic nonmalignant pain: systematic review of randomised trials of oral opioids. Arthritis Res. Ther. 2005;7(5):1046–51.
- Morita T., Takigawa C., Onishi H., Tajima T., Tani K., Matsubara T., Miyoshi I., Ikenaga M., Akechi T., Uchitomi Y. Opioid rotation from morphine to fentanyl in delirious cancer patients: an open-label trial. J. Pain Symptom Manage. 2005;30(1):96–103.
- Freye E., Levy J.V., Braun D. Effervescent morphine results in faster relief of breakthrough pain in patients compared to immediate release morphine sulfate tablet. Pain Practice. 2007;7:324–31.
- Cancer Pain. Assessment and management: edited by Bruera E.D., Potenoy R.K. 2nd edition. Cambridge Uniersity Press, 2010. 643 p.
- Kurz A., Sessler D.I. Opioid-induced bowel dysfunction: pathophysiology and potential new therapies. Drugs. 2003;63(7):649–71.
- Swarm R.A., Paice J. et al. National comprehensive cancer network NCCN Clinical practice Guidelines in oncology, 2014. https://utah.pure.elsevier.com/en/publications/adult-cancer-pain-clinical-practice-guidelines-in-oncology.
- Oscar A.L.C. Cancer pain: pharmacological, interventional, and palliative approaches. Saunders Elsevier. Philadelphia. USA. 2006. 591 p.
Диана Владимировна Невзорова, к.м.н., главный врач ГКУЗ «Хоспис № 1 им. В.В. Миллионщиковой ДЗМ», главный внештатный специалист по паллиативной помощи ДЗМ. Адрес: 119048, г. Москва, ул. Доватора,
д. 10. Тел.: (499) 245-59-69. E-mail: gyn_nevzorova@mail.ru
Гузель Рафаиловна Абузарова, д.м.н., руководитель Центра паллиативной помощи онкологическим больным ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена», профессор кафедры онкологии и радиотерапии ИПО ФГБОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова». Адрес: 125284, г. Москва, 2-й Боткинский пр., д. 3. E-mail: abuzarova_mnioi@bk.ru
Источник
1. 2014 Клинические рекомендации “Болевой синдром” (Общероссийская общественная организация «Ассоциация врачей общей практики (семейных врачей) Российской Федерации»)
Общие принципы диагностики и оценки боли у взрослых в амбулаторных условиях
При первичном осмотре пациента с жалобами на острую боль, в первую очередь необходимо исключить состояния, требующие экстренной госпитализации. Независимо от того, острая она или хроническая, необходимо провести ее оценку, что необходимо для разработки плана лечения.
Обследование пациента, предъявляющего жалобы на боль, должно включать выяснение обстоятельств, сопровождающих появление боли, что в дальнейшем может помочь как в уточнении диагноза, так и в выборе болеутоляющей терапии. Вот несколько вопросов, ответы на которые следует получить при осмотре пациента. Для простоты запоминания они обозначены только одним словом, первая буква которого выделена жирным шрифтом (ПОХИВ).
- Провокация (факторы, способствующие появлению боли и ее уменьшению)
- Область, являющаяся источником боли («карта боли»).
- Характер боли
- Интенсивность (в баллах)
- Время (когда боль началась, продолжительность и частота приступов)
Визуально-аналоговые шкалы (ВАШ)
Позволяют оценить интенсивность боли. Пациенту предлагают отметить на горизонтальной линии, соединяющей слова «нет боли» и «нестерпимая боль» тот участок, который, по его мнению, характеризует выраженность его болевых ощущений. Визуально-аналоговая шкала может быть представлена на линейке, имеющей 100 или 10 делений. Шкала оценки интенсивности боли может быть представлена не цифрами, а словами: нет боли, небольшая боль, терпимая, нестерпимая.Вербальная оценка боли позволяет выяснить характер болезненных ошущений.
Входит в состав краткой версии опросника канадского университета McGill (R. Melzack). Пациенту предлагается отметить то слово, которое в наибольшей степени соответствует его ощущениям.
- Пульсирующая
- Стреляющая
- Колющая
- Пронизывающая
- Ощущение тяжести
- Раскалывающая
- Тошнотворная
- Мучительная
- Спастическая
- Гложущая
- Обжигающая
- Распространенная
- Напряжение
- Изнуряющая
- Ужасная
Наряду с вербальной характеристикой боли предлагается оценивать степень ее интенсивности: слабая, умеренная, сильная.
Для более цельного представления о болевом синдроме используют его комплексную оценку. В этом случае комбинируют балльную, вербальную и поведенческую оценку проявлений болевого синдрома.
Оценка изменения поведения под влиянием боли проводится с помощью опросника, приведенного ниже (против соответствующего утверждения делается отметка).
- Шкала оценки изменения поведения под влиянием боли
- Боли нет ___
- Боль есть, но ее можно игнорировать ___
- Боль нельзя игнорировать, но она не нарушает жизнедеятельность ___
- Боль нельзя игнорировать и она мешает сосредоточиться____
- Боль нельзя игнорировать и она нарушает ритм жизни, за исключением посещения туалета и приема пищи___
- Боль нельзя игнорировать, требуется постельный режим____.
Оценка выраженности и характера болевого синдрома необходима для правильного выбора лечения. Кроме того, балльная оценка боли будет способствовать преемственности в лечении пациента с хроническим болевым синдромом разными специалистами, что может предотвратить неэффективность использования анальгетических средств.
Кроме оценки выраженности боли необходимо уточнить:
- не нарушает ли боль выполнение обычных функций (умывание, приготовление пищи);
- отношение самого пациента к изменению его состояния, его собственные мысли по поводу природы боли.
Полученная информация важна для разработки плана лечебных мероприятий, которые не должны сводиться только к медикаментозной терапии, но и включать обучение пациентов, физические упражнения, технические приспособления, которые снижают риск обострения болевого синдрома и повышают качество жизни.
Оценка боли при некоторых разновидностях болевого синдрома
Нейропатия
Нейропатическая боль развивается на фоне сахарного диабета, герпетической инфекции (постгерпетическая невралгия), невралгии тройничного нерва, радикулопатии, у больных с онкологическими заболеваниями как следствие химиотерапии или вовлечения нервов при распространении опухоли, а также при ВИЧ инфекции.
При подозрении на появление нейропатической боли необходимо уточнить диагноз заболевания, которое явилось причиной ее возникновения.
Подход трех «С» может помочь получить больше информации от пациента:
- Первое «С» — внимательно слушать рассказ пациента с описанием характерных признаков нейропатической боли
- Второе «С» — смотреть и оценивать локальные нарушения чувствительности
- Третье «С» — соотносить характер предъявляемых жалоб с результатами объективного осмотра
Пациенты могут описывать свои болевые ощущения различными словами: неприятные, колющие, кинжальные, жгучие, ошпаривающие, ноющие, как от удара током. Неврологический осмотр, включающий определение чувствительности, поможет выявить ее изменения, в частности аллодинию (появление боли при легком прикосновении, например, кисточкой). Для выявления нейропатии используют специальный опросник.
Симптом | Вариант ответа |
Ощущение жжения | Да/Нет |
Болезненное ощущение холода | Да/Нет |
Ощущение как от ударов током | Да/Нет |
Сопровождается ли боль одним или несколькими из симптомов в области ее локализации? | |
Пощипывание | Да/Нет |
Ощущение ползания мурашек | Да/Нет |
Покалывание | Да/Нет |
Зуд | Да/Нет |
Локализована ли боль в той же области, в которой при осмотре был выявлен один или оба следующих симптома? | |
Пониженная чувствительность к прикосновению | Да/Нет |
Пониженная чувствительность к покалыванию | Да/Нет |
Можно ли вызвать или усилить боль в области ее локализации проведением кисточкой? | Да/Нет |
Если количество ответов «Да» составляет 4 и более, боль, на которую жалуется пациент, является нейропатической или имеет нейропатический компонент.
- Диабетическая нейропатия-в стречается у 50% больных диабетом, предъявляющих жалобы на постоянную боль.
- Тригеминальная нейропатия-одной из причин развития этого вида нейропатии является деформация комплекса тройничного нерва и передней церебральной артерии, поэтому для уточнения диагноза таким больным показана МРТ. Тригеминальная нейропатия может быть симптомом таких серьезных заболеваний как опухоль задней черепной ямки и рассеянный склероз.
- Постгерпетическая невралгия-развивается спустя несколько месяцев после герпетических высыпаний. Однажды возникнув, постгерпетическая невралгия может рецидивировать в течение многих лет.
Нарушения функции мышечного аппарата
Выделяют два вида синдромов, связанных с болью в мышцах — фибромиалгию и мышечно-фасциальный синдром.
Этиология фибромиалгии окончательно не установлена. Факторами риска ее развития могут быть вирусные инфекции, перенесенные травмы, гипотиреоз, психическое напряжение.
Для фибромиалгии характерны диффузная боль в четырех квадрантах тела (выше и ниже пояса), гипералгезия, болезненность в определенных точках при надавливании и обширная их распространенность. Чаще всего болевые ощущения исходят из следующих анатомических зон:
- затылок в месте прикрепления субокципитальной мышцы;
- шейный отдел на уровне позвонков СV–CVII;
- середина верхней границы трапециевидной мышцы;
- над лопаткой около медиальной границы m. supraspinatus;
- у второго костно-хрящевого реберного сочленения;
- на 2 см дистальнее латерального надмыщелка локтя;
- верхний наружный квадрант ягодиц;
- билатерально кзади от большого вертела;
- область медиального надмыщелка бедра.
Кроме болевого синдрома пациенты жалуются на слабость, головную боль, плохой сон, скованность по утрам.
Для выявления фибромиалгии используется опросник FiRST.
Опросник FiRST для скрининга фибромиалгии
У меня боль по всему телу | Да/Нет |
Боль сочетается с постоянным чувством изнеможения | Да/Нет |
Боль похожа на жжение, удары током или судороги | Да/Нет |
Боль сопровождается другими необычными ощущениями по всему телу типа мурашек, покалывания или онемения | Да/Нет |
Боль сочетается с другими нарушениями (проблемы с пищеварением, мочеиспусканием, головные боли, непреодолимое желание двигать ногами при отходе ко сну) | Да/Нет |
Боль сильно влияет на мою жизнь, особенно на сон, и способность сконцентрироваться, я какой-то заторможенный | Да/Нет |
Пациенты, ответившие «Да» на 5 и более вопросов, должны быть направлены к специалисту (ревматологу/ неврологу) для проведения комплексного обследования и подтверждения диагноза.
Миофасциальный синдром имеет признаки, сходные с фибромиалгией. Обычно источником боли являются зоны шеи, плечевого пояса, груди и живота. В этой области образуются триггерные точки, представленные уплотнением в виде тяжа в области скелетной мышцы или ее фасции.
Механическая/компрессионная боль. Одной из причин может являться повышенная физическая активность. В этом случае боль исчезает самопроизвольно на фоне покоя. Особого внимания требуют пациенты с жалобами на боль в области спины, шейного отдела позвоночника, поскольку ХБС может быть обусловлен дегенеративными изменениями дисков; остеопорозом, сопровождающимся компрессионным переломом; метастазами опухоли (подробнее см. клинические рекомендации «Хроническая боль в спине»).
Боль при воспалении (ноцицептивная боль)
Этот тип боли наиболее характерен для заболеваний суставов, так как воспаление является причиной суставного синдрома различной этиологии, в том числе ревматической и инфекционной, обусловливает появление боли при травме и в послеоперационном периоде. Для воспаления характерны типичные признаки в виде местного повышения температуры и отека тканей.
Боль, вызванная онкологическими заболеваниями
Учитывая продолжительность болевого синдрома, сопровождающего онкологическое заболевание практически до летального исхода, ему присущи все характеристики ХБС, но на этом фоне может появиться и острая боль, связанная, например, с переломом костей при метастазировании.
Различают три типа болевого синдрома:
- в 75% боль связана с прорастанием опухоли;
- в 20% боль развивается в результате лечения заболевания (влияние лучевой терапии, химиотерапии);
- 5% — боль обусловлена другими заболеваниями.
Боль при онкологических заболеваниях может иметь черты ноцицептивной и нейропатической. Появление нейропатической боли свидетельствует о вовлеченности в патологический процесс периферической или центральной нервной системы. При развитии ХБС у пациентов нарастает ощущение безнадежности, что в еще большей степени способствует нарастанию интенсивности болевого синдрома.
Показания к консультации специалиста
Показания к консультации специалиста определяются основным заболеванием. При хронической боли разной этиологии при планировании программ немедикаментозной коррекции (физические упражнения, использование акупунктуры, физиотерапевтических процедур, проведение сеансов психотерапии), показаны консультации специалистов по лечебной физкультуре, физиотерапии, психотерапии, если региональные ресурсы здравоохранения позволяют их обеспечить в рамках реализации территориальных программ государственных гарантий на бесплатную для населения медицинскую помощь. При оказании помощи онкологическим больным врач общей практики работает в тесном контакте с онкологом, а также со специалистами в области паллиативной медицины.
Источник
