Метаболический синдром и ишемическая болезнь сердца
Дата публикации 26 марта 2018Обновлено 19 июля 2019
Определение болезни. Причины заболевания
Метаболический синдром (синдром Reaven) представляет собой симптомокомплекс, сочетающий в себе абдоминальное ожирение, инсулинорезистентность, гипергликемию (повышенное содержание глюкозы в крови), дислипидемию и артериальную гипертензию. Все эти нарушения связаны в одну патогенетическую цепь. Кроме того, такой синдром часто сочетается с гиперурикемией (избытком мочевой кислоты в крови), нарушением гемостаза (свёртываемости крови), субклиническим воспалением, синдромом обструктивного апноэ-гипопноэ сна (остановкой дыхания во сне).[4]
Метаболический синдром – хроническое, распространённое (до 35% в российской популяции), полиэтиологическое заболевание (возникающее по многим причинам), в котором главная роль принадлежит поведенческим факторам (гиподинамия, нерациональное питание, стресс). Имеет значение также наследственная предрасположенность к артериальной гипертензии, атеросклероззависимым заболеваниям и сахарному диабету второго типа.[5]
Практикующим врачам важно выделять группу риска метаболического синдрома. К данной группе относятся пациенты с начальными признаками заболевания и его осложнениями: артериальная гипертензия, углеводные изменения, ожирение и повышенное питание, ишемическая болезнь сердца, атеросклеротические заболевания периферических и мозговых артерий, нарушение пуринового обмена, жировая болезнь печени; синдром поликистозных яичников; постменопаузальный период у женщин и эректильная дисфункция у мужчин; гиподинамия, злоупотребление алкоголем, табакокурение, наследственная отягощенность по сердечно-сосудистым и обменным заболеваниям.[3][7]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы метаболического синдрома
Клинические проявления метаболического синдрома соответствуют симптомам его составляющих:
- абдоминального ожирения;
- артериальной гипертензии;
- изменениям углеводного, липидного и пуринового обмена.
Если изменения составляющих синдрома Reaven носят субклинический характер (что встречается довольно часто), то и течение заболевания носит асимптомный характер.
Патогенез метаболического синдрома
Инсулинорезистентность — первопричина развития метаболического синдрома. Представляет собой нарушение утилизации глюкозы в органах-мишенях (поперечнополосатой мускулатуре, липоцитах и печени), связанное с дисфункцией инсулина. Инсулинорезистентность уменьшает усвоение и поступление в клетки скелетной мускулатуры глюкозы; стимулирует липолиз и гликогенолиз, что приводит к липидным и углеводным патологическим изменениям. Кроме того, инсулинорезистентность усиливает секрецию инсулина, в результате чего возникает компенсаторная гиперинсулинемия и активация эндокринных систем (симпатоадреналовой, ренин-ангиотензин-альдостероновой) с формированием артериальной гипертензии, дальнейшим нарушением метаболических процессов, гиперкоагуляции, субклинического воспаления, дисфункции эндотелия и атерогенеза. Эти изменения, в свою очередь, способствуют усилению инсулинорезистентности, стимулируя патогенетический «порочный круг».
Классификация и стадии развития метаболического синдрома
Чёткой классификации и стадийности метаболического синдрома не существует. Его деление некоторыми авторами на полный, включающий все составляющие синдрома, и неполный представляется необоснованным. Несмотря на это, выраженность симптомов, количество компонентов синдрома Reaven и наличие осложнений оказывают влияние на стратификацию риска и выбор тактики лечения у конкретного пациента. Для этого следует учитывать:
- степень ожирения и артериальной гипертензии;
- выраженность метаболических изменений;
- наличие или отсутствие сахарного диабета и заболеваний, связанных с атеросклерозом.
В зависимости от индекса массы тела (ИМТ), который рассчитывается делением веса (кг) на рост (м2), классифицируются следующие типы массы тела (МТ):
- нормальная МТ — ИМТ ≥18,5 <25;
- избыточная МТ — ≥25 <30;
- ожирение I степени — ≥30 <35;
- ожирение II степени — ≥35 <40;
- ожирение III степени — ≥40.
ИМТ <18,5 характеризуется как дефицит массы тела.
Важную роль играет распределение жировой ткани. Различают два типа ожирения:
- гиноидный (по типу «груша»), когда избыточная жировая ткань распределяется преимущественно на бёдрах и ягодицах;
- андроидный (по типу «яблоко»; абдоминальное ожирение), с преимущественной локализацией жира в области верхней половины тела (живот, грудь, плечи, спина).

Второй тип ожирения является более патогенным в плане риска возникновения сердечно-сосудистых заболеваний и сахарного диабета. Это связано с ожирением внутренних органов, в том числе печени (висцеральное ожирение, неалкогольная жировая болезнь печени), снижением сатурации крови кислородом из-за перехода дыхания на грудной, поверхностный тип и эндокринной активностью висцеральной жировой ткани с патологическим изменением выработки адипокинов (лептин, грелин, адипонектин). Выявлена чёткая корреляция между увеличением абдоминальной жировой ткани и индекса массы тела с риском сопутствующих заболеваний. Считается, что риски начинают нарастать при увеличении окружности талии (ОТ) >80 см у женщин и 94 см у мужчин, а при ОТ >88 см и 102 см соответственно риск возрастает значительно.
Центральным патологическим звеном метаболического синдрома является изменение углеводного обмена. Концентрацию глюкозы оценивают в капиллярной крови (норма <5,6) и в венозной плазме (норма <6,1) натощак в ммоль/л. Гипергликемией натощак считается показатель ≥5,6 <6,1 и ≥6,1; <7,0; сахарный диабет — ≥6,1 и ≥6,1 <7,0, соответственно. Через 2 часа после углеводной нагрузки (75 гр глюкозы или 125 гр сахара рафинада, растворённых в 200 мл воды) нормальный показатель концентрации глюкозы в капиллярной и венозной крови — <7,8 ммоль/л; НТГ — ≥7,8 <11,1 и сахарный диабет — ≥11,1.
Ещё один важный компонент метаболического синдрома — артериальная гипертензия, которая может носить вторичный характер. Нормальным считается систолическое артериальное давление (САД) 120-129 мм рт.ст и диастолическое артериальное давление (ДАД) 80-84 мм рт.ст. САД <120 и ДАД <80 называют оптимальным давлением, а САД 130-139 и ДАД 85-89 — высоким нормальным артериальным давлением. Различают три степени артериальной гипертензии:
- 1 ст. – САД 140-159, ДАД 90-99;
- 2 ст. – САД 160-179, ДАД 100-109;
- 3 ст. – САД ≥180, ДАД ≥110.
Повышение артериального давления характеризуется повышением риска сердечно-сосудистых событий.
Для метаболического синдрома характерны также изменения липидного обмена, которые классифицированы в таблице ниже (в ммоль/л).
| Параметры липидов | Риск низкий | Риск умеренный | Риск высокий | Риск очень высокий |
|---|---|---|---|---|
| ОХ | ≤5,5 | ≤5 | ≤4,5 | ≤4 |
| ХС-ЛПНП | ≤3,5 | ≤3 | ≤2,5 | ≤1,8 |
| ХС-ЛПВП | муж. >1 жен. >1,2 | муж. >1 жен. >1,2 | муж. >1 жен. >1,2 | муж. >1 жен. >1,2 |
| Триглицериды | ≤1,7 | ≤1,7 | ≤1,7 | ≤1,7 |
| ХС не-ЛПВП | ≤4,3 | ≤3,8 | ≤3,3 | ≤2,6 |
| Примечание: ОХ — общий холестерин; ХС-ЛПНП — холестерин липопротеинов низкой плотности; ХС-ЛПВП — холестерин липопротеинов высокой плотности; ХС не-ЛПВП — холестерин, не связанный с липопротеинами высокой плотности. | ||||
Осложнения метаболического синдрома
Так как метаболический синдром является сочетанием факторов риска сердечно-сосудистых и обменных заболеваний, именно эти патологии и являются его осложнениями. Речь идёт, в первую очередь, о сахарном диабете, ишемической болезни сердца и их осложнениях: диабетическая ангио-, нейро- и нефропатия, острая коронарная недостаточность, сердечная недостаточность, нарушение сердечного ритма и проводимости, внезапная сердечная смерть, цереброваскулярные заболевания и болезни периферических артерий.[17] Прогрессирование артериальной гипертензии также приводит к поражению органов-мишеней и ассоциированным клиническим состояниям.
Диагностика метаболического синдрома
Для диагностики метаболического синдрома необходимо выявить у пациента основной признак — абдоминальное ожирение по измерению ОТ (>80 см у женщин и >94 см у мужчин) и хотя бы два дополнительных критерия, которые включают в себя:
- артериальную гипертензию (артериальное давление ≥140/90 мм рт.ст.);
- липидные показатели (ммоль/л) — повышение концентрации в крови триглицеридов ≥1,7; снижение ХС ЛПВП <1,0 у мужчин; <1,2 у женщин и повышение ХС ЛПНП >3,0;
- углеводные показатели (ммоль/л) — гипергликемия натощак ≥6,1 и НТГ 7,8 – <11,1.[8]
В клинических условиях нужно дифференцировать метаболический синдром от механического сочетания факторов риска, например артериальной гипертензии, избыточной массы тела без признаков абдоминального ожирения и повышения уровня ОХ крови, что встречается довольно часто (до 30%). В сомнительных случаях рекомендовано дополнительное определение инсулинорезистентности по следующим методикам:
- оценка базальной гиперинсулинемии в крови натощак (гиперинсулинемия — >18 мкед/мл);
- показатель HOMA-IR — произведение значения инсулина натощак (мкед/мл) на величину глюкозы (ммоль/л), разделить на 22,5 (значение большее, чем 2,27, считается инсулинорезистентностью);
- индекс Caro — соотношение тощаковой глюкозы (в ммоль/л) к инсулину (в мкед/мл) (инсулинорезистентность – значение < 0,33).[12]
Лечение метаболического синдрома
Лечение метаболического синдрома следует разделить на немедикаментозное и медикаментозное.
Немедикаментозное лечение синдрома Reaven — это ведение здорового образа жизни, отказ от курения и злоупотребления алкоголем, оптимальная двигательная активность[14], рациональное питание, а также разумное использование природных и преформированных физических лечебных факторов (массаж, подводный душ-массаж, гипокситерапия и гиперкапния, водолечение, талассотерапия, бальнео- и термотерапия, внутренний прём минеральных вод, общие магнитотерапевтические воздействия)[15], психотерапевтических методик и обучающих программ.[13]
Медикаментозное лечение метаболического синдрома, в зависимости от наличия тех или иных его компонентов, может включать гиполипидемические, антигипертензивные препараты, медикаменты для снижения инсулинорезистентности, постпрандиальной гипергликемии и веса.
Основными препаратами, которые используют при лечении артериальной гипертензии у больных синдромом Reaven и сахарным диабетом, являются ингибиторы ангиотензинпревращающего фермента, сартаны и агонисты имидазолиновых рецепторов. Однако для достижения целевого уровня артериального давления часто необходимо сочетание различных классов медикаментов, таких как пролонгированных блокаторов медленных кальциевых каналов, высокоселективных бета-адреноблокаторов и тиазидоподобных диуретиков (индапамид) в сочетании с медикаментами первой линии.[10]
Для коррекции нарушений липидного обмена при метаболическом синдроме первоначально используются статины, возможно их сочетание с эзетролом и фибратами. Основной механизм действия статинов — снижение внутриклеточного синтеза ОХ за счёт обратимого блокирования фермента 3-гидрокси-3-метилглютарил-кофермент А редуктазы. Оно ведёт к увеличению количества рецепторов к ХС-ЛПНП на поверхности гепатоцита и снижению концентрации ХС-ЛПНП в крови. Помимо этого, статины имеют плейотропные эффекты, такие как антитромбогенный, противовоспалительный, улучшение функции эндотелия, что приводит к стабилизации атеросклеротической бляшки. Современные статины способны вместе со снижением ХС-ЛПНП до 55% уменьшать триглицериды до 30% и повышать ХС-ЛПВП до 12%. В то же время, ключевое достоинство статинотерапии — снижение сердечно-сосудистых осложнений и общей смертности[1]. Эффективней всего использовать аторвастатин (10-80 мг/сут) или розувастатин (5-40 мг/сут).[11]
При неэффективности монотерапии статинами целесообразно присоединение эзетрола в дозе 10 мг/сут, который препятствует всасыванию ОХ в кишечнике и может усиливать снижение ХС-ЛПНП на 15-20%.
Фибраты — ещё один класс липидснижающих препаратов. Они расщепляют богатые триглицеридами жировые частицы, снижают синтез свободных жирных кислот и повышают ХС-ЛПВП путём увеличения распада ЛНП. Это приводит к значительному уменьшению триглицеридов (до 50%), ХС-ЛПНП (до 20%) и увеличению ХС-ЛПВП (до 30%). Фибраты также имеют плейотропные эффекты: снижают концентрацию мочевой кислоты, фибриногена и улучшают инсулиночувствительность, однако их положительное влияние на прогноз пациентов не доказано. Наиболее эффективный и безопасный препарат этой группы — фенофибрат 145 мг/сут.
Для снижения инсулинорезистентности препаратом выбора является метформин, который обладает доказанным положительным эффектом на тканевую инсулинорезистентность через усиление поглощения глюкозы тканями-мишенями. Метформин уменьшает скорость всасывания углеводов в тонкой кишке, оказывает периферическое анорексигенное действие, уменьшает продукцию глюкозы печенью, улучшает транспорт глюкозы внутри клеток. Положительное воздействие метформина (1500-3000 мг/сутки) на конечные точки обусловлено снижением инсулинорезистентности, системными метаболическими эффектами (снижение веса, липидных нарушений, факторов свёртываемости крови и т.д.).[9]
Для снижения постпрандиальной гипергликемии используют акарбозу, которая обратимо блокирует глюкоамилазы, сахарозы и мальтазы в верхнем отделе тонкой кишки. В итоге непереваренные углеводы достигают нижние отделы кишечника, и абсорбция углеводов пролонгируется. Вместе с тем, у акарбозы выявлены дополнительные эффекты. В исследовании STOP-NIDDM (2002 год) у больных метаболическим синдромом, принимающих акарбозу дозировкой 300 мг/сут, продемонстрировано снижение развития сахарного диабета на 36%, новых случаев артериальной гипертензии на 34% и суммарного показателя сердечно-сосудистых событий на 46%[6].
При наличии у пациента с синдромом Reaven сахарного диабета второго типа могут применяться современные классы сахароснижающих препаратов, такие как аналог глюкагоноподобного пептида-1, ингибитор дипептидилпептидазы-4 и ингибитор натрийзависимого переносчика глюкозы второго типа. Представитель последнего класса эмпаглифлозин (Джардинс) в исследовании EMPA-REG OUTCOME (2016 год) снизил сердечно-сосудистую смертность у больных сахарным диабетом второго типа на 36%.
Медикаментозная коррекция морбидного ожирения показана, если немедикаментозное лечение не приводит к снижению массы тела более чем на 5% от исходного. Препараты для лечения ожирения делятся на аноретики центрального действия (сибутрамин), и средства, воздействующие на желудочно-кишечный тракт, например орлистат (Ксеникал).
Препарат для снижения аппетита сибутрамин в меньшей степени воздействует на дофаминовые и холинергические процессы, но уменьшает потребление жиров и углеводов, что приводит к похудению и улучшает жировой и углеводный метаболизм. Артериальное давление и частота сердечных сокращений при этом повышается только на 5%.
Орлистат является ингибитором желудочной и панкреатической липаз, вследствие чего треть пищевых триглицеридов не всасывается и снижается их концентрация в крови, что приводит к уменьшению калоража пищи и веса. Кроме того, снижается артериальное давление, уровень глюкозы и инсулинорезистентности.
В медицинской практике лечение метаболического синдрома зависит от наличия и выраженности его компонентов. В таблице ниже показана тактика подбора терапии при вариантах синдрома Reaven, которые встречаются наиболее часто.
| АО+АГ+НТГ (СД) Умеренный ССР | АО+АГ+ДЛ Высокий ССР | АО+АГ+НТГ (СД)+ДЛ Высокий и очень высокий ССР | ||
|---|---|---|---|---|
| Д/ФН+АГП+ГГП | Д/ФН+АГП+ГЛП | Д/ФН+АГП+ГГП+ГЛП | ||
| Примечание ССР – сердечно-сосудистый риск; АГ – артериальная гипертензия; АО – абдоминальное ожирение; ДЛ – дислипидемия; НТГ – нарушение толерантности к глюкозе; СД – сахарный диабет; Д/ФН – диета/физическая нагрузка; АГП – антигипертензивный препарат; ГГП – гипогликемический препарат; ГЛП – гиполипидемический препарат. | ||||
Источник
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Поликарпов Л.С.
1
Яскевич Р.А.
1, 2
Хамнагадаев И.И.
3
Деревянных Е.В.
2
Харьков Е.И.
2
Балашова Н.А.
2
1 ФГБНУ «Научно-исследовательский институт медицинских проблем Севера»
2 ГБОУ ВПО «КрасГМУ им. проф. Ф.В. Войно-Ясенецкого» МЗ РФ
3 ФГАОУ ВПО «Белгородский государственный национальный исследовательский университет»
С целью изучения особенностей влияния компонентов метаболического синдрома на клиническое течение ишемической болезни сердца у мужчин с учетом компонентов массы тела и соматотипа обследовано 137 мужчин, жителей г. Красноярска (средний возраст 54,9±1,4 лет) с артериальной гипертонией и ишемической болезнью сердца. Обследование включало клинические, инструментальные, функциональные и лабораторные методы исследования, а также антропометрию с последующим соматотипированием. Установлено, что среди мужчин с ишемической болезнью сердца метаболический синдром встречался у 10,8% обследованных. Пациенты с ишемической болезнью сердца в сочетании с сопутствующей артериальной гипертонией имели более высокие уровни гликемии, инсулинемии и липидов, чем у пациентов с ишемической болезнью сердца без сопутствующей артериальной гипертонии. Показатели углеводного и липидного обменов у больных ишемической болезнью сердца с инфарктом миокарда в анамнезе выше в сравнении с больными ишемической болезнью сердца без перенесенного инфаркта миокарда. Среди обследованных мужчин наиболее чаще встречались соматотипы со значительным развитием жировой компоненты.
артериальная гипертония
ишемическая болезнь сердца
соматотип
метаболический синдром
1. Балева Е.С., Кром И.Л., Алешкина О.Ю. Объективизация отдалённого клинического прогноза больных ишемической болезнью сердца // Фундаментальные исследования. – 2013. – № 7 (часть 3). – С. 511-513.
2. Василькова Т. Н., Баклаева Т. Б., Матаев С. И. и др. Влияние различных типов жироотложения на состояние сердечно-сосудистой системы // Сердце: журнал для практикующих врачей. – 2014. – Т. 75, №1. – С. 45-49.
3. Козлов И.Д., Гракович А.А., Апанасевич В.В., Плащинская Л.И. Роль соматотипа в развитии и течении ишемической болезни сердца // Медицинские новости. – 2004. – №4. – С. 87-90.
4. Никитин Ю.П., Воевода М.И., Симонова Г.И. Сахарный диабет и метаболический синдром в Сибири и на Дальнем Востоке // Вестник РАМН. – 2012. – №1. – С.66-74.
5. Поликарпов Л.С., Яскевич Р.А., Хамнагадаев И.И. Сравнительная характеристика нарушений углеводного обмена у мужчин и женщин различных конституциональных типов с артериальной гипертонией // Сибирский медицинский журнал (г. Томск). – 2004. – Т. 19, № 4. – С. 60-63.
6. Пуликов А.С., Москаленко О.Л. Конституциональные особенности кардио-респираторной системы и адаптационные возможности юношей // В мире научных открытий. – 2012. – № 5.3(29). – С. 87-111.
7. Сибалак Ш. Некоторые эхографические характеристики левого желудочка сердца у людей различных соматотипов // Морфология. – 2003. – №3. – С.53 – 56.
8. Таптыгина Е.В., Яскевич Р.А., Поликарпов Л.С., Хамнагадаев И.И. Особенности углеводного обмена в зависимости от соматотипа у мужчин, больных ишемической болезнью сердца // Сибирский медицинский журнал (г. Томск). – 2007. – Т. 22, № 4. – С. 65-67.
9. Харьков Е.И., Петрова М.М., Марьянчик Е.Н., Каскаева Д.С. Состояние сердечно-сосудистой системы у призывников и молодых военнослужащих г. Красноярска, страдающих артериальной гипертонией в зависимости от соматотипа // Красноярск, Кларетианум. – 2005. – 81 с.
10. Яскевич Р.А., Поликарпов Л.С., Хамнагадаев И.И. Гиперинсулинемия и нарушения толерантности к глюкозе у женщин различных соматотипов с артериальной гипертонией // Сибирский медицинский журнал (г. Томск). – 2004. – Т.19, № 4. – С. 56-59.
В последние десятилетия одной из важнейших медико-социальных и экономических проблем современного общества являются различные гормонально–метаболические нарушения и/или заболевания, поскольку практически каждое из них, является фактором риска развития сердечно-сосудистых заболеваний (ССЗ), а их сочетание многократно увеличивает риск развития макрососудистых атеросклеротических заболеваний [4].
К таким факторам риска атеросклероза относятся нарушения в системе липопротеидов, проявляющиеся в виде гипертриглицеридемии и гипоальфахолестеринемии, нарушения в обмене углеводов, проявляющиеся в виде инсулинорезистентности, гиперинсулинемии, нарушение толерантности к глюкозе (НТГ) при пероральной нагрузке и в виде сформировавшегося инсулиннезависимого сахарного диабета (ИНСД) [4]. Отклонения этих биохимических параметров чаще, чем в норме, определялись у пациентов с артериальной гипертонией (АГ) и абдоминальным типом ожирения (АО) [2], а также показана взаимосвязь между инсулинорезистентностью и компенсаторной гиперинсулинемией у лиц с ишемической болезнью сердца (ИБС) при метаболическом синдроме (МС) [4].
В многочисленных исследованиях, проводимых с целью изучения зависимости между определенными конституциональными группами и заболеваниями, особое внимание уделяется роли конституции человека в кардиологии [1, 3, 6, 7, 9, 10]. Некоторые авторы считают, что для каждого конституционального типа характерна своя реакция сердечно-сосудистой системы [6]. Установлено, что систолическое и диастолическое артериальное давление и тонус сосудов были несколько выше у представителей брюшного соматотипа по сравнению с грудным [5, 9]. В работах других исследователей подтверждается большая вероятность развития АГ у лиц гиперстенического (брахиоморфного) телосложения [7]. Лица гиперстенической конституции наиболее подвержены возникновению коронарного атеросклероза [1, 3, 7], внезапной смерти и ИМ по сравнению с другими соматотипами. Гиперстения вносит независимый от других факторов риска (АГ, курения, гиперхолетеринемии) достоверно значимый вклад в возникновение ИБС. Показано, что лица гиперстенической конституции предрасположены к развитию ишемической болезни сердца и прежде всего острого несмертельного инфаркта миокарда. Среди больных гиперстенической конституции синдром стенокардии после перенесенного ИМ имеет место в 61,3% случаев [3].Это подтверждается наблюдениями клиницистов о преобладании среди пациентов с ИБС лиц гиперстенического типа и требует дальнейших исследований в данном направлении, в первую очередь изучения взаимодействия индивидуальной предрасположенности, обусловленной гиперстеническим соматотипом, и традиционных факторов риска ИБС [3].
Цель исследования: изучить особенности влияния компонентов метаболического синдрома на клиническое течение ишемической болезни сердца у мужчин с учетом компонентов массы тела и соматотипа.
Материалы и методы. Объектом исследования были мужчины, жители Центральной Сибири (г. Красноярск). Всего обследовано 137 человек (средний возраст 54,9±1,4 лет). Обследованные больные были разделены на три группы: 1группа – пациенты с АГ без ИБС (47 человек, средний возраст 55,6 ± 0,98 лет), 2 группа – пациенты с ИБС без АГ (31 человек, средний возраст 56,2 ± 1,96 лет) и 3 группа – пациенты с ИБС в сочетании с АГ (59 человек, средний возраст 58,22 ± 1,27 лет).
Клиническое обследование больных включало врачебный осмотр, анкетирование, двукратное измерение артериального давления, эхокардиографию, велоэргометрию, электрокардиографию.
Лабораторное обследование включало определение уровней общего холестерина (ОХС), холестерина липопротеидов высокой плотности (ЛПВП), триглицеридов (ТГ), проведение стандартного теста толерантности к глюкозе (СТТГ) и определение иммунореактивного инсулина (ИРИ) в сыворотки крови.
Соматотипирование проводилось по методу Бунака В.В. (1931) в модификации Чте-цова В.П. с соавт. (1978), основывалось на 5-бальной оценке трех компонентов состава тела человека: жирового, мышечного и костного. При определении соматотипа мужчин использовали терминологию, предложенную Бунаком В.В. (1931): грудной, грудно-мускульный, мускульно-грудной, мускульный, мускульно-брюшной, брюшно-мускульный, брюшной, грудно-брюшной, брюшно-грудной типы и т.п. Соматотипы определялись согласно схеме возможного сочетания баллов.
Диагноз МС устанавливали в соответствии с критериями ВНОК, 2009 г., согласно которым метаболический синдром устанавливался как сочетание основного критерия — абдоминального ожирения (окружность талии >94 см у мужчин и >80 см у женщин), — и 2 или более дополнительных критериев. К дополнительным критериям относили повышение уровня глюкозы натощак >6,1 ммоль/л; уровень АД более 140/90 мм рт.ст.; снижение ЛПВП<1,0 ммоль/л для мужчин и <1,2 ммоль/л для женщин; повышение триглицеридов >1,7 ммоль/л; повышение холестерина липопротеинов низкой плотности (ЛПНП) >3,0 ммоль/л.
Статистическая обработка данных производилась с помощью пакета прикладных программ Statistika 6.0. Использовались стандартные методы описательной статистики (вычисление средних, стандартных отклонений, стандартных ошибок и т.д.) и непараметрические критерии значимости (F-критерий Фишера, критерий Манна-Уитни).
Результаты и обсуждение. По данным проведенного исследования, частота встречаемости метаболического синдрома составила 12,1% от общего числа обследованных мужчин. При этом среди мужчин, страдающих ИБС, частота метаболического синдрома составила 10,8% и среди пациентов с АГ – 14%.
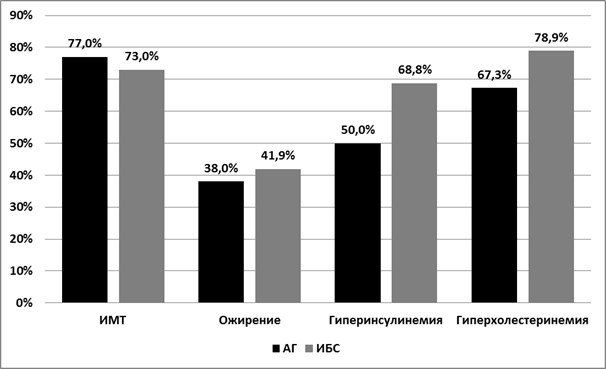
Анализ частоты встречаемости отдельных компонентов метаболического синдрома среди обследованных мужчин с АГ и ИБС (рис. 1.) показал, что на первом месте по частоте находилась избыточная масса тела (77% при АГ и 73% при ИБС соответственно). При этом среди больных ИБС чаще (41,9%) встречались лица с индексом массы тела (ИМТ) ≥25-29,9 кг/м2, чем при АГ (38%). Гиперинсулинемия также чаще выявлялась среди больных с ИБС, в сравнении с больными с АГ, и составила (68,8% при ИБС и 50% при АГ). Нарушенная толерантность к углеводам выявлена у 16,7% лиц с ИБС и у 12% – с АГ, гиперхолестеринемия (78,9% при ИБС и 67,3% при АГ).
Обследованные мужчины с АГ и ИБС были разделены на 2 группы в зависимости от наличия или отсутствия перенесенного ОИМ в анамнезе. Установлено, что ОИМ в анамнезе, встречался практически с одинаковой частотой, как в группе мужчин с ИБС без АГ (54,8%), так и у мужчин с ИБС в сочетании с АГ (57,9%,) соответственно.

Рис. 1. Частота встречаемости отдельных компонентов МС среди мужчин жителей г. Красноярска с сердечно-сосудистыми заболеваниями
Был проведен анализ влияния АГ на исследуемые показатели углеводного и липидного обменов у пациентов ИБС с ИМ и без него. Установлено, что наиболее низкие показатели гликемии при проведении СТТГ выявлены среди больных ИБС без АГ (табл. 1). Пациенты исследуемых групп не различались по уровням гликемии натощак и гликемии через 2 часа после нагрузки глюкозой. В то же время пациенты с ИБС и ИМ в анамнезе имели тенденции к более высоким значениям гликемии через 2 часа после нагрузки глюкозой в сравнении с лицами 1 и 2 групп.
Таблица 1
Показатели углеводного и липидного обмена у мужчин больных ишемической болезнью сердца и артериальной гипертонией
Глюкоза натощак | Глюкоза ч/з 2 часа | Инсулин натощак | Инсулин ч/з 2 часа | ЛПВП | ТГ | |
1. АГ | 4,3±0,14 | 4,3±0,24 | 11,4±1,33 | 22,52±4,29 | 1,2±0,17 | 1,55±0,14 |
2. ИБС без АГ | 4,1±0,15 | 5,2±0,25 | 14,83±2,4 | 32,51±4,85 | 1,18±0,29 | 1,85±0,21 |
3. ИБС с АГ | 4,3±0,15 | 5,5±0,28 | 18,58±2,1 | 47,45±5,6 | 1,1±0,2 | 2,24±0,23 |
р | – | р 1,2 < 0,05 | р 1,3 < 0,05 | р 1,3 < 0,05 | р 1,3 < 0,05 | р 1,3 < 0,05 |
Средние уровни ИРИ натощак (ИРИ0) и через 2 часа после нагрузки глюкозой (ИРИ2) у больных АГ были ниже в сравнении с пациентами с ИБС. Следует отметить, что у пациентов 2 и 3 группы средние уровни ИРИ0 и ИРИ2 превышали нормативные величины. Наиболее высокие уровни ИРИ0 и ИРИ2 отмечены в группе больных ИБС с АГ, а наиболее низкие – у больных ИБС без АГ.
По уровням липидов среди исследуемых групп имелись следующие особенности. В 2 и 3 группах уровни ТГ были выше, а уровни ЛПВП ниже в сравнении с 1 группой. Более благоприятные уровни липидов (низкие значения ТГ и высокие значения ЛПВП) отмечались в группе с ИБС без сопутствующей АГ, а менее благоприятные (высокие значения ТГ и низкие значения ЛПВП) – в группе с ИБС с АГ.
Таким образом, в ходе исследования выявлено, что показатели углеводного и липидного обменов у больных ИБС выше в сравнении с больными АГ, а уровни ИРИ натощак и через 2 часа после нагрузки глюкозой превышают нормативные значения. Пациенты с ИБС с сопутствующей АГ имели более высокие уровни гликемии, инсулинемии и липидов по сравнению с пациентами ИБС без сопутствующей АГ.
Проведенная антропометрия с соматотипированием показала, что в группе мужчин, страдающих АГ, в 64% случаев встречается брюшной соматотип; у больных ИБС чаще встречался мускульный соматотип (52%), у мужчин с ИБС и ИМ в анамнезе – брюшной 44% и мускульный 43%, при сочетанной патологии (ИБС и АГ) у 56% – мускульный соматотип.
Анализ полученных данных показал, что среди мужчин с МС наиболее чаще встречался мускульно-брюшной соматотип, реже – брюшно-мускульный и брюшной соматотипы, а также у 1 пациента с МС был выявлен неопределенный соматотип. При этом среди мужчин с МС без ИБС в 57% случаев преобладали лица брюшного соматотипа, а среди пациентов с ИБС и МС преимущественно встречались (75%) лица мускульно-брюшного соматотипа. Полученные результаты нашего исследования согласуются с полученными ранее данными других исследований, показавших, что наибольшей частотой максимального риска развития АГ и ИБС характеризуются соматотипы со значительным развитием жировой компоненты [9] или жировой и мускульной тканей одновременно: мезосомный (пикнический) тип [5, 10] или брюшно-мускульный и мускульно-брюшной варианты [7, 8] .
Было установлено, что у мужчин больных АГ наиболее высокие уровни ИРИ натощак определялись при брюшном и неопределенном соматотипах в сравнении грудным и мускульным соответственно. Наиболее высокие значения ИРИ через 1 час после нагрузки глюкозой отмечались при брюшном соматотипе. Мужчины брюшного соматотипа также имели более высокие показатели ИРИ через 2 часа после нагрузки глюкозой в сравнении с неопределенным, грудным и мускульным соматотипами.
Таким образом, проведенный анализ позволил выявить некоторые различия в показателях гиперинсулинемии у мужчин больных АГ различных соматотипов. Гиперинсулинемия чаще выявлялась при брюшном и неопределенном соматотипах, в 2 раза реже при мускульном соматотипе. У мужчин грудного соматотипа гиперинсулинемия отсутствовала.
Нарушенная толерантность к углеводам (НТУ) среди мужчин с ИБС различных соматотипов была выявлена: при брюшном соматотипе – у 3,57%, при мускульном соматотипе – у 7,32%, при неопределенном соматотипе – у 25% и при грудном соматотипе – у 50%. При этом НТУ чаще встречалась среди мужчин грудного соматотипа, в сравнении с мускульным (р<0,05) и брюшным (р<0,05) соматотипами. Гиперинсулинемия у больных ИБС брюшного, мускульного и неопределенного соматотипов выявлялась более чем у 50% обследованных, а при грудном соматотипе – отсутствовала.
Выводы:
1. Среди мужчин с артериальной гипертонией имеют метаболический синдром 14%, среди мужчин с ишемической болезнью сердца имеют метаболический синдром 10%.
2. Пациенты с ишемической болезнью сердца в сочетании с сопутствующей артериальной гипертонией имели более высокие уровни гликемии, инсулинемии и липидов, чем у пациентов с ИБС без сопутствующей артериальной гипертонии.
3. Показатели углеводного и липидного обменов у больных ишемической болезнью сердца с инфарктом миокарда в анамнезе выше в сравнении с больными ишемической болезнью сердца без перенесенного инфаркта миокарда.
4. Среди мужчин с метаболическим синдромом чаще встречаются соматотипы со значительным развитием жировой и мускульной компоненты.
Рецензенты:
Пуликов А.С., д.м.н., профессор, заведующий лабораторией функциональной морфологии, ФГБНУ «Научно-исследовательский институт медицинских проблем Севера», г. Красноярск.
Грицинская В.Л., д.м.н., главный научный сотрудник, ФГБНУ «Научно-исследовательский институт медицинских проблем Севера», г. Красноярск.
Библиографическая ссылка
Поликарпов Л.С., Яскевич Р.А., Яскевич Р.А., Хамнагадаев И.И., Деревянных Е.В., Харьков Е.И., Балашова Н.А. ВЛИЯНИЕ КОМПОНЕНТОВ МЕТАБОЛИЧЕСКОГО СИНДРОМА НА КЛИНИЧЕСКОЕ ТЕЧЕНИЕ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА У МУЖЧИН // Современные проблемы науки и образования. – 2014. – № 5.;
URL: https://science-education.ru/ru/article/view?id=14808 (дата обращения: 25.01.2021).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
