Миелодиспластический синдром какая группа инвалидности
МСЭ и инвалидность при хроническом миелолейкозе
| Медико-социальная экспертиза и инвалидность при хроническом миелолейкозеХронический миелолейкоз —- хроническое миелопролиферативное заболевание, возникающее из ранних предшественников миелопоэза, морфологическим субстратом которого являются преимущественно созревающие и зрелые гранулоциты, главным образом, нейтрофилы; число эритроидных предшественников и мегакариоцитов также может быть повышено.Эпидемиология. Хронический миелолейкоз занимает 5-е место среди гемобластозов, что составляет 20 %. Заболеваемость 1 -1,7 на 100000 населения. Мужчины болеют несколько чаще. Только 10% больных имеют возраст от 5 до 20 лет.Этиология и патогенез. Для хронического миелолейкоза характерно наличие Филадельфийской (Ph) хромосомы. Происходит перенос протоонкогена Ab1 (протоонкоген Абеля) 9-й хромосомы в локус Всг 22-й хромосомы. В результате транслокации и слияния генов образуется новый химерный ген Всг-Abl, который запускает синтез патологического белка Р210 Всг Аb1 приводящего к развитию миелопролиферативного синдрома. Заболевание характеризуется чрезмерной продукцией гранулоцитов в костном мозге. По мере прогрессирования болезни появляются очаги экстрамедуллярной пролиферации (селезенка, печень). Несмотря на преобладание гранулоцитов, патологический клон клеток включает эритроидный, мегакариоцитарный и моноцитарный ростки (миелопролиферативный синдром). Нормальные стволовые клетки вытесняются злокачественными. У части больных развивается миелофиброз.Клинические проявления. В дебюте хронического миелолейкоза какая-либо симптоматика часто отсутствует, и у многих заболевание диагностируется после случайного клинического анализа крови. Могут отмечаться неспецифические симптомы (утомляемость, слабость, потеря аппетита, повышение температуры тела, потливость по ночам), наиболее часто выявляется умеренная или выраженная спленомегалия.Критерии диагностики. 1. Лейкоцитоз за счет гранулоцитов, со сдвигом влево до промиелоцитов и миелобластов с наличием всех переходных форм. 2. Базофильно-эозинофильная ассоциация. 3. Снижение активности щелочной фосфатазы нейтрофилов. 4. Гепато- и спленомегалия. 5. Наличие Ph’ хромосомы или патологического Всг-Abl гена.Классификация. 1.Хроническая фаза: – отсутствие выраженной симптоматики, – отсутствие признаков фазы акселерации и бластного криза. 2.Фаза акселерации: 3.Бластный криз: Лечение часто носит паллиативный характер, лейкоцитоз целесообразно уменьшить ниже 25х10*9 /л. Обычно назначают гидроксимочевину или бусульфан. Терапия не позволяет достигнуть цитогенетической ремиссии, т.е. исчезновения Ph-позитивного клона клеток. Цитогенетическая ремиссия возможна при лечении а-интерфероном. Аллогенная трансплантация костного мозга позволяет добиться излечения.Течение и прогноз. Инвалидность не устанавливается в случае, если у больного имеется: Инвалидность 3-й группы устанавливается: Инвалидность 2-й группы устанавливается: Инвалидность 1-й группы устанавливается в случае, если у больного имеется: КРИТЕРИИ ИНВАЛИДНОСТИ ПРИ ХРОНИЧЕСКОМ МИЕЛОЛЕЙКОЗЕ У ДЕТЕЙ В 2020 ГОДУ Инвалидность не устанавливается в случае, если у ребенка имеется: Категория “ребенок-инвалид” устанавливается: Согласно пункту 16а) приложения к Постановлению Правительства РФ от 20.02.2006 N 95 (ред. от 14.11.2019) “О порядке и условиях признания лица инвалидом”: Получить официальное заключение о наличии (или отсутствии) оснований для установления инвалидности больной может только по результатам своего освидетельствования в бюро МСЭ соответствующего региона. Порядок оформления документов для прохождения МСЭ (включая и алгоритм действий при отказе лечащих врачей направлять больного на МСЭ) достаточно подробно расписан в этом разделе форума: Оформление инвалидности простым языком Источник | |
| Категория: Медико-социальная экспертиза при некоторых заболеваниях | Добавил: astra71 (02.01.2012) | |
| Просмотров: 29498 | Рейтинг: 5.0/3 |
Добавлять комментарии могут только зарегистрированные пользователи.
[
Регистрация
|
Вход
]
Источник
Онлайн всего: 5
Гостей: 5
Пользователей:
МСЭ и инвалидность при множественной миеломе
| Медико-социальная экспертиза и инвалидность при множественной миеломеМножественная миелома (миеломная болезнь) — злокачественное клональное В-лимфопролиферативное заболевание системы крови, морфологическим субстратом которого являются плазматические клетки костного мозга, продуцирующие моноклональный иммуноглобулин.Эпидемиология. Заболеваемость составляет 3 чел. на 100000 населения. Средний возраст больных 65 лет, менее 1% больных моложе 40 лет. Соотношение мужчин и женщин составляет 1,6 : 1.Этиология и патогенез. У большинства больных причина заболевания остается невыясненной. Факторами риска являются облучение высокими дозами, генетическая предрасположенность, хроническая антигенная стимуляция. При миеломной болезни нарушена продукция многих цитокинов, которые стимулируют рост миеломных клеток, способствуют их резистентности к лечению и становятся причиной остеолиза. В патогенез вовлечены такие механизмы, как неконтролируемый рост плазматических клеток, секреция моноклонального парапротеина (иммуноглобулины или легкие цепи) и подавление секреции нормальных иммуноглобулинов, замещение плацдарма нормального кроветворения опухолевыми клетками; стимуляция остеокластов и поражение костей, гиперкальциемия из-за остеолиза, поражение почек в результате отложения депозитов легких цепей в канальцах, гиперкальциемии, амилоидоза и инфильтрации почек миеломными клетками. Клиника. Трудоспособны больные с индолентной множественной миеломой, Критерии МСЭ: Инвалидность не устанавливается: Инвалидность 3-й группы устанавливается: Инвалидность 2-й группы устанавливается: Инвалидность 1-й группы устанавливается: КРИТЕРИИ ИНВАЛИДНОСТИ ПРИ МНОЖЕСТВЕННОЙ МИЕЛОМЕ У ДЕТЕЙ В 2020 ГОДУ Инвалидность не устанавливается в случае, если у ребенка имеется: Категория “ребенок-инвалид” устанавливается: Согласно пункту 16а) приложения к Постановлению Правительства РФ от 20.02.2006 N 95 (ред. от 14.11.2019) “О порядке и условиях признания лица инвалидом”: Получить официальное заключение о наличии (или отсутствии) оснований для установления инвалидности больной может только по результатам своего освидетельствования в бюро МСЭ соответствующего региона. Порядок оформления документов для прохождения МСЭ (включая и алгоритм действий при отказе лечащих врачей направлять больного на МСЭ) достаточно подробно расписан в этом разделе форума: Источник | |
| Категория: Медико-социальная экспертиза при некоторых заболеваниях | Добавил: astra71 (03.01.2012) | |
| Просмотров: 30485 | Рейтинг: 5.0/4 |
Добавлять комментарии могут только зарегистрированные пользователи.
[
Регистрация
|
Вход
]

Источник
Миелодиспластический синдром – группа гематологических заболеваний, при которых наблюдаются цитопения, диспластические изменения костного мозга и высокий риск возникновения острого лейкоза. Характерные симптомы отсутствуют, выявляются признаки анемии, нейтропении и тромбоцитопении. Диагноз устанавливается с учетом данных лабораторных анализов: полного анализа периферической крови, гистологического и цитологического исследования биоптата и аспирата костного мозга и т. д. Дифференциальный диагноз может представлять значительные затруднения. Лечение – переливание компонентов крови, химиотерапия, иммуносупрессивная терапия, пересадка костного мозга.
Общие сведения
Миелодиспластический синдром – группа заболеваний и состояний с нарушениями миелоидного кроветворения и высоким риском развития острого лейкоза. Вероятность развития увеличивается с возрастом, в 80% случаев данный синдром диагностируется у людей старше 60 лет. Мужчины страдают несколько чаще женщин. У детей миелодиспластический синдром практически не встречается. В последние десятилетия гематологи отмечают увеличение заболеваемости среди лиц трудоспособного возраста. Предполагается, что причиной «омоложения» болезни могло стать существенное ухудшение экологической обстановки.
До недавнего времени лечение миелодиспластического синдрома было только симптоматическим. Сегодня специалисты разрабатывают новые методы терапии, однако эффективное лечение этой группы болезней все еще остается одной из самых сложных проблем современной гематологии. Пока прогноз при миелодиспластическом синдроме, в основном, зависит от особенностей течения болезни, наличия или отсутствия осложнений. Лечение осуществляют специалисты в сфере онкологии и гематологии.
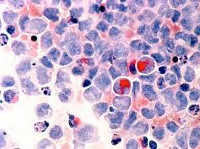
Миелодиспластический синдром
Причины и классификация миелодиспластического синдрома
С учетом причин развития различают два типа миелодиспластического синдрома: первичный (идиопатический) и вторичный. Идиопатический вариант выявляется в 80-90% случаев, диагностируется преимущественно у пациентов старше 60 лет. Причины возникновения установить не удается. В числе факторов риска первичного миелодиспластического синдрома – курение, повышенный уровень радиации при выполнении профессиональных обязанностей или проживании в неблагоприятной экологической зоне, частый контакт с бензином, пестицидами и органическими растворителям, некоторые наследственные и врожденные заболевания (нейрофиброматоз, анемия Фанкони, синдром Дауна).
Вторичный вариант миелодиспластического синдрома наблюдается в 10-20% случаев, может возникать в любом возрасте. Причиной развития становится химиотерапия или радиотерапия по поводу какого-то онкологического заболевания. В число лекарственных средств с доказанной способностью вызывать миелодиспластический синдром включают циклофосфан, подофиллотоксины, антрациклины (доксорубицин) и ингибиторы топоизомеразы (иринотекан, топотекан). Вторичный вариант отличается более высокой резистентностью к лечению, более высоким риском развития острого лейкоза и более неблагоприятным прогнозом.
В современной редакции классификации ВОЗ различают следующие типы миелодиспластического синдрома:
- Рефрактерная анемия. Сохраняется более полугода. В анализе крови бласты отсутствуют либо единичные. В костном мозге дисплазия эритроидного ростка.
- Рефрактерная анемия с кольцевыми сидеробластами. Сохраняется более полугода. В анализе крови бласты отсутствуют. В костном мозге дисплазия эритроидного ростка.
- Рефрактерная цитопения с многолинейной дисплазией. В анализе крови тельца Ауэра отсутствуют, бласты отсутствуют либо единичные, выявляются панцитопения и увеличение количества моноцитов. В костном мозге диспластические изменения менее 10% клеток в 1 миелоидной клеточной линии, бластов менее 5%, телец Ауэра нет.
- Рефрактерная анемия с избытком бластов-1. В анализе крови тельца Ауэра отсутствуют, бластов более 5%, цитопения и увеличение количества моноцитов. В костном мозге дисплазия одной либо нескольких клеточных линий, бластов 5-9%, телец Ауэра нет.
- Рефрактерная анемия с избытком бластов-2. В анализе крови увеличение количества моноцитов, цитопения, бластов 5-19%, могут выявляться тельца Ауэра. В костном мозге дисплазия одной либо нескольких клеточных линий, бластов 10-19%, обнаруживаются тельца Ауэра.
- Неклассифицируемый миелодиспластический синдром. В анализе крови цитопения, бласты отсутствуют либо единичные, тельца Ауэра отсутствуют. В костном мозге дисплазия одного мегакариоцитарного либо гранулоцитарного ростка, бластов более 5%, тельца Ауэра отсутствуют.
- Миелодиспластический синдром, ассоциированный с изолированной делецией 5q. В анализе крови анемия, бластов более 5%, возможен тромбоцитоз. В костном мозге более 5% бластов, тельца Ауэра отсутствуют, изолированная делеция 5q.
Симптомы миелодиспластического синдрома
Клиническая симптоматика определяется степенью нарушений миелопоэза. При мягко протекающих расстройствах возможно длительное бессимптомное или стертое течение. Из-за слабой выраженности клинических проявлений некоторые больные не обращаются к врачам, и миелодиспластический синдром обнаруживается во время проведения очередного медицинского осмотра. При преобладании анемии наблюдаются слабость, одышка, плохая переносимость физических нагрузок, бледность кожных покровов, головокружения и обморочные состояния.
При миелодиспластическом синдроме с тромбоцитопенией возникает повышенная кровоточивость, отмечаются десневые и носовые кровотечения, на коже появляются петехии. Возможны подкожные кровоизлияния и меноррагии. Миелодиспластический синдром с выраженными нейтропенией и агранулоцитозом проявляется частыми простудами, стоматитом, синуситом или стрептодермией. В тяжелых случаях возможно развитие пневмонии или сепсиса. Инфекционные заболевания нередко вызываются грибками, вирусами или условно-патогенными микробами. У каждого пятого пациента с миелодиспластическим синдромом выявляется увеличение лимфоузлов, селезенки и печени.
Диагностика миелодиспластического синдрома
Диагноз выставляется с учетом данных лабораторных исследований: анализа периферической крови, биопсии костного мозга с последующим цитологическим исследованием, цитохимических и цитогенетических тестов. В анализе периферической крови больных миелодиспластическим синдромом обычно обнаруживается панцитопения, реже выявляется дву- или одноростковая цитопения. У 90% пациентов наблюдается нормоцитарная либо макроцитарная анемия, у 60% – нейтропения и лейкопения. У большинства больных миелодиспластическим синдромом отмечается тромбоцитопения.
При исследовании костного мозга количество клеток обычно нормальное либо повышенное. Уже на ранних стадиях обнаруживаются признаки дизэритропоэза. Количество бластов зависит от формы миелодиспластического синдрома, может быть нормальным либо увеличенным. В последующем наблюдаются дисгранулоцитопоэз и дисмегакариоцитопоэз. У некоторых больных признаки дисплазии костного мозга выражены очень слабо. В процессе цитогенетического исследования у ¾ больных выявляются хромосомные нарушения. Дифференциальный диагноз миелодиспластического синдрома проводят с В12-дефицитной анемией, фолиево-дефицитной анемией, апластической анемией, острым миелолейкозом и другими острыми лейкозами.
Лечение и прогноз при миелодиспластическом синдроме
Тактика лечения определяется выраженностью клинической симптоматики и лабораторных изменений. При отсутствии явных признаков анемии, геморрагического синдрома и инфекционных осложнений осуществляется наблюдение. При миелодиспластическом синдроме с выраженной анемией, тромбоцитопенией и нейтропенией, а также при высоком риске возникновения острого лейкоза назначают сопроводительную терапию, химиотерапию и иммуносупрессивную терапию. При необходимости осуществляют пересадку костного мозга.
Сопроводительная терапия является самым распространенным методом лечения миелодиспластического синдрома. Предусматривает внутривенные инфузии компонентов крови. При длительном применении может провоцировать повышение уровня железа, влекущее за собой нарушения деятельности жизненно важных органов, поэтому переливания гемокомпонентов производят при одновременном приеме хелаторов (лекарственных средств, связывающих железо и способствующих его выведению).
Иммуносупрессоры эффективны при лечении миелодиспластического синдрома с отсутствием хромосомных аномалий, наличием гена HLA-DR15 и гипоклеточном костном мозге. Химиотерапию применяют при невозможности трансплантации костного мозга. Высокие дозы препаратов используют при трансформации миелодиспластического синдрома в острый лейкоз, а также при рефрактерных анемиях с избытком бластов при нормоклеточном и гиперклеточном костном мозге, низкие – при невозможности пересадки костного мозга. Наряду с перечисленными средствами пациентам назначают гипометилирующие средства (азацитидин). Наиболее надежным способом достижения полноценной длительной ремиссии является трансплантация костного мозга.
Прогноз зависит от типа миелодиспластического синдрома, количества хромосомных аномалий, необходимости в регулярных переливаниях компонентов крови, выраженности клинических проявлений и наличия осложнений. Различают 5 групп риска. Средняя выживаемость больных миелодиспластическим синдромом, входящих в группу с самым низким уровнем риска, составляет более 11 лет; с самым высоким – около 8 месяцев. Вероятность отторжения костного мозга после трансплантации – около 10%.
Источник
