Миопатический синдром что это такое у детей
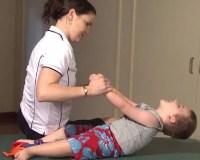
Миотонии, миопатии у детей и синдром вялого ребенка: причины, клиника, диагностикаМиотония — замедленная релаксация мышцы после её сокращения. Выявляется клинически и при ЭМГ. Дистрофическая миотония относительно распространённое заболевание наследуется по аутосомно-доминантному типу и вызвано «экспансией» повторов нуклеотидных триплетов. Это значит, что в поколениях может наблюдаться эффект антиципации, особенно при наследовании от матери. У новорождённых заболевание проявляется гипотонией, нарушениями питания и дыхания из-за мышечной слабости. В таком случае целесообразно исследовать мать на предмет миотонии. Первые симптомы проявляются при рукопожатии — больной медленно разжимает кисть, что облегчается сгибанием кисти в запястье. Симптом бывает слабовыраженным и незаметным. Необходимы методы с высокой чувствительностью, поскольку диагноз у новорождённого может иметь последствия для всей семьи. У детей старшего возраста бывают лицо миопата (атрофия мимических мышц), задержка умственного развития и миотония. У взрослых развивается катаракта, у мужчин — лобная алопеция и тестикулярная атрофия. Смерть обычно бывает вызвана кардиомиопатией. Метаболические миопатии у детейМетаболические изменения могут влиять на мышцы накоплением вещества, либо путём его депонирования, либо из-за недостаточности ферментов его расщепления. Проявляются синдромом «вялого» ребёнка, у детей старшего возраста — в виде мышечной слабости или мышечных судорог при физической нагрузке. Основные причины: Врожденные миопатииПроявляются при рождении или в грудном возрасте в виде генерализованной мышечной гипотонии и слабости. Названия заключают в себе изменения, обнаруживаемые при мышечной биопсии или электронной микроскопии. Они включают: Активность КФК нормальная или слегка повышенная.
Синдром «вялого» ребёнкаПерсистирующую гипотонию у грудных детей можно выявить при подъёме ребёнка, который стремится выскользнуть из рук или висит, как тряпичная кукла, при поддерживании ребёнка в положении лёжа. Отмечают выраженное запаздывание подъёма головы из положения лёжа с помощью рук. Клиническое обследование помогает определить уровень поражения — корковый или нейромышечный. Миотония центрального генеза связана с низким тонусом мышц туловища и сохранным тонусом в конечностях. Признаки дисморфогенеза свидетельствуют о генетической причине. Поражения периферического двигательного нейрона можно заподозрить при наличии позы лягушки, слабых антигравитационных движениях и отсутствии рефлексов. Причины синдрома «вялого» ребёнка: • Генетические. • Метаболические. • Нейромышечные. Нейромышечные заболевания у детей: • При острой поствоспалительной полинейропатии (синдроме Гийена—Барре) — восходящая симметричная слабость с отсутствием рефлексов и нарушениями в чувствительной и вегетативной сферах, бывают бульварный паралич и угнетение дыхания. • Миодистрофия Дюшенна наследуется по рецессивному Х-сцепленномутипу и проявляется утиной походкой и затруднением при подъёме по лестнице. – Также рекомендуем “Нейрокожные синдромы у детей: нейрофиброматоз, туберозный склероз, синдром Стерджа-Вебера” Оглавление темы “Детская неврология”:
|
Источник
Миотонический синдром у детей — это нервно-мышечная патология, для которой характерна затрудненная релаксация мускулатуры после ее напряжения. Встречается при наследственных генетических дефектах либо как проявление неврологических, эндокринных, метаболических, аутоиммунных заболеваний. Синдром характеризуется нарушениями двигательной активности, асимметрией мышц, задержкой психомоторного развития. Для диагностики необходим неврологический осмотр, инструментальные методы (ЭМГ, МРТ) и генетическое обследование. Лечение миотонии симптоматическое с применением физиотерапии, ЛФК и массажа, психолого-педагогической коррекции.
Общие сведения
Частота встречаемости наследственных форм миотонического синдрома (МС) варьирует от 14 до 23 случаев на 100 тыс. детского населения. В отношении приобретенных вариантов статистических данных нет, поскольку в таких случаях патология не регистрируется как самостоятельная нозологическая единица и входит в структуру других неврологических болезней. Актуальность проблемы в педиатрической практике заключается в прогрессирующем течении заболевания, невозможности назначить этиотропное лечение и значительном ухудшении качества жизни детей при наследственных видах патологии.

Миотонический синдром у детей
Причины
В детском возрасте манифестируют врожденные формы, которые передаются преимущественно по аутосомно-доминантному, реже — аутосомно-рецессивному типу (синдром Шварца-Джампела, в части случаев — болезнь Томпсона). Самая частая форма наследственного МС — миотоническая дистрофия Россолимо-Штейнерта-Баттена-Куршмана, которая составляет до 97% всех генетических миотоний и связана с мутацией гена DMPK на 19-й хромосоме. Реже это заболевание обусловлено генетическими дефектами в 3-й (3q21) и 15-й (15q21-q24) хромосомах.
Вторичным миотоническим синдромом могут сопровождаться:
- родовые травмы с церебральными повреждениями;
- тяжелые формы перинатальной энцефалопатии;
- органические поражения ЦНС (опухоли, последствия перенесенных энцефалитов, ЧМТ);
- врожденные и воспалительные миопатии;
- миоплегии (болезнь Гамсторпа, периодический паралич);
- дефицитные состояния (рахит);
- эндокринные и метаболические расстройства (микседема, гипофункция паращитовидных желез, гиперкалиемия);
- аутоиммунные нарушения (приобретенная нейромиотония);
- длительное лечение клофибратом, калийсберегающими диуретиками, препаратами калия.
Патогенез
В механизме развития заболевания ведущим является нарушение процесса расслабления мышцы в результате метаболического или ионного дисбаланса. При этом изменяются свойства мембран миоцитов, происходит их усиленная деполяризация и повышение возбудимости. При совершении определенного действия с участием мускулатуры миофибриллы долго не могут расслабиться и вернуться в исходное положение, вследствие чего и возникает феномен миотонической задержки.
Лучше всего изучен патогенез дистрофической миотонии 1 типа, связанной с нарушениями на уровне экспрессии нуклеотидного повтора CTG. У детей изменяется концентрация миотонин-протеинкиназы DMPK, которая присутствует в скелетной мускулатуре, миокарде и ЦНС. В редких случаях клинические проявления обусловлены дисфункцией ионных каналов клеточных мембран, которая отмечается при аутоиммунных нарушениях.
Симптомы
Главный признак миотонического синдрома — скованность мышечных групп в конце движения. Это проверяется с помощью симптома «кулака»: после сжатия пальцев ребенок несколько секунд не может разжать кулак, и для этого ему нужно прилагать много усилий. Синдром характеризуется затруднениями жевания, неспособностью быстро открыть глаза после зажмуривания. Для наследственных форм МС у детей типично усиление симптоматики при целенаправленных движениях, в холодное время года.
При врожденных формах миотонического синдрома возможно асимметричное развитие мускулатуры. Если патология проявляется с первых месяцев жизни, родители замечают, что ребенок не способен удерживать голову, слабо сосет грудь, у него хуже сформированы рефлексы. Для грудничков с миотоническим синдромом характерно запоздалое становление моторики. В раннем детстве наблюдается повышенная утомляемость малыша, отсутствие интереса к активным играм, отставание в физическом развитии.
На поздних стадиях заболевания у детей происходит атрофия мышц, поэтому типичные признаки миотонического синдрома ослабевают, а потом исчезают. В клинической картине преобладает выраженная мышечная слабость, особенно в дистальных мышцах конечностей. Это обуславливает изменение походки, приводит к появлению вялых парезов и параличей. Поражение лицевых мышц проявляется постоянно «печальным» выражением лица и бедностью мимики.
Осложнения
Врожденные миотонические синдромы относят к мультисистемным поражениям, поэтому у таких детей зачастую диагностируют сопутствующие сердечно-сосудистые, неврологические и эндокринные нарушения. Особую опасность представляет нарушение иннервации дыхательной мускулатуры, из-за чего у пациентов нарастать дыхательная недостаточность вплоть до асфиксии. Церебральные симптомы, как правило, сочетаются с когнитивными нарушениями.
Лечение наследственных разновидностей миотонического синдрома затруднено, поэтому нередки летальные исходы в молодом возрасте. До 80% смертей вызваны вторичной пневмонией на фоне аспирации пищи и нарушений глотания, жизнеугрожающими аритмиями, которые развиваются вследствие дегенерации проводящей системы сердца. У детей может возникать глубокая умственная отсталость, приводящая к инвалидности.
Диагностика
При физикальном осмотре детский невролог проверяет симптом «кулака», оценивает сохранность рефлексов, мышечную силу. На основании полного физикального осмотра специалисту удается поставить предварительный диагноз. Чтобы подтвердить наличие и выяснить причины миотонического синдрома, назначаются следующие диагностические исследования:
- Электромиография. Патогномоничный признак миотонии на ЭМГ — появление высокоамплитудных разрядов со звуковым феноменом при использовании игольчатых электродов. При прогрессировании болезни присутствуют симптомы миопатии: снижение амплитуды потенциалов, полифазные двигательные единицы.
- Биопсия мышц. На ранних стадиях в биоптате определяются неспецифические миопатические изменения: центрально расположенные ядра, уменьшение длины волокон, признаки денервации — наличие пикнотических ядерных глыбок и маленьких угловых мускульных волокон.
- Магнитно-резонансная томография. По результатам МРТ конечностей врач оценивает степень развития мускулатуры и замещения ее жировой тканью. Учитывая сопутствующее поражение ЦНС, рекомендована МРТ головного мозга для обнаружения структурных изменений белого вещества и желудочков.
- Генетическая диагностика. Исследование генома для выявления типичной мутации — «золотой стандарт» для постановки диагноза врожденных вариантов миотонического синдрома у детей. По показаниям можно проводить тестирование в антенатальном периоде, если в семьях родителей были случаи миотонии.
Лечение миотонического синдрома у детей
Консервативная терапия
Этиопатогенетическое лечение миотонического синдрома пока не разработано, поэтому в детской неврологии ограничиваются симптоматическими средствами. Медикаменты подбираются с учетом конкретной ситуации и выраженности патологических изменений. Для замедления прогрессирования проводится лечение противосудорожными средствами и миорелаксантами, для подавления аутоиммунных реакций назначают глюкокортикоиды.
Решающее значение в терапевтической схеме отводится упражнениям ЛФК, которые укрепляют мышечный корсет, помогают сбалансировать развитие разных групп мышц, что улучшает качество жизни больных детей. Показано физиотерапевтическое лечение в виде электрофореза с кальцием, электростимуляции мышц, бальнеотерапии. Для уменьшения миотонического синдрома полезен массаж.
Реабилитация
Учитывая серьезные двигательные нарушения, лечение дополняется регулярными занятиями в реабилитационных центрах с использованием тренажеров и индивидуальных методик. Нарушения артикуляции у детей корректируются занятиями с логопедом. При задержке умственного развития ребенку может потребоваться помощь олигофренопедагога либо обучение в специализированной школе.
Прогноз и профилактика
Если вовремя начать лечение, при приобретенных формах удается восстановить мышечную активность. Наследственный миотонический синдром отличаются сомнительным прогнозом. Средняя продолжительность жизни пациентов составляет 35 лет при раннем дебюте болезни. Специфические меры профилактики миотонического синдрома не разработаны. Семьям с отягощенным анамнезом требуется медико-генетическое консультирование.
Источник
Врожденная миопатия — врожденное заболевание, обусловленное генетически детерминированными нарушениями в строении мышечной ткани. Врожденная миопатия проявляется диффузной мышечной слабостью и снижением мышечного тонуса, выраженность которых значительно варьирует в зависимости от вида миопатии. В тяжелых случаях врожденная миопатия может привести к гибели ребенка от дыхательной недостаточности. Диагностируется врожденная миопатия в основном по результатам морфологического исследования образцов, полученных при биопсии мышц; электромиография, эргометрия и исследование мышечного тонуса имеют лишь вспомогательное значение. Врожденная миопатия может потребовать мероприятий по борьбе с дыхательными нарушениями, обеспечению зондового питания, коррекции имеющихся ортопедических деформаций и пр.
Общие сведения
Термин «врожденная миопатия» применяется в неврологии в отношении целой группы достаточно редких наследственных болезней, которые имеют сходную клиническую картину и дифференцируются лишь по специфическим морфологическим изменениям в строении мышечной ткани. К наиболее часто встречаемым видам врожденной миопатии относятся: болезнь центрального стержня, немалиновая миопатия, миотубулярная миопатия, миопатия с множественными стержнями и врожденная диспропорциональность типов мышечных волокон.
Врожденная миопатия является генетически обусловленным заболеванием. В зависимости от вида миопатии аномалия может локализоваться в различных локусах хромосом и передаваться по наследству доминантно, рецессивно или сцеплено с Х-хромосомой. Наличие аномального гена приводит к нарушению синтеза того или иного белка, входящего в структуру мышечной ткани. В результате изменяется строение мышечных волокон, что негативно отражается на их сократительной способности и приводит к генерализованной мышечной слабости. Обычно врожденная миопатия проявляется в раннем детском возрасте. Ее симптомы сохраняются в течение всей жизни пациента. В большинстве случаев врожденная миопатия характеризуется доброкачественным течением со слабым прогрессированием или вовсе без него.

Врожденная миопатия
Классификация врожденной миопатии
В основу классификации врожденной миопатии были положены 2 признака: наличие информации о локализации генной аномалии и данных о том, какой именно белок мышечной ткани является дефектным. В соответствии с этим выделяется врожденная миопатия с известным мутантным геном и определенным дефектным белком (немалиновая миопатия, болезнь центрального стержня, миотубулярная миопатия), врожденная миопатия с неопределенным дефектным белком, но установленным мутантным геном (десмин-связанная и актинзависимая миопатии) и врожденная миопатия, для которой неизвестными остаются и ген, и дефектный белок (врожденная диспропорция типов волокон, центронуклеарная миопатия, миопатия с множественными стержнями).
Симптомы врожденной миопатии
Врожденная миопатия в первые месяцы жизни ребенка характеризуется наличием синдрома «вялого ребенка»: диффузным снижением мышечного тонуса, легкой мышечной слабостью, плохим развитием мускулатуры и ослабленным сосанием. По мере развития ребенка мышечная слабость становится более заметной. Она проявляется невозможностью подняться с пола, залезть на стул, затруднениями при ходьбе и других действиях, которые без проблем выполняют другие дети того же возраста. Мышечная слабость при врожденной миопатии может быть выражена в различной степени. Обычно не наблюдается ее существенное прогрессирование. В тяжелых случаях ребенок так и не может встать на ноги и вынужден всю жизнь передвигаться на каталке. Но те навыки, которые были им приобретены, уже не утрачиваются.
Наибольшая опасность врожденной миопатии связана со слабостью дыхательной мускулатуры. При умеренной мышечной слабости отмечается постепенное развитие дыхательной недостаточности, частые бронхо-легочные заболевания (бронхит, очаговая пневмония, застойная пневмония и др.). Выраженная слабость дыхательных мышц может приводить к быстрому развитию дыхательной недостаточности и гибели ребенка в младенческом возрасте.
В некоторых случаях врожденная миопатия сочетается с дисморфичными чертами (высокое небо, удлиненная и узкая форма лица) и скелетными аномалиями (кифоз, сколиоз, косолапость, грудь сапожника, врожденный вывих бедра).
Характеристика отдельных видов врожденной миопатии
Болезнь центрального стержня наследуется аутосомно-доминантно, известны также отдельные спорадические случаи заболевания. Врожденная миопатия этого вида проявляется задержкой двигательного развития в период первого года жизни, реже обнаруживается у взрослых пациентов, часто сопровождается слабостью мимической мускулатуры. Характерен небольшой рост больных и хрупкая фигура, наличие скелетных деформаций. У пациентов с этим видом врожденной миопатии отмечается повышенный риск возникновения злокачественной гипертермии. В биоптате мышечной ткани выявляют мышечные волокна с единичными или множественными зонами асептического некроза.
Немалиновая врожденная миопатия включает актинопатию, небулинопатию, тропомиозинопатию и тропонинопатию. Ее наследование происходит чаще по аутосомно-доминантному принципу, но также встречается рецессивное наследование и спорадические случаи заболеваемости. Классическая форма немалиновой врожденной миопатии характеризуется синдромом вялого ребенка. Тяжелая форма проявляется еще во внутриутробном периоде в виде акинезии плода, а при рождении ребенка — тяжелыми двигательными нарушениями, слабостью мышц лица и дыхательной недостаточностью. Легкая форма этого типа врожденной миопатии диагностируется после периода раннего детства, иногда — в подростковом возрасте, и протекает без слабости лицевой мускулатуры. Существует также специфическая форма немалиновой врожденной миопатии, при которой возможно развитие офтальмоплегии, кардиомиопатии, синдрома ригидного позвоночника. Морфологическое исследование обнаруживает наличие в мышцах характерных палочко- или нитеподобных телец.
Миотубулярная врожденная миопатия чаще наследуется как аутосомная, при которой мышечная слабость выражена в легкой степени и может наблюдаться как у девочек, так и у мальчиков. Х-сцепленная миотубулярная врожденная миопатия поражает только лиц мужского пола и характеризуется более тяжелым течением со слабостью лицевых мышц, расстройством глотания и дыхательной функции. В биоптате мышечной ткани преобладает поражение волокон I типа. Отмечается центральное расположение ядер миоцитов, что соответствует мышечной ткани эмбриона на 8-10 недели беременности. В связи с эти большинство исследователей рассматривают миотубулярную миопатию как результат недоразвития мышечной ткани.
Миопатия с множественными стержнями чаще наблюдается как аутосомно-рецессивное заболевание, хотя возможен и доминантный тип наследования. Типична мышечная слабость в проксимальных отделах, которая наблюдается в грудном возрасте. Намного реже заболевание дебютирует в более старшем возрасте. В таких случаях отмечается генерализованная мышечная слабость. В мышечном биоптате определяются клетки с отсутствием митохондрий, деструкция сакромеров и гипотрофия мышечных волокон.
Врожденная диспропорция типов мышечных волокон проявляется генерализованной слабостью мышц, в том числе и лицевых, мышечной гипотонией, аномалиями скелета. Тип наследования этой врожденной миопатии пока не установлен. В биоптате мышц наблюдается увеличение количества и малый размер волокон I типа на фоне гипертрофии или нормального размера волокон II типа.
Диагностика врожденной миопатии
В легких случаях только прицельный осмотр с исследованием мышечной силы и тонуса позволяет неврологу заподозрить наличие у ребенка врожденной миопатии. Тщательное исследование мышц с проведением силового тестирования (эргометрии), стандартной и стимуляционной электромиографии, миотонометрии или электротонометрии позволяет получить дополнительные данные, свидетельствующие в пользу диагноза «врожденная миопатия». Исключить генерализованную воспалительную миопатию (дерматомиозит, полимиозит) и диффузный миозит позволяет отсутствие болевого синдрома, уплотнений и воспалительной отечности мышц.
Окончательно врожденная миопатия может быть диагностирована только после результатов морфологического исследования мышечной ткани, полученной путем биопсии мышц. Лишь это обследование позволяет определить специфичные для каждого вида миопатии изменения и установить точный диагноз. Однако даже биопсия не всегда позволяет достоверно верифицировать тип врожденной миопатии.
Лечение врожденной миопатии
К сожалению, на сегодняшний день не существует достаточно эффективных способов лечения и врожденная миопатия сохраняет свои проявления в течение всей жизни больного. Возможные методы терапии направлены на поддержание как можно более высокого уровня жизнеспособности пациента. Если врожденная миопатия сопровождается значительным снижением мышечной силы, в первые месяцы жизни медицинские мероприятия заключаются в борьбе с дыхательной недостаточностью, обеспечении питания через желудочный зонд, купировании бронхо-легочных осложнений. Благоприятное влияние на состояние больных в любом возрасте оказывает массаж, водолечение и физиотерапевтические процедуры. В более старшем возрасте может потребоваться ортопедическая коррекция имеющихся нарушений и социальная адаптация пациентов.
Источник

