Множественные пороки развития плода синдром
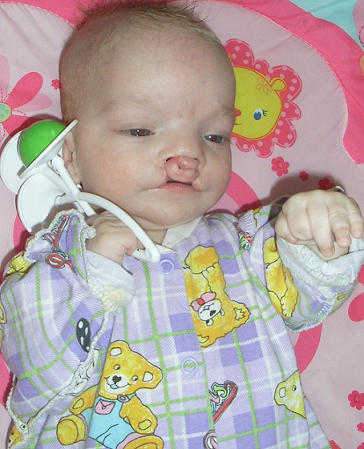
УЗИ плода на выявление генетических патологий — это выявление трисомий (дополнительной третьей хромосомы в генетическом наборе плода), приводящих к рождению малыша с серьёзными наследственными заболеваниями и физическими уродствами. Обнаружить пороки плода на УЗИ можно уже на первых этапах развития беременности.
На 1000 новорождённых приходится 5-7 младенцев с аномалиями половых (наследственных) или соматических (ненаследственных) клеток. Чаще всего эмбрион с хромосомным нарушением погибает на начальных сроках беременности, когда у женщины возникает выкидыш. С помощью УЗИ можно увидеть различные аномалии и патологии, поэтому ультразвуковое исследование на выявление пороков развития обязательно для каждой беременной женщины.
Аномалии развития плода закладываются уже в момент оплодотворения сперматозоидом яйцеклетки. Например, такая патология, как триплоидия (наличие трех хромосомом в ряду цепочки, а не двух, как положено), возникает в случае проникновения в яйцеклетку двух сперматозоидов, каждый из которых оставляет по одной хромосоме. Естественно, с таким набором живой организм не может выжить, поэтому на определённом этапе происходит выкидыш или замершая беременность.
Никто не застрахован от рождения малыша с генетическими отклонениями. Если раньше к группе риска относили матерей старше 35 лет, диабетиков, женщин, имеющих хронические заболевания (почечная недостаточность, проблемы с щитовидкой), то в наши дни больные дети рождаются у молодых матерей в возрасте от 20 до 30 лет.
Данные статистики наводит на мрачные мысли. Так, риск рождения малыша с хромосомными аномалиями у 20-летних женщин составляет 1:1667, а у 35-летних уже 1:192. А на деле это означает, что в 99,5% случаев ребёнок у тридцатипятилетней матери родится здоровым.
В 1 семестре на сроке от 10 до 14 недель (до 10 недели УЗИ неинформативно) беременная проходит исследование, именуемое скринингом. Он состоит из биохимического анализа крови и УЗИ исследования эмбриона. Результатом скрининга является выявление следующих патологий:
На 20-24 неделе делается ещё одно УЗИ. Среди генетических заболеваний плода, видимых на ультразвуковом исследовании во 2 семестре, можно отметить:
На 3 семестре проводится допплерометрия – УЗИ исследование с определением сосудистой системы плода, плаценты и матери. Начиная с 23 недели беременности проверяются артерия пуповины, маточная артерия и средняя мозговая артерия. Исследуется систолический (при сокращении сердечной мышцы) и диастолический (при расслаблении сердечной мышцы) кровоток. У малыша с хромосомными нарушениями кровоток атипичен.
Ультразвуковая диагностика представляет широкий спектр исследований. Существует несколько видов УЗИ, которые с предельной точностью определяют внутриутробные пороки развития малыша.
Стандартное УЗИ. Оно обычно совмещено с биохимическим анализом крови. Оно проводиться не раньше 10 недель беременности. В первую очередь у плода выявляют толщину воротниковой зоны, которая не должна превышать 3 мм, а также визуализацию носовой кости. У малыша с синдромом Дауна воротниковая зона толще нормы, а носовые кости не развиты. Также на увеличение толщины влияют следующие факторы:
Генетические патологии бывают как специфические (синдром Дауна, опухоль Вильмса), так и общие, когда внутренний орган развивается неправильно. Для выявления общих аномалий существует анатомическое исследование плода. Оно проводится на 2 семестре начиная с 20 недели беременности. В этот период можно увидеть личико малыша и определить его пол.
Продольная и поперечная проекция позвоночника подтверждает или опровергает правильное расположение костей, можно убедиться в целостности брюшной стенки. Отсутствие патологий сердца подтверждают одинаковые размеры предсердий и желудочков. О нормальной работе желудка говорит его наполненность околоплодными водами. Почки должны располагаться на своём месте, а моча из них свободно поступать в мочевой пузырь. Врач чётко видит конечности плода, кроме пальчиков ног.
Патология
Как и когда выявляют
В чём суть патологии
Характерные черты
Психическое и интеллектуальное развитие
Синдром Дауна
Проводится биопсия хориона, увеличенное воротниковое пространство у плода, недоразвитость костей носа, увеличенный
мочевой пузырь, тахикардия у плода
Хромосомы 21-й пары вместо положенных 2 представлены 3 в цепочке
Раскосый монголоидный разрез глаз независимо от расы ребёнка, неразвитая переносица, неглубоко посаженные глаза, полукруглое плоское ухо, укороченный череп, плоский затылок, укороченный нос
Задержка интеллектуального развития, маленький словарный запас, отсутствует абстрактное мышление, нет концентрации внимания, гиперактивность
ПРОГНОЗ
Синдром Патау
Маленькая голова на 12 неделе на УЗИ, несимметричные полушарии, лишние пальцы
В 13-й хромосоме присутствует трисомия
Дети рождаются с микроцефалией (неразвитость головного мозга), низкий лоб, скошенные глазные щели, расщелины губы и нёба, помутнение роговицы, дефекты сердца, увеличены почки, аномальные половые органы
Глубокая умственная отсталость, отсутствие мышления и речи
ПРОГНОЗ
Синдром Эдвардса
Биопсия хориона, внутриутробное взятие крови из пуповины, на УЗИ видна микроцефалия
В 18-й хромосом есть трисомия
Рождаются в основном девочки (3/4), а плод мужского пола погибает ещё в утробе. Низкий скошенный лоб, маленький рот, недоразвитость глазного яблока, расщелины верхней губы и нёба, узкий слуховой проход, врождённые вывихи, косолапость, тяжёлые аномалии сердца и ЖКТ, недоразвитость мозга
Дети страдают олигофренией (органическим поражением головного мозга), умственной отсталостью, имбецильностью (средней умственной отсталостью), идиотией (отсутствием речи и умственной деятельности)
ПРОГНОЗ
Синдром Шерешевского-Тёрнера
Рентген костных структур плода, МРТ миокарда
Аномалия, встречающаяся в Х-хромосоме
Встречается чаще у девочек. Укороченная шея со складками, отёчны кисти и ступни, тугоухость. Отвисшая нижняя губа, низкая линия роста волос, недоразвитая нижняя челюсть. Рост во взрослом возрасте не превышает 145 см. Дисплазия суставов. Аномальное развитие зубов. Половой инфантилизм (нет фолликул в яичниках), недоразвитость молочных желез
Страдает речь, внимание. Интеллектуальные способности не нарушены
ПРОГНОЗ
Полисомия по Х-хромосоме
Скрининг на 12 неделе беременности, биопсия хориона, анализ амниотической жидкости. Настораживает увеличение воротниковой зоны
Вместо двух Х-хромосом встречается три и более
Встречается у девочек и редко у мальчиков. Характерен половой инфантилизм (не развиваются вторичные половые признаки), высокий рост, искривление позвоночника, гиперпигментация кожи
Антисоциальное поведение, агрессия, умственная отсталость у мужчин.
ПРОГНОЗ
Полисомия по Y-хромосоме
Вместо ХY-хромосом есть лишняя Y-хромосома
Встречается у мальчиков. Вырастают высокого роста от 186 см, тяжёлая массивная нижняя челюсть, выпуклые надбровные дуги, узкие плечи, широкий таз, сутулость, жир на животе
Умственная отсталость, агрессия, эмоциональная неустойчивость
ПРОГНОЗ
Синдром Карнелии де Ланге
При анализе крови беременной женщины в сыворотке не обнаружено протеина-А плазмы (РАРР-А), которого обычно много
мутациями в гене NIPBL или SMC1A
Тонкие сросшиеся брови, укороченный череп, высокое нёбо, аномально прорезавшиеся зубы, недоразвитые конечности, мраморная кожа, врождённые пороки внутренних органов, отставание в росте
Глубокая умственная отсталость,
ПРОГНОЗ
Синдром Смита-Лемли-Опитца
УЗИ показывает аномалии черепа у плода, не просматриваются рёберные кости
мутация в гене DHCR7, отвечающий за выработку холестерина
Узкий лоб, опущены веки, косоглазие, деформация черепа, короткий нос, низко расположенные уши, недоразвитые челюсти, аномалии половых органов, сращение пальцев
Повышенная возбудимость, агрессия, понижение мышечного тонуса, нарушения сна, отставание в умственном развитии, аутизм
ПРОГНОЗ
Синдром Прадера-Вилли
Отмечается низкая подвижность плода, неправильное положение,
В 15-й хромосоме отсутствует отцовская часть хромосомы
Ожирение при низком росте, плохая координация, слабый мышечный тонус, косоглазие, густая слюна, плохие зубы, бесплодие
Задержка психического развития, речевое отставание, отсутствие навыков общения, слабая мелкая моторика. Половина больных имеет средний уровень интеллекта, умеют читать
ПРОГНОЗ
При постоянных занятиях ребёнок может научиться читать, считать,запоминает людей. Следует вести борьбу с перееданием
Синдром Ангельмана
Начиная с 12-й недели наблюдается отставание развития плода в росте и массе
Отсутствуют или мутирует ген UBE3A в 15-й хромосоме
Частый необоснованный смех, мелкий тремор, много ненужных движений, широкий рот, язык вываливается наружу, ходьба на абсолютно прямых ногах
“Синдром счастливой марионетки”: ребёнок часто и беспричинно смеётся. Задержка психического развития, гиперактивность, нарушение координации движения, хаотичное махание руками
ПРОГНОЗ
Синдром Лангера-Гидеона
На 4D УЗИ заметна челюстно-лицевая аномалия
трихоринофаланговый синдром, заключающийся в нарушении 8-й хромосомы
Длинный нос грушевидной формы, недоразвитость нижней челюсти, очень оттопыренные уши, неравномерность конечностей, искривление позвоночника
Задержка психического развития, умственная отсталость различной степени, отсутствие речи
ПРОГНОЗ
Синдром Миллера-Диккера
На УЗИ заметно аномальное строение черепа, лицевые диспропорции
Патология в 17-й хромосоме, вызывающая разглаживание мозговых извилин. Вызывается интоксикацией плода альдегидами при злоупотреблении матерью алкоголя
Дизморфия (алкогольный синдром), пороки сердца, почек, судороги
Лиссэнцефалия (гладкость извилин больших полушарий), недоразвитость головного мозга, умственная отсталость
ПРОГНОЗ
Аномалия ДиДжорджи
В некоторых случаях на УЗИ выявляются различные пороки органов у малыша, особенно сердца (тетрада Фалло)
Заболевание иммунной системы, нарушение участка 22-й хромосомы
Гипоплазия тимуса (недоразвитость органа, отвечающего за выработку иммунных клеток), деформация лица и черепа, порок сердца. Отсутствуют паращитовидные железы, отвечающие за обмен кальция и фосфора
Атрофия коры головного мозга и мозжечка, задержка умственного развития, сложности с моторикой и речью
ПРОГНОЗ
Лечение иммуностимуляторами,пересадка тимус, кальциевосполняемая терапия. Дети редко доживают до 10 лет, умирают от последствий иммунодефицита
Синдром Уильямса
На УЗИ видны диспропорции в развитии скелета, эластичность суставов
Генетическое заболевание, вызванное отсутствием звена в 7-й хромосоме
Нарушен синтез белка эластина, у детей типично “лицо Эльфа”: припухшие веки, низко расположенные глаза, острый подбородок, короткий нос, широкий лоб
Повышенная чувствительность к звуку, импульсивность, навязчивая общительность, эмоциональная неустойчивость, тревожность, экспрессивная речь
ПРОГНОЗ
Синдром Беквита-Видеманна
На УЗИ заметны аномально непропорциональные конечности, превышение массы тела, патология почек
Генетическое заболевание, вызванное отсутствием звена в 11-й хромосоме
Бурный рост в раннем возрасте, аномально большие внутренние органы, склонность к раковым опухолям. У ребёнка пупочная грыжа, аномально большой язык, микроцефалия (недоразвитость мозга).
Эмоциональное и психическое развитие в некоторых случаях не отстаёт от нормы. Иногда встречается выраженная умственная отсталость
ПРОГНОЗ
Синдром Тричера Коллинза
На УЗИ видны ярко выраженная асимметрия черт лица
Генетическая мутация в 5-й хромосоме, вызывающая нарушение костных структур
У ребёнка практически нет лица, ярко выраженное физическое уродство
Абсолютно нормальное психо-эмоциональное развитие
ПРОГНОЗ
Предотвратить большинство проблем с вынашиванием и патологиями плода, можно заранее планируя беременность. Проходя обследование при планировании оба партнера сдают анализы, четко показывающие вероятность генетических отклонений. Также проводится спектр тестов на инфекции, способные вызвать уродства у малыша (ТОРЧ-комплекс) и другие исследования.
Приглашаем пройти УЗИ на патологии плода в Санкт-Петербурге в клинике Диана. У нас установлен новейший УЗИ аппарат с доплером. Обследование проводится в 3-Д и 4-Д фоматах. На руки выдается диск с записью.
Источник

О множественных врожденных пороках развития (МВПР) говорят тогда, когда отмечается нарушение структуры и функционирования минимум двух органов или систем. Обычно такие изменения сильно отражаются на жизнедеятельности, нередко становятся причиной внутриутробной гибели плода или неонатальной смерти. Некоторые множественные врожденные пороки развития (МВПР) не сокращают продолжительность жизни, но снижают ее качество, требуют постоянного контроля со стороны специалистов или определенных условий содержания.
Причины множественных врожденных пороков развития
Все этиологические факторы МВПР можно разделить на две группы:
- эндогенные — включают в себя генные, геномные и хромосомные мутации, заболевания эндокринной системы, метаболические нарушения, возраст родителей;
- экзогенные — физические (травмы), химические (лекарственные препараты, промышленная и бытовая химия) и биологические (вирусы, бактерии) агенты.
Эти причины приводят к хромосомным, генным и геномным нарушениям, влияют на процессы клеточного и тканевого развития. Большое число множественных врожденных пороков (МВПР) отличаются типом наследования, патогенезом, клиническими проявлениями, прогнозом для пациента.
Примеры множественных врожденных пороков развития (МВПР)
- Синдром Дауна. Развивается в результате трисомии по 21-й хромосоме. Пациенты имеют характерные черты лица, страдают задержкой умственного и речевого развития, у них нередко выявляется мышечная гипотония, катаракта, пороки сердца. Средняя продолжительность жизни составляет около 50 лет.
- Синдром Эдвардса. Данная разновидность множественных врожденных пороков развития (МВПР) обусловлена трисомией по 18-й хромосоме. У пациентов выявляется нарушение строения черепа, отсутствие или сужение слухового прохода, широкая грудная клетка, пороки сердечно-сосудистой системы, гипоплазия мозжечка, слабый тонус мускулатуры, судороги, тяжелая умственная отсталость. Характеризуется высокой летальностью.
- Синдром Марфана. Возникает при мутации в гене, который кодирует образование фибриллина. Данное соединение входит в состав практически всех эластичных волокон, поэтому у пациентов отмечается патология опорно-двигательного аппарата, органов зрения, сосудов. При регулярном и правильном лечении продолжительность жизни не снижается.
Другие виды множественных врожденных пороков развития (МВПР) оказывают существенное влияние на жизнедеятельность человека. При этом лечение возможно только симптоматическое, так как изменить дефекты в генах или хромосомах невозможно.
Методы диагностики
Диагностика множественных врожденных пороков развития (МВПР) может осуществляться дородовыми и послеродовыми способами. В первом случае проводятся скрининговые исследования, которые включают в себя УЗИ плода и анализ крови на специфические белки. Такое сочетание позволяет выявить большое количество множественных врожденных пороков развития (МВПР). Врач также может назначать дополнительные методы диагностики: биопсию ворсин хориона и амниоцентез. В этом случае получают не кровь матери, а материал плода, который затем отправляют на генетическое исследование.
Послеродовые методики также подразумевают генетические тесты, которые позволяют выявлять мутации в генах или определять кариотип. Пройти такое исследование можно в медико-генетическом центре «Геномед».
Нажимая на кнопку получить консультацию, Вы соглашаетесь на обработку персональных данных
Источник
Полувековой практикой клинической генетики и цитогенетики доказано, что для большинства хромосомных болезней, обусловленных численными или структурными аномалиями хромосом, характерны множественные врожденные пороки развития (МВПР). Если среди всех врожденных пороков на долю хромосомного дисбаланса приходится около 6 % [534], то среди МВПР удельный вес хромосомных болезней может достигать 51 % [181]. Именно поэтому цитогенетические исследования являются ведущими при выяснении причин МВПР.
Между тем МВПР могут быть следствием не только хромосомных, но и генных мутаций, а также результатом воздействия различных тератогенов, либо сочетанным эффектом этих факторов. Общепринятой классификации нехромосомных синдромов МВПР не существует, и при их описании используются различные подходы. Отечественные синдромологи выделяют несколько групп нехромосомных МВПР [28, 97].
- Моногенные синдромы — многочисленная группа (40 % от всех нехромосомных синдромов), представленная как доминантными, так и аутосомно-рецессивными формами, в том числе Х-сцепленными.
- Синдромы с неуточненным типом наследования, к которым могут относиться и мультифакториальные болезни с полигенным наследственным компонентом.
- Синдромы, вызванные действием внешних факторов. Так, около 5 % МВПР обусловлено внутриутробными инфекциями и заболеваниями матери [534].
- Неклассифицированные комплексы МВПР (сочетание пороков, не выделенных в синдромы), которые представляют отдельную группу нехромосомных синдромов.
Если при хромосомных синдромах для диагностики достаточно анализа кариотипа, то цитогенетические исследования при других формах МВПР лишь отвергают хромосомную природу данного комплекса пороков развития, но не позволяют точно установить диагноз. Что касается диагностики нехромосомных синдромов, то за последние десятилетия на биологических моделях лабораторных животных достигнут значительный прогресс в понимании структуры и функций генов, ответственных за изолированные пороки у человека [894]. Определенные надежды вселяют успехи в изучении на экспериментальных объектах семейств генов SOX, HOX, PAX, которые принимают участие в регуляции раннего эмбрионального развития у млекопитающих (см. главу 11).
Как известно, большинство врожденных пороков развития, в том числе и МВПР, являются следствием новых мутаций. Так, с мутациями de novo связано более 90 % случаев хромосомных синдромов и свыше 80 % синдромов с аутосомно-доминантным типом наследования [31]. При этом фенотипическая гетерогенность характерна для всех МВПР, независимо от их этиологической причины.
Следует иметь в виду, что в клинической генетике врачам приходится иметь дело с уже сформировавшимися пороками и синдромами, то есть с конечными фенотипическими эффектами геномных, хромосомных и генных мутаций. Естественно ожидать, что более полная информация о контроле процессов онтогенеза может быть получена при исследовании особенностей фенотипического проявления мутаций на более ранних стадиях развития человека, то есть еще до рождения.
Цитогенетические исследования в эмбриогенезе представляют большой интерес еще и потому, что многие хромосомные нарушения у человека, летальные на ранних стадиях, уже не встречаются в более поздние сроки и у новорожденных (см. главу 5). Предполагалось, что сравнительные цитогенетические и патоморфологические исследования позволят выяснить роль хромосомного дисбаланса не только в эмбриональной гибели, но и в формировании врожденных пороков развития, как совместимых, так и несовместимых с жизнью.
70-е годы ХХ века были ознаменованы крупномасштабными исследованиями спонтанных абортусов человека. Патоморфологическому описанию были подвергнуты тысячи эмбрионов и зародышевых оболочек, у которых были выявлены практически все типы геномных мутаций и многие структурные хромосомные аберрации. Так, было показано, что хромосомный дисбаланс приводит к различным по характеру и выраженности патологическим изменениям — бласто-, эмбрио- и фетопатиям, которые проявляются на клеточном, тканевом и органи- зменном уровнях [77, 91, 93]. Эти исследования сыграли важную роль в понимании специфичности и неспецифичности пороков развития, в формировании представлений о клеточном синдроме как патоморфологической основе хромосомных болезней [46, 47, 93, 96].
Вместе с тем, уже первые исследования спонтанных абортов обнаружили безусловную ограниченность такого подхода, связанную с особенностями исследуемого материала. Главная трудность заключалась в дифференциации первичных нарушений морфогенеза от вторичных, посмертных изменений. Между тем такая дифференциация имеет принципиальное значение при определении стадии, на которой прекратилось развитие, и тех изменений, которые привели к этой остановке [47]. Аутолиз тканей абортусов создает также определенные трудности при культивировании клеток, полученных из абортивного материала [93]. Успешное кариотипирование обычными методами возможно только у 46 % спонтанных абортусов. Установить кариотип у остальных можно только на интерфазных клетках с использованием молекулярно-цитогенетических методов анализа [100]. Естественно, что по своей точности «интерфазная» цитогенетика значительно уступает стандартному метафазному анализу.
Реальные возможности прижизненного изучения эмбрионов человека с хромосомными аберрациями появились только с разработкой методов исследования плода с помощью ультразвукового сканирования в сочетании с их кариотипированием на образцах материала, полученных на разных стадиях внутриутробного развития.
За последнее десятилетие ультразвуковые исследования стали неотъемлемой частью обследования плода. Ультразвуковая диагностика применяется как в качестве рутинного клинического метода определения сроков беременности и жизнеспособности плода, так и для выявления различных аномалий развития. Следует отметить, что изначально УЗИ с целью выявления пороков развития у плода применяли, главным образом, во II триместре беременности [879].
В настоящее время разрешающая способность ультразвуковых приборов и большой опыт многих тысяч УЗ-исследований позволяет подробно анализировать фенотипические особенности плода и в I триместре беременности [152, 178].
Такие исследования очень быстро привели к формированию представлений об ультразвуковых маркерах хромосомных болезней (sonogram indicators). Термин УЗ-маркеры используется для обозначения отклонений биометрических параметров и анатомических структур, позволяющих предполагать наличие хромосомной болезни у плода [749]. Изначально к таким ультразвуковым маркерам (УЗМ) относили синдром ВЗРП, некоторые аномалии скелета и лицевого черепа. По мере накопления знаний и совершенствования техники число УЗМ, рекомендуемых для скрининговых УЗИ, постоянно пополняется. При этом прогностическая значимость для диагностики хромосомной патологии у плода каждого из УЗМ различна и зависит от срока беременности. Однако, если спектр выявляемых аномалий во втором триместре достаточно велик, то основными УЗМ хромосомных болезней у плода с 10-й по 14-ю недели беременности являются толщина воротникового пространства (ТВП) и состояние оссификации носовых костей, толщина и число сосудов пуповины, размеры нижней челюсти. Увеличение ТВП является ультразвуковым маркером не только хромосомных болезней, но и таких достаточно частых аномалий как пороки сердца и магистральных сосудов, лимфатической и мочевыделительной систем и некоторых других [133, 152].
Дальнейшее совершенствование УЗ-техники (цветное сканирование, допплерометрия, трехмерное изображение и пр.) значительно увеличивает возможности детального прижизненного анализа анатомии плода практически на любой стадии развития и даже позволяет получить ценную информацию о состоянии и функциях некоторых органов и систем плода в развитии. Не случайно на сегодняшний день именно ультразвуковое исследование является наиболее эффективным методом изучения фенотипа плода в норме и при патологии.
Вполне закономерна, хотя реально весьма уязвима, наметившаяся в последние годы тенденция постановки диагноза конкретного наследственного синдрома исключительно по результатам УЗИ [40, 152, 178]. Действительно, некоторые пороки развития органов и систем и/или транзиторные состояния, не соответствующие сроку развития, чаще встречаются у плодов с определенными хромосомными болезнями. Однако строгой специфичности УЗМ по отношению к хромосомной патологии у плода вообще и, тем более, патогномоничных для определенных хромосомных синдромов не выявлено. Синдромологический подход в УЗ-диагностике, равно как и в клинической генетике и патологической анатомии, позволяет зарегистрировать аномалию развития, в первую очередь — изолированные и множественные пороки, и с той или иной вероятностью заподозрить наличие хромосомной патологии. Очевидно, что постановка диагноза хромосомной патологии у плода реально возможна только путем его кариотипирования. Кроме того, следует учитывать, что у многих плодов с хромосомным дисбалансом пороки развития отсутствуют, а фенотипические признаки столь невыразительны, что вполне могут оказаться не зарегистрированными в качестве УЗМ. Наконец, разграничение эхографических признаков на ВПР и УЗМ хромосомных болезней, учитывая транзиторный характер не только многих УЗМ, но и некоторых пороков развития, коррекция которых осуществляется за счет компенсаторных механизмов в процессе дальнейшего внутриутробного развития, также неубедительно. На наш взгляд, термин УЗМ хромосомных болезней может быть использован применительно к любым отклонениям в развитии, в том числе и порокам, независимо от степени их тяжести. Исключениями из этого правила являются лишь некоторые, в основном, изолированные пороки развития (например, анэнцефалия или дефекты заращения нервной трубки), при которых хромосомные нарушения у плода являются случайными находками. Это утверждение отнюдь не противоречит факту существования пороков развития, включая МВПР, хромосомной и генной этиологии. Анализ мутаций в генах-регуляторах эмбрионального развития, роль которых в возникновении ВПР доказана на модельных объектах, обсуждается в качестве перспективного направления профилактики врожденной и наследственной патологии (см. главы 9 и 11). Следовательно, кариотипирование является способом дифференциальной диагностики хромосомных и нехромосомных ВПР.
Таким образом, существующие представления об аномалиях эмбрионального развития плодов с хромосомным дисбалансом основаны на информации, полученной преимущественно при изучении спонтанных абортусов или новорожденных с МВПР Инвазивные методы позволяют провести пренатальное кариотипирование практически на любом сроке беременности (см. главу 9). При помощи УЗ-сканирования, ставшего неотъемлемой частью комплексных исследований состояния плода человека в рамках пренатальной диагностики, могут быть получены сведения об анатомических и функциональных особенностях развивающегося плода. Прижизненные особенности развития, дополненные патоморфологическими исследованиями абортного материала, который не подвергся аутолизу, помогают воссоздать картину фенотипического проявления хромосомного дисбаланса на разных сроках развития. Между тем, данные УЗ- и патоморфологического исследований, как правило, разрозненны, нередко противоречивы. Учитывая эти обстоятельства, очевидно, что полная информация может быть получена при тесном союзе специалистов по клинической генетике, ультразвуковой диагностике, патологической анатомии и физиологии. Возможно, такой альянс окажется продуктивным для решения целого ряда актуальных задач генетики развития. Так, до сих пор дискуссионным остается патогенез многих ВПР, не изучена динамика их формирования. Неясными остаются генез сочетанных пороков при возникновении достаточно устойчивых комплексов МВПР, их роль в реализации хромосомных эмбриолета- лей, в том числе крайне низкой жизнеспособности плодов с полным или мозаичным вариантом синдрома Шерешевского-Тернера и т. д.
Следует отметить, что такой комплексный анализ, включающий прижизненное фенотипирование плодов с хромосомными аномалиями, позволяет получить новую информацию, важную как для фундаментальной науки, так и для практической медицины. С одной стороны, выяснение взаимосвязи между дисбалансом отдельных хромосом или их сегментов и отклонениями в развитии плода способствует пониманию роли структурных и регуляторных генов в процессах раннего онтогенеза человека. С другой — выявление пороков или УЗМ у плода после кариотипирования позволяет оценить информативность изолированных и сочетанных УЗМ в качестве маркеров хромосомной патологии, что способствует повышению эффективности пренатальной диагностики.
Рассмотрение принципов патоморфологического анализа с целью точной диагностики ВПР выходит за рамки настоящей главы. Мы не касаемся также возможностей и эффективности ультразвуковой диагностики, подробно рассмотренных в специальной литературе [40, 133,152, 153, 178]. Отметим, однако, что не только срок беременности и уровень УЗ-обследования, но и квалификация врача УЗД существенно влияют на частоту и характер выявленных фенотипических признаков (маркеров), а знание эмбриологии человека и основ медицинской генетики — на своевременность и эффективность инвазивной пренатальной диагностики хромосомных болезней, более детально рассмотренной в главе 9.
Источник
