Мутация в 4 хромосоме синдром

Каждая беременная женщина должна проходить обследования. Это помогает уберечь здоровье матери и предотвратить развитие отклонений у ребенка. Однако существуют такие заболевания, которые невозможно предугадать и впоследствии вылечить. Речь пойдет о наследственных патологиях плода, которые помогут выявить маркеры хромосомной патологии.

Маркеры хромосомной патологии плода
Маркерами называют признаки различных наследственных заболеваний, которые можно выявить посредством анализов и тестов. Во время исследований врач должен оценить процесс развития разных частей тела плода, а также его внутренних органов. Пренатальный скрининг при беременности дает возможность выявить биохимические маркеры маркеры хромосомной патологии и ультразвуковые (эхографические). Скрининг включает анализ крови и УЗИ с замерами разных величин плода.
Обычно скрининг не проводят, хватает простого ультразвукового сканирования. Развернутое обследование возможно по желанию пациентки или при подозрении на хромосомные патологии плода.
В группе риска такие категории беременных:
- в чьем роду были наследственные заболевания;
- замерзшая беременность, выкидыш, мертворождение в анамнезе;
- возраст матери больше 35 лет, возраст отца больше 40;
- прием лекарств, которые могут навредить ребенку;
- инфекции или воспаления в первом триместре.
Скрининг проводят в I, II и III триместрах.
Хромосомные патологии
Понятия хромосомных и наследственных заболеваний, по сути, синонимы. Они обусловлены изменениями структуры разных генов или их количества. В генетике сотни хромосомных патологий, которые вызывают различные мутации и отклонения, но мало знаний об их причинах.
Совокупность хромосом, которые содержат гены, называют геномом. У здорового человека есть 23 пары хромосом, которые несут наследственную информацию: 22 пары аутосомных хромосом (парные неполовые) и пара половых хромосом.
Частой причиной развития хромосомных патологий являются мутации в половых клетках родителей. Если у матери и отца в роду имелись наследственные отклонения, стоит изучить вопрос о хромосомных патологиях и пройти расширенное обследование. Такая строгость мер обусловлена тем, что заболевания, вызываемые мутациями в хромосомах, зачастую развиваются в процессе роста плода в чреве матери.
Диагностика направлена на благо родителей и малыша. От степени повреждения генома будет зависеть комфорт его жизни и жизни родителей. Часто детям с хромосомными аномалиями сложно жить: возникают проблемы не только с контролем тела и поддержанием жизни (дыхание, питание и прочее), но также имеются трудности в восприятии и преобразовании информации.
При обнаружении маркеров сложных хромосомных аномалий медицина может предложить родителям только прерывание беременности. Как бы жестоко это ни было, но такая мера позволяет избежать страданий ребенка и его родителей. Однако не стоит оценивать ситуацию по первым результатам. Нередко врачи, изучающие эту сложную область, ошибаются.
Также стоит помнить, что все нормы усреднены. Приближение к максимально допустимым значениям одного показателя не может быть свидетельством патологии.

Причины мутаций хромосом
Побеспокоиться о здоровье своих детей нужно еще до зачатия, так как патологии хромосом начинаются в момент образования зиготы (слияние сперматозоида с яйцеклеткой). Проконтролировать этот процесс не представляется возможным, так как его специфика плохо изучена.
Для предотвращения наследственных заболеваний врачи настоятельно рекомендуют не пренебрегать этапом подготовки к беременности. Пара должна выявить текущее состояние своего здоровья, вместе с врачом проанализировать анамнез и всех ближайших родственников, оценить свои условия проживания. При плохих результатах врач обязательно расскажет о рисках. В таких случаях паре предлагают искусственное оплодотворение спермой донора (если существует риск передачи болезни по отцовской линии) или суррогатное материнства (при наследственных болезнях по женской линии или от рода матери).
Последние исследования подтверждают связь между генными мутациями и следующими факторами:
- родители старше 35 лет;
- факт патологий в роду;
- неблагоприятные рабочие условия или условия проживания.
Эти факторы повышают риск возникновения хромосомной аномалии. Если пара подтверждает все из них, врачи не рекомендуют зачатие. Когда беременность уже наступила, медицина способна только выяснить степень поражения, определить шансы на выживание и уровень жизни ребенка.
Какие бывают маркеры
Стоит помнить, что все существующие маркеры хромосомных патологий считаются условными. Наука еще не изучила возникновение и развитие отклонений в достаточной мере.
Основные маркеры
- боли тянущего характера внизу живота, которые могут указывать на выкидыш;
- отсутствие активности плода;
- гипоксия (нехватка кислорода);
- маловодие и многоводие;
- деформации лица;
- размеры носовых костей;
- увеличение шейной складки (маркер называют толщиной воротничкового пространства или сокращенно ТВП);
- замедление роста трубчатых костей;
- размер верхнечелюстной кости;
- размер мочевого пузыря;
- увеличение почечных лоханок;
- гидронефроз (расширение лоханок и чашечек почек, связанное с нарушениями в процессе оттока мочи);
- кисты в пуповине или мозге;
- отечность шеи и спины;
- ускоренное старение плаценты;
- гипоплазия (недоразвитость) плаценты;
- состояние кишечника (гиперэхогенность, при которой орган выглядит слишком ярким на УЗИ).

Маркеры крови
- пониженный уровень РАРР-А (протеин-А плазмы);
- пониженный уровень АФП (белок в организме плода);
- повышенный уровень ХГЧ (гормон, вырабатываемый плацентой).
Также беспокойство врача могут вызвать плохие результаты допплерометрии и кардиотокографии. При обнаружении одного или двух маркеров не стоит паниковать. Наличие отклонений может быть связано с индивидуальными особенностями организма ребенка и не свидетельствовать о развитии серьезной патологии.
Выявление маркеров хромосомных патологий
Наиболее информативным считается первый скрининг или двойной тест. Его проводят на 12 неделе беременности. Это исследование включает УЗИ и анализ крови, которые при наличии покажут все маркеры, описанные выше. Хотя даже эти тесты не могут полностью подтвердить или опровергнуть хромосомную патологию плода.
Первый скрининг нужен для подсчета рисков. Врачи выбрали УЗИ и анализ крови по той причине, что это самые безопасные методы диагностики заболеваний у беременных женщин. Благодаря современному оборудованию ультразвуковые волны не влияют на малыша.
Дополнительные исследования
Для получения более точных результатов нужны инвазивные методы диагностики. Самыми предпочтительными считаются биопсия хориона (плаценты), анализ пуповинной крови или амниотической жидкости. Эти тесты дают до 98% достоверности в постановке диагноза, но есть 2% риска выкидыша.
Таблица индекса амниотической жидкости представлена ниже.
| Неделя беременности | Возможные отклонения | Средние показатели |
| 16 | 73-201 | 121 |
| 17 | 77-211 | 127 |
| 18 | 80-220 | 133 |
| 19 | 83-225 | 137 |
| 20 | 86-230 | 141 |
| 21 | 88-233 | 143 |
| 22 | 89-235 | 145 |
| 23 | 90-237 | 146 |
| 24 | 90-238 | 147 |
| 25 | 89-235 | 147 |
| 26 | 89-242 | 147 |
| 27 | 85-245 | 147 |
| 28 | 86-249 | 146 |
| 29 | 84-254 | 145 |
| 30 | 82-258 | 145 |
| 31 | 79-263 | 144 |
| 32 | 77-269 | 144 |
| 33 | 74-274 | 143 |
| 34 | 72-278 | 142 |
| 35 | 70-279 | 140 |
| 36 | 68-279 | 138 |
| 37 | 66-275 | 135 |
| 38 | 65-269 | 132 |
| 39 | 64-255 | 127 |
| 40 | 63-240 | 123 |
Расшифровка маркеров
После первого скрининга анализируют все маркеры, которые были выявлены в ходе тестов. Их количество и степень вреда позволяют высчитать все риски.
| Количество маркеров | Риск хромосомной патологии |
| 1 | 2 % |
| 2 | 11 % |
| 3 | 32 % |
| 4 | 52 % |
| 5 | 66 % |
| 7 | 69 % |
| 8 и более | 92 % |
Первым тревожным звонком становится толщина воротникового пространства (ТВП).
| Размер воротникового пространства | Риск хромосомной патологии |
| 3 | 7 % |
| 4 | 27 % |
| 5 | 53 % |
| 6 | 49 % |
| 7 | 83 % |
| 8 | 70 % |
| 9 | 78 % |
Еще один важный маркер – длина носовых костей. Однако этот показатель изменяется с течением беременности.
| Неделя беременности | Длина носовых костей (мм) |
| 12-13 | меньше 2 |
| 14-15 | 3 |
| 16-17 | 3,6 |
| 18-19 | 5,2 |
| 20-21 | 5,7 |
| 22-23 | 6 |
| 24-25 | 6,9 |
| 26-27 | 7,5 |
| 28-29 | 8,4 |
| 30-31 | 8,7 |
| 32-33 | 8,9 |
| 34-35 | 9 |
Врач анализирует все маркеры, которые были обнаружены. Для подтверждения делают анализ крови.
Расшифровка маркеров крови
Уровень ХГЧ
Хорионический гонадотропин человека включает две субъединицы – альфа и бета. Уникальный свободный бета-ХГЧ является биохимическим маркером.
| Неделя беременности | Норма свободного бета-ХГЧ (нг/моль) |
| 10 | 25,8-181,6 |
| 11 | 17,4-130,4 |
| 12 | 13,4-128,5 |
| 13 | 14,2-114,7 |
| 14 | 8,9-79,4 |
Повышение уровня свободного бета-ХГЧ может свидетельствовать о таких явлениях:
- синдром Дауна (превышение нормы в два раза);
- многоплодие;
- сахарный диабет у беременной;
- гестоз (повышение давления, отечности, белок в моче);
- аномальное развитие плода;
- хориокарцинома (злокачественная опухоль, которая образуется из клеток плода);
- пузырный занос (развитие плода нарушается, ворсины хориона разрастаются в пузыри).
Низкий уровень свободного бета-ХГЧ иногда говорит о:
- синдроме Эдвардса, синдроме Патау;
- задержке развития;
- угрозе выкидыша;
- хронической плацентарной недостаточности.

Уровень PAPP
РАРР-А – протеин-А плазмы. Отклонения от нормы зачастую указывают на пороки развития. Считается, что после 14 недели анализ на РАРР-А более не информативен.
| Неделя беременности | РАРР (мЕд/мл) |
| 10-11 | 0,32-2,42 |
| 11-12 | 0,46-3,73 |
| 12-13 | 0,7-4,76 |
| 13-14 | 1,03-6,01 |
Понижение уровня РАРР-А может указывать на:
- многоплодие;
- низкое расположение плаценты;
- большие размеры плода или плаценты.
Понижение уровня РАРР-А характерно при:
- синдроме Дауна, синдроме Эдвардса, синдрома Патау, синдроме Корнелии де Ланге;
- выкидыше, гибели плода;
- преэклампции (тяжелая степень гестоза, когда артериальное давление повышается до критических отметок);
- фетоплацентарной недостаточности, гипотрофии плода (из-за нехватки питания снижается масса тела ребенка).
Обычно эти показатели изучают совместно. При снижении уровня РАРР-А и повышении ХГЧ есть риск возникновения синдрома Дауна, а при нехватке обоих – синдрома Патау или синдрома Эдвардса.
Уровень АФП
Альфа-фетопротеин – белок, который выделяется желточным мешком плода в начале беременности и печенью под конец. АФП также синтезируется в желтом теле яичников женщины до 5-й недели. Уровень белка разнится для отдельных периодов беременности.
Роль АФП заключается в транспортировке белков и жиров от матери ребенку, поддержании давления в сосудах плода, мешает гормонам матери повлиять на него. Также АФП играет важную роль в осуществлении иммуносупресии между матерью и ребенком (подавление выработки антител иммунитетом матери на неизвестный организм).
| Неделя беременности | Концентрация АФП (МЕ/мл) |
| 1-13 | 0,5-15 |
| 14-16 | 15-60 |
| 17-20 | 15-95 |
| 21-24 | 27-125 |
| 25-28 | 52-140 |
| 29-30 | 67-150 |
| 31-32 | 100-250 |
| 33-42 | показатель не информативен |
Уровень эстрадиола
Во втором триместре посредством анализа крови выявляют также уровни ингибина А, плацентарного лактогена и неконъюгированного эстрадиола. Подсчет результатов совершается компьютером.
| Результат | Вероятность хромосомных патологий |
| 1:100 | очень высокая |
| 1:1000 | норма, при заниженном показателе могут быть аномалии развития |
| 1:10000 | низкая |
При результате ниже 1:400 тест проводят второй раз. Если показатели выше, женщина может спокойно доносить малыша.

Расшифровка маркера по росту трубчатых костей
| Неделя беременности | Бедренная кость | Кость голени | Плечевая кость | Кости предплечья (локтевая и лучевая) |
| 11-12 | 3,4-4 | |||
| 13-14 | 7-9 | |||
| 15-16 | 13-17 | 15 | 15 | 12 |
| 17-18 | 20-23 | 17-20 | 17-20 | 15-17 |
| 19-20 | 26-29 | 23-26 | 23-26 | 20-22 |
| 21-22 | 32-26 | 29-31 | 29-31 | 24-26 |
| 23-24 | 37-40 | 34-36 | 34-36 | 29-31 |
| 25-26 | 42-45 | 37-41 | 39-41 | 33-35 |
| 27-28 | 47-49 | 43-45 | 43-45 | 37-39 |
| 29-30 | 50-52 | 47-49 | 47-49 | 40-42 |
| 31-32 | 54-56 | 50-51 | 51-52 | 44-45 |
| 33-34 | 58-60 | 53-33 | 54-55 | 46-48 |
| 35-36 | 62-64 | 56-57 | 57-58 | 49-50 |
| 37-38 | 66-68 | 59-60 | 59-60 | 51-52 |
| 39-40 | 69-70 | 61-62 | 60-61 | 53-54 |
Показатели зрелости плаценты
| Неделя беременности | Степень зрелости |
| до 30 | |
| 30-34 | 1 |
| 35-39 | 2 |
| после 39 | 3 |
Прогноз
Еще во время обследования родители должны принять тот факт, кто вылечить ребенка с хромосомными отклонениями невозможно. Если маркеры будут обнаружены, это поможет не впасть в ступор от шока.
К сожалению, на данном этапе развития медицины врачи могут предложить паре только искусственное прерывание беременности. Это не выход, но мера поможет избежать многих проблем и горестей, если имеется серьезная патология, которая несет угрозу для здоровья и жизни ребенка. Врач должен оценить шансы на выкидыш и мертворождение прежде, чем советовать родителям аборт.
Перед принятием этого решения нужно трезво оценить такие факторы:
- какие неудобства патология будет причинять ребенку после рождения;
- будет ли ему больно;
- сможет ли малыш питаться, дышать, ходить, говорить, видеть или слышать;
- будет ли ребенок понимать хотя бы простые вещи, сможет ли он адекватно воспринимать информацию;
- сможет ли ребенок ухаживать за собой самостоятельно, когда вырастет;
- сколько проживет ребенок с возможной патологией;
- готовы ли мужчина и женщина стать родителями инвалида, зарабатывать больше денег, уделять много времени ребенку и терпеть трудности.
Несмотря на все эти факторы, в последнее время статистика абортов при наличии маркеров хромосомных отклонений снизилась. Это обусловлено тем, что люди перестали бояться возможности воспитывать больного ребенка. Появились эффективные методики обучения детей с отклонениями, способы общаться с ними и понимать их мировосприятие. Показательно и то, что все больше детей с подобными синдромами растут спокойными, общительными и добрыми. Некоторые из них не только заканчивают школы, но и получают образование в университете, снимаются в кино.
Возможные заболевания
Болезни, которые вызывают мутации хромосом, можно разделить на такие группы:
- патологии, возникающие по причине нарушения количества хромосом;
- аномалии из-за неправильной структуры хромосом.
Заболеваний много, поэтому они вызывают различные патологии, которые отличаются по степени сложности. Нарушения на генном уровне могут привести к внешним уродствам, навредить системам внутренних органов (вплоть до центральной нервной системы). Степень сложности зависит от того, какая именно мутация произошла с хромосомами: изменилось количество или структура.
Если говорить о патологиях, которые вызваны увеличение количества хромосом, тут различают анеуплоидию и полиплоидию. Первое обозначает увеличение на одну-две хромосомы в паре. Второе же указывает на кратное увеличение числа хромосом. Полиплоидия проводит к летальному исходу до рождения, в то время как при анеуплодии дети рождаются и часто могут нормально существовать.

Распространенные наследственные заболевания
Маркеры хромосомной патологии помогут выявить следующие заболевания, связанные с нарушением количества хромосом:
- Синдром Дауна (сразу три хромосомы в 21-й паре). Дети отличаются задержкой развития, слабоумием. Ребенка с синдромом Дауна можно узнать по плоскому лицу, косоглазию, выпученности глаз, постоянному открытию рта, коротким конечностям.
- Синдром Патау (третья хромосома в 13-й паре). Тяжелое заболевание, которые сопровождается множественными пороками: идиотия (самая глубокая степень умственной отсталости), нарушения внутренних органов, многопалость, глухота. Дети с синдромом Патау редко живут больше года.
- Синдром Эдвардса (трисомия 18-й пары). Зачастую синдром диагностируют у детей, чья мать забеременела в пожилом возрасте. Симптомы: узкие и короткие глаза, маленькая нижняя челюсть, небольшой рот, деформация ушей. Большинство детей погибают в возрасте до трех месяцев из-за порока сердца или остановки дыхания. Некоторые доживают до года, и еще меньше детей живут дольше.
- Трисомия 9-й пары. Симптомы: высокий лоб, глубокая посадка глаз, деформация ушных раковин, широкая переносица, нёбо с расщелиной, короткая шея. Также возможны патологии опорно-двигательного аппарата, дисплазия тазобедренных суставов, деформация ребер, вывихи локтевых и коленных суставов. При трисомии 9-й пары хромосом диагностируют заболевания сердца и сосудов, почек, ЖКТ. Большинство детей погибают до четырех месяцев. Главной опасностью выступают респираторные инфекции.
- Трисомия 14-й пары. У детей наблюдается асимметрия лица, полные губы, короткий нос, высокий лоб, низко посаженные ушные раковины, небольшие мочки, короткая шея, деформация грудной клетки, маленький пенис у мальчиков. Патология опасна развитием пороков сердечно-сосудистой системы, почек, легких и кожи. Чаще всего дети умирают рано, однако есть случаи выживания до 10-13 лет.
- Полисомия Х- или Y-хромосом. Возможно снижение интеллектуальных способностей, шизофрения, психозы. Полисомия Х-хромосомы вызывает деформацию скелета и половых органов, умственную отсталость. Реже патология не приводит к физическим и психическим отклонениям, но влияет на интеллект. Для полисомии Y-хромосомы характерны такие проявления: чрезмерная агрессия, склонность к гомосексуализму, ассоциативность. Однако в большинстве случаев физические и умственные способности не нарушены.
Заболевания, связанные с аномальными структурами хромосом
- Синдром Шерешевского-Тернера (отсутствие или дефект половой хромосомы Х). Результатом нарушения в хромосоме становится неправильное развитие половых желез. Чаще болезнь возникает у девочек. Симптомы: половой инфантилизм, деформированные локтевые суставы, складки в области шеи. Пациенты с таким заболеванием нередко выживают и могут вести нормальный образ жизни, хотя роды проходят очень сложно. Беременность возможна с помощью ЭКО.
- Синдром Клайнфельтера (дефект Х-хромосомы у мальчиков). Большая часть детей с этим синдромом выживают после родов. Симптомы: бесплодие, иногда умственная отсталость, отсутствие волос на теле, половой инфантилизм.
- Синдром кошачьего крика (мутация в 5-й паре). Вызывает умственную отсталость (имбецильность). Плач ребенка становится похож на крик кошки. У больного может быть косоглазие, широкая переносица, деформированные уши, необычный разрез глаз. Нередко аномально развиваются почки, возможен крипторхизм. Срок жизни будет зависеть от тяжести осложнений.
- Синдром Вольфа-Хиршхорна (нарушения в 4-й паре). Симптомы: худоба, маленький рот, клювовидный нос, крупные уши, невыраженные мочки, расщелины губ. У больных нередко диагностируют поликистоз почек и пороки сердечно-сосудистой системы. Задержка психомоторного развития неизбежна.
- Синдром Альфи (аномалия 9-й пары). Пациент имеет короткую шею, маленький рот с увеличенной верхней губой, деформацию переносицы и сосков, короткие ногти, удлиненные пальцы. У девочек наблюдается гипоплазия половых губ, а у мальчиков гипоплазия внешних половых органов. Нередко развиваются патологии сердца и почек. Возможна имбецильность, иногда дебилизм. Больные выживают. По характеру спокойные и ласковые.
- Синдром Орбели (мутация 13-й пары). У больных детей выявляют болезни почек, кишечника, ануса. Внешние признаки таковы: широкая переносица, маленький подбородок, катаракта, деформация лица, скелетные аномалии. Пациенты резко отстают в развитии (идиотия или имбецильность). Сложные пороки приводят к смерти до года, но также есть больны старше 30-40 лет.
И это далеко не все патологии, которые могут появиться у ребенка. На сегодняшний день изучено более 300 синдромов хромосом. Наука все еще пытается выяснить причину и специфику развития хромосомных мутаций. Эти патологии составляют только 5% от общего числа выявляемых у плода в процессе его развития.
Какие гормональные препараты вы принимали для стимуляции овуляции?
Источник
Синдром фрагильной Х-хромосомы (ломкой Х-хромосомы, ФХС, FRAX-А, синдром Мартина-Белла) – клиника, диагностикаСиндром фрагильной Х-хромосомы (синдром ломкой Х-хромосомы) (ФХС, иногда упоминается в литературе как «FRAX-А» и синдром Мартина-Белла) представляет собой сочетание соматических и поведенческих характеристик, связанных с фрагильным участком (и локусом гена) длинного плеча Х-хромосомы в области Xq27.3, который обнаруживается только в культуре с умеренным дефицитом фолата. Данное заболевание является второй после синдрома Дауна причиной задержки умственного развития с коэффициентом IQ менее 50 и наиболее частой причиной семейных случаев умственной отсталости и предпосылкой для развития различных поведенческих проблем, включая аутизм и синдром гиперактивности (Percy et al., 1990; Reiss и Freund, 1990; Hagerman и Hagerman, 2002). У многих пациентов отмечаются специфические нарушения речи, языковых навыков, поведения и социальных навыков. «Беспорядочная» речь является характерным признаком (Hanson et al., 1986). Типичны гиперактивность и дефицит внимания, а аутизм выявляется в 23% случаев (Bregman et al., 1987; Thake et al., 1987; Vieregge и Froster-Iskenius, 1989). Тем не менее, поведенческий фенотип отличается от проявлений аутизма, вызванного другими причинами, а гиперактивность может быть особенно ярко выражена (Baumgardner et al., 1995; Hagerman et al., 2005). Женщины, являющиеся носителями полной мутации одной из Х-хромосом, обычно имеют нормальный фенотип. Приблизительно в 35% случаев отмечается задержка умственного развития, обычно легкая, а у 15% пациенток отмечается пограничный уровень интеллекта, сложности в обучении или и то и другое (Kemper et al., 1986). Таким образом, ФХС является важной причиной легкой задержки умственного развития у женщин. Кроме того, приблизительно у 10% женщин с нормальным интеллектом, являющихся носительницами патологической хромосомы, могут отмечаться психиатрические заболевания, в особенности аффективное или шизоидное расстройство (Reiss и Freund, 1990). а) Патогенез. Синдром вызван увеличением «нормального» количества дупликаций тринуклеотида ЦГГ на участке Xq27.3 гена FMR1, кодирующего белок FMRR Имеются сообщения о развитии премутации при наличии более 55 повторов (51-54 повтора—пограничное число), а полная мутация отмечается, когда количество повторов превышает 200. Передача синдрома от мужчин без симптомов заболевания предполагает наличие премутаций, связанных с повтором 55-200 копий. Премутация имеет тенденцию к стабильности в процессе сперматогенеза, но часто превращается в полную мутацию в процессе овогенеза; таким образом, дочери мужчин-носителей всегда являются носительницами только премутации, в то время как у детей женщин-носительниц часто развивается клинически выраженная форма заболевания. У мужчин с полной мутацией практически всегда отмечается задержка умственного развития, в то время как у женщин это осложнение встречается лишь в 30-50% случаев и по сравнению с мужчинами менее выражено (Staley et al., 1993). Выявление фрагильного участка возможно только в 30-50% случаев. Присутствие полной мутации препятствует трансляции гена в белок (в результате метилирования) (Knight et al., 1993). Отсутствие гена FMRP в редких случаях регистрируется у пациентов без увеличения количества тринуклеотидов, а с множественными делециями или точечными мутациями гена FMR1 (Hirst et al., 1995). Зарегистрированы редкие случаи, когда у мужчин с полной мутацией сохранялись нормальные когнитивные способности (Smeets et al., 1995). Ген FMRP экспрессирован во многих тканях, с особым изобилием в нейронах. Его содержание у лиц с премутациями остается нормальным (Devys et al., 1993). Функции гена FMRP до сих пор до конца не изучены. Полная мутация гена может стать причиной аутизма, неспособности к обучению, тревожных расстройств и задержки умственного развития. Имеются данные о том, что аутизм также встречается у молодых мужчин, являющихся носителями премутантных аллелей. В ходе одного из недавних исследований было продемонстрировано, что приблизительно у 30% пациентов с ФХС отмечается аутизм; среди пациентов с аутизмом (по сравнению с пациентами только с ФХС) выявляются более низкие когнитивные способности, более выраженные проблемы с речью и отклонения поведения. Другие отклонения, связанные с премутантными формами гена, включают «синдром тремора-атаксии» (ФХТАС) среди пожилых мужчин и в редких случаях у женщин и преждевременную недостаточность яичников (Hagerman et al., 2005). У пациентов с синдромом фрагильной Х-хромосомы (ФХС) отмечается нарушение регуляции путей, связанных с метаботрофным рецептором глутамата-5; считается, что данное нарушение метаболизма обусловливает характерный фенотип.
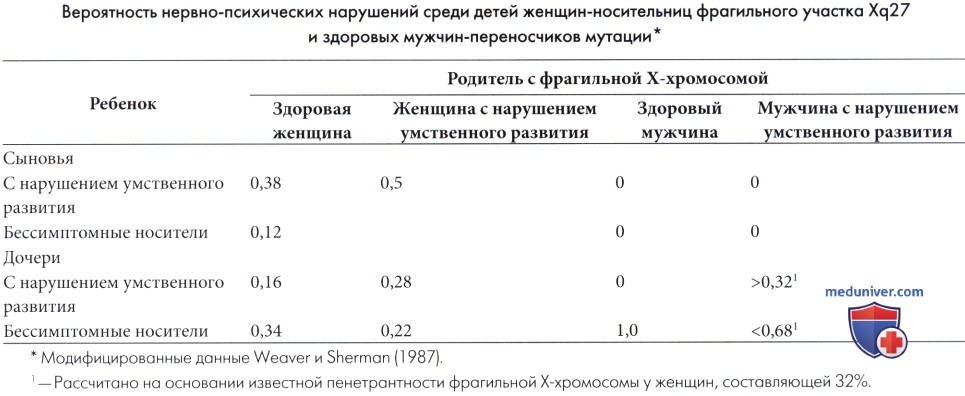
б) Распространенность. Синдром фрагильной Х-хромосомы (ФХС) (полная мутация ДНК) встречается с частотой приблизительно 1:4000 (среди мужчин) и 1:8000 (среди женщин), но учитывая, что исследования ДНК населения в целом не проводились, невозможно сделать вывод о достоверности данных сведений (Hagerman и Hagerman, 2002). Носительство премутаций отмечается с частотой 1:750-1000 мужчин и 1:250-350 женщин. С учетом того, что не у всех носителей фрагильной Х-хромосомы уровень IQ ниже 70, и они (не всегда) могут иметь лишь незначительные проблемы с учебой без гендерных различий, истинная распространенность ФХС (полной мутации и премутации с клинически значимыми отклонениями), вероятно, выше. У большинства мужчин с полной мутацией отмечаются отклонения от умеренной до тяжелой степени выраженности, в то время как у женщин проявления заболевания имеют менее выраженный характер, тем не менее, около трети пациенток имеют коэффициент IQ менее 70. Распространенность ФХС среди детей с трудностями в обучении от умеренной до тяжелой степени выраженности и без специфических дисморфических проявлений варьирует от 2% до 10% (Slaney et al., 1995). в) Диагностика. Диагноз синдрома фрагильной Х-хромосомы (ФХС) можно предположить на основании фенотипа; диагноз легко установить в постпубертатном периоде у мальчиков и затруднительно в препубертатном периоде у мальчиков и у девочек-носительниц, без типичных соматических изменений. Крупные уши и макроорхизм, напротив, часто не связаны с фрагильной Х-хромосомой (Hagerman, 1987). Семейный анамнез задержки умственного развития показателен, но обнаруживается только в трети случаев (Simko et al., 1989). Исследования ДНК в настоящее время надежны и оправдывают затраты (Rousseau et al., 1991, 1994; Oostra et al., 1993; Wang et al., 1993; Hagerman и Hagerman, 2002a). Экспресс-метод реакции антител, позволяющий выявить ген FMRP в лимфоцитах, был предложен в качестве скрининга для выявления полной мутации (Willemsen et al., 1995). Пренатальная диагностика синдрома фрагильной Х-хромосомы (ФХС) возможна с использованием культуры амниотических клеток или клеток ворсин хориона и методом анализа ДНК. Тем не менее, возникают этические проблемы, так как только у некоторых носителей мутации (особенно среди женщин) в дальнейшем разовьется заболевание. В настоящее время рассчитана (Weaver и Sherman, 1987) вероятность задержки умственного развития у детей больных родителей, но точные рекомендации остаются затруднительными.
г) Клинические проявления. Заболевание легче выявить у подростков, чем у детей в препубертатном возрасте. Наиболее важными проявлениями являются отсутствие замедленного физического развития, типично связанного с многими причинами умственной отсталости и, в особенности, нормальная или увеличенная окружность головы, вытянутое лицо с выступающей челюстью и макроорхизм (Но et al„ 1989). Классические проявления в виде вытянутого узкого лица и выступающих ушей часто незаметны в препубертатном периоде, хотя иногда бывают ярко выражены у молодых мужчин с ФХС. У взрослых женщин с полной мутацией часто отмечаются такие же изменения лица, но многие из них выглядят более «нормально», по сравнению с мужчинами. Макроорхизм отмечается приблизительно у трети мальчиков с ФХС и более чем у 90% взрослых мужчин. Другие частые изменения включают повышенную подвижность суставов пальцев, два сустава на первом пальце руки, плоские стопы, мягкую кожу, мышечную гипотонию, шум или дополнительный тон сердца (часто связанный с пролапсом митрального клапана или расширением корня аорты), косоглазие и высокое небо различной степени выраженности. В детском возрасте чрезвычайно часто встречается рецидивирующий средний отит, особенно по сравнению со здоровыми сибсами и детьми в общей популяции. В препубертатном возрасте у детей выявляются только следующие признаки: большая голова, большие уши и высокое небо. Помочь в установлении диагноза может также обнаружение повышенной гибкости суставов и мягкие уши. Несмотря на отсутствие макроорхизма у пациентов раннего возраста, в 15-50% случаев отмечается некоторое увеличение яичек (Simko et al., 1989). Типичные соматические проявления синдрома фрагильной Х-хромосомы (ФХС) представлены в таблице ниже. Задержка умственного развития при синдроме фрагильной Х-хромосомы (ФХС) обычно выражена слабо или умеренно, но с тенденцией к утяжелению в подростковом и взрослом возрасте (Borghgraef et al., 1987; Hagerman, 1987,1989; Wisniewski et al., 1989). У большинства мужчин по результатам стандартных тестов уровень IQ составляет менее 70 (чаще всего 35-40), но часть пациентов обладает нормальным или низко нормальным коэффициентом IQ. Вербальные навыки обычно превосходят способность к выполнению заданий и зрительно-пространственные навыки. Эпилепсия является достаточно частым проявлением и встречается в 15-25% случаев (Hagerman и Hagerman, 2002). Приступы часто имеют сложный парциальный характер, относительно доброкачественны и склонны к разрешению в подростковом возрасте, тем не менее, изредка отмечаются тяжелые и сложные случаи эпилепсии. Существует гипотеза о возможной связи припадков с аномалиями червя мозжечка, выявляемыми при ФХС. В подавляющем большинстве случаев у мужчин отмечаются явные признаки социальной дисфункции. Практически у всех мужчин присутствуют проявления аутизма, но лишь у немногих развивается полный синдром аутизма в сочетании с задержкой умственного развития или без нее. Фрагильная Х-хромосома наиболее распространена среди известных причин аутизма. Часто (приблизительно у половины мальчиков с полной мутацией) встречается гиперкинетический синдром в сочетании с аутизмом или без него, обычно с аутистическими проявлениями (Sullivan et al., 2006). Показатели когнитивных функций при ФХС отличаются от встречающихся при низкофункциональном аутизме, но достаточно часто соответствуют таковым при высокофункциональном аутизме и синдроме Аспергера. Некоторые авторы описывают сочетание синдрома Аспергера и синдрома фрагильной хромосомы (Hagerman, 1989). Некоторые варианты поведения, наиболее часто встречающиеся у пациентов мужского пола, включают избегание зрительного контакта, оборонительное поведение при прикосновении и социальную самоизоляцию (в возрасте от 0 до 2 лет); избегание зрительного контакта и приветственного поведения (отворачивание головы и тела при приветствии других людей), застенчивость, двигательные стереотипии различных видов и гиперактивность (в возрасте 3-4 лет); эхолалия, беспорядочная речь, «нервная непоседливость», хлопанье в ладоши, стереотипное махание вещами, кусание запястья или суставов пальцев, избегание зрительного контакта и приветственного поведения вместо стремления к социальной близости и заинтересованности в других людях (в возрасте 5-8 лет); сохраняющаяся застенчивость, избегание зрительного контакта и «нервозность», часто также привязанность к определенным вещам или людям на фоне общей картины умеренной задержки умственного развития с быстрой, беспорядочной речью с эхолалиями (очень часто отмечается разговор полушепотом, «нервный» смех) (в возрасте 9-12 лет); сохраняющиеся отклонения, часто усиливающиеся различными проблемами, связанными с началом пубертатного периода, включая трансвестизм, гипервозбудимость, самодеструктивное поведение и проблемы с одеждой (в связи с большим размером гениталий) (в возрасте 13-20 лет). В пубертатном периоде часто отмечается остановка когнитивного развития или даже ухудшение когнитивных функций. Сходная клиническая картина изредка отмечается у больных женщин, но в основном отклонения менее выраженные. У небольшого количества пациентов выявляется резко выраженный аутизм, а застенчивость и избегание зрительного контакта являются достаточно частыми проявлениями даже среди относительного большого числа боль? |