Нефритический синдром при остром гломерулонефрите
Нефритический синдром развивается при диффузных воспалительных изменениях в клубочках, характерных для первичного и вторичного гломерулонефрита, при остром неинфекционном тубулоинтерстициальном нефрите. Данный синдром может протекать в острой или хронической форме.
Острый нефритический синдром (острый гломерулонефрит)
Острый нефритический синдром, называемый также острым гломерулонефритом – это проявление острого воспаления клубочков, которое развивается быстро (в течение нескольких суток). Заболеваемость взрослых – 1–2 случая на 1000 случаев хронического гломерулонефрита. Чаще острый гломерулонефрит развивается у детей 3–7 лет и у взрослых 20–40 лет.
Этиология и патогенез
Основным этиологическим фактором заболевания является нарушение гуморального иммунитета после перенесенной стрептококковой инфекции (ангина, скарлатина, пневмония), вакцинации, введения лекарственных средств; при системной красной волчанке, инфекционном эндокардите, геморрагическом васкулите.
В крови появляются нефритогенные аутоантитела, причиной образования которых могут быть, во-первых, попадающие в организм антигены, похожие на собственные антигены почек, во-вторых, появление аутоантигенов на поверхности мезангиальных клеток при экспрессии молекул НLA класса II поступающими антигенами и, в-третьих, поликлональная активация антигенами В-лимфоцитов, вырабатывающих нефритогенные аутоантитела.
Острый гломерулонефрит начинается с:
- отложения иммунных комплексов в клубочке, механизм этого процесса может быть обусловлен соединением циркулирующих аутоантител с нормальными антигенами клубочков;
- осаждения циркулирующих антигенов в клубочке, где с ними связываются циркулирующие антитела (местное образование иммунных комплексов);
- осаждения в клубочке циркулирующих иммунных комплексов.
В результате развивается иммунное воспаление клубочков, которое характеризуется поступлением лейкоцитов и тромбоцитов в клубочек. Возможно отложение иммунных комплексов и развитие воспаления на внутренней стороне базальной мембраны (субэндотелиально) и в мезангии, но и на ее наружной стороне или внутри ее. Одновременно активируется комплемент и образуются мощные факторы хемотаксиса лейкоцитов, сопровождающиеся выбросом медиаторов воспаления. При аутоиммунном воспалении невозможен фагоцитоз, и высокотоксические вещества (свободные радикалы, протеолитические и другие ферменты) лейкоцитов поступают непосредственно в ткани, разрушая клетки и межклеточное вещество.
Для острого гломерулонефрита характерно увеличение глии в клубочке. Вначале выявляют лейкоциты воспалительного инфильтрата, позже размножаются собственные клетки клубочка – мезангиальные и эндотелиальные. Пролиферация клеток при остром гломерулонефрите прекращается через несколько недель или месяцев. Длительно существующие отложения иммунных комплексов в мезангии приводят к накоплению мезангиального матрикса, проникающего внутрь базальной мембраны, развитию склероза и хронической почечной недостаточности.
Чаще всего острый нефритический синдром развивается после стрептококковой инфекции (ангины, скарлатины, пневмонии, дерматита, воспаления среднего уха). Но в культурах мочи и почечной ткани стрептококк не обнаруживается. Иммунологическое повреждение клубочков может быть при инфекционном эндокардите, висцеральных абсцессах, ветряной оспе, инфекционном гепатите (НВ S Аg – положительный) и других заболеваниях.
Болезни, приводящие к развитию острого нефритического синдрома (Брэйди Х., Омира И., Бреннер Б., 2002) | |
| Иммунокомплексные поражения | Идиопатический Пролиферативный гломерулонефрит Экстракапиллярный гломерулонефрит Мезангиопролиферативный гломерулонефрит |
| Постинфекционный гломерулонефрит, включая инфекционный эндокардит и инфицированные шунты | Волчаночный эндокардит Криоглобулинемия IgA-нефропатия Геморрагичексий васкулит Фибриллярный гломерулонефрит Абсцессы внутренних органов |
| Антительный гломерулонефрит | Синдром Гудпасчера |
| Иммунонегативный гломерулонефрит | Гранулематоз Вегенера Идиопатический экстракапиллярный гломерулонефрит Микроангиит |
| Прочие | Злокачественная гипертония Гемолитико-уремический синдром Тромботическая тромбоцитарная пурпура Интерстициальный нефрит Почечный склеродермический криз Преэклампсия Атероэмболия |
Симптомы
Клиническая картина характеризуется бурным началом, появляются отеки, олигурия, макрогематурия (моча в виде “мясных помоев”). При значительной задержке жидкости увеличивается масса тела, развивается гиперволемия и артериальная гипертензия, сопровождающаяся головной болью и расстройством зрения. Гиперволемия и артериальная гипертензия могут привести к левожелудочковой недостаточности с одышкой, переходящей в сердечную астму и отек легких. Но почти у половины больных субъективных симптомов нет.
Почечный кровоток и СКФ снижаются, усиливается канальцевая реабсорбция натрия и воды. В мочевом осадке содержатся измененные эритроциты, эритроцитарные цилиндры и лейкоциты. Протеинурия имеет различную степень выраженности. У некоторых больных развивается острая почечная недостаточность с анурией, азотемией, гиперкалиемией, преходящей слепотой. Иногда течение заболевания осложняется гипертензивной энцефалопатией с тяжелым судорожным синдромом.
В крови нарастает титр антител к стрептококковым антигенам – антистрептолизина-О, антистрептокиназы, антигиалуронидазы и антидезоксирибонуклеазы В. Уровни комплемента в сыворотке (С3, С4, СН50) снижаются, иммунные комплексы выявляются только в течение первых двух-трех недель. Криоглобулинемия стойко удерживается в течение нескольких месяцев.
Лечение
Специфического лечения нет. Кортикостероиды и иммунодепрессанты неэффективны. При наличии очага инфекции назначают антимикробную терапию. Но при длительной значительной протеинурии более 1 месяца назначают преднизолон в дозе 1 мг/кг/сут, при развитии нефротического синдрома преднизолон применяют в сочетании с гепарином.
При гломерулонефритах, опосредованных иммунными комплексами и антителами против гломерулярной базальной мембраны (антиГБМ), назначают внутривенно больным до 200 мг преднизолона или проводят плазмаферез с одновременным назначением поддерживающих доз преднизолона и циклофосфамида по 1 мг/кг/сут или хлорамбуцила по 6–8 мг/кг/сут.
При сердечной недостаточности, отеках или тяжелой гипертензии ограничивают потребление натрия и назначают тиазидовые петлевые диуретики. При стойкой артериальной гипертензии проводят лечение нитропруссидом натрия, лабетололом, диазоксидом, гидралазином и триметафеном. При азотемии и метаболическом ацидозе ограничивают белок в пищевом рационе. При развитии тяжелой почечной недостаточности необходимо проведение диализа.
Прогноз
Острый нефритический синдром у большинства больных имеет хороший прогноз. Пролиферация почечных клеток исчезает в течение нескольких недель, однако воспалительная реакция варьирует и сравнительно часто развивается остаточный склероз. Протеинурия и гематурия могут сохраняться годами.
Хронический нефритический синдром (хронический гломерулонефрит)
Хронический нефритический синдром, называемый также хроническим гломерулонефритом – медленнопрогрессирующий синдром, развивающийся при различных почечных заболеваниях, приводящих к диффузному склерозу клубочков и утрате функции почек. У 80–90% больных данный синдром имеет бессимптомное начало и выявляется обычно случайно при анализе мочи. Частота синдрома составляет 0,5–1,0%. В анамнезе острый нефритический синдром бывает у 10–15%. Заболевают чаще мужчины в возрасте 35–40 лет.
Этиология и патогенез
Этиология хронического нефритического синдрома различна. Существует мнение о значении β-гемолитического стрептококка как этиологического фактора. Но серологические исследования на стрептококковую инфекцию неубедительны.
Высказывают предположения о роли НВs-антигена и паразитарных инфекциях (малярии, филяритоза) в этиологии данного синдрома и связанных с ними иммуновоспалительных реакций. Возможным подтверждением этого является обнаружение иммуноглобулинов и комплемента в клубочках, канальцах и интерстиции.
Существует мнение о токсической этиологии (лекарственные средства и промышленные производственные факторы). Но убедительных доказательств токсической этиологии нет. При гистологическом исследовании в почках обнаруживают фибринопептиды, образующиеся при активации системы свертывания, в моче, крови и иногда в почечной паренхиме. Но является их наличие причиной повреждения или следствием, неизвестно.
По данным гистологических исследований, хронический нефритический синдром развивается у 30% больных с очаговым и сегментарным склерозом, у 25% – с диффузным мезангиальным пролиферативным гломерулонефритом, у 15% – с диффузным эндокапиллярным гломерулонефритом, у 4% – с диффузным серповидным гломерулонефритом.
В клубочках происходит увеличение внеклеточного мезангиального матрикса и спадение капиллярных петель без выраженного отложения иммуноглобулинов, сопровождающееся склерозом клубочков. Одновременно вовлекается интерстиций, и возможна атрофия канальцев. Прогрессирование гломерулонефрита может быть обусловлено протеинурией и токсическим действием макромолекул плазмы крови на эпителий канальцев. Развиваются диффузный, тяжелый гломерулярный склероз и поражения интерстиция, несоизмеримые со степенью гломерулярных изменений.
Симптомы
Начало заболевания обычно установить не удается, так как у большинства больных отсутствуют субъективные симптомы, а почечная функция нормальная. Диагностируется хронический нефрит при обнаружении в моче небольшого количества белка и эритроцитов. Нередко заболевание впервые диагностируется при выявлении уремических симптомов (утомляемости, кожного зуда, одышки, тошноты и рвоты), характеризующих конечную стадию болезни.
У некоторых больных заболевание рецидивирует и протекает с выраженной протеинурией (более 3,5 г/сут), олигурией и отеками различной степени выраженности (нефротическая форма гломерулонефрита по Е.М. Тарееву) или эпизодами микрогематурии (до 20–30 эритроцитов в поле зрения) и реже – макрогематурией (гематурическая форма гломерулонефрита).
Часто бывает гипертензия любой тяжести с гипертрофией левого желудочка, изменениями глазного дна, сердечной недостаточностью и минимальными изменениями в моче. При гипертензивной форме сравнительно рано развивается почечная недостаточность.
Диагностика
В моче постоянно обнаруживаются протеинурия, гематурия и эритроцитарные цилиндры. В мочевом осадке содержатся в небольших количествах мелко- и крупнозернистые и гиалиновые цилиндры. Восковидные цилиндры появляются только при сморщивании почек и атрофии канальцев.
При прогрессировании синдрома в крови повышается уровень азота мочевины и в сыворотке – уровень креатинина, выявляются метаболический ацидоз, анемия и другие биохимические показатели хронической почечной недостаточности. Клинические и лабораторные проявления почечных заболеваний, приведших к развитию хронического нефритического синдрома, бывают идентичными.
Достоверным методом дифференциального диагноза на ранних стадиях является только биопсия почки. При выраженной хронической почечной недостаточности, обусловленной сморщиванием почки, биопсия не показана, так как гистологическое исследование не дает информации о начале заболевания.
Лечение
Этиологический метод лечения у большинства больных осуществить невозможно. Используют методы патогенетической и симптоматической терапии.
Рекомендуется применение глюкокортикоидов, способных тормозить образование антител и иммунных комплексов и стабилизировать клеточные мембраны. Назначают преднизолон в дозе 1 мг/кг массы тела больного ежедневно в течение 1 мес с постепенным медленным снижением дозы. Но убедительных доказательств эффективности глюкокортикоидной терапии не существует. Поддерживающая терапия проводится в течение 3–4 мес.
Глюкокортикоиды противопоказаны при высокой артериальной гипертензии и ХПН даже начальной стадии. Известно, что одинаковые курсы лечения преднизолоном у разных больных дают противоположные результаты. Кроме того, глюкокортикоиды вызывают побочные эффекты, ухудшающие прогноз заболевания.
Для подавления клеточного и гуморального иммунитета используют цитостатики: азатиоприн (имуран) – 1,5–3 мг/кг/сут, циклофосфамид (циклофосфан) – 2–3 мг/кг/ сут, хлорамбуцил (лейкеран) – 6–8 мг/сут длительно (8–12 месяцев и более). С цитостатиками назначают небольшие дозы преднизолона. Но и эта терапия не предупреждает рецидивирование заболевания.
В общий курс лечения включают с учетом показаний, противопоказаний и побочных эффектов антикоагулянты (гепарины) и антитромбоцитарные препараты (аспирин, клопидогрел), нестероидные противовоспалительные средства (индометацин, ибупрофен), препараты 4-аминохинолинового ряда (делагил и плаквинил). При этом лечении необходимо регулярно контролировать показатели гомеостаза, уровень креатинина и калия в крови, величины КФ, АД и диуреза. При выраженной активности хронического нефритического синдрома возможно назначение плазмафереза.
Методы лечения уремии описаны в другой статье.
Источник
Острый гломерулонефрит – это заболевание иммуновоспалительного характера, характеризующееся вовлечением структурных единиц почек – нефронов и преимущественным поражением клубочкового аппарата. Патология протекает с развитием экстраренальных синдромов (отечного и гипертонического) и ренальных проявлений (мочевого синдрома). В диагностике применяется исследование мочи (общий анализ, проба Реберга, Зимницкого, Нечипоренко), УЗИ почек, биохимическое и иммунологическое исследование крови, биопсия почечной ткани. Лечение требует соблюдения постельного режима и диеты, назначения стероидных гормонов, гипотензивных, диуретических средств.
Общие сведения
Острый гломерулонефрит развивается преимущественно у детей в возрасте 2-12 лет и взрослых до 40 лет. Мужчины заболевают в 15,2 раза чаще, чем женщины. Пик заболеваемости приходится на влажное и холодное время года. При болезни происходит преимущественное поражение клубочков (почечных телец), кроме этого в патологический процесс вовлекаются канальца и межуточная ткань обеих почек. Поражение почек связано со специфической иммунной реакцией, обусловленной инфекционным или аллергическим процессом.

Острый гломерулонефрит
Причины
В большинстве случаев развитие острого гломерулонефрита сопряжено с перенесенной стрептококковой инфекцией – фарингитом, ангиной, обострением тонзиллита, скарлатиной, рожистым воспалением кожи. Этиологическим агентом в этих случаях, как правило, выступает b-гемолитический стрептококк группы А. О стрептококковой этиологии острого гломерулонефрита свидетельствует определение повышенного титра антител к стрептококковой гиалуронидазе и стрептолизину-О, увеличение ЦИК, содержащих антигены к стрептококку.
Иногда развитию болезни предшествует вирусная инфекция – грипп, эпидемический паротит, ветряная оспа, краснуха, инфекционный мононуклеоз, герпес, гепатит. Реже патология возникает после дифтерии, стафилококковых и пневмококковых пневмоний, малярии, бруцеллеза, инфекционного эндокардита, брюшного и сыпного тифа и других инфекций.
Кроме инфекционно-иммунных острых гломерулонефритов встречаются неинфекционно-иммунные формы заболевания, вызванные введением сывороток и вакцин, индивидуальной непереносимостью пыльцы растений, приемом нефротоксичных лекарственных препаратов, укусом насекомых или змей, алкогольной интоксикацией и др. причинами. Предрасполагающими факторами служат переохлаждение, анатомо-физиологическая незавершенность строения нефронов у детей.
Патогенез
Специалисты в сфере современной урологии придерживаются мнения, что острый гломерулонефрит – это иммунокомплексная патология. После инфекционного или аллергического воздействия происходит изменение реактивности организма, что проявляется образованием антител к чужеродным антигенам. Взаимодействуя с комплементом, иммунные комплексы откладываются на поверхностях базальных мембран капилляров клубочков. Изменяется структура капиллярных стенок, увеличивается проницаемость сосудов, создаются условия для тромбообразования.
Расстройство трофики почечной ткани ведет к тому, что в ишемической почке активизируется функция ренин-ангиотензин-альдостероновой системы, что приводит к спазму периферических сосудов и, как следствие, повышению АД. На этом фоне нарушаются процессы фильтрации и реабсорбции, происходит задержка Na и воды, в моче появляются патологические элементы.
Классификация
По вызывающим поражение причинам различают первичный, идиопатический и вторичный гломерулонефрит. Первичный гломерулонефрит связан с инфекционным, аллергическим или токсическим воздействием на почечную ткань; вторичный – служит проявлением системной патологии (геморрагического васкулита, СКВ и др.); идиопатический гломерулонефрит развивается по неопределенным причинам. В зависимости от этиофакторов гломерулонефриты могут быть инфекционно-иммунными и неинфекционно–иммунными.
В зависимости от объема поражения клубочкового аппарата различают очаговую (поражено <50% клубочков) и диффузную (поражено <50% клубочков) формы болезни. Существует несколько различных морфологических типов – пролиферативный эндокапиллярный, пролиферативный экстаракапилярный, мезангиопролиферативный, мембранозно-пролиферативный, склерозирующий.
По клиническому течению заболевание может развиваться в классической развернутой форме (с гипертензивным, отечным и мочевым синдромами), в бисиндромной форме (сочетание мочевого синдрома с отечным или гипертензивным) или моносиндромной форме (только с мочевым синдромом). В МКБ-10 для обозначения острого диффузного гломерулонефрита используется понятие «острый нефритический синдром».
Симптомы острого гломерулонефрита
Классическая картина включает триаду симптомокомплексов: почечный (ренальный) – мочевой синдром и внепочечные (экстраренальные) – отечный и гипертензивный синдромы. Патология обычно манифестирует спустя 1-2 недели после имевшего место этиологического воздействия (инфекции, аллергической реакции и т. д.).
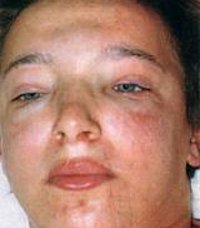
Появление отеков – наиболее ранний и частый признак острого гломерулонефрита, встречается у 70-90% пациентов, у половины из них отеки бывают значительными. Отеки располагаются преимущественно в области лица: наиболее выражены по утрам и спадают днем, сменяясь отечностью лодыжек и голеней. В дальнейшем отечный синдром может прогрессировать до анасарки, гидроперикарда, гидроторакса, асцита. В некоторых случаях видимые отеки могут отсутствовать, однако ежедневное увеличение массы тела пациента свидетельствует о задержке жидкости в тканях.
Артериальная гипертензия обычно выражена умеренно: у 60-70% пациентов АД не превышает 160/100 мм рт. ст. Однако стойкая длительная гипертензия имеет неблагоприятный прогноз. Для острого гломерулонефрита характерно сочетание артериальной гипертензии с брадикардией менее 60 уд. в мин., которая может держаться на протяжении 1-2 недель. При остро развивающейся гиповолемии возможны явления недостаточности левого желудочка, выражающейся сердечной астмой и отеком легких.
Нередко отмечается развитие церебральных нарушений, обусловленных отеком головного мозга – головной боли, тошноты и рвоты, снижения зрения, «пелены» перед глазами, понижения слуха, психо-моторной возбудимости. Крайним проявлением церебрального синдрома может стать развитие ангиоспастической энцефалопатии – эклампсии (тонико-клонических судорог, потери сознания, набухания шейных вен, цианоза шеи и лица, урежения пульса и т. д.).
Течение патологии может сопровождать болевой синдром различной степени выраженности: боли в пояснице чаще симметричны и обусловлены растяжением почечных капсул и нарушением уродинамики. Мочевой синдроме характеризуется ранним развитием олигурии и даже анурии в сочетании с сильной жаждой. При этом отмечается повышение относительной плотности мочи, появление в моче гиалиновых и зернистых цилиндров, эритроцитов, большого количества белка.
Эритроцитурия может протекать в виде микрогематурии (Er- 5 –50 – 100 в поле зрения) или макрогематурии, при которой моча становится цвета «мясных помоев». Протеинурия и гематурияе в большей степени выражены в первые сутки заболевания. Реже острый гломерулонефрит развивается по типу моносиндромной (мочевой) формы без отеков и при нормальном АД. На фоне болезни может формироваться нефротический синдром.
Диагностика
При диагностике острого гломерулонефрита учитывается наличие типичных клинических синдромов, изменений в моче, биохимическом и иммунологическом анализе крови, данные УЗИ и биопсии почки. Общий анализ мочи характеризуется протеинурией, гематурией, цилиндрурией. Для пробы Зимницкого типично уменьшение количества суточной мочи и повышение ее относительной плотности. Проба Реберга отражает снижение фильтрационной способности почек.
Изменения биохимических показателей крови могут включать гипопротеинемию, диспротеинемию (уменьшение альбуминов и увеличение концентрации глобулинов), появление СРБ, и сиаловых кислот, умеренную гиперхолестеринемию и гиперлипидемию, гиперазотемию. При исследовании коагулограммы определяются сдвиги в свертывающей системе – гиперкоагуляционный синдром. Иммунологические анализы позволяют выявить нарастание титра АСЛ-О, антистрептокиназы, антигиалуронидазы, антидезоксирибонуклеазы В; повышение содержания IgG, IgM, реже IgА; гипокомплементемию СЗ и С4.
УЗИ почек обычно показывает неизмененные размеры органов, уменьшение эхогенности, снижение скорости клубочковой фильтрации. Показаниями к проведению биопсии почки служат необходимость дифференциации острого и хронического гломерулонефрита, быстропрогрессирующее течение заболевания. При острой форме болезни в нефробиоптате определяются признаки клеточной пролиферации, инфильтрация клубочков моноцитами и нейтрофилами, наличие плотных депозитов иммунных комплексов и др. При гипертензивном синдроме необходимо проведение исследования глазного дна и ЭКГ.
Лечение острого гломерулонефрита
Терапия проводится в урологическом стационаре и требует назначения строгого постельного режима, бессолевого диетического питания с ограничением потребления животных белков, жидкости, назначением «сахарных» и разгрузочных дней. Производится строгий учет количества потребляемой жидкости и объема диуреза. Основная терапия заключается в применении стероидных гормонов – преднизолона, дексаметазона курсом до 5-6 недель.
При выраженных отеках и артериальной гипертензии одновременно назначаются диуретические и гипотензивные средства. Антибиотикотерапия проводится при имеющихся признаках инфекции (тонзиллите, пневмонии, эндокардите и др.). При острой почечной недостаточности может потребоваться назначение антикоагулянтов, проведение гемодиализа. Курс стационарного лечения составляет 1-1,5 месяца, после чего пациента выписывают под наблюдение врача-нефролога.
Прогноз и профилактика
В большинстве случаев патология хорошо поддается терапии кортикостероидными гормонами и заканчивается выздоровлением. В 1/3 случаев возможен переход в хроническую форму; смертельные исходы крайне редки. На этапе диспансерного наблюдения пациенту требуется динамическое исследование мочи.
Профилактика развития первичного острого гломерулонефрита и его рецидивов заключается в лечении острых инфекций, санации хронических очагов в носоглотке и полости рта, повышении сопротивляемости организма, недопущении охлаждения и длительного нахождения во влажной среде. Лицам с повышенным аллергическим фоном (крапивницей, бронхиальной астмой, сенной лихорадкой) профилактические вакцинации противопоказаны.
Источник
