Нефротический синдром липоидного нефроза у детей
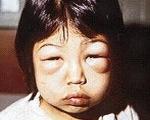
Липоидный нефроз – это заболевание, характеризующееся дистрофическим поражением клубочков с развитием нефротического синдрома. На начальных стадиях симптомы не определяются, в дальнейшем развиваются отеки подкожной жировой клетчатки, слабость, сильная жажда, нарушения аппетита. Диагностика производится на основании результатов лабораторных исследований (общие и биохимические анализы крови и мочи), осмотра больного, УЗИ почек. В спорных случаях назначается биопсия ткани органа для последующего гистологического изучения. Лечение заключается в разработке специальной диеты, применении кортикостероидных и диуретических средств, инфузионной терапии.
Общие сведения
Липоидный нефроз (болезнь подоцитов, идиопатический нефротический синдром детей, ИНСД) – редкое заболевание неясной этиологии, первично поражающее пациентов в возрасте до 4-5 лет. Аналогичные изменения в почках возникают у взрослых с инфекционными состояниями (туберкулез, дифтерия, сифилис) или интоксикацией организма тяжелыми металлами. Согласно статистическим данным, мальчики страдают от первичной патологии в два раза чаще девочек, вторичные формы не имеют особенностей в половом распределении.
Причина состояния кроется в нарушенной работе подоцитов – клеток, покрывающих капилляры в клубочках нефрона. Именно с этим связано синонимичное название заболевания. Среди всех поражений почечной системы доля данного нефроза колеблется в пределах 0,4-0,6%, при этом количество взрослых составляет около 20% от всех заболевших.
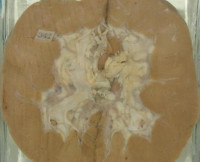
Липоидный нефроз
Причины
Этиология первичного липоидного нефроза на сегодняшний момент неизвестна. Предполагается влияние преимущественно эндогенных факторов. Изучение патогенетических процессов выявило нарушение некоторых звеньев Т-клеточного иммунитета, приводящее к повышенному выделению специфических цитокинов. У ряда больных помимо почечных нарушений отмечаются аллергические патологии и поражения кожи (псориаз).
Примерно у 70% пациентов с идиопатическим нефрозом обнаруживаются особые формы генов главного комплекса гистосовместимости – HLA-B8 и HLA-DR7. Эти серотипы также ассоциируют с определенными разновидностями псориаза. Основная зона их распространения – Северная и Западная Европа – соответствует области наибольшей встречаемости ИНСД.
Вторичное поражение почечной ткани, аналогичное липоидному нефрозу, обычно возникает на фоне хронических патологий инфекционного, опухолевого или интоксикационного генеза. Причиной заболевания также считается аномальная активность иммунной системы, приводящая к избирательному поражению подоцитов клубочков.
Считается, что у лиц с вторичными формами нефроза имеется генетическая предрасположенность к нефротическому состоянию, а системная патология выступает провоцирующим фактором, увеличивая вероятность опосредованного повреждения почек. Нередко отличить липоидные изменения от некоторых форм гломерулонефрита можно только при исследовании ультраструктуры почек посредством электронной микроскопии.
Патогенез
Установлено, что липоидный нефроз обусловлен нарушениями в Т-клеточном сегменте иммунной системы. При идиопатическом нефротическом синдроме детей эти аномалии являются первичными, обусловлены генетическими факторами. Некоторые системные заболевания также могут аномальным образом активировать иммунитет. В результате происходит резкое увеличение популяции Т-супрессоров на фоне значительного выделения цитокинов и интерлейкинов (ИЛ).
Особенно пагубно на клубочки нефрона воздействуют повышенные концентрации ИЛ-8, который уменьшает заряд мембран подоцитов. В результате увеличивается проницаемость стенок капилляров для белков, главным образом – альбуминов, имеющих отрицательный заряд. Попадая в канальцевую систему, протеины закупоривают ее и способствуют деградации эпителиальных клеток, в конечном итоге нефрон полностью перестает выполнять свои функции.
Потеря значительных количеств белка потенцирует изменение реологических свойств плазмы крови. Снижение онкотического давления наряду с нарушением реабсорбции воды и ионов натрия в почках становится причиной отеков. В качестве компенсаторной реакции для улучшения вязкости крови развивается гиперлипидемия. Массовое «выключение» нефронов приводит к хронической почечной недостаточности. С мочой теряются не только альбумины, но и другие протеины, в частности иммуноглобулины классов A и G. Этим обусловлено снижение сопротивляемости организма инфекциям вплоть до вторичного иммунодефицита.
Классификация
Изучение причин липоидного нефроза и разработка принципов классификации данного состояния продолжаются. В настоящее время в практической урологии выделяют две основные группы патологии – идиопатический и вторичный нефроз. Первый тип возникает преимущественно у детей, некоторыми исследователями считается «истинным» липоидным нефрозом. Второй вариант заболевания развивается у взрослых при системных патологиях – отдельные авторы относят его к разновидностям гломерулонефрита. Минимальные гломерулярные нарушения у взрослых по этиологическому признаку разделяют на следующие виды:
- Инфекционного характера. Включают формы нефроза, возникающие под воздействием туберкулеза, сифилиса, дифтерии, малярии и других заболеваний. Инфекции считаются самой распространенной причиной ЛН у лиц старше 16 лет.
- Опухолевого характера. Определенные виды онкологических заболеваний (лимфомы, лимфогранулематоз) способны приводить к иммунным нарушениям с выделением больших количеств цитокинов. Результатом становится поражение подоцитов, характерное для липоидного нефроза.
- Интоксикационного характера. К этой группе относят дистрофические поражения клубочков, вызванные хроническим отравлением тяжелыми металлами – чаще всего ртутью или свинцом.
Приведенная выше классификация считается спорной. Изучение патологии осложняется тем, что для достоверного определения болезни подоцитов необходимо ультрамикроскопическое исследование. По клиническим и гистологическим (посредством световой микроскопии) данным липоидный нефроз очень сильно похож на ряд воспалительных поражений почечной ткани – например, мембранозный гломерулонефрит.
Симптомы липоидного нефроза
Клиническая картина обычно неясная, на начальном этапе заболевание ничем себя не проявляет. Первыми симптомами становятся слабость, разбитость, повышенная утомляемость, нарушения аппетита. Затем возникают отеки, сначала обычно на нижних конечностях, потом на лице, шее, в области поясницы. При тяжелом течении к ним присоединяется накопление жидкости в полостях тела – асцит, гидроторакс, проявляющиеся увеличением живота, затруднением дыхания. Кожные покровы бледные, отечные, ткани рыхлые, на них долго остаются следы от пальцев или других оказывающих давление предметов.
У детей симптомы идиопатического нефротического синдрома аналогичны клинической картине у взрослых. Развитию заболевания часто предшествует перенесенная вирусная инфекция или ангина. Вначале родители отмечают снижение двигательной активности ребенка, сонливость, капризность, нередко – отказ от пищи. После этого появляются отеки и признаки асцита.
Особенностью детской разновидности патологии является возникновение недостатка витаминов А, С, В1. Полигиповитаминоз сопровождается сухостью кожи, образованием кровоизлияний из-за ломкости капилляров, трещинами в углах рта. Возможны неврологические нарушения – чаще всего, снижение кожной чувствительности. Моча при любой форме заболевания приобретает бурый цвет и мутность, ее суточное количество снижается (олигурия).
Липоидный нефроз характеризуется волнообразным течением, периоды обострений с развитием отеков и иных нарушений чередуются с эпизодами спонтанной ремиссии. В межприступный период патология не проявляется, ее наличие можно определить только по протеинурии в результатах общего анализа мочи. При частых обострениях у больных развивается иммунодефицит, обусловленный потерей глобулинов крови. Его признаками являются пневмонии, бронхиты, частые гнойничковые поражения кожи. Характерно появление кожных трещин в области отеков с последующим развитием рожистого воспаления.
Осложнения
На высоте обострения липоидный нефроз опасен развитием шока из-за тяжелых электролитных нарушений и снижения объема циркулирующей крови. Возможны проблемы с дыханием из-за пневмоторакса, усугубленного респираторной инфекцией. Определенную угрозу несут бактериальные поражения кожи, часто принимающие тяжелый характер, существует риск развития сепсиса. При высокой частоте приступов заболевания отмечается гипохромная анемия. При отсутствии лечения со временем возможно формирование вторично-сморщенной почки, что становится причиной ХПН. По некоторым данным, липоидное поражение в отдаленной перспективе повышает риск возникновения амилоидоза.
Диагностика
Диагноз «липоидный нефроз» чаще применяют в современной педиатрической практике. У взрослых аналогичная клиническая картина зачастую определяется врачами-нефрологами как «минимальные гломерулярные изменения». Однако в большинстве случаев речь идет об одном и том же процессе – поражении подоцитов и клубочков при отсутствии иммунных комплексов. Для выявления патологии используют множество диагностических методик, часть из которых направлена на исключение иных почечных патологий со схожим течением. Алгоритм определения данного нефроза включает в себя следующие этапы:
- Осмотр и опрос. При осмотре выявляется отечность подкожной клетчатки различной локализации несимметричного характера, одутловатое лицо, суженные глазные щели. На ощупь отеки рыхлые, неэластичные, легко смещаются, кожные покровы над ними иногда имеют трещины и иные повреждения. При расспросе определяется слабость, отсутствие аппетита, утомляемость, повышенная жажда.
- Лабораторные исследования. Наиболее показательным признаком заболевания является наличие протеинурии в анализах мочи. Потери белка могут составлять до 16 грамм в сутки. Биохимический анализ крови подтверждает гипоальбуминемию до 20-30 г/л, гиперлипидемию за счет увеличения уровня холестерина и фосфолипидов. Показатели креатинина и общего азота при отсутствии осложнений обычно находятся в пределах нормы.
- Ультразвуковые исследования. УЗИ почек обнаруживает увеличение размеров органов, ослабление дифференциации между мозговым и корковым веществом. На поздних этапах развития патологии при многолетнем течении может выявляться сморщивание и уменьшение почек.
- Гистологические исследования. Взятие биопсии тканей почки с последующим микроскопическим исследованием считается золотым стандартом в диагностике данного нефроза. Определяются дистрофические изменения в клубочках, в эпителии проксимальных канальцев обнаруживаются отложения липидов. При иммунногистохимическом исследовании иммунные комплексы отсутствуют – важный признак отличия заболевания от гломерулонефрита.
При вторичном характере патологии производят определение наличия инфекционных, опухолевых или интоксикационных состояний и их тяжести. Дифференциальную диагностику проводят с мембранозным и другими типами гломерулонефрита, амилоидозом почек, пиелонефритом. Отличительной особенностью липоидного нефроза является относительное сохранение фильтрационной способности мочевыделительной системы на протяжении длительного времени.
Лечение липоидного нефроза
Терапевтические мероприятия направлены на устранение отеков, восполнение недостатка протеинов, профилактику инфекционных осложнений. Необходимо ослабить дистрофические процессы в почках, замедлить прогрессирование заболевания. С этой целью разрабатывается сложное комплексное лечение, включающее в себя не только использование лекарственных средств, но и специальную диету. Основными компонентами терапии болезни в нефрологии являются:
- Диета. В рационе больных должны преобладать белки, суточная потребность в которых возрастает до 2,5 грамм в сут. на килограмм массы тела. Для снижения отечности рекомендуется уменьшить потребление поваренной соли (не более 1-2 грамм в день). При выраженной гиперлипидемии следует использовать продукты, содержащие мало жиров (птица, белая рыба, овощи).
- Назначение диуретиков. Мочегонные средства применяют для устранения отеков, особенно в острый период заболевания. При этом важно следить за электролитным составом плазмы крови во избежание осложнений.
- Иммуносупрессивная терапия. Глюкокортикостероиды являются практически единственной группой препаратов для этиотропного лечения липоидного нефроза. Они эффективно снижают активность иммунитета и продукцию цитокинов, ослабляя пагубное воздействие ИЛ-8 на подоциты.
- Лечение инфекционных осложнений. При наличии гнойничкового поражения кожи, пневмонии, ОРЗ назначают антибактериальные или противовирусные средства. При бактериальном заражении эффективны антибиотики и сульфаниламидные препараты.
- Инфузионная терапия. Для улучшения реологических свойств крови показано капельное вливание специальных коллоидных растворов. При угрожающей гипопротеинемии возможно переливание донорской плазмы.
Особенностью лечения патологии у взрослых является одновременное устранение провоцирующего заболевания. В таком случае врач должен учитывать все возможные варианты взаимодействия лекарственных средств из разных групп. В период ремиссии больным рекомендуется санаторно-курортное лечение в регионах с теплым и сухим климатом.
Прогноз и профилактика
При своевременном выявлении липоидного нефроза у ребенка и активном лечении прогноз заболевания относительно благоприятный. Длительность течения может достигать 20 лет, в период обострений пациент временно теряет работоспособность по причине выраженных отеков и сопутствующих нарушений. При вторичном типе состояния прогноз во многом зависит от особенностей течения провоцирующей болезни.
Специфическая профилактика нефроза отсутствует, рекомендуется в полном объеме лечить заболевания, способные стимулировать такое поражение почек. Больным в бессимптомной стадии для предотвращения развития приступа следует придерживаться диеты, избегать переохлаждений и контактов с источниками инфекций. Необходимо регулярно проходить обследование у нефролога с контролем уровня белка в моче для профилактики осложнений.
Источник
Нефротический синдром у детей — это симптомокомплекс, который клинически проявляется отеками и снижением диуреза. Лабораторные признаки патологии — протеинурия, гиперлипидемия, гипоальбуминемия и диспротеинемия. Синдром развивается при первичных гломерулопатиях, аутоиммунных, онкогематологических и сердечно-сосудистых заболеваниях. Для диагностики проводят анализы крови и мочи, биопсию почки, ЭхоКГ и ЭКГ. Лечение включает длительные курсы иммуносупрессорной терапии (глюкокортикоиды, алкилирующие агенты, ингибиторы кальциневрина) в комбинации с нефропротекторными, гипотензивными и мочегонными препаратами.
Общие сведения
Распространенность нефротического синдрома составляет 12-16 случаев на 100 тыс. детского населения. Ежегодно нефрологи выявляют от 2 до 7 новых случаев заболевания на 100 тысяч пациентов младше 18 лет. Патология не относится к самостоятельным нозологическим единицам, а представляет собой один из синдромов почечных или внепочечных болезней. Актуальность этой проблемы в педиатрической практике обусловлена сложностью терапии и частыми случаями резистентности к лекарствам.

Нефротический синдром у детей
Причины
У детей чаще выявляются первичные формы нефротического синдрома, вызванные поражением клубочкового аппарата почек. В 85% морфологическим субстратом является болезнь минимальных изменений, до 5-7% составляет фокально-сегментарный гломерулосклероз, 4-6% отводится мезангиопролиферативному гломерулонефриту. Вторичный вариант заболевания имеет несколько этиологических факторов:
- Аутоиммунные процессы. Они сопровождаются образованием иммунных комплексов и провоспалительных цитокинов, которые откладываются в почечных капиллярах, нарушая работу фильтрационной системы органа. У детей причиной могут послужить системные васкулиты, системная красная волчанка, синдром Шегрена.
- Злокачественные опухоли. Почечные поражения возникают при лимфоме Ходжкина и неходжкинских новообразованиях, которые зачастую встречаются в детском возрасте. Среди менее распространенных онкологических факторов выделяют множественную миелому, солидные опухоли.
- Токсические повреждения почек. Нефротический синдром возможен при длительном и бесконтрольном приеме ребенком нестероидных противовоспалительных средств и некоторых антибиотиков. Поражение почек также наблюдается при отравлении солями тяжелых металлов, ядами змей и перепончатокрылых насекомых.
- Нарушения почечного кровотока. Повышенная секреция белка в мочу происходит при структурных повреждениях почечных клубочков на фоне тотальной ишемии. Она может быть вызвана тромбозом почечной вены, серповидно-клеточной анемией, злокачественной гипертензией.
- Врожденные гломерулопатии. У детей встречается синдром Альпорта, для которого характерны мутации коллагеновых волокон в базальных мембранах клубочков. Реже диагностируется болезнь Фабри, когда нефропатия связана с нарушениями метаболизма сфинголипидов.
Патогенез
На начальных этапах нефротического синдрома развивается протеинурия, вызванная повышением проницаемости почечного фильтра для белков. Это обусловлено структурно-функциональными повреждениями компонентов почечного клубочка. Большую роль в этом процессе имеют аутоиммунные механизмы: активированные Т-лимфоциты вырабатывают специфические цитокины, которые повреждают клеточные мембраны и «щелевые» контакты подоцитов.
Повышенная потеря белков с мочой снижает онкотический показатель крови. Как следствие, жидкость по градиенту давления начинает перемещаться из сосудистого русла в ткани. Таким образом формируются массивные нефротические отеки. Их интенсивность зависит от степени белковых потерь и активности компенсаторных механизмов. В 10% случаев отечный синдром развивается вследствие первичной задержки натрия в организме.
Симптомы
Для патологии типично острое начало, связь с перенесенной инфекцией, переохлаждением, вакцинацией или обострением хронической соматической болезни. Сначала ребенок жалуется на общую слабость, недомогание, сонливость и заторможенность. Реже беспокоят головные и абдоминальные боли, тошнота, снижение аппетита. У девочек-подростков бывают нарушения менструального цикла.
Основное проявление нефротического синдрома — отеки. Вначале они возникают на лице (утром) и на голенях (вечером, после длительной ходьбы), а затем постепенно распространяются по всему телу. Первоначально они мягкие, расположены симметрично, кожа над ними теплая и сухая. Параллельно с этим снижается количество суточной мочи. Периферические отеки дополняются полостными — асцитом, гидроперикардом, гидротораксом, что ухудшает состояние ребенка.
Осложнения
Негативные последствия нефротического синдрома вызваны потерей альбуминов, которые в норме выполняют ряд физиологических функций. Потеря иммуноглобулинов ухудшает иммунную защиту организма, что проявляется частыми респираторными инфекциями, рецидивирующими тонзиллитами и синуситами. Снижение количества трансферрина (переносчика железа) приводит к рефрактерной железодефицитной анемии.
Значимым осложнением для детей младшего возраста является потеря витамин-Д-связывающего белка. В результате формируется рахитоподобный синдром, нарушается минерализация и рост костей скелета. В редких случаях развивается повышенная кровоточивость из-за дефицита прокоагулянтов. При стероидорезистентном варианте болезнь в течение 5-10 лет прогрессирует до терминальной ХПН.
Диагностика
При физикальном осмотре детский нефролог обращает внимание на симметричность и расположение отеков, проводит аускультацию сердца и легких, определяет признаки асцита и увеличения печени. Симптомы не дают возможности установить клинический диагноз, поэтому врач назначает полное обследование. Составляющие диагностического комплекса:
- Анализ мочи. Патогномоничными признаками нефротического синдрома являются протеинурия более 50 мг/кг/сутки, соотношение протеин/креатинин более 2 и экскреция альбумина свыше 40мг/м2/час. Для исключения эритроцитурии и лейкоцитурии показан анализ по Нечипоренко. Функцию почек оценивают с помощью пробы Реберга.
- Анализ крови. При биохимическом исследовании выявляют уровень альбумина сыворотки менее 30 г/л, повышение уровня холестерина и триглицеридов, увеличение показателя креатинина. Уровни натрия и кальция крови снижаются, а калий может быть повышен. В коагулограмме наблюдается повышение фибриногена.
- ЭхоКГ. Ультразвуковая визуализация необходима для обнаружения гидроперикарда, морфометрических изменений крупных сосудов вследствие отеков. Также рекомендована ЭКГ, которая позволяет вовремя заметить нарушения ритма и проводимости, связанные с электролитными нарушениями.
- Биопсия почки. Пункционный забор материала выполняется при нефротическом синдроме у младенцев до 1 года и подростков старше 12 лет, а также при неэффективности стандартной медикаментозной терапии. Биоптаты подвергают световой, электронной и иммунофлюоресцентной микроскопии.
Лечение нефротического синдрома у детей
Дети с острым нефротическим синдромом подлежат обязательной госпитализации на 2-3 недели. Двигательная активность при этом не ограничивается и соответствует самочувствию больного. В диете необходимо поддерживать высокий уровень белков, а подросткам с массивными отеками рекомендовано снизить потребление поваренной соли. При выраженных потерях протеинов назначается коррекция гомеостаза коллоидными и кристаллоидными растворами.
Основу патогенетического лечения детей с нефротическим синдромом составляет иммуносупрессивная терапия с применением глюкокортикоидов. Препараты уменьшают образование и поступление в патологический очаг воспалительных клеток, угнетают секрецию медиаторов воспаления, приостанавливают формирование токсических иммунных комплексов. Терапия глюкокортикоидами проводится в 3-х режимах:
- Постоянный. Показан в начале лечения, чтобы быстро достичь фазы ремиссии. Гормоны принимаются перорально в первой половине дня в суточной дозировке 1-2 мг/кг.
- Альтернирующий. Назначается после достижения ремиссии. Стандартные дозы глюкокортикоидов используются через день, чтобы сохранить клинический эффект, но снизить риски побочных реакций.
- Пульс-терапия. Применяется при тяжелом течении нефротического синдрома. Гормоны вводятся внутривенно капельно, чтобы в короткие сроки достичь высоких концентраций лекарства в крови.
При развитии тяжелых побочных эффектов на гормональные препараты или стероидорезистентном варианте заболевания переходят на другие виды иммуносупрессоров. В детской нефрологии наилучший результат показывают ингибиторы кальциневрина, алкилирующие агенты, некоторые моноклональные антитела к лимфоцитам. Они могут вызывать нефротоксичность, поэтому во время лечения врачи контролируют уровень СКФ.
Для устранения массивных отеков проводится терапия петлевыми диуретиками в возрастных дозировках. С целью ликвидации рефрактерных полостных отеков назначаются комбинации петлевых и тиазидных мочегонных. В качестве гипотензивных и нефропротекторных средств у детей лучше всего работают ингибиторы АПФ и блокаторы рецепторов ангиотензина. Коррекцию остеопении производят препаратами витамина Д.
Прогноз и профилактика
У детей с хорошим ответом на стероидную терапию в 95% наблюдается полное выздоровление без снижения функции почек. Менее благоприятный прогноз при стероидорезистентности, поскольку у таких пациентов высокий риск формирования хронической почечной недостаточности. Однако, своевременное применение иммуносупрессоров и нефропротекторов позволяет замедлить патологический процесс.
Первичная профилактика включает рациональное назначение лекарств, раннюю диагностику и терапию аутоиммунных процессов, избегание контактов с нефротоксическими веществами. Вторичная профилактика предполагает курсы гормональной терапии при обострении основной патологии либо в случае интеркуррентного заболевания. Это необходимо для предупреждения рецидивов нефротического синдрома.
Источник
