Оценка болевого синдрома у детей
Комментарии
Опубликовано в журнале:
«Практика педиатра», сентябрь 2012, с. 40-42
Н.А. Супонева, ФБГУ Научный центр неврологии РАМН, к. м. н., старший научный сотрудник
Одной из самых частых причин обращений в педиатрической практике является болевой синдром, причины которого разнообразны. Согласно определению Международной ассоциации по изучению боли (IASP), наряду с сенсорным переживанием, обусловленным непосредственным раздражением болевых рецепторов поврежденной ткани, важнейшим компонентом боли является ее эмоциональное переживание [1], базирующееся на социальном и личном опыте.
Оценка степени выраженности болевого синдрома у ребенка является непростой, но крайне важной задачей, поскольку от этого зависит лечебная тактика. Восприятие боли и реакция на нее в зависимости от возраста разная. Золотым стандартом оценки боли у взрослых является визуальная аналоговая шкала, которую можно применять у детей с 5–6-летнего возраста [14]. Детям в возрасте 3–5 лет с этой целью можно предложить модифицированную шкалу, где цифры заменены рисунками в виде выражений эмоций на лице, или так называемую лестницу боли, по которой ребенок должен ответить, на сколько ступеней могла бы подняться игрушка, если бы ей было так же больно, как и малышу. Кроме эмоциональной, боль также вызывает ряд патофизиологических и поведенческих реакций, которые могут быть использованы для объективной оценки степени выраженности болевого синдрома.
Дети разных возрастных групп выражают свою боль иначе, чем взрослые. Так, тело младенцев может интенсивно напрягаться, вытягиваться, одновременно выгибаясь дугой, а на лице наблюдается гримаса боли (брови опущены и наклонены друг к другу, глаза зажмурены, рот открыт в форме квадрата [3]). Ребенок громко и безутешно плачет, прижимает колени к груди, гиперчувствителен или раздражен. Следует отметить, что плач является самым неспецифическим симптомом и может считаться проявлением реакции на боль только в том случае, когда исключены другие, наиболее частые причины (голод, жажда, тревога, желание привлечь внимание родителей). Малыши постарше выражают словесную агрессию, отстраняются от общения и игр, физически сопротивляются, отталкивая болевой стимул после его применения, щадят область тела, причиняющую страдания. Таким образом, у детей в возрасте старше 3 лет оценка болевого синдрома существенно облегчается, поскольку в этом возрасте ребенок может достаточно определенно выразить и идентифицировать боль с помощью специальных оценочных шкал (например, Faces Pain Rating Scale [2]), а также четко показать место, где болит, на своем теле или на картинке. Однако следует помнить о том, что дети, страдая от боли, не всегда предъявляют активные жалобы. Причиной тому могут быть: боязнь врача или болезни, обида или раздражение на родителей или окружающих, боязнь инъекций или лекарств, а также того, что их могут положить в больницу, опасения в проведении дополнительных обследований. В связи с этим врачам рекомендуется максимально использовать информацию, полученную при опросе родителей, тестированиях по шкалам и оценке физиологических и поведенческих реакций.
Дошкольники уже могут описать интенсивность боли, цепляются за родителей, требуя дополнительной эмоциональной поддержки (поцелуи, объятия), осознают, что из своего состояния можно извлечь выгоду, а в ряде случаев воспринимают боль как наказание. Дети школьного возраста в описании боли используют объективные характеристики и сравнительные прилагательные, могут жаловаться на ночные кошмары, а также сжимают кулаки, стискивают зубы, нахмуривают брови, закрывают глаза, напрягают мышцы туловища, щадят больное место, а также ведут себя как дети более младшего возраста. Старшие дети осознанно локализуют и вербализируют боль, их поведение неустойчиво и может изменяться (раздражительность, капризы, грубость). В любом возрасте может нарушаться аппетит и сон.
В интерпретации и оценке болевого синдрома у новорожденных и младенцев, а также у детей с задержкой психомоторного развития и нарушением коммуникативных функций существенную помощь оказывает использование специально разработанных шкал, позволяющих в комплексе оценить поведенческие и физиологические реакции ребенка: шкала Neonatal/Infant Pain Scale (NIPS) для детей до 1 года [4], шкала FLACC [5] для детей от 1 до 3–4 лет и др. Дополнительную помощь может оказать использование шкалы прикроватной оценки боли, а также с помощью родительской шкалы [6], согласно которым болевые ощущения ребенка градируются как отсутствие боли, легкая боль, умеренная и тяжелая.
К немедикаментозным методам облегчения боли у ребенка относятся: эмоциональная продержка со стороны родителей, в том числе обеспечение возможности их совместного пребывания во время болезни или болезненных диагностических процедур; физические методы, к которым относятся поглаживание, массаж, вибрация, укачивание, местное применение холода или тепла, контролируемое глубокое спокойное дыхание; когнитивные методы, такие как отвлечение ребенка, чтение книг, рисование, пение, игры, посещение церкви, молитвы. Известно, что применение 0,5–1мл 30%-го раствора глюкозы перорально за 1–2 минуты до проведения болезненной процедуры (забор крови, инъекции) вместе с пустышкой облегчают восприятие боли у новорожденных и младенцев до 3-месячного возраста. Все вышеперечисленные методы являются дополнительными, широко применяются в зарубежной педиатрической практике обезболивания, но ни в коей мере не заменяют лекарственных препаратов.
Легкая и умеренная боль в детской практике встречается наиболее часто, что обуславливает необходимость остановиться на способах ее купирования более подробно. Такая боль наблюдается при прорезывании зубов, болях в ухе при отитах и евстахиитах, головной боли, болях в мышцах и суставах, в том числе после ушибов и растяжений, при радикулитах и артритах, при местной поствакцинальной реакции. Наиболее часто используемыми анальгетиками являются парацетамол и ибупрофен (Ибуфен). Традиционно рекомендуемой с целью снижения температуры тела дозы парацетамола обычно достаточно для обезболивания: перорально 20 мг/кг, а затем 15–20 мг/кг каждые 6–8 часов, или ректально 30–40 мг/кг, а затем 15–20 мг/кг каждые 6 часов, но не более 90–100 мг/кг/сут для детей и 60 мг/кг/сут для новорожденных. Такая максимальная суточная доза разрешена у детей до 3 месяцев жизни в течение не более 2 дней, а для детей старше 3 месяцев – не дольше 3 суток [6]. Однако, как показывает практика, обезболивающее действие у парацетамола у многих детей бывает слабо выражено, а противовоспалительный эффект вовсе отсутствует.
В таких случаях неоспоримым преимуществом обладает единственный разрешенный у детей с 3-месячного возраста препарат из группы нестероидных противовоспалительных препаратов (НПВП) – Ибуфен (ибупрофен). Его тройной эффект обеспечивает уменьшение жара, обезболивание и подавление воспаления. Основной патогенетический механизм действия Ибуфена заключается в подавлении циклооксигеназы [7]. Обезболивание достигается путем уменьшения образования простагландинов, брадикинина, эндогенных пирогенов, радикалов кислорода и оксида азота, что в свою очередь угнетает воспалительную реакцию и уменьшает болевую рецепцию непосредственно в области повреждения. Такое удачное сочетание общего и локального механизмов действия Ибуфена дает возможность существенно облегчить состояние малыша путем назначения всего одного медикамента.
Разовая доза Ибуфена составляет 5–10 мг /кг с кратностью приема каждые 6–8 часов, но не более 30 мг/кг в сутки (максимум 500 мг /сут). Ибуфен выпускается в двух формах – с ложкой-дозатором и шприцем-дозатором, что позволяет родителям выбрать оптимальный способ ввода лекарства своему ребенку.
Эффективность и безопасность ибупрофена была подтверждена Bertin с соавт. в 1996 году, когда 219 детей с острым отитом в возрасте от 1 до 6 лет были включены в рандомизированное двойное слепое мультицентровое контролируемое исследование. Из них 71 человек получал ибупрофен (Ибуфен) в дозе 10 мг/кг, 73 человека – парацетамол, 75 человек – плацебо, перорально трижды в день в течение 2 суток. Одновременно всем проводилась антибиотикотерапия в течение 7 дней. В ходе исследования был доказан очевидный обезболивающий эффект ибупрофена (Ибуфен) по сравнению с плацебо, сопоставимый с эффектом парацетамола [10]. Bertin с соавт. [15] оценивали анальгезирующий эффект ибупрофена (Ибуфен) в дозе 10 мг/кг по сравнению с парацетамолом (10 мг/кг) или плацебо у 231 ребенка с тонзиллитом и фарингитом, дополнительно принимавших в течение 7 дней антибиотики. Уже в течение 48 часов 80% детей в группе ибупрофена (Ибуфен) и 70,5% детей в группе парацетамола не отмечали спонтанных болей и болей при глотании, что существенно отличалось от группы плацебо (55% детей, р<0,01).
Ибуфен – безопасный препарат, что особенно актуально в педиатрической практике. Lesko S.M. с соавт., проанализировав 84 000 детей, получавших ибупрофен (Ибуфен) с фарингитом, средним отитом, ОРВИ или гастроэнтеритом в дозе 5 или 10 мг/кг коротким курсом, показали, что этот препарат не увеличивает риск госпитализаций вследствие желудочно-кишечных кровотечений, почечной недостаточности, синдрома Рея или анафилаксии [13]. Безопасность Ибуфена была подтверждена и в ходе другого исследования, проведенного McIntyre J. и Hull D. [11]. В этом рандомизированном контролируемом исследовании принимали участие 150 детей с лихорадкой различного генеза. Результаты продемонстрировали одинаковую антипиретическую эффективность препарата, а также низкую частоту побочных эффектов. Таким образом, было доказано, что суспензия Ибуфена является эффективным и хорошо переносимым жаропонижающим средством у детей.
Бронхиальная обструкция у детей, особенно раннего возраста, является частым симптомом ОРВИ. Lesko S.M. с соавт. в 2002 году в ходе крупномасштабного рандомизированного двойного слепого ацетаминофен-контролируемого клинического исследования, включавшего 1879 детей с бронхиальной астмой, не имеющих непереносимости аспирина, сумели доказать, что ибупрофен (Ибуфен) не увеличивает риск бронхоспазма у этой категории больных [12]. Однако ибупрофен, как все НПВП, может увеличивать время кровотечения, что следует учитывать при его назначении у пациентов с адено-/тонзилэктомией или другими оперативными вмешательствами [9].
Таким образом, необходимость в адекватном и одновременно безопасном обезболивании в педиатрической практике возникает достаточно часто. Этим требованиям в полной мере соответствует Ибуфен, рекомендуемый Всемирной организацией здравоохранения.
Список литературы находится в редакции.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
Содержание
NIPS – Neonatal Infant Pain Scale
FLACC (Face, Legs, Activity, Cry, Consolability)
Шкала Вонга-Бейкера (Face scale)
Шкала Oucher
Шкала Эланда (Eland Body Tool)
Шкала рук (Hand scale)
Poker Chip tool
Визуально-аналоговая шкала (ВАШ)
Шкала тактильной и визуальной оценки боли (Touch Visual Pain – TVP scale)
Пошаговое руководство ВОЗ по применению и интерпретации шкалы для оценки боли
Для оценки боли применяются специальные шкалы. Чтобы использовать их эффективно, нужно подбирать шкалы в зависимости от возраста ребенка. Для новорожденных, детей до 3-х лет, от 3-х до 7-лет, для подростков разработаны разные инструменты. Шкалы могут применять как врачи и медсестры, так и родители детей.
При оценке боли учитываются невербальные знаки со стороны пациента, уровень его развития и интеллекта. При заполнении шкалы у вербальных пациентов старше 3-х лет нужно ориентироваться на то, что ребенок говорит о своей боли. Однако стоит помнить, что если ребенок не говорит о боли, это не значит, что ее нет. Возможно он боится последствий, например, уколов, или наоборот, считает, что отрицание боли – проявление силы и храбрости.
Дети чуть постарше могут описывать интенсивность своей боли и локализовать ее. Если это ребенок в возрасте 1,5-2 лет, он может не употреблять слово «боль», используя близкие ему слова-определения (например, «бо-бо»). Дети старше 8 лет способны описывать боль в контексте своего опыта, а подростки – подробно рассказывать о причинах боли и детально описывать свои болевые ощущения.
Всегда необходимо спрашивать о боли не только ребенка, но и тех, кто находится рядом, видит ребенка каждый день и может оценить его состояние в динамике. Мамы и папы, опекуны, няни или медсестры могут дать действительно важную информацию: ел ли сегодня ребенок, отказывался ли он от питья, разговаривает ли он сегодня, как можно оценить его позу и насколько она для него естественна.
При заполнении шкалы необходимо не только оценивать поведение пациента, физиологические параметры, но и обязательно выявить причину боли, чтобы по возможности устранить ее и обезболить ребенка.
Важно сказать, что идеальных шкал для оценки боли нет. Они не всегда дают нам объективную ситуацию, и относиться к ним нужно как к ориентировочным методикам. Но несмотря на это, нужно их обязательно использовать, так как это дает возможность оценки интенсивности боли.
Важно
Нужно выбрать одну методику для пациента и применять ее постоянно.
NIPS – Neonatal Infant Pain Scale
И спользуют для оценки боли у детей в возрасте до 1 года. Шкалу могут заполнить родители, ориентируясь на выражение лица ребенка, на плач, дыхание, положение верхних и нижних конечностей, состояние сознания. Сумма баллов выше трех означает наличие боли.
Источник: БФ «Детский паллиатив»
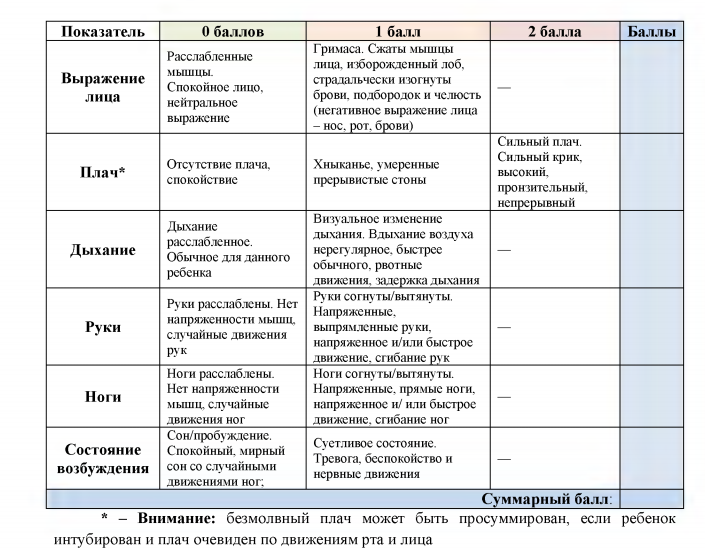
FLACC (Face, Legs, Activity, Cry, Consolability)
Эта поведенческая шкала применяется для детей в возрасте до 3 лет. Она учитывает выражение лица ребенка, положение или подвижность ног, характер крика и то, насколько ребенок поддается успокоению. Боль оценивается по десятибалльной шкале. Чем выше оценка, тем сильнее боль, и тем хуже себя чувствует ребенок.

Источник: БФ «Детский паллиатив»
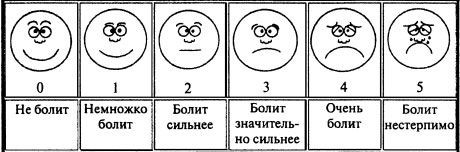
Шкала Вонга-Бейкера (Face scale)
Используется для детей в возрасте от 3 до 7 лет. При работе с этой рейтинговой шкалой ребенку необходимо выбрать одно из нарисованных лиц, которое соответствует его самочувствию. Иногда, используя эту шкалу, ребенок может больше ориентироваться на свои эмоции, чем на боль. 0 – счастлив, нет боли, 5 – плачет, несчастен, испытывает нестерпимую боль. Поэтому эта шкала не всегда бывает адекватна для оценки боли.
Шкала Oucher
Аналог предыдущей шкалы – десятибалльная шкала Oucher, на которой представлены фотографии лиц детей с нарастающей болью и без нее.

Источник: www.oucher.org
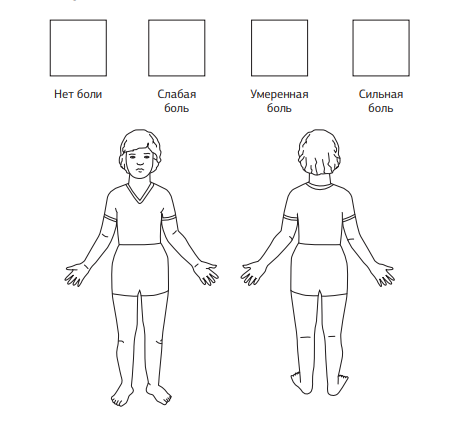
Шкала Эланда (Eland body tool)
Также для детей этого возраста применяется цветная шкала Эланда (Eland body tool). Интенсивность боли ребенок определяет с помощью цвета: сильная боль – красный цвет, умеренная боль – оранжевый, слабая боль – желтый. Также шкала позволяет определить локализацию боли.
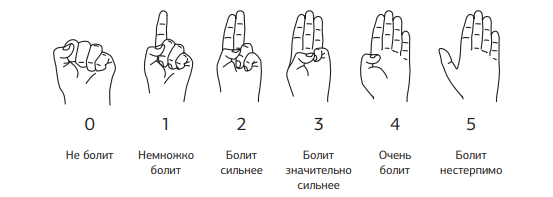
Шкала рук (Hand scale)
Пятибалльная шкала, которая показывает колебания боли при помощи одной руки. Сжатая в кулак рука означает отсутствие боли, полностью раскрытая ладонь – нестерпимую боль. Применяется для детей старше 3 лет.
Poker Chip tool
В некоторых странах согласно ВОЗ для оценки боли у детей 3-12 лет используется шкала с фишками для покера (Poker Chip tool). Однако ее использование требует уверенности, что у ребенка развит навык сортировки по размеру. Среди недостатков – необходимость мытья фишек после каждого использования, риск потери фишек и ограниченное число вариантов ответа от 0 (отсутствие боли) до 4 – сильная боль. Шкала доступна с переводом на английский, арабский, испанский и тайский языки. При ее использовании будьте уверены, что ваш лечащий врач тоже может пользоваться этой шкалой.
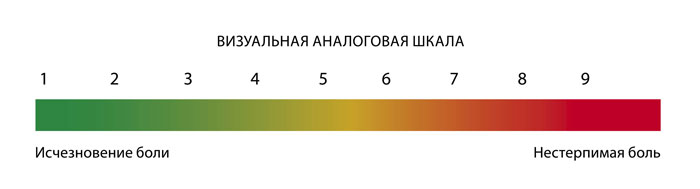
Визуально-аналоговая шкала (ВАШ)
Подходит для детей старше 7 лет, которые понимают значение цифр. На вертикальной шкале с изображением цифр от 0 до 10 ребенок должен подвинуть полоску вверх или вниз (или показать пальцем) на ту высоту шкалы, с которой он ассоциирует свои болевые ощущения. Аналог такой шкалы – нумерологическая оценочная шкала (НОШ).
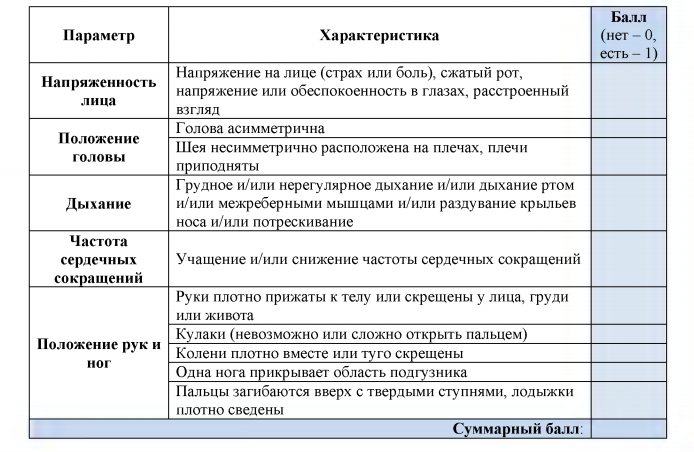
Шкала тактильной и визуальной оценки боли (Touch Visual Pain – TVP scale)
Была создана для ВИЧ-инфицированных детей с мультиорганной патологией. При оценке боли используются прикосновения к ребенку и наблюдение за ним. Боль оценивается по десятибалльной шкале: 0 – нет боли, 10 – нестерпимая боль.
Источник: БФ «Детский паллиатив»
Пошаговое руководство ВОЗ по применению и интерпретации шкалы для оценки боли
- Если возможно, ознакомить ребенка со шкалой боли, когда он ее не испытывает, потому что боль будет нарушать концентрацию внимания.
- Объяснить ребенку, что методика применяется для оценки интенсивности боли, а не его тревоги или страха перед болью.
- Дать ребенку возможность потренироваться применять шкалу в гипотетических ситуациях с отсутствием боли, слабой и сильной болью. По возможности получать регулярные оценки боли и наблюдать эффект обезболивающих мер, а также клинических вмешательств, способных усилить боль, таких как инъекции.
- Учитывать записанные оценки боли при планировании лечения.
- У детей раннего возраста и детей с когнитивными нарушениями применять наблюдательные методики.
- Стараться не просить ребенка оценивать боль, которую он испытал давно, т. к. оценки припоминаемой боли скорее всего будут неточными.
- Оценка боли по шкале не должна заменять беседы с ребенком, всегда следует просить ребенка рассказать о боли.
- Расхождения оценок боли, данных ребенком, родителем и врачом, часто можно прояснить в ходе обсуждения.
Источники: Методические рекомендации «Обезболивание взрослых и детей при оказании медицинской помощи», рекомендации ВОЗ по лечению персистирующей боли у детей, интервью медицинского директора фонда «Детский паллиатив» Эллы Кумировой, лекция специалиста по паллиативной помощи Линды Брук.
Подготовила Диана Карлинер
Источник
Боль — неприятное сенсорноэмоциональное переживание, связанное с истинным или потенциальным повреждением тканей [4].
Долгое время бытовало мнение, что дети устойчивы к болевому воздействию, а польза от проводимой лечебной процедуры значительно важнее, чем эмоциональная реакция ребенка [2]. До середины 1970х годов адекватную анальгезию в неонатальном периоде не проводили, исходя из убеждения о незрелости периферических болевых рецепторов, неполной миелинизации проводящих нервных волокон [3, 4]. Исследования последних лет показали, что болевые воздействия вызывают у детей патологические реакции. К их числу относятся такие нарушения, как энурез, потеря недавно сформировавшихся навыков, перевозбуждение, трудности засыпания, ночные кошмары, негативные эмоциональные реакции, избегающее поведение ребенка [1]. У новорожденных, которые подвергались обрезанию без анестезии, отмечалась более сильная реакция дистресса при обычной иммунизации в возрасте 4 и 6 месяцев по сравнению со сверстниками, не подвергшимися обрезанию или перенесшими обрезание под местной анестезией [10]. Работы Anand и соавт. показали, что у недоношенных новорожденных после хирургического вмешательства с минимальной анестезией возникали более сильные ответные реакции (возрастание концентрации катехоламинов, глюкагона, кортикостероидов), у них наблюдалось больше послеоперационных осложнений, выше оказывалась смертность по сравнению с группой новорожденных, получивших полную анестезию. McCrath и Unruh доказали, что незрелость новорожденных касается не их способности переживать боль, а исключительно неспособности сигнализировать о ней взрослым [6, 7].
Во время и после болевого воздействия отмечается повышение артериального давления (АД), изменение частоты (ЧСС) и ритма сердечных сокращений, частоты и механики дыхания, при длительном плаче ребенка возможно повышение внутричерепного давления [4].
Боль является одной из рано формирующихся психофизических функций, связанной с самыми «древними» структурами мозга. Все нейрофизиологические компоненты, необходимые для восприятия боли новорожденным ребенком, имеются у плода уже с середины гестационного периода. Незавершенная миелинизация вовсе не подразумевает отсутствие функции, а лишь немного замедляет время передачи импульсов, что компенсируется более короткими межнейронными расстояниями. Поэтому анестезиолог всегда должен помнить, что новорожденные, даже глубоко недоношенные, способны испытывать боль и реагируют на нее гипертензией, тахикардией, увеличением внутричерепного давления, выраженной нейроэндокринной реакцией. Более того, болевой порог у новорожденных значительно ниже, чем у старших детей или взрослых. Маленький ребенок не может локализовать боль, и ответная реакция имеет более диффузный характер, быстро истощая компенсаторные возможности. При этом в первую очередь нарушается нормальное функционирование системы дыхания и кровообращения [4].
Причин возникновения боли даже у новорожденных детей может быть множество, и свидетельствовать они могут о различных заболеваниях: родовой травме, гнойновоспалительных заболеваниях, некротическом энтероколите, остеомиелите, менингоэнцефалите, гидроцефалии, врожденных пороках развития. Кроме того, появление боли может быть связано с медицинскими манипуляциями и оперативными вмешательствами [8].
Субъективный характер боли делает ее трудноизмеримым понятием. Особенно это касается тех, кто не может выразить свою боль словами. Вот почему важную роль в распознавании и оценке болевого синдрома у новорожденного играет способность врача правильно интерпретировать клинические данные. С этой целью разработано несколько шкал оценки болевого синдрома, в основе которых лежат физиологические и поведенческие реакции новорожденного в ответ на болевое раздражение.
Первыми клиническими симптомами «болевого прорыва» у новорожденного ребенка являются нарушение сна, беспокойство и плач, затем повышается ЧСС и артериальное давление, уменьшается дыхательный объем и жизненная емкость легких, снижается сатурация (табл. 1).
/032/032.jpg)
Оценить выраженность болевых реакций можно с помощью оценочных шкал, использующихся в неонатальной анестезиологии.
Одной из наиболее популярных шкал оценки боли у новорожденных является шкала DAN (Douleur Aiguedu Nouveaune). Она используется для оценки острой и хронической боли у новорожденных по внешним признакам (табл. 2) [9].
/032/032_2.jpg)
Еще один метод, разработанный для использования у младенцев и детей до 7 лет, называется «Лицо — ноги — активность — плач — утешаемость» (FLACC: face, legs, activity, cry, consolabylitу). Этот метод оценивает боль по пяти поведенческим признакам, соответственно — выражению лица, движению ног, подвижности, плачу и утешаемости (табл. 3).
/033/033.jpg)
Шкала CRIES (табл. 4) разработана для использования у новорожденных с 32 недель гестационного возраста до 6 месяцев. Каждый из пяти показателей этой шкалы (плач, потребность в кислороде при сатурации ниже 95 %, повышение АД и ЧСС, выражение лица и сон) оценивается от 0 до 2 баллов.
/033/033_2.jpg)
Для оценки степени боли в послеоперационном периоде используют следующие методы:
1. Шкала CHEOPS (табл. 5) [10], которая включает в себя следующие категории: крик (1), гримаса (2), вербальный ответ (3), тонус мышц спины (4), активность в ответ на прикасание к хирургической ране (5) и движения ног (6). Каждый признак оценивается в баллах от 0 до
/034/034.jpg)
3. Первоначально шкала CHEOPS использовалась только у детей от 1 до 7 лет.
2. Объективная шкала боли (OPS) является достоверным и надежным методом оценки боли (табл. 6) [10].
/034/034_2.jpg)
В OPS оцениваются артериальное давление (1), крик (2), движение (3), возбуждение (4) и вербализация (5). Каждый параметр оценивается в баллах от 0 до 2. Особенность данного метода в том, что он включает оценку состояния сердечнососудистой системы как фактора боли в послеоперационном периоде. Однако одновременно могут присутствовать другие причины, которые влияют на гемодинамику у ребенка. Шкала OPS чаще используется для оценки боли у детей старше 1 года, у новорожденных — редко, что связано с неспособностью вербально выразить боль.
3. Более часто для оценки боли у новорожденных, которые находятся на искусственной вентиляции легких (ИВЛ), используют шкалу COMFORT (табл. 7).
/035/035.jpg)
В ней оцениваются девять показателей: тревожность, беспокойство и ажитация, дыхательные нарушения, плач, физическая подвижность, мышечный тонус, мимический тонус, среднее артериальное давление и ЧСС [12]. Каждый показатель оценивается по шкале от 1 до 5. Суммарное значение может варьировать от 9 до 45. Значения от 17 до 26 свидетельствуют об адекватной седации и обезболивании.
Оценка боли должна проводиться каждые 4–6 часов с документацией результатов. Для этого должен привлекаться обученный средний медицинский персонал.
Как же обстоят дела в диагностике боли у новорожденных с позиций доказательной медицины? С.А. Бочкаревой и А.Б. Пальчик (СанктПетербургская государственная педиатрическая медицинская академия) были обследованы две группы детей, в одной из которых болевое раздражение (внутримышечная инъекция) наносилось без предварительной анальгезии, а во второй место инъекции предварительно обрабатывали смесью местных анестетиков. Оценка болевого синдрома проводилась с помощью существующих оценочных шкал, применяемых в неонатологии. Исследование показало, что применение смеси местных анестетиков влияет на болевой ответ новорожденного: уменьшается продолжительность крика и флексорная реакция, наступает более быстрое успокоение, изменяются вегетососудистые показатели по данным пульсоксиметрии. Однако по большинству сравниваемых показателей (более 20) достоверных различий между группами не получено.
Это скорее всего свидетельствует о том, что большинство рассматриваемых общепринятых болевых параметров не являются специфичными для болевого стресса у новорожденного, а служат показателями реакции новорожденного на внешнее вмешательство. Следовательно, значительная часть физиологических поведенческих показателей, принятых как возможные маркеры боли у новорожденного, не являются специфичными, а следовательно, на изменении этих параметров не может строиться корректная диагностика боли с позиций доказательной медицины [5]. Данное исследование убеждает в необходимости дальнейшей разработки специфичных и достоверных методов определения болевого синдрома у новорожденных.
Список литературы
1. Клипинина Н.В. Некоторые особенности восприятия и переживания боли детьми: взгляд психолога // Рус. мед. журн. — 2007. — 9.
2. Снисарь В.И. Боль у детей // Здоровье Украины. — 2007. — 1518.
3. Степанов А.А., Яцык Г.В., Намазова Л.С. Метод профилактики боли у детей раннего возраста при вакцинации // Педиатрич. фармакол. — 2007. — Т. 4, № 1. — С. 8285.
4. Шабалов Н.П., Иванов С.Л. Боль и обезболивание в неонатологии. — М., 2004. — 156 с.
5. Бочкарева С.А. Принципы доказательной медицины в диагностике боли у новорожденных детей / Пальчик А.Б., Бочкарева С.А. // Сборник материалов Междисциплинарного конгресса «Ребенок и лекарство». — СПб., 2006. — С. 3335.
6. Cowley Ch. Business briefing: longterm healthcare strategies. — 2003.
7. Wintgens М.A. et al. Posttraumatic stress symptoms and medical procedures in children // Can. J. Psychiatry. — 1997. — Vol. 42. — 611616.
8. Pain response in newborns to the order of injecting BCG and HepatitisB vaccines: a randomized trial // Indian J. Pediatr. — 2011. — 78(6). — 6937.
9. Carbajal R., Chauvet X. et al. Randomised trial of analgesic effects of sucrose glucose and pacifiers in term neonates // BMJ. — 1999. — 319. — 13931397.
10. McGrath P.J., Johnson G., Goodman J.T. CHEOPS: A Behavioral Scale for Rating Postoperative Pain in Children // Advances in Pain Researchand Therapy. — New York, NY: Raven Press, 1985. — Vol. 9. — 395402.
11. Hannallah R.S., Broadman L.M., Belman A.B. et al. Comparison of caudal and ilioinguinal/iliohypogastric nerve blocks for control of postorchiopexy pain in pediatric ambulatory surgery // Anesthesiology. — 1987. — 66(6). — 8324.
12. Van Dijk M., de Boer J.B., Koot H.M. et al. The reliability and validity of the COMFORT scale as a postoperative pain instrument in 0 to 3yearold infants // Pain. —2000. — 84 (2–3). — 3677.
Источник
