Поражение легких при синдроме гудпасчера

Синдром Гудпасчера – аутоиммунная патология, характеризующаяся образованием аутоантител к базальным мембранам почечных клубочков и легочных альвеол. Клинически синдром Гудпасчера проявляется рецидивирующими легочными кровотечениями, прогрессирующим гломерулонефритом и почечной недостаточностью. Диагноз синдрома Гудпасчера подтверждается выявлением антител к базальной мембране клубочков (Anti GBM), данными биопсии почек и легких, рентгенологического исследования легких. Лечение синдрома Гудпасчера включает иммуносупрессивную терапию (глюкокортикостероиды, цитостатики), плазмаферез, по показаниям – гемодиализ, трансплантацию почек.
Общие сведения
Синдром Гудпасчера – иммуно-воспалительное поражение капилляров почек и легких, протекающее с развитием гломерулонефрита и геморрагического пневмонита. Впервые признаки данной патологии были описаны в 1919 г. американским патофизиологом Э.У. Гудпасчером, за что болезнь и была названа его именем. В ревматологии синдром Гудпасчера относится к системным васкулитам и нередко обозначается как «геморрагический легочно-почечный синдром», «геморрагическая пневмония с гломерулонефритом», «идиопатический гемосидероз легких с нефритом». Частота развития синдрома Гудпасчера составляет 1 случай на 1 млн. населения. Отмечается два возрастных пика заболеваемости – в 20-30 лет и 50-60 лет; болеют преимущественно мужчины. При отсутствии лечения синдрома Гудпасчера летальность среди пациентов достигает 75-90%.
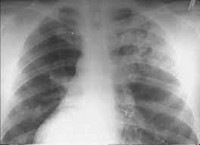
Синдром Гудпасчера
Причины синдрома Гудпасчера
Этиологические механизмы заболевания достоверно не определены. Клинические наблюдения указывают на связь развития синдрома Гудпасчера с перенесенной вирусной инфекцией (гриппом, вирусным гепатитом А и др.), приемом лекарственных препаратов (карбимазола, пеницилламина), производственными вредностями (вдыханием паров органических растворителей, лаков, бензина), переохлаждением, курением. Отмечена генетическая предрасположенность к данному синдрому у лиц–носителей HLA-DRwl5, HLA-DR4 и HLA-DRB1 аллелей. Описаны семейные случаи синдрома Гудпасчера.
Под воздействием того или иного этиологического фактора, в результате изменения толерантности иммунной системы, в организме начинается выработка аутоантител к базальным мембранам легочных альвеол и почечных клубочков. Предполагается, что в роли аутоантигена выступает структурный компонент а-3 цепи коллагена IV типа, присутствующий в базальных мембранах легочных и почечных капилляров. Сформировавшиеся антитела (GВМ-антитела) в присутствии С3-комплемента связываются с антигенами; образовавшиеся иммунные комплексы откладываются вдоль базальных мембран, индуцируя иммуно-воспалительное поражение почечных клубочков (гломерулонефрит) и альвеол (альвеолит). В развитии аутоиммунного воспаления большая роль принадлежит активации клеточных элементов (Т-лимфоцитов, эндотелиоцитов, моноцитов, альвеолярных макрофагов, полиморфноядерных лейкоцитов), цитокинов (инсулиноподобного, тромбоцитарного факторов роста, факторов некроза опухоли, интерлейкина-1), свободных радикалов, протеолитических ферментов и других факторов, повреждающих почечную и легочную ткань.
Патоморфологическими субстратами синдрома Гудпасчера служат геморрагический некротизирующий альвеолит и нефрозонефрит. При гистологическом исследовании почечной ткани обнаруживается пролиферативно-мембранозный, пролиферативный или некротизирующий гломерулонефрит, склероз клубочков и фиброз почечной паренхимы. Морфологическое исследование легочной ткани выявляет капиллярит межальвеолярных перегородок, легочные инфильтраты, гемосидероз, пневмосклероз.
Симптомы синдрома Гудпасчера
Выделяют три варианта клинического течения синдрома Гудпасчера: злокачественный, умеренный и медленный. Для злокачественного течения характерны рецидивирующая геморрагическая пневмония и стремительно прогрессирующий гломерулонефрит. При втором типе легочно-почечный синдром развивается медленнее и выражен умеренно. При третьем варианте синдрома Гудпасчера преобладают явления гломерулонефрита и ХПН; легочные проявления развиваются поздно.
Злокачественный вариант синдрома Гудпасчера дебютирует легочным кровотечением и острой почечной недостаточностью, требующими проведения интенсивной терапии (устранения водно-электролитных нарушений, возмещения кровопотери, ингаляций кислорода, ИВЛ, гемодиализа или перитонеального диализа). В других случаях заболевание может начинаться с общих симптомов: субфебрилитета, недомогания, похудания. Иногда появлению жалоб предшествует перенесенная ОРВИ. Из специфических симптомов обычно первыми развиваются признаки поражения легких – кашель, прогрессирующая одышка, цианоз, боль в грудной клетке, рецидивирующее кровохарканье или легочное кровотечение. Поражение легких при синдроме Гудпасчера нередко осложняется сердечной астмой и отеком легких.
Вскоре к легочным проявлениям добавляется почечная симптоматика: гематурия, олигурия, периферические отеки, артериальная гипертензия. У 10-15% пациентов синдром Гудпасчера манифестирует с клинических признаков гломерулонефрита. Во многих случаях течение заболевания сопровождается миалгиями, артралгиями, геморрагиями кожи и слизистых оболочек, интраретинальными кровоизлияниями, перикардитами.
Диагностика синдрома Гудпасчера
При осмотре пациентов с синдромом Гудпасчера обращает на себя внимание бледность кожных покровов, пастозность или отеки лица. В легких выслушиваются сухие и влажные хрипы, количество которых увеличивается в момент кровохарканья и после него. В общем анализе крови обнаруживается гипохромная анемия, анизоцитоз, пойкилоцитоз, лейкоцитоз, резкое увеличение СОЭ. Для общего анализа мочи характерна протеинурия, цилиндрурия, эритроцитурия; проба по Зимницкому выявляет изогипостенурию. В биохимическом анализе крови определяется нарастание уровня креатинина, мочевины, серомукоида; снижение концентрации железа. Для синдрома Гудпасчера типично обнаружение большого количества эритроцитов, сидерофагов и гемосидерина в общем анализе мокроты.
Наиболее чувствительным и специфичным методом диагностики синдрома Гудпасчера служит определение антител к базальной мембране клубочков (Anti-GBM) с помощью ИФА или РИА. На рентгенограммах легких выявляются множественные очаговые тени. Морфологическое подтверждение синдрома Гудпасчера основывается на данных биопсии легких и почек. Вспомогательное значение имеют результаты инструментальной диагностики: спирометрии, УЗИ почек, ЭКГ, ЭхоКГ.
В рамках проведения диагностических мероприятий необходимо исключить рак легких, туберкулез, бронхоэктазы, идиопатический гемосидероз легких, системную красную волчанку, узелковый периартериит, геморрагический васкулит, синдром Черджа-Стросс, гранулематоз Вегенера, микроскопический полиангиит, криоглобулинемию. Диагностика и лечение синдрома Гудпасчера должны проводиться совместными усилиями специалистов – ревматологов, пульмонологов, нефрологов.
Лечение и прогноз синдрома Гудпасчера
В остром периоде синдрома Гудпасчера показано назначение пульс-терапии метилпреднизолоном или комбинированной пульс-терапии (метилпреднизолон+циклофосфан) с последующим переводом на поддерживающую терапию после достижения клинико-лабораторной и рентгенологической ремиссии. С целью элиминации циркулирующих иммунных комплексов проводится плазмаферез. Симптоматическая терапия синдрома Гудпасчера включает переливания эритроцитарной массы и плазмы крови, назначение препаратов железа. При развитии терминальной почечной недостаточности применяются сеансы гемодиализа. Возможно выполнение нефрэктомии с последующей трансплантацией почки, однако это не исключает рецидива некротизирующего гломерулонефрита в трансплантате.
Течение синдрома Гудпасчера неуклонно прогрессирующее; прогноз – мало обнадеживающий. Гибель пациентов происходит, как правило, вследствие профузных легочных кровотечений, тяжелой почечной или дыхательной недостаточности. При злокачественном варианте летальный исход наступает в считанные недели; в остальных случаях средняя продолжительность жизни колеблется от нескольких месяцев до 1-3 лет. В литературе описаны единичные спонтанные ремиссии синдрома Гудпасчера.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 6 сентября 2018;
проверки требуют 12 правок.
Синдром Гудпасчера — системный капиллярит с преимущественным поражением альвеол лёгких и базальных мембран гломерулярного аппарата почек по типу геморрагических пневмонита и гломерулонефрита. Для СГ характерно бимодальное возрастное распределение заболеваемости с двумя пиками: первый в возрасте 20–30 с преобладанием у мужчин (страдают в три раза чаще[3][4]), характеризующийся более высокой частотой легочных кровотечений[5]. Второй пик характеризуется преобладанием женщин в возрасте 60–70 лет, страдающих почечнокаменной болезнью.[5]
Есть теория о наследственности болезни.[источник не указан 3193 дня]
Этиология и патогенез[править | править код]
Причина образования аутоантител против коллагена IV типа (к домену NC1 а3-цепи коллагена типа IV, необходимого для поддержания супраструктуры клубочков почек[3]) до сих пор неизвестна. Поскольку эпитопы (EA, EB[5][6]) коллагена, вызывающие образование антиколлагеновых антител, обычно находятся внутри молекулы гексамерного домена NC1, предполагается, что некоторые факторы окружающей среды демаскируют эпитопы[3][4], увеличивая связывание антител с a3 цепью до 15 раз[5]. Факторы возникновения заболевания неизвестны, однако отмечается связь с вирусной (в частности, вирус гриппа А[6]) и бактериальной инфекцией, переохлаждением, приёмом лекарственных препаратов (D-пенициллинамин[7], алемтузумаб[6], карбимазол), курением[6]. Первое описания болезни сделал американский врач и патофизиолог Э. У. Гудпасчер (E.W.Goodpasture) (1886–1960) во время эпидемии гриппа в 1919 году у 18-летнего юноши, у которого через месяц после перенесённого гриппа развились поражение почек в виде нефрита и пневмония, сопровождавшаяся кровохарканьем.
Клиника[править | править код]
Выделяют три варианта течения синдрома Гудпасчера:
- Злокачественный вариант характеризуется рецидивирующей геморрагической пневмонией и быстро прогрессирующим гломерулонефритом.
- С более медленным развитием изменений в почках и лёгких.
- С преобладанием прогрессирующего гломерулонефрита и быстрым развитием почечной недостаточности.
Начало острое с высокой лихорадкой, кровохарканьем или лёгочным кровотечением, одышкой. При аускультации отмечается рассеянные сухие и влажные хрипы в средних и нижних отделах лёгких.[8] При рентгенографии определяются рассеянные очаги уплотнения легочной ткани[3], либо множественные затемнения с нечеткими контурами[9], инфильтраты определяются в обоих лёгких, чаще в прикорневой и срединной зонах. Тяжёлый, прогрессирующий гломерулонефрит развивается почти одновременно, быстро приводя к почечной недостаточности. Повторные кровохарканье и потеря крови с мочой ведут, как правило, к анемии, усугубляющейся при почечной недостаточности. При лабораторном исследовании: анемия, увеличение количества лейкоцитов в крови и повышенная СОЭ. Характерным иммунологическим признаком болезни является наличие антител к базальным мембранам почки. Прогноз обычно неблагоприятен — смерть наступает в течение 12 месяцев от начала болезни при явлениях лёгочно-сердечной или почечной недостаточности.
Также имели место случаи с быстрым прогрессированием заболевания. Стадии от лихорадки до предсмертного состояния проходили в течение недели.
Изредка заболевание может начаться с поражения почек, а поражение лёгких развивается лишь в его конце. Нередко при этом поражение лёгких протекает без кровохарканья или оно очень скудное.[10]
Лечение[править | править код]
Для успешного лечения важна своевременная диагностика и ликвидация причинного фактора. Назначаются кортикостероиды в больших дозах (метилпреднизолон) в сочетании с цитостатическими препаратами (циклофосфамид). При сопутствующей анемии: препараты эритропоэтина, колониостимулирующие факторы, препараты железа. Успешно применяется плазмаферез и иммуноабсорбция.
- ↑ база данных Disease ontology (англ.) — 2016.
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 3 4 Robbins and Cotran pathologic basis of disease.. — 8th ed.. — Philadelphia, PA: Saunders/Elsevier, 2010. — xiv, 1450 pages с. — ISBN 978-1-4160-3121-5, 1-4160-3121-9, 978-0-8089-2402-9, 0-8089-2402-8, 978-1-4377-0792-2, 1-4377-0792-0.
- ↑ 1 2 Billy G. Hudson, Karl Tryggvason, Munirathinam Sundaramoorthy, Eric G. Neilson. Alport’s Syndrome, Goodpasture’s Syndrome, and Type IV Collagen (англ.) // New England Journal of Medicine. — 2003-06-19. — Vol. 348, iss. 25. — P. 2543–2556. — ISSN 1533-4406 0028-4793, 1533-4406. — doi:10.1056/NEJMra022296.
- ↑ 1 2 3 4 Patrick Nachman, Ashley Henderson. Pathogenesis of Lung Vasculitis (англ.) // Seminars in Respiratory and Critical Care Medicine. — 2011-06. — Vol. 32, iss. 03. — P. 245–253. — ISSN 1098-9048 1069-3424, 1098-9048. — doi:10.1055/s-0031-1279822.
- ↑ 1 2 3 4 Antonio Greco, Maria Ida Rizzo, Armando De Virgilio, Andrea Gallo, Massimo Fusconi. Goodpasture’s syndrome: A clinical update (англ.) // Autoimmunity Reviews. — 2015-03. — Vol. 14, iss. 3. — P. 246–253. — doi:10.1016/j.autrev.2014.11.006.
- ↑ Болезни органов дыхания: Руководство для врачей В 4 томах. Частная пульмонология. / под ред. Палеева Н. Р.. — М.: Медицина, 1990. — Т. 4. — С. 49—50. — ISBN 5-225-01159-4.
- ↑ Кумар В, Аббас А. К. Основы патологии заболеваний по Роббинсу и Котрану. — Логосфера, 2016. — Т. 2. — С. 806—807, 1037—1038, 1045. — ISBN 978-5-98657-053-2.
- ↑ Шабалов Н. П. Детские болезни: учебник для вузов. — 6-е изд. — Питер, 2011. — Т. 1. — С. 497, 499. — ISBN 978-5-459-00609-4. — ISBN 978-5-459-00608-7.
- ↑ В. Е. Кочетов. К вопросу отдельных форм легочных геморрагических синдромов // Вестник экстренной медицины. — 2019. — Т. 12, вып. 2. — ISSN 2010-9881.
Источник
Медицинский эксперт статьи

х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Синдром Гудпасчера – аутоиммунный синдром, включающий альвеолярное легочное кровотечение и гломерулонефрит, вызванный циркулирующими анти-GBM-антителами. Синдром Гудпасчера чаще всего развивается у людей с наследственной предрасположенностью, которые курят сигареты, но возможными дополнительными факторами являются вдыхание углеводорода и вирусные инфекции дыхательных путей. Симптомы синдрома Гудпасчера включают одышку, кашель, усталость, кровохарканье и/или гематурию. Синдром Гудпасчера подозревается у пациентов с кровохарканьем или гематурией и подтверждается наличием анти-GВМ-антител в крови. Лечение синдрома Гудпасчера включает плазмаферез, глюкокортикоиды и иммунодепрессанты типа циклофосфамида. Прогноз благоприятен, если лечение начато до развития дыхательной или почечной недостаточности.
Синдром Гудпасчера впервые описано Гудпасчером в 1919 году. Синдром Гудпасчера представляет собой комбинацию гломерулонефрита и альвеолярного кровотечения в присутствии анти-GВМ-антител. Синдром Гудпасчера чаще всего проявляется сочетанием диффузного альвеолярного кровотечения и гломерулонефрита, но иногда вызывает изолированный гломерулонефрит (10-20 %) или поражение легких (10 %). Мужчины болеют чаще, чем женщины.
 [1], [2], [3], [4], [5]
[1], [2], [3], [4], [5]
Что вызывает синдром Гудпасчера?
Причина заболевания точно не установлена. Предполагается генетическая предрасположенность к синдрому Гудпасчера, ее маркером считают наличие HLA-DRW2. Существует точка зрения о возможной роли перенесенной вирусной инфекции (вирус гепатита А и др. вирусные заболевания), производственных вредностей, лекарственных препаратов (прежде всего D-пеницилламина).
Основой патогенеза синдрома Гудпасчера является образование аутоантител к базальным мембранам капилляров клубочков почек и альвеол. Эти антитела относятся к классу IgG, они связываются с антителами базальных мембран в присутствии С3-компонента комплемента с последующим развитием иммунного воспаления почек и альвеол легких.
Анти-GВМ-антитела направлены против неколлагенового (NC-1) домена аЗ цепи коллагена IV типа, который в наиболее высокой концентрации находится в базальных мембранах почечных и легочных капилляров. Воздействие экологических факторов – курения, вирусных ОРЗ и вдыхания гидрокарбонатных взвесей (более часто) – и, менее часто, пневмонии активизирует презентацию антигенов альвеолярных капилляров циркулирующим антителам у людей с наследственной предрасположенностью (наиболее часто это носители HLA-DRwl5, – DR4 и – DRB1 аллелей). Циркулирующие анти-GВМ-антитела связываются с базальными мембранами, фиксируют комплемент и вызывают клеточный воспалительный ответ, приводящий к развитию гломерулонефрита и/или легочного капиллярита.
Вероятно, существует определенная общность ауто-антигенов базальной мембраны капилляров клубочков почек и альвеол. Аутоантиген формируется под влиянием повреждающего действия этиологического фактора. Неизвестный этиологический фактор повреждает и модифицирует структуру базальных мембран почек и легких. Экскреция образовавшихся продуктов деградации базальных мембран клубочков почек при их поражении замедляется и уменьшается, что, естественно, создает предпосылки для развития аутоиммунного поражения почек и легких До сих пор окончательно неизвестно, какой компонент базальной мембраны становится ауто-антигеном. В настоящее время предполагается, что это внутренний структурный компонент базальной мембраны клубочка почки а3-цепь коллагена 4 типа.
Сформировавшиеся иммунные комплексы откладываются вдоль базальных мембран капилляров клубочков, что приводит к развитию иммуновоспалительного процесса в почечном клубочке (гломерулонефрит) и альвеолах (альвеолит). Основными клетками, принимающими участие в развитии этого иммунного воспаления, являются Т-лимфоциты, моноциты, эндотелиоциты, полиморфноядерные лейкоциты, альвеолярные макрофаги. Взаимодействие между ними обеспечивается молекулярными медиаторами, цитокинами (факторы роста – тромбоцитарный, инсулиноподобный, b-трансформирующий; интерлейкин-1, фактор некроза опухоли и др ). Большую роль в развитии иммунного воспаления играют метаболиты арахидоновой кислоты, свободные радикалы кислорода, протеолитические ферменты, адгезивные молекулы.
В развитии альвеолита при синдроме Гудпасчера огромное значение имеет активация альвеолярных макрофагов. В активированном состоянии они выделяют около 40 цитокинов. Цитокины I группы (хемотаксины, лейкотриены, интерлейкин-8) усиливают поступление полиморфноядерных лейкоцитов в легкие. Цитокины II группы (факторы роста – тромбоцитарный, макрофагальный) способствуют перемещению в легкие фибробластов. Альвеолярные макрофаги продуцируют также активные формы кислорода, протеазы, повреждающие легочную ткань.
Патоморфология синдрома Гудпасчера
Основными патоморфологическими проявлениями синдрома Гудпасчера являются:
- преимущественное поражение микроциркуляторного русла почек и легких. В легких наблюдается картина венулитов, артериолитов, капилляритов с выраженными явлениями деструкции и пролиферации; поражение капилляров наблюдается преимущественно в межальвеолярных перегородках, развивается альвеолит с геморрагическим экссудатом в альвеолах. Поражение почек характеризуется развитием экстракапиллярного пролиферативного гломерулонефрита с последующим формированием гиалиноза и фиброза, что приводит к развитию почечной недостаточности;
- выраженные внутриальвеолярные кровоизлияния;
- развитие гемосидероза легких и пневмосклероза различной степени выраженности, как итог эволюции альвеолита.
Симптомы синдрома Гудпасчера
Заболевание чаще всего начинается с клинических проявлений легочной патологии. Кровохарканье – наиболее заметный симптом; однако кровохарканье может отсутствовать при наличии геморрагических проявлений, и у пациента могут обнаруживаться только инфильтративные изменения на рентгенографии грудной клетки или инфильтрат и респираторный дистресс-синдром и/или недостаточность. Часто развиваются одышка (преимущественно при физической нагрузке), кашель, недомогание, снижение трудоспособности, боль в грудной клетке, лихорадка и потеря массы тела. До 40 % пациентов имеют макрогематурию, хотя легочное кровотечение может предшествовать почечным проявлениям на недели и годы.
Во время кровохарканья одышка может увеличиваться. Беспокоит также слабость, снижение трудоспособности.
Симптомы синдрома Гудпасчера варьируют в течение долгого времени в диапазоне от чистых легких при аускультации до трескучих и сухих хрипов. У некоторых пациентов наблюдаются периферические отеки и бледность вследствие анемии.
При осмотре обращает на себя внимание бледность кожи, цианоз слизистых оболочек, пастозность или выраженные отеки лица, снижение мышечной силы, потеря массы тела. Температура тела обычно повышена до фебрильных цифр.
При перкуссии легких может определяться укорочение перкуторного звука над обширными очагами легочных кровоизлияний, но это наблюдается редко, чаще изменений перкуторного звука нет.
Характерным аускультативным признаком синдрома Гудпасчера являются сухие и влажные хрипы, количество их значительно увеличивается во время или после кровохарканья.
При исследовании сердечно-сосудистой системы выявляется артериальная гипертензия, возможно увеличение границы относительной тупости сердца влево, приглушенность сердечных тонов, негромкий систолический шум, при развитии тяжелой почечной недостаточности появляется шум трения перикарда. При прогрессирующем поражении почек на фоне значительной артериальной гипертензии возможно развитие острой левожелудочковой недостаточности с картиной сердечной астмы и отека легких. Обычно эта ситуация развивается в терминальной стадии заболевания.
Как правило, поражение почек проявляется позже, спустя определенное время после развития легочной симптоматики. Характерными клиническими признаками почечной патологии являются гематурия (иногда макрогематурия), быстро прогрессирующая почечная недостаточность, олигоанурия, артериальная гипертензия.
В 10-15% случаев синдром Гудпасчера начинается с клинических признаков почечной патологии – появляется клиника гломерулонефрита (олигурия, отеки, артериальная гипертензия, выраженная бледность), а затем присоединяются симптомы поражения легких. У многих больных могут иметь место миалгии, артралгии.
Независимо от вариантов начала синдром Гудпасчера в большинстве случаев протекает тяжело, заболевание неуклонно прогрессирует, развивается тяжелая легочная и почечная недостаточность. Длительность жизни больных от начала заболевания колеблется от нескольких месяцев до 1-3 лет. Чаще всего больные погибают от уремии или легочного кровотечения.
Диагностика синдрома Гудпасчера
Диагноз синдрома Гудпасчера требует выявления сывороточных анти-GВМ-антител методом непрямой иммунофлюоресценции или, если имеется возможность, прямым твердофазным иммуноферментным анализом (ИФА) с рекомбинантным человеческим NC-1 аЗ. Другие серологические тесты, например тест на антиядерные антитела (ANA), применяются для выявления СКВ, титр антистрептолизина-О – для выявления постстрептококкового гломерулонефрита, который может быть причиной многих случаев легочно-почечного синдрома. ANCA положительны (в периферических образцах) в 25 % случаев синдрома Гудпасчера. При наличии гломерулонефрита (гематурия, протеинурия, сладжи эритроцитов в анализе мочи и/или почечная недостаточность) может назначаться биопсия почек. Быстро прогрессирующий фокальный сегментарный некротизирующий гломерулонефрит с прогрессирующим течением обнаруживается при биопсии при синдроме Гудпасчера и всех остальных причинах легочно-почечного синдрома. Иммунофлюоресцентное окрашивание почечной или легочной ткани классически выявляет линейное отложение IgG вдоль гломерулярных или альвеолярных капилляров. Это также встречается при диабетической почке и фибриллярном гломерулонефрите – редком заболевании, вызывающем легочно-почечный синдром, но фиксация GBM-антител при этих заболеваниях неспецифична.
Исследования функции легких и бронхоальвеолярный лаваж не являются диагностическими при синдроме Гудпасчера, но могут использоваться для подтверждения наличия диффузной альвеолярной геморрагии у пациентов с гломерулонефритом и легочными инфильтратами, но без кровохарканья. Лаважная жидкость, которая остается геморрагической после многократных промываний, позволяет подтвердить диффузный геморрагический синдром, особенно при сопутствующем снижении гематокрита.
 [6], [7]
[6], [7]
Лабораторная диагностика синдрома Гудпасчера
- Общий анализ крови. Характерны железодефицитная гипохромная анемия, гипохромия, анизоцитоз, пойкилоцитоз эритроцитов. Наблюдается также лейкоцитоз, сдвиг лейкоцитарной формулы влево, значительное увеличение СОЭ.
- Общий анализ мочи. В моче обнаруживаются белок (степень протеинурии может быть значительной), цилиндры (зернистые, гиалиновые, эритроцитарные), эритроциты (может быть макрогематурия). По мере прогрессирования хронической почечной недостаточности снижается относительная плотность мочи, в пробе по Зимницкому развивается изогипостенурия.
- Биохимический анализ крови. Наблюдается повышение содержания в крови мочевины, креатинина, гаптоглобина, серомукоида, а2 и гамма-глобулинов, снижение содержания железа.
- Иммунологические исследования. Может обнаруживаться снижение количества Т-лимфоцитов-супрессоров, выявляются циркулирующие иммунные комплексы. Антитела к базальной мембране капилляров клубочков и альвеол выявляются методом непрямой иммунофлюоресценции или радиоиммунологическим методом.
- Анализ мокроты. В мокроте много эритроцитов, обнаруживается гемосидерин, сидерофаги.
Инструментальная диагностика синдрома Гудпасчера
- Рентгенологическое исследование легких. Характерными рентгенологическими признаками являются легочные инфильтраты в прикорневой области с распространением на нижние и средние отделы легких, а также прогрессирующие, симметричные двусторонние облаковидные инфильтраты.
- Исследование функции внешнего дыхания. Спирография выявляет рестриктивный тип дыхательной недостаточности (снижение ЖЕЛ), по мере прогрессирования заболевания присоединяется обструктивный тип дыхательной недостаточности (снижение ОФВ1, индекса Тиффно).
- ЭКГ. Выявляются признаки выраженной миокардиодистрофии анемического и гипоксического генеза (снижение амплитуды зубцов Т и интервала ST во многих отведениях, чаще в левых грудных). При выраженной артериальной гипертензии появляются признаки гипертрофии миокарда левого желудочка.
- Исследование газового состава крови. Выявляется артериальная гипоксемия.
- Исследование биоптатов легких и почек. Биопсия легочной ткани (открытая биопсия) и почек производится для окончательной верификации диагноза, если невозможно точно диагностировать заболевание неинвазивными методами. Выполняется гистологическое и иммунологическое исследование биоптатов. Характерными для синдрома Гудпасчера являются следующие признаки:
- наличие морфологических признаков гломерулонефрита (чаще всего экстракапиллярного), геморрагического альвеолита, гемосидероза и интерстициального фиброза;
- выявление иммунофлюоресцентным методом линейных отложений IgG и С3-компонента комплемента на базальных мембранах легочных альвеол и почечных клубочков.
Диагностические критерии синдрома Гудпасчера
При постановке диагноза синдрома Гудпасчера целесообразно пользоваться следующими критериями.
- Сочетание легочной патологии и патологии почек, т.е. кровохарканья (нередко легочного кровотечения), одышки и симптоматики гломерулонефрита.
- Неуклонно прогрессирующее течение заболевания с развитием дыхательной и почечной недостаточности.
- Развитие железодефицитной анемии.
- Выявление при рентгенологическом исследовании легких множественных двусторонних облаковидных инфильтратов на фоне сетчатой деформации легочного рисунка.
- Обнаружение в крови высоких титров циркулирующих антител к базальной мембране почечных клубочков и альвеол.
- Обнаружение линейных депозитов IgG и С3-компонента комплемента на базальных мембранах капилляров клубочков и альвеол.
- Отсутствие других системных (кроме легочных и почечных) проявлений.
 [8], [9], [10], [11], [12]
[8], [9], [10], [11], [12]
Дифференциальная диагностика синдрома Гудпасчера
Синдром Гудпасчера приходится дифференцировать с рядом заболеваний, проявляющихся кровохарканьем или легочным кровотечением. Необходимо исключать онкологические заболевания бронхов и легких, туберкулез, абсцессы легких, бронхоэктазы, болезни сердца и сосудов (приводящие к застою и гипертензии в малом круге), системные васкулиты, геморрагические диатезы.
 [13], [14], [15], [16], [17]
[13], [14], [15], [16], [17]
Программа обследования при синдроме Гудпасчера
- Общие анализы крови, мочи.
- Биохимический анализ крови: определение содержания общего белка и белковых фракций, креатинина и мочевины, трансаминаз, серомукоида, гаптоглобина, фибрина, железа.
- Анализ мокроты: цитологическое исследование, определение сидерофагов.
- Иммунологические исследования: определение содержания В- и Т-лимфоцитов, субпопуляций Т-лимфоцитов, иммуноглобулинов, циркулирующих иммунных комплексов, антител к базальным мембранам клубочков почек и альвеол.
- Рентгенологическое исследование легких.
- ЭКГ.
- Спирография.
- Исследование биоптатов легких и почек.
Какие анализы необходимы?
Лечение синдрома Гудпасчера
Лечение синдрома Гудпасчера включает ежедневный или проводимый через день плазмаферез в течение 2-3 нед (плазмозамещение 4 л) для удаления aHTH-GBM-антител в сочетании с внутривенным введением глюкокортикоидов (обычно метилпреднизолон 1 г в течение не менее 20 мин через день 3 раза с преднизолоном по 1 мг/кг массы тела ежедневно) и циклофосфамида (2 мг/кг 1 раз в сутки) на протяжении 6-12 мес, чтобы предотвратить формирование новых антител. Терапия может быть уменьшена, когда прекращается улучшение легочной и почечной функции. Отдаленная смертность связана со степенью нарушения функции почек в начале заболевания; пациенты, требующие диализа в самом начале, а также те, кто имел более 50 % нефронов с полумесяцами на биопсии, имеют выживаемость менее 2 лет и часто требуют диализа, если не проводится трансплантация почек. Кровохарканье может быть хорошим прогностическим признаком, поскольку приводит к более раннему обнаружению заболевания; меньшинство пациентов, которые являются ANCA-положительными, лучше отвечают на лечение синдрома Гудпасчера. Рецидив встречается в малом проценте случаев и связан с продолжением курения и инфекцией дыхательных путей. У пациентов с терминальной стадией почечной недостаточности, которым была проведена трансплантация почек, заболевание может рецидивировать в трансплантате.
Какой прогноз имеет синдром Гудпасчера?
Синдром Гудпасчера часто быстро прогрессирует и может быть фатальным, если не проводятся быстрая диагностика и лечение синдрома Гудпасчера; прогноз благоприятен, когда лечение начинается до развития дыхательной или почечной недостаточности.
Непосредственная выживаемость в момент легочного кровотечения и дыхательной недостаточности связана с обеспечением проходимости дыхательных путей; эндотрахеальное зондирование и искусственная вентиляция легких рекомендуются пациентам с пограничным уровнем газов артериальной крови и угрожающей дыхательной недостаточностью.
Источник
