Порочный круг и синдром приводящей петли
Синдром приводящей петли. Демпинг-синдромСиндром приводящей петли может быть результатом погрешностей в оперативной технике, а также спаечного процесса, когда эвакуация из приводящей петли затруднена. Гораздо чаще причиной этого страдания бывают нарушения функции двенадцатиперстной кишки. Наиболее часто патология возникает в течение первого года после операции, реже — в отдаленные сроки. Заболевание проявляется чувством тяжести и болями в эпигастрии, больше справа, рвотой желчью или желчью с пищей. После рвоты, как правило, наступает облегчение. Нередко заболевание сочетается с грыжей пищеводного отверстия диафрагмы, и тогда в клинической картине проявляются такие симптомы, как срыгивание, отрыжка, изжога, загрудинные боли. Различают три степени тяжести синдрома: легкую, которая проявляется чувством тяжести, небольшими болями и периодически рвотой желчью, среднюю, когда симптомы заболевания выражены резче, и тяжелую—при крайней их выраженности (интенсивные боли, регулярная рвота, похудание, слабость). У ряда больных со временем клинические проявления заболевания уменьшаются. Диагностика проводится на основании характерной клинической картины. Рентгенологическое исследование не имеет решающего значения, так как попадание бария в приводяшее колено анастомоза наблюдается после резекции желудка у многих больных, не страдающих синдромом приводящей петли. Консервативная терапия при синдроме легкой и средней степени тяжести обычно дает хороший эффект. Следует ограничить прием пищи, которая провоцирует синдром (молочные продукты, сладкое). Питаться больной должен небольшими порциями 5—6 раз в день.
Хороший эффект дает переливание крови, белковых препаратов, аминокислот, витаминов. Большую пользу может принести санаторно-курортное лечение. Демпинг-синдром является наиболее частой патологией оперированного желудка. Несомненно, что причинными факторами в развитии этого синдрома служат удаление важной секретирующей зоны и ликвидация привратникового регулирующего механизма. Чаще демпинг-синдром наблюдается у больных с различного рода психоневрологическими изменениями и выраженными вегетативными расстройствами, у которых общие проявления язвенной болезни доминируют над местными. Отмечено, что после резекции желудка по методу Бильрот I демпинг-синдром развивается реже, чем после операции по Бильрот II; имеет значение ликвидация дуоденального пассажа. Определенная роль в патогенезе демпинг-синдрома принадлежит, по-видимому, декомпенсации отводящей петли анастомоза. Клиника демпинг-снндрома характеризуется приступами слабости, наступающими вслед за приемом пищи, как правило, сладкой или молочной. Больные жалуются также на чувство жара, холодный нот, головокружение, сердцебиение, стеснение в груди, тахикардию. В тяжелых случаях возможен обморок. При легком демпинг-синдроме приступы слабости наблюдаются лишь периодически после приема значительного количества сладостей. Диагностика демпинг-синдрома основана па клинических проявлениях. Из рентгенологических признаков имеет значение выявляемая ускоренная эвакуации при наличии клиники демпинг-синдрома. Консервативная терапия предусматривает те же мероприятия, что и при синдроме приводящей петли. Следует значительно ограничить прием пищевых продуктов, которые провоцируют появление демпинг-синдрома. Обычно это сладкая и молочная пища. Отмечено, что подобные больные хорошо переносят более грубую пищу: мясо, рыбу, и том числе соленую, овощи, квашеную капусту. Диету следует подбирать индивидуально, потому что нередко больные плохо переносят один — два определенных вида пищи. Главное, чтобы питание было регулярным, частым и небольшими порциями. Санаторно-курортное лечение также весьма-полезно. Рациональное консервативное лечение у большинства больных дает хороший эффект, в некоторых случаях даже при тяжелом демпинг-синдроме. При безуспешности консервативного лечения показана операция. Если позволяют условия, выполняют реконструкцию операции Бильрот II и Бильрот I. Больным с гистаминрезистентной ахлоргидрией показана реконструктивная гастродуоденоеюнопластика. Эта операция позволяет получить хороший отдаленный результат у 80% больных. – Также рекомендуем “Доброкачественные опухоли желудка. Неэпителиальные опухоли желудка” Оглавление темы “Язвенная болезнь желудка. Опухоли желудка”: |
Источник
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Введение
Синдром приводящей петли является послеоперационным осложнением, которое наблюдается в ближайшем или отдаленном периоде после резекции желудка и различных операций наложения гастроэнтероанастомоза. Он обусловлен нарушением опорожнения 12-перстной кишки, что приводит к характерным расстройствам: боли в правом верхнем квадранте живота после еды и обильная рвота желчью, приносящая облегчение (С.П. Сазонов, 1976). Различают острый и хронический синдром приводящей петли механической и функциональной природы (В.В. Сергеев, 1973). Для его диагностики используются в основном различные рентгенологические и эндоскопические методы, однако имеются единичные сообщения о применении эхографии в распознавании синдрома приводящей петли (Y.T. Ko и соавт, 1993). Кроме того, ультразвуковое исследование (УЗИ) позволяет выявить различные сопутствующие заболевания, например гепатобилиарной системы. Приводим наше наблюдение синдрома приводящей петли, в котором расширенная петля 12-перстной кишки симулировала “забрюшинную кисту”.
Описание случая
Больная 50 лет поступила в МНРЦ с жалобами на боли в эпигастрии с иррадиацией в поясничную область, тошноту, слабость, которые постепенно увеличивались на протяжении последних 2-х недель. За 5 лет до этого больной проведено комбинированное лечение по поводу рака желудка,которое включало предоперационное облучение и операцию (субтотальная резекция желудка с формированием позадиободочного гастроэнтероанастомоза и межкишечным соустьем по Брауну и его фиксацией в окне брыжейки). При динамическом наблюдении на протяжении 5 лет признаков рецидива,метастазов в печень и регионарные лимфатические узлы не определялось.
Проведено комплексное рентгенэндоскопическое и ультразвуковое обследование. При рентгеноскопии желудочно-кишечного тракта культя желудка обычной формы, желудочно-кишечный анастомоз свободно проходим,отводящая петля тонкой кишки без изменений. При релаксационной энтерографии изображение межкишечного анастомоза и 12-перстной кишки не получено. Гастроскопия: культя желудка не увеличена, в ней небольшое количество слизи, слизистая на большом протяжении атрофирована, анастомоз широкий, слизистая передней стенки гиперемирована, отечна, воспалительные изменения распространяются на стенку тонкой кишки. В легких патологических изменений не выявлено.
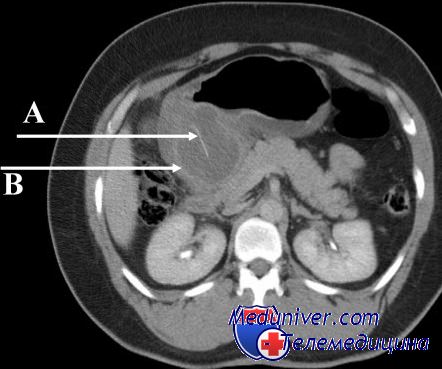
При УЗИ в печени патологических изменений не выявлено, желчные протоки и сосуды печени не расширены. Желчный пузырь увеличен в размерах – 10,4 x 4 x 6 см, стенки не утолщены, в нем определяется слой сгущенной желчи. Спустя 45 мин. после приема стандартного желчегонного завтрака отмечено незначительное сокращение желчного пузыря до 9,5 x 5,5 см. Поджелудочная железа смещена кверху и тесно прилежит к культе желудка. Размеры железы не увеличены, контуры местами нечеткие, вирсунгов проток не расширен, узловых и кистозных образований не выявлено. Кзади и ниже поджелудочной железы определяется полостное образование неправильной овальной формы величиной 13,6 x 4,8 см с наличием эхопрозрачного жидкого содержимого (рис. 1). При эхоскопии через различные промежутки времени размеры и форма образования, его содержимое даже после изменения положения больной оставались стабильными. Данное образование было расценено как “послеоперационная забрюшинная киста” и проведена пункция под ультразвуковым контролем. Эвакуировано 150 мл жидкости светло-зеленого цвета с наличием хлопьевидных образований. После пункции отмечено значительное уменьшение размеров “кисты” (рис. 2). Биохимическое исследование полученного содержимого: общий билирубин – 77,1, щелочная фосфатаза – 691, амилаза – 205, АЛТ – 28, АСТ – 23, рН – 7,0, белок не определяется, реакция на билирубин положительная. Микроскопия: билирубинат кальция в значительном количестве, множественные бактерии. Цитологическое исследование пунктата: клеточные элементы не обнаружены.

Рис. 1. Панорамная эхограмма брюшной полости в поперечной проекции. Отчетливо определяется полостное образование овальной формы с эхопрозрачным содержимым. Желчный пузырь (стрелка).
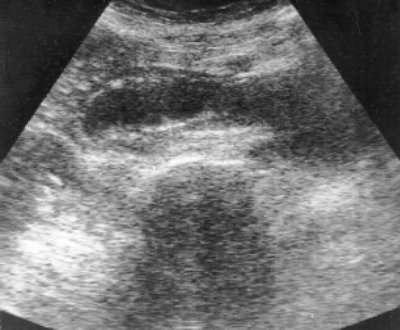
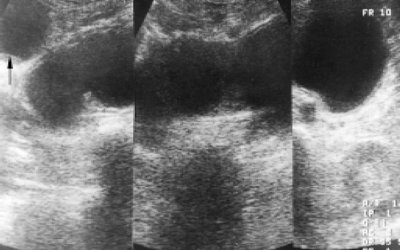
Рис. 2. Уменьшение размеров “кисты” после аспирации содержимого под ультразвуковым контролем.
При последующей операции выявлены следующие изменения: в брюшной полости умеренный спаечный процесс, печень без изменений, желчный пузырь увеличен в обьеме, напряжен, при пальпации опорожняется. В брыжейке тонкой кишки выявлены единичные увеличенные лимфатические узлы, в зоне брауновского соустья определяется конгломерат, вовлекающий в себя брауновский анастомоз, участок поперечно-ободочной кишки, приводящую петлю тонкой кишки. Дистальная часть 12-перстной кишки резко расширена за счет содержания желчи (рис. 3). Морфологическое исследование операционного материала: в лимфатическом узле – реактивные изменения, в жировой клетчатке – сочетанное хроническое воспаление с выраженным фиброзом и очагами гнойного воспаления, в 12-перстной кишке и толстой кишке – хронические язвы с выраженным фиброзом стенки. Элементов опухоли не обнаружено. Проведена реконструктивная операция.
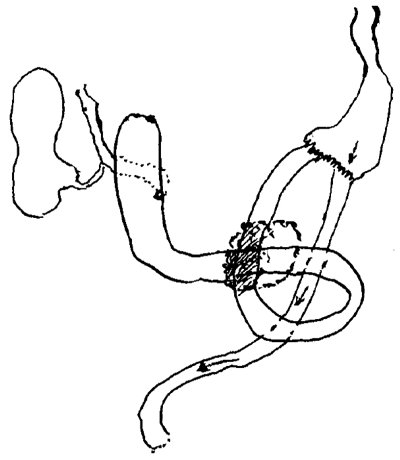
Рис. 3. Схема расположения воспалительного инфильтрата, вызвавшего сдавление 12-перстной кишки.
Обсуждение
Синдром приводящей петли после различных операций может быть обусловлен различными причинами: рецидивом опухоли, внутренней грыжей, краевыми язвами или спайками (А.Ф. Черноусов и соавт., 1995, S.R. Wilson, 1991). По данным Y.T. Ko и соавт. (1993), расширенная петля 12-перстной кишки легко распознается, так как она располагается в правой верхней половине живота и продолжается в медиальном направлении, при этом на уровне средней линии она располагается кзади от пересекающих ее брыжеечных сосудов, что наблюдается при артериомезентериальной компрессии 12-перстной кишки. Это положение верно при отсутствии ранее выполненных интраабдоминальных операций, так как после них наблюдаются самые различные осложнения в виде “полостных образований”: накопление жидкости в малой сальниковой сумке, гематомы, кисты и другие образования (P.R. Mueller et al., 1985).
В приведенном случае трудность дифференциальной диагностики расширенной петли 12-перстной кишки от различных послеоперационных осложнений была обусловлена следующими причинами: отсутствием в приводящей кишке комочков пищи и пузырьков газа, при этом прозрачность содержимого “кисты” сохранялась даже при изменении положения больной; полным отсутствием перистальтики и складок слизистой. Ранее было отмечено, что при длительной обструкции в расширенном сегменте тонкой кишки перистальтика может не определяться, что затрудняет дифференциацию паралитической непроходимости от механической. Кроме того, рентгенологические исследования могут быть неэффективными, так как на обзорном снимке патологические изменения могут не всегда определяться, а приводящая петля может не заполняться бариевой взвесью (D.H. Lee и соавт., 1991). Мы полагаем, что в этих случаях аспирация содержимого подобных “кистозных образований” под ультразвуковым контролем и его тщательное лабораторно-биохимическое исследование позволяют установить правильный диагноз.
Литература
- Сергеев В.В. Хронический синдром приводящей петли после резекции желудка. Дисс… канд. мед. наук. – М., 1973.
- Сазонов С.П. О причинах механического синдрома приводящей петли после резекции желудка при язвенной болезни//Вестник хирургии. – 1976. – 12. – С.27-30.
- Черноусов А.Ф, Богопольский П.М, Аба М. Диагностика и лечение синдрома приводящей петли//Хирургия. – 1995. – 1. – С.41-45.
- Ko Y.T., Lim J.H., Lee D.H. et al. Small bowel obstruction: sonographic evaluation. Radiology, 1993, 3, р.649-653.
- Lee D.H., Lim J.H., Ko Y.T. Afferent loop syndrome: sonographic findings in seven cases AJR, 1991, 157, 1, р.41-43.
- Mueller P.R., Ferrucci J.T., Simeone J.F. et al. Lesser sac abscesses and fluid collections: drainage by transhepatic approach. Radiology. 1985, 155, р.615-618.
- Wilson S.R. The gastrointestinal tract. In: Rumack C.M., Wilson S.R., Charboneau J.W. (eds). “Diagnostic ultrasound”, St.Louis, Mo Mosby, 1991, р.181-206.

УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Источник
Синдром приводящей петли. Кровотечение из гастроеюноанастомоза.
Синдром приводящей петли – редкое осложнение резекции желудка по Billroth II, которое обычно обусловлено избыточным накоплением желчных и панкреатических секретов в приводящей петле. Это осложнение обычно возникает в результате дефектов техники наложения гастроеюнального анастомоза, и очень редко синдром обусловлен слипанием кишки в результате перегиба приводящей петли, который служит препятствием для оттока застойного содержимого петли. У некоторых пациентов часть потребляемой жидкости может затекать в приводящую петлю и значительно увеличивать количество ее содержимого.
Больные обычно предъявляют жалобы на чувство переполнения в животе и боль в эпигастрии, сопровождающуюся рвотой, которая приносит облегчение. Рвота может быть многократной и содержать остатки пищи. Синдром приводящей петли может появиться через несколько дней после операции или в отдаленные сроки.
Этот синдром впервые был описан Mimpris и Birt в 1948 году и, позднее, — Wellj и Welbourn. Согласно Alexander-Williny, он объясняется не только накоплением желчи и секрета поджелудочной железы в приводящей петле, но и наличием гастрита с пониженной кислотностью. Как Jordan так и Herington утверждают, что синдром приводящей петли необходимо дифференцировать с гастритом с пониженной кислотностью. Кданному заключению пришли также Du-Plessis, Janson, Bushkin, Danlgren идругие.
Клинические проявления синдрома приводящей петли незначительны, но в случае, когда интенсивность и частота симптомов увеличиваются, может потребоваться хирургическое вмешательство.
Для лечения этого осложнения предложено несколько операций. Одна из них— выведение петли тощей кишки между культей желудка и даенадцатиперстной кишкой по Henley, причем эту операцию всегда следует дополнять стволовой ваготомией. Была предложена также реконструкция анастомоза по Billroth II в вариант с анастомозом по Roux-en-Y или перевод Billroth II в Billroth I. Последний вариант, вероятно, более предпочтителен. Одна из этих операций будет описана ниже.
В случае, когда тяжелое состояние пациента обусловлено частой и обильной рвотой, некоторые хирурги накладывают простой анастомоз между приводящей и отводящей петлей (еюноеюностомия по Braim). Хотя эта операция и не является оптимальной, ее все же можно выполнять в неотложных случаях. Вместе с тем анастомоз по Braun благоприятствует развитию язв анастомоза, так как щелочной секрет поджелудочной железы и желчь будут проходить не через гастроеюностому, а через Брауновское соустье.
Кровотечение из гастроеюноанастомоза.
Послеоперационное кровотечение из линии швов, наложенных между желудком и тощей кишкой, — редкое осложнение, развивающеея при неправильном наложении шва. Кровотечение возникает в раннем послеоперационном периоде и его источником являются подслизистые артериолы желудка. При их пересечеш-ш эти артериолы обильно кровоточат. Если не перевязать хотя бы один из этих сосудов, это может привести к смерти больного. Поэтому один из важнейших моментов в технике резекции желудка это отдельная перевязка каждой под слизистой артериолы до пересечения желудка.
В течение первого дня после операции по зонду Levine отделяется серозно-геморрагическая жидкость, которая позднее меняется на окрашенную желчью. Если по зонду вместо серозно-геморрагической жидкости продолжает истекать кровь, это означает, что кровотечение продолжается. В этом случае желудок следует промыть холодной водой. Если потеря крови продолжается, необходимо переливать больному одну или более порции крови, назначить Н2-блокаторы (ранитидин) или ингибиторы протоновго насоса (омепразол). Следует попытаться остановить кровотечение эндоскопическими методами (электрокоагуляция или лазерная фотокоагуляция). Если кровотечение не удается остановить эндоскопически, необходимо оперативное вмешательство.
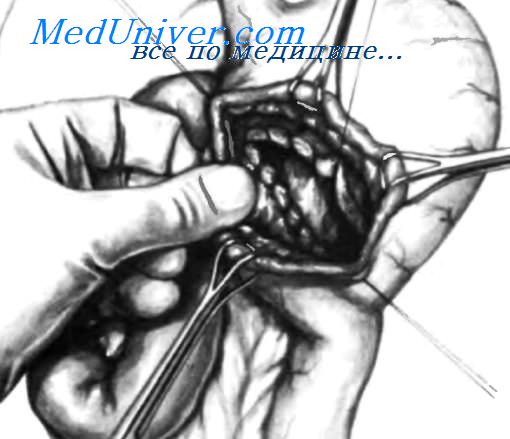
В большинстве случаев гемостаз может быть достигнут без рассечения апоневроза между желудком и тощей кишкой, а путем вскрытия передней стенки желудка параллельно анастомозу на 3—4 см выше него. После рассечения стенки желудка руками извлекают оставшиеся сгустки крови и обследуют полость желудка, чтобы исключить возможность кровотечения из не замеченной хирургом поверхностной язвы желудка. Осмотрев линию шва. осуществляют гемостаз по методике Nissen, которая успешно используется различными хирургами. Далее мы приводим ее описание.
После рассечения брюшины брюшную полость изолируют салфетками во избежание ее инфицирования. Поперечный разрез начинают на передней стенке желудка на 3-4 см выше линии шва между желудком и тощей кишкой. Двумя руками извлекают сгустки крови. Не рекомендуется аспирировать содержимое желудка с помощью металлической канюли, так как это может спровоцировать диффузное кровотечение из слизистой желудка. На верхний край стенки желудка накладывают два или три зажима Babcock или Duvai. Этим достигают двух целей: гемостаза и улучшения визуализации внутренней стенки желудка при подтягивании зажимов кверху. Наложив один или более зажимов Babcock или Duval, нижний край стенки желудка оттягивают книзу. Пальцами левой руки хирург оттягивает нижний край стенки желудка, одновременно поддавливает кпереди заднюю часть гастроеюноанастомоза, при этом гастроеюностома становится доступной обзору. Если кровотечение продолжается на небольшом участке, гемостаз осуществляют наложением нескольких лигатур. В редких случаях, при диффузном кровотечении, поверх первого ряда швов между желудком и тощей кишкой накладывают непрерывный шов нерассасывающеися нитью, как показано на рисунке. Когда гемостаз достигнут, гастротомическсе отверстие ушивают двумя рядами швов и помещают конец зонда Levine в полость культи желудка для эффективной аспирации содержимого.
– Также рекомендуем “Внутренние грыжи после резекции желудка. Профилактика внутренних грыж после резекции желудка.”
Оглавление темы “Редкие осложнения резекции желудка. Опухоли желудка.”:
1. Синдром приводящей петли. Кровотечение из гастроеюноанастомоза.
2. Внутренние грыжи после резекции желудка. Профилактика внутренних грыж после резекции желудка.
3. Демпинг-синдром. Диагностика и лечение демпинг-синдрома.
4. Некроз культи желудка. Тощекищечно-желудочная инвагинация.
5. Перевод резекции по Billroth II в Billroth I. Техника перевода резекции желудка по Soupault-Boucaille.
6. Хирургическое лечение дивертикулов желудка. Операции при дивертикулах желудка.
7. Доброкачественные опухоли желудка. Хирургическое лечение доброкачественных опухолей желудка.
8. Хирургическое лечение полипов желудка эпителиального происхождения. Доброкачественные опухоли неэпителиального происхождения.
9. Хирургическое удаление полипа желудка на ножке. Резекция полипа желудка.
10. Эпидемиология рака желудка. Выбор метода лечения рака желудка.
Источник