Респираторный дистресс синдром у детей причины

Медицинский эксперт статьи

х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Респираторный дистресс-синдром у детей, или «шоковое» легкое, представляет собой симптомокомплекс, развивающийся вслед за перенесенным стрессом, шоком.
 [1], [2], [3], [4], [5], [6], [7], [8], [9]
[1], [2], [3], [4], [5], [6], [7], [8], [9]
Что вызывает респираторный дистресс-синдром у детей?
Пусковыми механизмами РДС являются грубые нарушения микроциркуляции, гипоксия и некроз тканей, активация медиаторов воспаления. Респираторный дистресс-синдром у детей может развиться при множественной травме, тяжелой кровопотере, сепсисе, гиповолемии (сопровождающихся явлениями шока), Инфекционных заболеваниях, отравлениях и т. д. Кроме того, причиной респираторного дистресс-синдрома у детей могут быть синдром массивных гемотрансфузий, неквалифицированное проведение ИВЛ. Он развивается после перенесенной клинической смерти и реанимационных мероприятий как составная часть постреанимационной болезни в сочетании с поражением других органов и систем (СПОН).
Считается, что форменные элементы крови в результате гипоплазмии, ацидоза и изменения нормального поверхностного заряда начинают деформироваться и слипаться друг с другом, образуя агрегаты, – сладж-феномен (англ. sludge – тина, отстой), что вызывает эмболию мелких легочных сосудов. Слипание форменных элементов крови между собой и с эндотелием сосудов запускает процесс ДВС крови. Одновременно начинается выраженная реакция организма на гипоксические и некротические изменения в тканях, на проникновение в кровь бактерий и эндотоксинов (липополисахаридов), что в последнее время трактуется как синдром генерализованной воспалительной реакции (Sistemic inflammatory responce syndrome – SIRS).
Респираторный дистресс-синдром у детей, как правило, начинает развиваться в конце 1-х-начале 2-х суток после выведения больного из состояния шока. Происходит увеличение кровенаполнения в легких, возникает гипертензия в системе легочных сосудов. Повышенное гидростатическое давление на фоне увеличенной проницаемости сосудов способствует выпотеванию жидкой части крови в интерстициальную, межуточную ткань, а затем и в альвеолы. В результате уменьшается растяжимость легких, снижается продукция сурфактанта, нарушаются реологические свойства бронхиального секрета и метаболические свойства легких в целом. Возрастает шунтирование крови, нарушаются вентиляционно-перфузионные отношения, прогрессирует микроателектазирование легочной ткани. В далеко зашедших стадиях «шокового» легкого в альвеолы проникает гиалин и формируются гиалиновые мембраны, резко нарушающие диффузию газов через альвеолокапиллярную мембрану.
Симптомы респираторного дистресс-синдрома у детей
Респираторный дистресс-синдром у детей может развиться у детей любого возраста, даже в первые месяцы жизни на фоне декомпенсированного шока, сепсиса, однако данный диагноз у детей устанавливают редко, трактуя выявляемые клинико-рентгенологические изменения в легких как пневмонию.
Выделяют 4 стадии респираторного дистресс-синдрома у детей.
- В I стадии (1-2-е сутки) наблюдается эйфория или беспокойство. Нарастают тахипноэ, тахикардия. В легких прослушивается жесткое дыхание. Развивается гипоксемия, управляемая кислородотерапией. На рентгенограмме легких определяются усиление легочного рисунка, ячеистость, мелкоочаговые тени.
- Во II стадии (2-3-и сутки) больные возбуждены, усиливаются одышка, тахикардия. Одышка имеет инспираторный характер, вдох становится шумным, «с надрывом», в акте дыхания участвует вспомогательная мускулатура. В легких появляются зоны ослабления дыхания, симметричные рассеянные сухие хрипы. Гипоксемия становится резистентной к оксигенации. На рентгенограмме легких выявляются картина «воздушной бронхографии», сливные тени. Летальность достигает 50 %.
- III стадия (4-5-е сутки) проявляется диффузным цианозом кожных покровов, олигопноэ. В задненижних отделах легких прослушиваются влажные разнокалиберные хрипы. Отмечается выраженная гипоксемия, торпидная к кислородотерапии, сочетающаяся с тенденцией к гиперкапнии. На рентгенограмме легких выявляется симптом «снежной бури» в виде множественных сливающихся теней; возможен плевральный выпот. Летальность достигает 65-70 %.
- В IV стадии (позже 5-го дня) у больных наблюдаются сопор, резко выраженные нарушения гемодинамики в виде цианоза, аритмии сердца, артериальная гипотония, гаспинг-дыхание. Гипоксемия в сочетании с гиперкапнией становится резистентной к ИВЛ с высоким содержанием кислорода в подаваемой газовой смеси. Клинически и рентгенологически определяется развернутая картина альвеолярного отека легких. Летальность достигает 90-100 %.
Диагностика и лечение респираторного дистресс-синдрома у детей
Диагностика РДС у детей – достаточно сложная задача, требующая от врача знания прогноза течения тяжелого шока любой этиологии, клинических проявлений «шокового» легкого, динамики газов крови. Общая схема лечения респираторного дистресс-синдрома у детей включает:
- восстановление проходимости дыхательных путей с помощью улучшения реологических свойств мокроты (ингаляции физиологического раствора, детергентов) и эвакуации мокроты естественным (кашель) или искусственным (отсасывание) путем;
- обеспечение газообменной функции легких. Назначают кислородотерапию в режиме ПДКВ с помощью мешка Мартина-Бауэра или по методу Грегори при спонтанном дыхании (через маску или интубационную трубку). При III стадии РДС обязательно применение ИВЛ с включением режима ПДКВ (5-8 см вод. ст.). Современные аппараты ИВЛ позволяют использовать инверсированные режимы регуляции соотношения времени вдоха и выдоха (1:Е = 1:1,2:1 и даже 3:1). Возможна комбинация с высокочастотной ИВЛ. При этом необходимо избегать высоких концентраций кислорода в газовой смеси (P2 выше 0,7). Оптимальной считается P02=0,4-0,6 при ра02 не менее 80 ммрт. ст.;
- улучшение реологических свойств крови (гепарин, дезаггрегирующие препараты), гемодинамики в малом круге кровообращения (кардиотоники – допамин, добутрекс и др.), снижение внутрилегочной гипертензии при II-III стадии РДС с помощью ганглиоблокаторов (пентамин и др.), а-адреноблокаторов;
- антибиотики в лечении РДС имеют второстепенное значение, но назначаются всегда в комбинации.
 [10], [11], [12], [13], [14], [15], [16], [17], [18], [19], [20]
[10], [11], [12], [13], [14], [15], [16], [17], [18], [19], [20]
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 23 июня 2014;
проверки требуют 18 правок.
Респираторный дистресс-синдром новорождённых (синонимы: синдром дыхательных расстройств, болезнь гиалиновых мембран), РДСН — тяжёлое расстройство дыхания у недоношенных новорождённых, обусловленное незрелостью лёгких и первичным дефицитом сурфактанта (с англ. — «поверхностно активное вещество»). Обычно формируется в пренатальном и неонатальном периодах развития ребёнка. Как правило, болезнь регистрируется у недоношенных детей (60 % — при 28 недельном сроке гестации, 15—20 % — при сроке 32—36 недель). При рациональном и своевременном лечении младенцев летальность составляет примерно 1 %[1].
Этиопатогенез[править | править код]
Заболевание в основном наблюдается у новорождённых детей от матерей с сахарным диабетом, сердечно-сосудистыми заболеваниями, маточными кровотечениями незрелость и/или обусловленное гипоксией нарушение функции клеток, вырабатывающих поверхностно-активное вещество – сурфактант. Способствовать возникновению РДСН может также внутриутробная гипоксия, асфиксия и гиперкапния. Из-за гипоксии и гиперкапнии возможно нарушение лёгочного кровообращения, происходит пропитывание межальвеолярных перегородок серозной жидкостью с просветлением альвеол плазмы. Определённое значение в возникновении РДСН имеет нехватка плазминогена, α2-микроглобулина и развитие локального или диссеминированного свертывания крови.
Все беременные в срок между 22-й и 34-й неделями гестации при наличии угрожающих и начинающихся преждевременных родов рассматриваются как пациентки, которым показана антенатальная профилактика РДСН глюкокортикоидами, способствующая созреванию сурфактанта лёгких плода.
Схемы приема: 2 дозы по 12 мг бетаметазона в/м через 24 ч или 4 дозы по 6 мг дексаметазона в/м через 12 ч;
Клиническая картина[править | править код]
К ранним признакам РДСН относят:
- одышка с частотой дыхания более 60 в минуту, возникающая в первые минуты или часы жизни;
- экспираторный стон (“хрюкающий выдох”) в результате развития компенсаторного спазма голосовой щели на выдохе, препятствующего спадению альвеол;
- западение грудной клетки на вдохе (втяжение мечевидного отростка грудины, подложечной области, межреберий, надключичных ямок) с одновременным раздуванием крыльев носа и щёк.
- цианоз;
- бледность кожных покровов;
- крепитирующие хрипы при аускультации
При прогрессировании болезни нарастают и симптомы: усиливается цианоз, может возникнуть рассеянная крепитация, наблюдается апноэ, пенистые и кровянистые выделения изо рта.
Для оценки тяжести дыхательных расстройств у недоношенных новорожденных используется шкала Сильвермана.
Для доношенных доношенных новорожденных используется шкала Даунса.
| Баллы | |||
|---|---|---|---|
| Признаки | 0 | 1 | 2 |
| Частота дыхания в 1 мин. | <60 | 60-80 | >80 |
| Цианоз | Нет | При FiO2=0,21 | При FiO2=>0.4 |
| Раздувание крыльев носа | Нет | Еле заметное | Умеренное или выраженное |
| Затруднённый выдох (экспираторный стон) | Нет | Слышен при аускультации | Слышен на расстоянии |
| Аускультация | Дыхание прослушивается хорошо | Дыхание ослабленное | Дыхание едва слышно |
Результат оценивают по сумме баллов:
2-3 балла- лёгкое расстройство дыхания;
4-6 баллов- расстройство дыхания средней тяжести;
более 6 баллов — тяжёлое расстройство дыхания.
Диагностика[править | править код]
Пренатальная диагностика (прогнозирование риска развития РДСН) основана на исследовании липидного спектра околоплодных вод (в крупных специализированных стационарах и региональных перинатальных центрах). Наиболее информативны следующие методы.
1) Коэффициент соотношения лецитина к сфингомиелину (в норме >2). Если коэффициент менее 1, то вероятность развития РДСН около 75%. Коэффициент от 1 до 2 – вероятность развития РДСН 50%. У новорожденных от матерей с сахарным диабетом РДС может развиться при соотношении лецитина к сфингомиелину более 2,0.
2) Уровень насыщенного фосфатидилхолина (в норме более 5 мкмоль/л) или фосфатидилглицерина (в норме более 3 мкмоль/л). Отсутствие или резкое снижение концентрации насыщенного фосфатидилхолина и фосфатидилглицерина в амниотической жидкости свидетельствует о высокой вероятности развития РДСН.
Диагноз основывается на данных анамнеза (факторах риска), клинической картине, результатах рентгенологического исследования.
Дифференциальную диагностику проводят с сепсисом, пневмонией, транзиторным тахипноэ новорождённых, синдромом аспирации мекония.
Лечение и прогноз[править | править код]
Лечение респираторного дистресс синдрома новорожденных (РДСН) необходимо начинать как можно раньше. Современное лечение РДСН заключается в введении сурфактанта в трахею ребёнка в первые минуты жизни и использовании респираторной поддержки — СРАР терапии через назальные канюли. «Золотой» первый час жизни позволяет уменьшить тяжесть течения заболевания. Данная методика позволяет минимизировать инвалидизацию ребёнка, улучшает качество жизни.
Куросурф- натуральный сурфактант животного происхождения (добывается из лёгких свиней) для лечения и профилактики РДС у недоношенных новорожденных с доказанной высокой эффективностью и безопасностью. Начальная доза 200 мг/кг. При необходимости применяют дополнительные половинные дозы 100 мг/кг с интервалом 12 часов. При неэффективности респираторной СРАР — терапии показаниями для перевода на традиционную ИВЛ является дыхательный ацидоз: pH ниже 7,2 и pCO2 более 60 мм.рт.ст.; частые (более 4 в час) или глубокие (необходимость в масочной ИВЛ) 2 и более раз в час приступы апноэ. С целью стимуляции регулярного дыхания и предотвращения апноэ используют метилксантины: кофеин- бензоат натрия из расчета 20 мг/кг нагрузочная доза и 5 мг/кг поддерживающая доза каждые 12 часов капать под язык.
Созревание и функциональная способность легких являются критичными для выживания. Основываясь на степени недоношенности, легкие могут быть частично, или полностью незрелыми, и соответственно, не способными обеспечить адекватную дыхательную функцию из-за отсутствия или недостаточного количества, вырабатываемого сурфактанта. В таких ситуациях новорожденному показано проведение сурфактант-заместительной терапии.
Прогноз[править | править код]
Прогноз в большинстве случаев благоприятный, однако при развитии отечно-геморрагического синдрома и гиалиновых мембранах довольно тяжёлый.
Примечания[править | править код]
- ↑ Под редакцией А.И. Воробьева. Полный справочник практикующего врача. — Москва: Оникс, 2010. — 880 с. — 2500 экз. — ISBN 978-5-94666-545-2.
Ссылки[править | править код]
РДС новорожденных (респираторный дистресс-синдром новорожденных) – статья с ресурса “Перинатальный помощник PeriHelp.ru”
Источник
Причины респираторного дистресс-синдрома (РДС) у доношенных новорожденных. Особенности
У новорождённых с нарушениями дыхания развиваются следующие признаки респираторного дистресса:
• Тахипноэ (<60 в минуту).
• Затруднённое дыхание с западением грудной клетки (особенно впадение грудинных и субкостальных промежутков) и расширением ноздрей.
• Стонущее дыхание на выдохе.
• В тяжёлых случаях цианоз.
Причины респираторного дистресс-синдрома у рождённых в срок младенцев перечислены ниже.
I. Типичные легочные причины респираторного дистресс-синдрома у новорожденных: рранзиторное тахипноэ новорождённых
II. Менее типичные легочные причины респираторного дистресс-синдрома у новорожденных:
– Аспирация мекония
– Пневмония РДС
– Пневмоторакс
– ПЛГН
– Аспирация молока
III. Редкие легочные причины респираторного дистресс-синдрома у новорожденных:
– Диафрагмальная грыжа
– ТЭС
– Гипоплазия лёгких
– Обструкция дыхательных путей, например атрезия хоан
– Лёгочное кровотечение
IV. Внелёгочные причины респираторного дистресс-синдрома у новорожденных:
– Врождённые пороки сердца
– Внутричерепная родовая травма / энцефалопатия
– Тяжёлая анемия
– Метаболический ацидоз
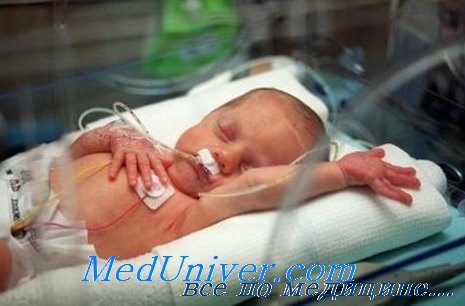
Младенцы с этими нарушениями должны быть помещены в неонатальное отделение для мониторинга сердечного и дыхательного ритма, оксигена-ции и кровообращения. Рентгенография грудной клетки может потребоваться в целях установления причин, требующих немедленной терапии, например пневмоторакса или диафрагмальной грыжи. Дополнительное поступление кислорода извне, механическая вентиляция и поддержка кровообращения применяются по мере необходимости.
Транзиторное тахипноэ новорождённых как причина респираторного дистресс-синдрома (РДС). Это наиболее распространённая причина РДС новорождённых, рождённых в срок. Она возникает в результате задержки резорбции жидкости в лёгких и наиболее часто наблюдается у детей, родившихся посредством кесарева сечения. На рентгенограммах грудной клетки выявляется жидкость в горизонтальной борозде. Может потребоваться поступление кислорода извне. Этот диагноз устанавливается после оценки и исключения всех остальных причин.
Аспирация мекония как причина респираторного дистресс-синдрома (РДС). Меконий выделяется до рождения у 8-20% младенцев. Он редко формируется у недоношенных младенцев, и его образование прямо пропорционально гестационному возрасту, выявляясь в 20-25% случаев при родах на сроке родов 42 нед. Он может выделяться в ответ на гипоксию плода. При рождении эти младенцы могут ингалировать твёрдый меконий.
При асфиксии младенцы могут начать задыхаться и аспирировать меконий до рождения. Меконий раздражает лёгкие и приводит как к механической обструкции, так и к химическому пневмониту, равно как и предрасполагает к инфицированию. При аспирации мекония лёгкие перерастянуты, вперемешку с участками коллапсов и уплотнений. Имеется высокая распространённость утечки воздуха, приводящая к пневмотораксу и пневмомедиастинуму. Часто требуется ИВЛ.
У младенцев с аспирацией мекония может развиваться персистирующая лёгочная гипертензия новорождённых (ПЛГН), которая может создавать сложности для адекватной оксигенации несмотря на высокое давление вентиляции (см. ниже). Тяжёлая аспирация мекония сопровождается высокой распространённостью патологии и смертности.
Пневмония как причина респираторного дистресс-синдрома (РДС). Длительный разрыв плодных оболочек, хорионамнионит и НВР предрасполагают к пневмонии. Новорождённым с РДС обычно требуется обследование для выявления любой инфекции. Начинают раннее введение антибиотиков широкого спектра действия до того, как будут получены результаты инфекционного обследования.
Пневмоторакс как причина респираторного дистресс-синдрома (РДС). Пневмоторакс может развиваться спонтанно до 2% родов. Он обычно бессимптомный, однако может вызывать респираторный дистресс-синдром. Пневмоторакс также происходит вторично по отношению к аспирации мекония, РДС или как осложнение ИВЛ. Лечение описано в соответствующей главе.
Аспирация молока как причина респираторного дистресс-синдрома (РДС). Это происходит чаще у недоношенных младенцев и у имеющих респираторный дистресс-синдром или неврологические повреждения. У младенцев с БПД часто наблюдается ГЭР, который создаёт предпосылки для аспирации. Младенцы с «волчьей пастью» имеют склонность к аспирации респираторных секретов или молока.
Персистирующая лёгочная гипертензия новорождённых (ПЛГН) как причина респираторного дистресс-синдрома (РДС). Это жизнеугрожающее состояние обычно связано с асфиксией в родах, аспирацией мекония, септицемией или РДС. Иногда оно развивается как первичное заболевание. В результате высокого сопротивления легочных сосудов имеется право-левый сброс в лёгких и на уровне предсердий и протока.
Цианоз развивается вскоре после рождения. Сердечные шумы и признаки сердечной недостаточности часто отсутствуют. На рентгенограмме грудной клетки выявляется нормальный размер сердца и может присутствовать лёгочная олигемия. Необходимо проведение экстренной ЭхоКГ для установления, что у ребёнка отсутствуют врождённые пороки сердца.
Большинству младенцев требуются механическая вентиляция и поддержка кровотока в целях достижения адекватной оксигенации. Ингаляция оксида азота, потенциального вазодилататора, часто приносит улучшение. Другой вазодилататор, силденафил, стал применяться недавно. Иногда помогает высокочастотная или осциллирующая вентиляция.
Экстракорпоральная мембранная оксигенация (ЭКМО), когда ребёнку проводится шунтирование сердца и лёгких в течение нескольких дней, показана в тяжёлых случаях, однако проводится лишь в некоторых специальных центрах.
Диафрагмальная грыжа как причина респираторного дистресс-синдрома (РДС). Патология выявляется приблизительно у 1 из 4000 новорождённых. В настоящее время во многих случаях диафрагмальная грыжа диагностируется при антенатальном УЗИ. В период новорождённое™ она обычно проявляется РДС. В большинстве случаев происходит левостороннее выбухание содержимого брюшной полости через заднелатеральное отверстие в диафрагме.
Пульсация верхушки сердца и сердечные тоны могут быть смещены в правую часть грудной клетки, снижена вентиляцией левого лёгкого. Неумелая реанимация может вызвать пневмоторакс в нормальном лёгком, таким образом, способствуя ухудшению ситуации. Диагноз подтверждается рентгенографией грудной клетки и живота. При предположении этого диагноза вводится широкая назогастральная трубка и проводится аспирация для предотвращения растяжения внутригрудной части кишечника.
После стабилизации диафрагмальная грыжа устраняется хирургически, однако у большинства новорождённых с этим состоянием основной проблемой является гипоплазия лёгких — когда сдавление грыжевым содержимым (из внутренних органов) во время беременности нарушило развитие лёгких у плода. Если имеется гипоплазия лёгких, смертность высока. Для дыхательной поддержки применяется до- и постоперационная ЭКМО.
Другие причины респираторного дистресс-синдрома (РДС). Другие причины РДС перечислены выше. Если он связан с сердечной недостаточностью, на аускультации могут выслушиваться патологические сердечные тоны и/или сердечные шумы. Полезным признаком является увеличение печени вследствие венозного застоя.
Необходимо пропальпировать бедренные артерии у всех младенцев с РДС, поскольку коарктация аорты и коарктация дуги аорты являются значимыми причинами сердечной недостаточности у новорождённых.
– Также рекомендуем “Причины инфекции у новорожденных. Определяемся”
Оглавление темы “Особенности недоношенных новорожденных”:
- Проблемы новорожденных с очень низким весом при рождении (ОНВР). На что обратить внимание?
- Причина желтухи у новорожденного младенца. Как определить?
- Лечение желтухи у новорожденного ребенка. Рекомендации
- Причины респираторного дистресс-синдрома (РДС) у доношенных новорожденных. Особенности
- Причины инфекции у новорожденных. Определяемся
- Инфицирование новорожденного стрептококком группы В. Причины
- Инфицирование новорожденного моноцитогенной листерией. Причины
- Конъюнктивит, пупочные инфекции новорожденного. Причины
- Инфицирование новорожденного вирусом простого герпеса (ВПГ), гепатитом В. Причины
- Причины судорог у новорожденных. Неонатальные судороги
Источник
