Респираторный дистресс синдром у детей реферат
Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Респираторный дистресс-синдром у детей, или «шоковое» легкое, представляет собой симптомокомплекс, развивающийся вслед за перенесенным стрессом, шоком.
[1], [2], [3], [4], [5], [6], [7], [8], [9]
Что вызывает респираторный дистресс-синдром у детей?
Пусковыми механизмами РДС являются грубые нарушения микроциркуляции, гипоксия и некроз тканей, активация медиаторов воспаления. Респираторный дистресс-синдром у детей может развиться при множественной травме, тяжелой кровопотере, сепсисе, гиповолемии (сопровождающихся явлениями шока), Инфекционных заболеваниях, отравлениях и т. д. Кроме того, причиной респираторного дистресс-синдрома у детей могут быть синдром массивных гемотрансфузий, неквалифицированное проведение ИВЛ. Он развивается после перенесенной клинической смерти и реанимационных мероприятий как составная часть постреанимационной болезни в сочетании с поражением других органов и систем (СПОН).
Считается, что форменные элементы крови в результате гипоплазмии, ацидоза и изменения нормального поверхностного заряда начинают деформироваться и слипаться друг с другом, образуя агрегаты, – сладж-феномен (англ. sludge – тина, отстой), что вызывает эмболию мелких легочных сосудов. Слипание форменных элементов крови между собой и с эндотелием сосудов запускает процесс ДВС крови. Одновременно начинается выраженная реакция организма на гипоксические и некротические изменения в тканях, на проникновение в кровь бактерий и эндотоксинов (липополисахаридов), что в последнее время трактуется как синдром генерализованной воспалительной реакции (Sistemic inflammatory responce syndrome – SIRS).
Респираторный дистресс-синдром у детей, как правило, начинает развиваться в конце 1-х-начале 2-х суток после выведения больного из состояния шока. Происходит увеличение кровенаполнения в легких, возникает гипертензия в системе легочных сосудов. Повышенное гидростатическое давление на фоне увеличенной проницаемости сосудов способствует выпотеванию жидкой части крови в интерстициальную, межуточную ткань, а затем и в альвеолы. В результате уменьшается растяжимость легких, снижается продукция сурфактанта, нарушаются реологические свойства бронхиального секрета и метаболические свойства легких в целом. Возрастает шунтирование крови, нарушаются вентиляционно-перфузионные отношения, прогрессирует микроателектазирование легочной ткани. В далеко зашедших стадиях «шокового» легкого в альвеолы проникает гиалин и формируются гиалиновые мембраны, резко нарушающие диффузию газов через альвеолокапиллярную мембрану.
Симптомы респираторного дистресс-синдрома у детей
Респираторный дистресс-синдром у детей может развиться у детей любого возраста, даже в первые месяцы жизни на фоне декомпенсированного шока, сепсиса, однако данный диагноз у детей устанавливают редко, трактуя выявляемые клинико-рентгенологические изменения в легких как пневмонию.
Выделяют 4 стадии респираторного дистресс-синдрома у детей.
- В I стадии (1-2-е сутки) наблюдается эйфория или беспокойство. Нарастают тахипноэ, тахикардия. В легких прослушивается жесткое дыхание. Развивается гипоксемия, управляемая кислородотерапией. На рентгенограмме легких определяются усиление легочного рисунка, ячеистость, мелкоочаговые тени.
- Во II стадии (2-3-и сутки) больные возбуждены, усиливаются одышка, тахикардия. Одышка имеет инспираторный характер, вдох становится шумным, «с надрывом», в акте дыхания участвует вспомогательная мускулатура. В легких появляются зоны ослабления дыхания, симметричные рассеянные сухие хрипы. Гипоксемия становится резистентной к оксигенации. На рентгенограмме легких выявляются картина «воздушной бронхографии», сливные тени. Летальность достигает 50 %.
- III стадия (4-5-е сутки) проявляется диффузным цианозом кожных покровов, олигопноэ. В задненижних отделах легких прослушиваются влажные разнокалиберные хрипы. Отмечается выраженная гипоксемия, торпидная к кислородотерапии, сочетающаяся с тенденцией к гиперкапнии. На рентгенограмме легких выявляется симптом «снежной бури» в виде множественных сливающихся теней; возможен плевральный выпот. Летальность достигает 65-70 %.
- В IV стадии (позже 5-го дня) у больных наблюдаются сопор, резко выраженные нарушения гемодинамики в виде цианоза, аритмии сердца, артериальная гипотония, гаспинг-дыхание. Гипоксемия в сочетании с гиперкапнией становится резистентной к ИВЛ с высоким содержанием кислорода в подаваемой газовой смеси. Клинически и рентгенологически определяется развернутая картина альвеолярного отека легких. Летальность достигает 90-100 %.
Диагностика и лечение респираторного дистресс-синдрома у детей
Диагностика РДС у детей – достаточно сложная задача, требующая от врача знания прогноза течения тяжелого шока любой этиологии, клинических проявлений «шокового» легкого, динамики газов крови. Общая схема лечения респираторного дистресс-синдрома у детей включает:
- восстановление проходимости дыхательных путей с помощью улучшения реологических свойств мокроты (ингаляции физиологического раствора, детергентов) и эвакуации мокроты естественным (кашель) или искусственным (отсасывание) путем;
- обеспечение газообменной функции легких. Назначают кислородотерапию в режиме ПДКВ с помощью мешка Мартина-Бауэра или по методу Грегори при спонтанном дыхании (через маску или интубационную трубку). При III стадии РДС обязательно применение ИВЛ с включением режима ПДКВ (5-8 см вод. ст.). Современные аппараты ИВЛ позволяют использовать инверсированные режимы регуляции соотношения времени вдоха и выдоха (1:Е = 1:1,2:1 и даже 3:1). Возможна комбинация с высокочастотной ИВЛ. При этом необходимо избегать высоких концентраций кислорода в газовой смеси (P2 выше 0,7). Оптимальной считается P02=0,4-0,6 при ра02 не менее 80 ммрт. ст.;
- улучшение реологических свойств крови (гепарин, дезаггрегирующие препараты), гемодинамики в малом круге кровообращения (кардиотоники – допамин, добутрекс и др.), снижение внутрилегочной гипертензии при II-III стадии РДС с помощью ганглиоблокаторов (пентамин и др.), а-адреноблокаторов;
- антибиотики в лечении РДС имеют второстепенное значение, но назначаются всегда в комбинации.
[10], [11], [12], [13], [14], [15], [16], [17], [18], [19], [20]
Источник
Респираторный дистресс-синдром взрослых (РДСВ) – крайне тяжелое проявление дыхательной недостаточности, сопровождающееся развитием некардиогенного отека легких, нарушений внешнего дыхания и гипоксии. Несмотря на многообразие факторов, приводящих к РДВС, в его основе лежат повреждения легочных структур, вызывающие несостоятельность транспортировки кислорода в легкие. Другими названиями респираторного дистресс-синдрома являются «шоковое», «влажное», «травматическое» легкое.
Общие сведения
Респираторный дистресс-синдром взрослых (РДСВ) – крайне тяжелое проявление дыхательной недостаточности, сопровождающееся развитием некардиогенного отека легких, нарушений внешнего дыхания и гипоксии. Несмотря на многообразие факторов, приводящих к РДВС, в его основе лежат повреждения легочных структур, вызывающие несостоятельность транспортировки кислорода в легкие. Другими названиями респираторного дистресс-синдрома являются «шоковое», «влажное», «травматическое» легкое.
Резкое снижение оксигенации и вентиляции организма вызывает кислородную недостаточность сердца и головного мозга и развитие угрожающих для жизни состояний. При РДСВ летальность в случае несвоевременно или неадекватно оказанной помощи достигает 60-70%.
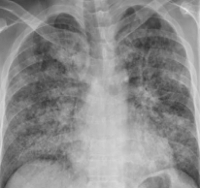
Респираторный дистресс-синдром
Причины и механизм развития РДСВ
Механизмом, запускающим развитие респираторного дистресс-синдрома, служит эмболизация мелких сосудов легких микросгустками крови, частичками поврежденных тканей, каплями жира на фоне образующихся в тканях токсичных биологически активных веществ — кининов, простагландинов и др. Микроэмболизация легочных сосудов развивается в результате прямого или опосредованного воздействия на капиллярно-альвеолярную мембрану легочных ацинусов различного рода повреждающих факторов.
Прямое повреждающее воздействие оказывает аспирация крови, рвотных масс и воды, вдыхание дыма и токсических веществ, контузия легких, перелом ребер, разрыв диафрагмы, передозировка наркотических средств. Опосредованное, непрямое повреждение капиллярно-альвеолярных мембран вызывает активация и агрегация форменных элементов крови при бактериальных и вирусных пневмониях, сепсисе, ожогах, сочетанных травмах и травматическом шоке, сопровождающихся массивной кровопотерей, панкреатите, аутоиммунных процессах, электротравме, эклампсии и т. д.
Повышение проницаемости мембраны для белка и жидкости вызывает отек интерстициальной и альвеолярной тканей, снижение растяжимости и газообменной функции легких. Эти процессы приводят к развитию гипоксемии, гиперкапнии и острой дыхательной недостаточности. Респираторный дистресс-синдром может развиваться на протяжении нескольких часов или суток от момента воздействия повреждающего фактора. В течении РДСВ выделяют три патоморфологические фазы:
- Острая фаза РДСВ (до 2-5 суток) – интерстициальный и альвеолярный отек легких, поражение капилляров легких и эпителия альвеол, развитие микроателектазов. В случае благоприятного течения респираторного дистресс-синдрома спустя несколько дней острота явлений стихает, транссудат рассасывается; в противном случае возможен переход в подострое либо хроническое течение.
- Подострая фаза РДСВ – развитие бронхоальвеолярного и интерстициального воспаления.
- Хроническая фаза РДСВ – соответствует развитию фиброзирующего альвеолита. Происходит утолщение и уплощение капиллярно-альвеолярных мембран, разрастание в них соединительной ткани, формирование микротромбозов и запустевание сосудистого русла. Исходом хронической фазы респираторного дистресс-синдрома служит развитие легочной гипертензии и хронической дыхательной недостаточности. Выраженный альвеолярный фиброз может возникнуть уже спустя 2-3 недели.
Симптомы респираторного дистресс-синдрома
Развитие респираторного дистресс-синдрома взрослых характеризуется последовательной сменой стадий, отражающих патологические изменения в легких и типичную картину остро нарастающей дыхательной недостаточности.
I (стадия повреждения) – первые 6 часов со времени воздействия стрессового фактора. Жалобы, как правило, отсутствуют, клинико-рентгенологические изменения не определяются.
II (стадия мнимого благополучия) – от 6 до 12 часов со времени воздействия стрессового фактора. Развиваются нарастающая одышка, цианоз, тахикардия, тахипноэ (учащение дыхания более 20 в мин.), беспокойство пациента, кашель с пенистой мокротой и прожилками крови. Одышка и цианоз не купируются кислородными ингаляциями, содержание кислорода в крови неуклонно падает. Аускультативно в легких – хрипы, крепитация; рентгенологические признаки соответствуют диффузному интерстициальному отеку.
III (стадия дыхательной недостаточности) – спустя 12-24 часа после воздействия стрессового фактора. Клокочущее дыхание с выделением пенистой розовой мокроты, нарастающая гипоксемия и гиперкапния, поверхностное дыхание, увеличение центрального венозного и снижение артериального давления. По всей поверхности легких выслушиваются влажные, множественные хрипы различного калибра. На рентгенограммах определяется слияние очаговых теней. В этой стадии происходит образование гиалиновых мембран, заполнение альвеол фибрином, экссудатом, распадающимися кровяными тельцами, поражение эндотелия капилляров с образованием кровоизлияний и микроателектазов.
IV (терминальная стадия) – метаболический ацидоз, гипоксемия и гиперкапния не устраняются предельно большими объемами интенсивной терапии и ИВЛ. Ложноположительная рентгенологическая динамика (появление очагов просветлений) вызвана разрастанием соединительной ткани, замещающей паренхиму легких. В этом терминальном периоде респираторного дистресс-синдрома развивается полиорганная недостаточность, характеризующаяся:
- артериальной гипотонией, выраженной тахикардией, фибрилляцией предсердий, желудочковой тахикардией;
- гипербилирубинемией, гиперферментемией, гипоальбуминемией, гипохолестеринемией;
- ДВС-синдромом, лейкопенией, тромбоцитопенией ;
- повышением мочевины и креатинина, олигурией;
- желудочно-кишечными и легочными кровотечениями;
- угнетением сознания, комой.
Осложнения
Диагностика респираторного дистресс-синдрома
Респираторный дистресс-синдром является критическим состоянием и требует экстренной оценки состояния пациента. Ранними объективными проявлениями РДСВ служат нарастающие одышка, тахикардия и цианоз. Аускультативная картина легких изменяется соответственно стадиям респираторного дистресс-синдрома: от жесткого «амфорического» дыхания к клокочущим влажным хрипам и симптому «немого» («молчащего») легкого в терминальной стадии.
Характерным показателем газового состава крови при РДСВ является РаО2 ниже 50 мм рт. ст. (гипоксемия), несмотря на проводимую оксигенотерапию (при FiО2 более >60%.), нарастание гиперкапнии. У пациентов с РДСВ выраженная дыхательная недостаточность и гипоксемия сохраняются даже при ингаляциях высококонцентрированной кислородной смеси.
Биохимические показатели венозной крови характеризуются гипоальбуминемией, повышением свертывающих факторов, нарастанием трансаминаз и билирубина. При рентгенографии легких на периферии выявляются диффузные множественные тени (симптом “снежной бури”), снижение прозрачности легочной ткани, плевральный выпот обычно отсутствует.
Показатели функции внешнего дыхания свидетельствуют об уменьшении всех дыхательных объемов и статического растяжения легочной ткани менее 5 мл/мм вод. ст. Измерение давления в легочной артерии катетером Суона–Ганца показывает его «заклинивание» на уровне менее 15 мм рт.ст. Респираторный дистресс-синдром следует отличать от кардиогенного отека легких, пневмонии, ТЭЛА.
Лечение респираторного дистресс-синдрома
Лечение респираторного дистресс-синдрома осуществляется в условиях отделения интенсивной терапии и реанимации. Мероприятия по купированию РДСВ включают:
- устранение стрессового повреждающего фактора;
- коррекцию гипоксемии и острой дыхательной недостаточности;
- лечение полиорганных нарушений.
На первом этапе лечения респираторного дистресс-синдрома устраняются прямые повреждающие факторы легких, назначается массивная антибактериальная терапия при бактериальных пневмониях, сепсисе, осуществляется соответствующее лечение ожогов и травм. Для устранения гипоксии проводится подбор адекватного режима кислородотерапии с динамическим контролем газов крови (с поддержанием РО2 не менее 60 мм рт.ст.). Подача кислорода может осуществляться чрез маску или носовой катетер, при неэффективной оксигенации показана ИВЛ (при ЧД 30 в минуту).
Для профилактики развития ДВС-синдрома назначаются ацетилсалициловая кислота, дипиридамол и реополиглюкин, гепарин. Несмотря на интерстициальный и альвеолярный отек, проводится инфузионная терапия для улучшения питания органов, нормализации диуреза и поддержания уровня АД. Эффективность лечения респираторного дистресс-синдрома зависит от его своевременности: оно успешно лишь на ранних стадиях данного состояния до наступления необратимых поражений легочной ткани.
Прогноз и профилактика респираторного дистресс-синдрома
Летальность в III стадии респираторного дистресс-синдрома составляет около 80%, в терминальной стадии, соответствующей полиорганной недостаточности, обычно все пациенты погибают. При благоприятном исходе после купирования РДСВ функция легких может практически полностью восстановиться, однако чаще требуется длительная поддерживающая терапия.
Специфические профилактические мероприятия респираторного дистресс-синдрома отсутствуют. Следует остерегаться воздействия стрессовых повреждающих факторов, ведущих к развитию РДСВ.
Источник
Респираторный дистресс-синдром новорожденных (синдром дыхательных расстройств) – неинфекционные патологические процессы (первичные ателектазы, болезнь гиалиновых мембран, отечно-геморрагический синдром), формирующиеся в пренатальном и раннем неонатальном периодах развития ребенка и проявляющиеся нарушением дыхания. Частота развития респираторного дистресса зависят от степени недонашивания и составляет в среднем 60 % у детей, родившихся при сроке беременности менее 28 недель, 15-20 % – при сроке 32-36 недель и 5 % – при сроке 37 недель и более. При рациональном выхаживании таких детей летальность приближается к 10 %.
Признаки
Большинство детей рождаются в состоянии асфиксии и врожденной гипоксии, но расстройства дыхания могут появиться не сразу, а спустя несколько часов после рождения. Типичными являются резко выраженные признаки дыхательной недостаточности: одышка с частотой дыханий 60 и более в 1 мин (нередко с апериодическим дыханием), цианоз (периоральный, акроцианоз, генерализованный), бледность кожных покровов, участие в акте дыхания вспомогательной мускулатуры (напряжение крыльев носа, втяжение уступчивых мест грудной клетки – межреберных промежутков, мечевидного отростка грудины, втягивание надключичных ямок), ригидность грудной клетки, иногда пена у рта, затрудненный “ворчащий” вдох (спазм голосовой щели), раздувание щек. Отмечается снижение двигательной активности, гипорефлексия, мышечная гипотония. Для раннего выявления и оценки тяжести дыхательных расстройств у новорожденных используют шкалу Сильвермана. Оценка производится в динамике каждые 6 ч на протяжении 2-3 дней.
По мере прогрессирования болезни дыхательные расстройства и симптомы угнетения нервной системы нарастают, усиливается цианоз, появляются апноэ, “хрюкающий” выдох и парадоксальное дыхание (при выдохе передненижние отделы грудной клетки втягиваются, а живот выпячивается), рассеянная крепитация. Часто появляются местные и генерализованные отеки; пенистые, иногда кровянистые выделения изо рта. Поражается сердечно-сосудистая система, наблюдаются тахикардия, глухие тоны сердца, сохраняются плодовые коммуникации с праволевым шунтом, нарастают признаки легочной гипертензии, развивается кардио- и гепатомегалия.
Описание
Развивается в основном у недоношенных детей от матерей с отягощенным акушерским анамнезом (сердечно-сосудистые заболевания, сахарный диабет, нефропатии, патология плаценты, маточные кровотечения). Имеет значение внутриутробная гипоксия, асфиксия и гиперкапния в родах при наличии незрелости ткани легкого. Под действием гипоксии и гиперкапнии наступает нарушение легочного кровообращения, происходит пропитывание межальвеолярных перегородок серозной жидкостью с выходом в просвет альвеол составных частей плазмы, в частности фибрина. Образование гиалиновых мембран возможно и в результате снижения фибринолитической активности крови. Отмечается также отсутствие или резкое снижение активности антиателектатического фактора (сурфактанта), что способствует возникновению ателектазов. Определенное значение имеет дефицит плазминогена, альфа2-макроглобулина и развитие локального или диссеминированного внутрисосудистого свертывания крови. Отмечаются недоразвитие эластической ткани легкого, незрелость альвеол, аспирация околоплодной жидкости и слизи, особенно у глубоконедоношенных детей.
Диагностика
Диагноз респираторного дистресса основывается на данных клинической картины. Его можно предсказать на основании изучения содержания лецитина или тромбопластической активности околоплодных вод.
Если отношение уровней сфингомиапин – лецитин в околоплодных водах более 2,0, то вероятность развития респираторного дистресса 2 %, если менее 2,0- 50 %, если менее 1,0-100 %. Может быть использован также простой тест на зрелость легких – “пенистый тест” Клементса с содержимым желудка, полученным при зондировании.
Дифференциальный диагноз проводят с пневмониями, пороками развития легких и сердца, внутричерепной родовой травмой, диафрагмальной грыжей.
Лечение
Прежде всего, это профилактика охлаждения (последнее снижает или прекращает синтез сурфактанта). Ребенка сразу после рождения заворачивают и помещают под лучистый источник тепла, а далее в кувез. Проводят мероприятия по оживлению и восстановлению дыхания. Хорошие результаты дает противоацидотическая терапия. Основным показанием к коррекции гидрокарбонатом натрия считается общее тяжелое состояние ребенка (менее 6 баллов по Апгар) и развитие декомпенсированного ацидоза (рН<7,3). Раствор гидрокарбоната натрия вводят повторно в последующие 2-3 дня до нормализации показателей кислотно-основного состояния (рН 7,35-7,4). Широко применяют введение витаминов, сердечных средств, эуфиллина и др.
Инфузионная терапия должна проводиться медленно в небольшом объеме со скоростью 3-5 капель в 1 мин. Состав вводимой жидкости определяется поставленной целью: доставка организму калорий, снижение процессов катаболизма и степени ацидоза, улучшение водно-солевого обмена, предупреждение гипо- или гиперкалиемии и гипераминоацидемии. При шоке и кровопотере показаны гемотрансфузии. Необходима постоянная ингаляция 30 % кислородно-воздушной смеси.
Эффективно применение кислородно-гелиевых смесей. Большое значение имеет уход: покой, содержание в кувезе. Время начала кормления определяют индивидуально с учетом функционального состояния ребенка и степени недоношенности. При тяжелом течении, особенно при нарушении координации глотания, сосания и дыхания, назначают кормление через зонд. По мере выздоровления детей переводят на кормление сцеженным женским молоком, а затем прикладывают к груди матери.
Прогноз при развитии отечно-геморрагического синдрома и гиалиновых мембранах тяжелый, в остальных случаях благоприятный.
© Большая медицинская энциклопедия
Источник
