Ревматологические синдромы при поражении органов жкт
Ирина Александровна Зборовская – директор Федерального бюджетного государственного учреждения «Научно-исследовательский институт клинической и экспериментальной ревматологии» РАМН, профессор кафедры госпитальной терапии с курсом клинической ревматологии факультета усовершенствования врачей Волгоградского государственного медицинского университета, д.м.н.
Ревматические заболевания относятся к системным заболеваниям, а это значит, что поражаются все органы и системы, в том числе, и желудочно-кишечный тракт. Причем, специфика поражений ЖКТ связана с особенностью патогенеза этих заболеваний.
I. Системная склеродермия.
Например, при системной склеродермии (ССД) это самое частое из всех поражений внутренних органов. Поражение ЖКТ при ССД имеет столь четкую очерченную и своеобразную клинико-рентгенологическую картину, что по своей диагностической значимости выходит на первый план среди других висцеральных проявлений ССД.
1. В начале заболевания возникает потеря вкусовой чувствительности, затруднение при жевании, довольно частая отрыжка. Затем присоединяется дисфагия, которая осложняет прием пищи. У многих больных отмечается значительное уменьшение массы тела.
2. Дисфункция пищевода встречается у 80% больных
а) Нарушение моторики пищевода и рефлюкс.
– Возникают в результате замещения коллагеном гладких мышц нижней трети пищевода, вследствие этого возникает дисфункция нижнего пищеводного сфинктера.
– Поперечнополосатая мускулатура верхней трети пищевода обычно не повреждается.
– Характеризуется картиной своеобразного рефлюкс-эзофагита, который проявляется: дисфагией, нарушением глотания твердой и даже жидкой пищи, болезненными срыгиваниями.
б) Дисфункция нижнего пищеводного сфинктера приводит также к развитию пептического эзофагита. Образуются язвы пищевода. Чаще всего они локализуются в месте соединения пищевода с желудком. В терминальной стадии назначается парентеральное питание.
в) Может развиться склероз уздечки языка.
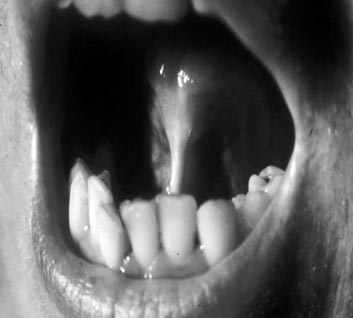
Рис. Склероз уздечки языка
г) Стриктуры пищевода
– Возникают вследствие постоянного рефлюкса.
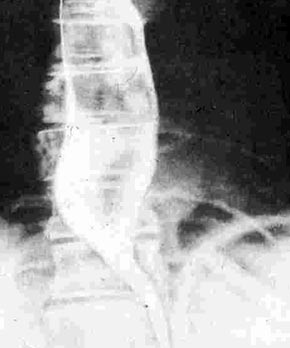
– При этом рентгенологически в положении больного лежа отмечают значительное расширение пищевода в верхних отделах и сужение в нижней трети, значительную задержку пассажа бариевой взвеси по пищеводу, замедление перистальтики.
д) У трети пациентов с ССД обнаруживают синдром Баррета – тонкокишечную метаплазию эпителия пищевода. Прием ингибиторов протонной помпы в больших дозах (40-80 мг/сут омепразола и цизаприда) облегчает состояние больных.

3. Изменения в кишечнике подобны изменению в пищеводе; они также встречаются в 80% случаев.
а) Выявляются признаки склеродермического дуоденита – язвенноподобный синдром: нарушение моторики кишечника, спазмы, диарея.
б) При поражении тонкой кишки может возникнуть синдром нарушения всасывания и бактериального роста. Это происходит при преимущественном поражении тонкого кишечника – спруподобный синдром. Больных беспокоит тошнота, вздутие живота, урчание переливание в нем, поносы. Одной из причин диареи является синдром избыточного размножения бактерий. В этом случае эффективны антибиотики.
в) При поражении толстого кишечника – упорные запоры, иногда с признаками частичной рецидивирующей непроходимости.
г) Дивертикулы.
Могут возникать дивертикулы поперечно-ободочной и нисходящей кишок.
д). Из редких осложнений – кистозный пневматоз кишки, изъязвление и перфорация стенки кишки.
4. Развитие билиарного цирроза печени (редко).
II. Изменение желудочно – кишечного тракта
при дерматомиозите
1. Отмечаются нередко и проявляются нарастающей дисфагией (вследствие поражения поперечно-полосатой мускулатуры глоточного кольца и верхнего отдела пищевода), отсутствием аппетита, иногда болями в животе и симптомами гастроэнтероколита, уменьшением массы тела, вплоть до кахексии. По данным различных авторов, дисфагия выявляется у 36-84% больных. Она развивается постепенно и носит прогрессирующий характер. Нарушение процесса жевания и глотания может усугубиться поражением жевательных мышц и мышц языка, пищевода, слизистой оболочки полости рта и глотки, иногда с отеком, инфильтрацией и изъязвлением и наблюдается гиперсаливация, поперхивание (из-за поражения мышц гортани, в том числе надгортанника и мягкого нёба) и попадание пищи в дыхательные отделы. Поперхивание представляет реальную опасность аспирации пищи с последующим развитием аспирационной пневмонии.
2. Тяжелая форма прогрессирующей дисфагии. Когда твердая пища срыгивается, а жидкая выливается через нос, представляет непосредственную угрозу жизни больного и является прямым показанием к срочной терапии максимальными дозами кортикостероидов и (или) цитостатиков. Аспирационные пневмонии – тяжелые проявления дерматомиозита. Однако такая развернутая картина наблюдается не сразу. В начале заболевания выявляются только легкие расстройства глотания. Поэтому необходим тщательный и целенаправленный расспрос.
3. Помимо патологии глотки и пищевода у больных дерматомиозитом может возникнуть поражение различных отделов желудочно-кишечного тракта, в том числе и сфинктеров проявляющиеся клинически анорексией, запорами, абдоминалгиями, реже – диспептическими явлениями, гипотонией желудка и кишечника. Абдоминалгии могут в своей основе иметь несколько причин: у одних больных они обусловлены поражением мышц живота, у других – спастико-атоническими явлениями в кишечнике, а также васкулитом в различных отделах желудочно-кишечного тракта.
4. Описаны случаи дерматомиозита, при которых отмечались желудочно-кишечные кровотечения, с кровавой рвотой или меленой, перфорация желудка вследствие васкулита и некроза по ходу пищеварительного тракта.
5. Увеличение печени и селезенки.
а) Умеренное увеличение печени с изменением функциональных проб наблюдается примерно у 1/3 больных.
б) Реже наблюдается при дерматомиозите гепатолиенальный и железисто-селезеночный синдромы, увеличиваются лимфоузлы.
в) Важно отметить, что у 10 – 20% пациентов с ДМ обнаруживают злокачественные новообразования в желудке или толстой кишке.
III. Системная красная волчанка
СКВ может дебютировать и проявляться асцитом (признак полисерозита), часто наблюдается локальный перитонит с перигепатитом и периспленитом. Тошнота, диарея, желудочно-кишечные кровообращения, по данным некоторых исследователей, развиваются у 1/3 больных. Морфологической основной изъязвления стенки тонкой или толстой кишки с развитием кровотечения и перфорации считают волчаночный васкулит.
VI. Ревматоидный артрит.
1. Специфическим проявлением этого заболевания может быть поражение височно-нижнечелюстного сустава, в этом случае возникают трудности при еде, и именно это может быть причиной уменьшения массы тела, иногда существенного.
2. Применение НПВП и кортикостероидов при этом заболевании обуславливает проблемы, связанные с профилактикой эрозивно-язвенных гастродуоденальных поражений, которые, по данным некоторых авторов, наблюдаются у 30% больных ревматоидным артритом, получающих активную терапию. Это мы с Вами уже обсуждали ранее.
3. Поражение тонкой и толстой кишки при этом заболевании обусловлено васкулитом и сходно с аналогичной патологией при системной красной волчанке.
4. Важно помнить о том, что в некоторых случаях синдром нарушенного всасывания при ревматоидном артрите развивается вследствие амилоидоза. Диарея может быть обусловлена не только васкулитом мезентериальных сосудов, но также препаратами золота и колитом, вызываемым Cl. difficile.
V. Болезнь Бехчета
Системные ревматические заболевания очень непредсказуемы и могут иногда удивлять своими проявлениями. Вот, например, редкий случай поражения пищевода у больной с болезнью Бехчета, у которой развилось тяжелое поражение желудочно-кишечного тракта с вовлечением пищевода. Диагноз болезни Бехчета был верифицирован на основании рецидивирующего афтозного стоматита, язв гениталий и поражения кожи в виде узловатой эритемы. Особенностью случая явилось обширное вовлечение желудочно-кишечного тракта в виде множественного язвенного поражения илеоцекальной области и эзофагита, приведшего к образованию дивертикулов и сужению пищевода. Данный случай демонстрирует последствия поздней диагностики болезни Бехчета, так как диагноз был установлен через 18 лет после появления первых симптомов.
Для установления диагноза потребовалось проведение консилиума из ревматологов, эндоскопистов, морфологов и генетиков. Особенностью заболевания является обширное вовлечение ЖКТ, требовавшее проведения эндоскопических процедур, а также исследований биопсийного материала из очагов поражения. Тяжесть заболевания обусловлена наличием достаточно типичного поражения кишечника в виде множественного язвенного процесса в илеоцекальном секторе, а также таким редким проявлением как эзофагит, приведшим к образованию дивертикулов и сужению пищевода.
VI. Болезнь Бехтерева
Поражение кишечника считается «малым» критерием ББ. Язвенные дефекты определяются во всех отделах ЖКТ, однако наиболее уязвимой является именно илеоцекальная область.
1. Проведение дифференциального диагноза при вовлечении ЖКТ между ББ и болезнью Крона в ряде случаев затруднено вследствие отсутствия патогномоничных признаков язвенного процесса. И болезнь Бехтерева и болезнь Крона могут вызывать неспецифические язвенные поражения в любом отделе ЖКТ. Однако было показано, что язвы отличаются по форме: круглые или овальные характерны для ББ, линейные – для болезни Крона. При обоих заболеваниях язвы располагаются беспорядочно, но при ББ они склоны к локальности, а при болезни Крона носят сегментарный или диффузный характер. Для ББ характерна большая глубина язвенных поражений.
2. Необычным для ББ является эзофагит. В литературе эзофагит считается редким проявлением болезни, так как описано не более 30 таких случаев. Подчеркивается, что эзофагит сочетался с другими симптомами ББ, включая поражение различных отделов ЖКТ. Отмечается, что эзофагиты при ББ не имеют определенной морфологической картины и могут проявляться эрозиями, распространенным воспалением, перфоративными язвами, и тяжелым стенозом.
Гистологические исследования, зачастую демонстрируют лишь неспецифическое воспаление.
Источник
Изучение хронических воспалительных заболеваний кишечника (ХВЗК) является актуальной проблемой не только детской гастроэнтерологии, но и детской ревматологии вследствие частого дебюта этих патологических состояний именно с суставных проявлений и дальнейшего течения клинически взаимосвязанных кишечного и суставного синдромов.
Распространенность ХВЗК среди детского населения составляет 2,2–6,8 на 100 тыс. детей [1, 2]. С наибольшей частотой в детском возрасте диагностируются такие заболевания этой группы, как болезнь Крона и язвенный колит. Отмечено, что язвенный колит чаще встречается у мальчиков, а болезнь Крона — у мальчиков и девочек с примерно с одинаковой частотой [2].
Болезнь Крона (регионарный энтерит, гранулематозный илеит) — воспалительное заболевание с вовлечением в процесс всех слоев кишечной стенки; характеризуется прерывистым (сегментарным) характером поражения различных разделов желудочно-кишечного тракта. Для него характерна диарея с примесью слизи и крови, боли в животе (часто в правой подвздошной области), потеря массы тела, лихорадка.
Язвенный колит (неспецифический язвенный колит, идиопатический колит) — язвенно-деструктивное поражение слизистой оболочки толстой кишки, которое локализуется преимущественно в ее дистальных отделах. В клинической картине характерны: кровотечения из прямой кишки, учащенное опорожнение кишечника, тенезмы; боли в животе менее интенсивны, чем при болезни Крона, локализуются чаще всего в левой подвздошной области. Примерно у 30% пациентов юношеского возраста язвенный колит начинается внезапно с появления болей в животе и диареи с примесью крови.
По данных разных авторов, внекишечные проявления ХВЗК отмечаются в 5–25% случаев. Наибольшая их доля приходится на тотальные формы неспецифического язвенного колита (87,5%) и болезни Крона с вовлечением в процесс толстой (29%) или толстой и тонкой кишки (58,1%) [3]. Системные проявления ХВЗК по патогенетическому принципу разделяют на три группы. К первой группе относят проявления, возникающие вследствие системной гиперсенсибилизации, — поражения суставов, глаз, кожи, слизистой оболочки рта; ко второй — обусловленные бактериемией и антигенемией в портальной системе — поражения печени и билиарного тракта. Выделяют также явления, развивающиеся вторично при длительно существующих нарушениях в толстой кишке, — анемии, электролитные расстройства.
Патогенез суставных проявлений остается неясным. Обсуждается значение повышенной проницаемости стенки кишечника, отмечающейся у больных язвенным колитом и болезнью Крона, в результате чего в кровь в большом количестве попадают компоненты оболочки стенок бактерий. Эти компоненты выступают в качестве пептидных антигенов, способных приводить к развитию артритов. Связываясь с молекулами комплексов гистосовместимости и активируя в дальнейшем Т-лимфоциты, пептиды приводят к возникновению воспаления суставов [3].
С точки зрения ревматолога суставные проявления ХВЗК относят к т. н. серонегативным спондилоартропатиям. Это большая гетерогенная группа клинически пересекающихся, хронических воспалительных ревматических заболеваний [4]. Помимо артритов, связанных с воспалительными заболеваниями кишечника, в эту группу включают такие ревматические заболевания детского возраста, как ювенильный спондилоартрит, ювенильный реактивный артрит, ювенильный псориатический артрит, а также недифференцированные спондилоартропатии (дактилит, увеит, сакроилеит в отсутствии полного набора критериев). Несмотря на гетерогенность заболеваний данной группы, клинически серонегативные спондилоартропатии имеют общие признаки и характеризуются:
- патологическими изменениями в крестцово-подвздошном отделе и/или других суставах позвоночника;
- синдромом периферической воспалительной артропатии, проявляющейся асимметричным артритом преимущественно нижних конечностей;
- энтезопатическим синдромом;
- ассоциацией с антигеном гистосовместимости HLA-B27;
- тенденцией к накоплению этих заболеваний в семьях;
- частым наличием внесуставных симптомов (поражение глаз, клапанов аорты, кожи) [5, 6]. В МКБ-10 поражения суставов при рассматриваемых нами заболеваниях кодируются следующим образом: М07.4 Артропатия при болезни Крона (К50); М07.5 Артропатия при язвенном колите (К51).
Поражения суставов при ХВЗК встречаются в 20–40% случаев и протекают в виде артритов (периферической артропатии), сакроилеита и/или анкилозирующего спондилита [3].
Артриты
Артриты относятся к наиболее частым суставным проявлениям хронических воспалительных заболеваний кишечника. Нередко они сочетаются с поражением кожи в виде узловатой эритемы. Частота возникновения артритов, распространенность поражения толстой кишки коррелируют с воспалительной активностью основного заболевания. В некоторых случаях артриты могут предшествовать кишечным проявлениям за много месяцев и даже лет, а также сохраняться в фазу ремиссии [7].
Клиническая картина артритов при болезни Крона и язвенном колите идентична. Характерно ассиметричное, мигрирующее поражение суставов чаще нижних конечностей. Преимущественно страдают коленные и голеностопные суставы, далее следуют локтевые, тазобедренные, межфаланговые и плюснефаланговые суставы. Число пораженных суставов обычно не превышает пяти. Суставной синдром течет с чередованием периодов обострений, длительность которых не превышает 3–4 месяцев, и ремиссий. Могут выявляться энтезопатии, талалгии. Артриты, как правило, начинаются остро. Однако нередко больные предъявляют жалобы только на артралгии, и при объективном обследовании изменения не обнаруживаются. Со временем обострения артритов становятся реже. У большинства больных артриты не приводят к деформации или деструкции суставов.
Выделяют два типа поражения периферических суставов. Для первого характерно поражение небольшого количества крупных суставов, ассиметричность суставного синдрома, острое течение. Часто при этом типе суставной синдром предшествует клинической картине основного заболевания, ассоциируется с его обострениями и сочетается с другими внекишечными проявлениями ХВЗК. Второй тип протекает по типу симметричного полиартрита, его обострения не совпадают по времени с обострениями основного процесса в кишечнике и другими системными проявлениями заболевания [7, 8].
Проведение колэктомии у больных язвенным колитом способствует прекращению рецидивирующих артритов [3].
Сакроилеит
По данным рентгенологического исследования, сакроилеит обнаруживается примерно у 50% больных ХВЗК. При этом у 90% он имеет бессимптомное течение. Он не ассоциируется с повышенной частотой выявления у больных HLA-B27. Также наличие сакроилеита не коррелирует с активностью воспалительного заболевания кишечника. Существуя на протяжении нескольких лет, может быть предшественником язвенного колита или болезни Крона. Сакроилеит может быть единственной локализацией изменений со стороны суставов, но часто сочетается с первым типом течения артритов. Необходимо помнить, что сакроилеит может быть ранним симптомом анкилозирующего спондилита. Терапия кишечного синдрома не приводит к изменению клинической картины сакроилеита [7].
Анкилозирующий спондилит
Анкилозирующий спондилит (АС) при ХВЗК клинически, как и сакроилеит, не отличается от идиопатического анкилозирующего спондилита. Чаще встречается у лиц мужского пола. По наблюдениям, у лиц женского пола поражение шейного отдела позвоночника манифестирует в более молодом возрасте и протекает тяжелее. Симптомы АС обычно предшествуют манифестации болезни Крона или язвенного колита и не коррелируют с активностью воспаления в кишечнике. Отмечаются боли в позвоночнике, чувство утренней скованности, нарастает ограничение подвижности в шейном, грудном, поясничном отделах позвоночника. Активная терапия основного заболевания не приводит к изменению клинической картины спондилита [3, 7, 9, 10].
Клиническое наблюдение
Иллюстрацией к вышеизложенному материалу может служить клиническое наблюдение за течением болезни Крона с внекишечными суставными проявлениями у пациента подросткового возраста.
Клинический диагноз: болезнь Крона (поражение тонкого, толстого кишечника, желудка, пищевода), фаза ремиссии, внекишечные проявления (лихорадка в анамнезе, лимфаденопатия, гепатомегалия, железодефицитная анемия). Осложнения: стеноз устья баугиниевой заслонки, сужение входа в слепую кишку.
Ювенильный спондилоартрит, активность I степени, рентгенологическая стадия I–II, НФ-1.
Из анамнеза жизни следует отметить, что мальчик от 2-й беременности, протекавшей физиологически, от первых срочных родов, осложнившихся слабостью родовой деятельности (акушерское пособие — наложение проходных щипцов). Находился на раннем искусственном вскармливании. На первом году жизни наблюдался неврологом. В дальнейшем редкие ОРВИ. Привит по календарю. Детскими инфекциями не болел. Наследственность отягощена по заболеваниям сердечно-сосудистой системы.
Анамнез заболевания: в сентябре 2008 г. после травмы левого голеностопного суставе у ребенка отмечался отек и болезненность в левом голеностопном сустава. Получал местно мази с нестероидными противовоспалительными препаратами (НПВП). Также применялось физиотерапевтическое лечение, что вызвало ухудшение состояния: появилась субфебрильная лихорадка, усилились артралгии в левом голеностопном суставе, также появилась болезненность в височно-нижнечелюстных суставах с ограничением подвижности в них. За три месяца мальчик похудел на 12 кг. Обследован по месту жительства: в анализе крови скорость оседания эритроцитов (СОЭ) 47–55 мм/ч, лейкоцитоз, в биохимическом анализе повышение аспартатаминотрансферазы (АСТ) до 2 норм, С-реативный белок (СРБ)++. Выявлена кишечная инфекция: титр к S. flexneri 1:400. Проводимая терапия (НПВП, антибиотики — цефазолин, цефтриаксон, амикацин) эффекта не дала. На фоне приема антибиотиков появился неустойчивый, разжиженный стул, боли в околопупочной области. В НИИ фтизиатрии исключен туберкулез. При компьютерной томографии левого голеностопного сустава выявлено: сужение суставной щели, краевая узура в медиальной лодыжке, выпот в полость сустава. Исключена ортопедическая патология. С января 2009 г. наблюдается в Университетской детской клинической больнице (УДКБ) Первого МГМУ им. И. М. Сеченова. При поступлении состояние средней степени тяжести. Бледен, выражены симптомы интоксикации. Дистрофия. Суставной синдром в виде выпота, ограничения подвижности, повышения местной температуры и болезненности в левом голеностопном суставе, ахиллобурсит слева, умеренная атрофия мышц левой голени, походка нарушена. Ригидность грудного отдела позвоночника (+ 1 см), ограничение подвижности в височно-нижнечелюстных суставах. Отмечаются боли в животе, разжиженный стул. Высокая гуморальная активность: СОЭ до 50 мм/ч, лейкоцитоз до 22 000 в 1 мкл с палочкоядерным сдвигом до 24%, анемия — гемоглобин (Hb) 109 г/л, однократно повышения уровней АСТ и аланинаминотрансферазы (АЛТ) до 1,5–2 норм. Обследован на артритогенные инфекции: результат отрицателен. При иммуногенетическом обследование выявлены HLA 1-го класс: А2, В 64 (14), В38 (16). Ребенку выставлен предварительный диагноз: ювенильный спондилоартрит. Использовали пульс-терапию глюкокортикоидами, введение внутривенного иммуноглобулина, НПВП, проведена внутрисуставная пункция левого голеностопного сустава с введением Депо-медрола. В качестве базисного препарата ребенку назначен сульфасалазин 1500 мг/сутки. На фоне проводимой терапии отмечалась положительная динамика, несколько снизилась лабораторная активность, купированы боли в животе, нормализовался стул, возрос объем движений в левом голеностопном суставе, однако сохранялась отечность и утренняя скованность в нем. В марте 2009 г. вновь обострение суставного синдрома, лихорадка до 37,8 °C, боли в животе, неустойчивый стул, появилась отечность правого голеностопного сустава. Ребенок вновь госпитализирован в УДКБ в мае-июне 2009 г.: СОЭ 29 мм/ч, гипохромная анемия, тромбоцитоз, СРБ ++, IgG 2150 мг/дл, в копрограмме эритроциты до 40 в поле зрения однократно. Выполнена ректороманоскопия: сигмоидит, проктит, эндоскопические признаки колита. На эзофагогастродуоденоскопии: эрозивный гастрит, дуоденит, еюнит. Рекомендовано проведение колоноскопии, от проведения которой родители ребенка отказались. Мальчику была повышена доза сульфасалазина до 1750 мг/сутки. Но состояние пациента оставалось нестабильным: сохранялись неустойчивый стул, отечность, болезненность и нарушение функции левого голеностопного сустава. В октябре 2009 г. вновь госпитализирован в УДКБ: СОЭ 34 мм/ч, наросла гипохромная анемия Hb 90 г/л, тромбоцитоз, лейкоцитоз до 16 тыс. в 1 мкл, СРБ ++. Ребенку проведена колоноскопия: болезнь Крона, глубокие язвы в ободочной кишке, язвенный терминальный илеит, проктит, колит, сигмоидит. По данным магнитно-резонасной томографии илеосакральных сочленений — левосторонний сакроилеит. Мальчику проводилась коррекция терапии: сульфасалазин отменен, назначен Салофальк 2000 мг/сутки, продолжал получать НПВП. На фоне терапии состояние с положительным эффектом — купирован кишечный синдром, нормализовался стул. Однако в декабре 2009 г. после ОРВИ вновь обострение основного заболевания: повышение температуры до фебрильных цифр, СОЭ 50 мм/ч, отек голеностопных суставов, скованность в них. С конца декабря 2009 г. отмечаются схваткообразные боли в животе, разжиженный стул. В январе 2010 г. в связи с высокой лабораторной и клинической активностью основного заболевания, неэффективностью традиционной терапии (монотерапии Салофальком), прогрессирующей инвалидизацией пациента начата терапия инфликсимабом. 3.02.2010 г. проведено первое введение, на фоне которого отмечена выраженная положительная динамика, купирован кишечный синдром, возрос объем движений в голеностопных суставах, уменьшилась экссудация в них, снизилась активность лабораторных показателей. 17.02.2010 и 17.03.2010 проведены второе и третье внутривенное введение Ремикейда по 100 мг на 1 введение. На фоне лечения отчетливая положительная динамика, полностью купирован кишечный синдром, прибавил в весе 7 кг, однако сохранялось снижение Hb до 87 г/л. При госпитализации в мае-июле 2010 г. СОЭ 23 мм/ч, Hb 91 г/л. При повторной колоноскопии выявлено сужение поперечной ободочной кишки, не проходимое для эндоскопа. Проведена ирригоскопия: слепая, восходящая, 1/2 поперечной кишок деформированы, с выраженным спазмом, с постстенотическим расширением поперечной и нисходящей ободочной кишки. Продолжилась терапия инфликсимабом, с учетом увеличения веса пациента доза повышена. Всего мальчик получил 24 введений инфликсимаба. Состояние его полностью стабилизировалось. Он поправился на 22 кг, вырос на 25 см. Полностью купированы кишечный и суставные синдромы. Полностью нормализовались лабораторные показатели СОЭ 5–14 мм/час. Hb 151 г/л. Мальчик ведет активный образ жизни.
Литература
- Яблокова Е. А. Клинические особенности и нарушение минерализации костной ткани у детей с воспалительными заболеваниями кишечника. Дисс. канд. мед. наук. М., 2006. 185 с.
- Tourtelier Y., Dabadie A., Tron I., Alexandre J. L., Robaskiewicz M., Cruchant E., Seyrig J. A., Heresbach D., Bretagne J. F. Incidence of inflammatory bowel disease in children in Britani (1994 –1997). Breton association of study and research on digestive system diseases (Abermad) // Arch Pediatr. 2000 Apr; 7 (4): 377–384.
- Гвидо Адлер. Болезнь Крона и язвенный колит. М.: ГЭОТАР-МЕД, 2001.
- Шостак Н. А., Правдюк Н. Г., Абельдяев Д. В. Серонегативные спондилоартропатии — совершенствование подходов к ранней диагностике и лечению // РМЖ. 2013, № 6, 1002–1008.
- Справочник по ревматологии / Хаким А., Клуни Г., Хак И.; пер. с англ. Н. И. Татаркиной. М.: ГЭОТАР-Медиа, 2010. 560 с.
- Dougados M., Hermann K. G., Landewe R. et al. Assess spondyloarthritis to international Society (ASAS) handbook: a guide The Assessment of spondyloArthritis // Ann Rheum Dis. 2009. Vol. 68. Р. 1–44.
- Ревматология. Национальное руководство под ред. Е. Л. Насонова, В. А. Насоновой. М.: ГЭОТАР-Медиа, 2008. 720 с.
- D’Incà R., Podswiadek M., Ferronato A., Punzi L., Salvagnini M., Sturniolo G. C. Articular manifestation in inflammatory bowel disease patients. A prospective study // Dig Liver Dis. 2009, Mar 9.
- Rodriguez V. E., Costas P. J., Vazquez M., Alvarez G., Perez-Kraft G., Climent C., Nazario C. M. Prevalence of spondyloarthropathy in Puerto Rican patients with inflammatory bowel disease/Ethn Dis. 2008, Spring; 18 (2 Suppl 2): S2–225–9.
- Руководство по детской ревматологии / под ред. Н. А. Геппе, Н. С. Подчерняевой, Г. А. Лыскиной. М.: ГЕОТАР-Медиа, 2012. 720 с.
А. В. Мелешкина1, кандидат медицинских наук
С. Н. Чебышева, кандидат медицинских наук
Е. С. Жолобова, доктор медицинских наук, профессор
М. Н. Николаева
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
1 Контактная информация: meleshkina.angel@mail.ru
Abstract. The article covers specifics of development of articular manifestations under chronic inflammatory bowel diseases and provides clinical example of crohn’s disease development starting with un-bowel manifestations in forn of articular syndrome.
Источник
