Роттердамские критерии диагностики синдрома поликистозных яичников

До настоящего времени существует определённая путаница и несогласованность среди врачей ультразвуковой диагностики в оценке эхоструктуры яичников, а среди пациентов непонимание того, что означает термин “поликистозные яичники”.
Уважаемые читатели, представляю вашему вниманию мой перевод замечательной статьи, посвящённой этой проблеме. Статья опубликована в официальном журнале ISUOG – Ultrasound in Obstetrics & Gynecology (UOG), так же известном как «Белый Журнал».
«Подсчет фолликулов яичника: обновленный порог для диагностики гиперандрогенной ановуляции
Первое описание связи между увеличенными яичниками и субфертильностью было опубликовано почти 300 лет назад, когда Валлиснери описал «молодую крестьянку», которая была «умеренно толстой, бесплодной, с яичниками, больших размеров чем обычно (с голубиное яйцо, бугристыми, блестящими с белым налётом. Более распространенный термин, используемый для описания таких яичников – «поликистозные яичники» – не вводился до 1935 года, и с середины 1950-х годов связанные с ним состояния здоровья, включая субфертильность, нарушения менструального цикла и гиперандрогенизм, назывались «синдром поликистозных яичников» (СПКЯ). Сообщается, что СПКЯ встречается у 5–10% женщин репродуктивного возраста, а среди женщин с ожирением распространенность еще выше.
Почему следует избегать использования термина “поликистозный”
Описание яичников как поликистозных вводит в заблуждение; этот термин имеет негативное значение, и его использование отвлекает от реальных проблем, связанных с бесплодием, менструальными нарушениями и гиперандрогенизмом. Многие женщины и некоторые медицинские работники смущены этим термином; часто женщины обращаются за повторным ультразвуковым исследованием, чтобы увидеть, присутствуют ли «кисты» и, если они есть, могут ли они быть удалены хирургическим путем. Более того, Австралийское исследование показало, что почти половина женщин с данным состоянием ошибочно посчитала кисты яичников в качестве ключевого результата УЗИ.
На самом же деле, эти яичники содержат множество функциональных фолликулов (из которых можно извлечь ооциты для созревания in vitro), которые растут при стимуляции, что приводит к повышенному риску синдрома гиперстимуляции яичников. Поэтому мы считаем, что следует избегать термина «поликистозный», чтобы предотвратить ненужную озабоченность и, следовательно, беспокойство у многих женщин, которым ежедневно диагностируют это состояние.
Выбор наилучшего термина для замены «поликистозный»
Хотя в некоторых недавних публикациях были предложены альтернативы, они довольно громоздки, а в некоторых случаях даже сложны для понимания. По нашему мнению, сонографический вид яичника лучше описать просто как увеличение количества фолликулов или «мультифолликулярный». Кроме того, мы считаем, что состояние было бы легче объяснить и понять, если бы вместо «СПКЯ» оно было названо «гиперандрогенной ановуляцией» (ГА). Этот термин заключает в себе суть состояния: эндокринное расстройство с репродуктивными особенностями или, в частности, связь между гиперандрогенизмом и ановуляцией. ГA может быть либо идиопатической, либо иметь известную причину (например, резистентность к инсулину, врожденная гиперплазия надпочечников). Основная проблема в попытке объединить все причины в один «синдром» состоит в том, что он становится слишком сложным или разнородным, чтобы его можно было понять. Кроме того, классификация всех женщин с ГА как имеющих одно заболевание вводит в заблуждение: резистентность к инсулину, которая связана с ожирением, метаболическим синдромом и повышенным риском сердечно-сосудистых заболеваний, является одной из причин ГА и, следовательно, чаще встречается среди женщин с ГА; однако это не означает, что у всех женщин с ГА имеется резистентность к инсулину и последующий повышенный риск метаболического синдрома и сердечно-сосудистых заболеваний. Простое указание на то, что ожирение и последующая резистентность к инсулину могут вызывать ГА (а не наоборот), должно помочь прояснить, почему потеря веса может скорректировать менструальные нарушения и развеять распространенное заблуждение, что избавление от «кист яичников» (например, с помощью гормональных оральных контрацептивов, которые повышают риск венозного тромбоза), также поможет при ожирении, метаболическом синдроме и снизит риск сердечно-сосудистых осложнений.
Было показано, что разные фенотипы СПКЯ имеют разные клинические последствия. Однако мы полагаем, что само разделение на различные фенотипы возникло только из-за излишне низкого Числа Фолликулов в каждом Яичнике (FNPO ≥12), которое было предложено в качестве диагностического критерия для ГА в 2003 году, и что это можно преодолеть, используя более высокий порог (таблица 1). Люди с ГА могут иметь или не иметь большое количество фолликулов в яичниках, нет необходимости классифицировать их основываясь на этом. Тем не менее, количество фолликулов может быть важным для определения наиболее вероятной причины ГА.
Таблица 1. Предлагаемая классификация яичников основана на Количестве Фолликулов в каждом Яичнике (FNPO), для использования в обычной ультразвуковой практике, и на Подсчёте Общего Количества Антральных Фолликулов (AFC), для использования в центрах репродукции.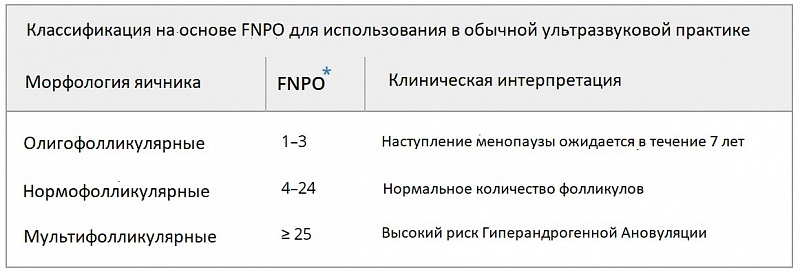
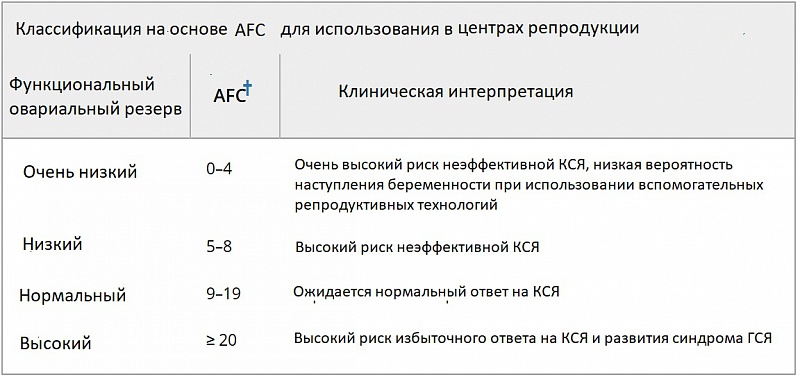
Примечание: необходимы дополнительные доказательства для изучения того, полезны ли эти предложенные системы классификации в клинической практике. Подсчет фолликулов как для FNPO, так и для общего AFC следует проводить преимущественно на ранней фолликулярной фазе и при отсутствии гормональной контрацепции.
* Использование правого или левого яичника, в зависимости от того, какое значение FNPO самое высокое.
† Использование суммы антральных фолликулов из правого и левого яичников.
КСЯ- контролируемая стимуляция яичников; ГСЯ – гиперстимуляция яичников.
Подсчет фолликулов яичников у женщин с нарушениями менструального цикла
Гиперандрогенная ановуляция
Количество фолликулов, используемых в качестве диагностического критерия для ГА, необходимо обновить. С начала 1980-х годов в нескольких исследованиях сообщалось об ультразвуковых особенностях строения яичников у женщин с ГA. Несмотря на это, в 1990 году Национальный Институт Здравоохранения США (NIH) рекомендовали использовать в качестве диагностических критериев только гиперандрогенизм и овуляторную дисфункцию, и не принимать во внимание результаты УЗИ. Однако диагностические критерии Роттердамского соглашения ASRM (Американское Общество Репродуктивной Медицины) / ESHRE (Европейское Общество Репродукции и Эмбриологии Человека) 2003 года, принятые большинством практиков, признают важность ультразвука в качестве диагностического инструмента, предполагая, что диагноз следует подозревать когда присутствуют два из следующих трех критериев: олиго- / аменорея; клинические и / или биохимические признаки гиперандрогении; и поликистоз яичников, выявленный с помощью УЗИ.
Пороговым значением ASRM / ESHRE для определения поликистозных яичников при ультразвуковом исследовании было наличие 12 или более фолликулов диаметром 2–9 мм или увеличенный объем яичника (> 10 мл) по крайней мере в одном яичнике. Этот порог в 12 фолликулов был основан на исследовании, опубликованном Jonard et al. В 2003 году, в котором сообщалось, что FNPO 12 или более предлагает лучший компромисс между специфичностью (99%) и чувствительностью (75%) в обнаружении ГA . Однако недавние исследования с использованием новых ультразвуковых аппаратов с улучшенным разрешением показали высокую распространенность яичников с более чем 12 фолликулами у здоровых молодых женщин.
Целевая группа из Общества изучения Андрогенного Избытка и Синдрома Поликистозных Яичников (AE-PCOS) рассмотрела результаты недавно опубликованных исследований и сообщила о срочной необходимости обновления диагностических критериев, рекомендовав увеличить порог до ≥ 25 фолликулов при использовании современных ультразвуковых аппаратов. Мы согласны, этот новый порог должен начать использоваться немедленно. Мы также согласны с предложением целевой группы AE-PCOS, что возможно использование только объема яичника ≥ 10 мл в диагностике ГА (при отсутствии доминантного фолликула или жёлтого тела), в тех случаях, когда современный ультразвуковой аппарат недоступен. Настало время внести изменения, как в ультразвуковые критерии, так и в название этого состояния здоровья.
Менопауза
Женщины, приближающиеся к менопаузе, имеют уменьшенное количество фолликулов яичников. В связи с этим, независимо от того, много или мало, число фолликулов следует всегда отображать в протоколе УЗИ у женщин, проходящих обследование в связи с нарушением менструального цикла (Таблица 1). Недавнее исследование показало, что женщины с общим количеством фолликулов ≤ 4 (сумма антральных фолликулов в обоих яичниках) имеют высокую вероятность наступления менопаузы в течение 7 лет. Однако следует иметь в виду, что использование гормональной контрацепции может снизить общее количество фолликулов.
Подсчет фолликулов яичников у бессимптомных женщин
Многим женщинам без нарушения менструального цикла, проводятся УЗИ органов малого таза на определённых этапах их репродуктивной жизни; у некоторых из них будет большое количество фолликулов, в то время как у других будет небольшое количество. Мы считаем, что яичники без каких-либо признаков заболевания (например, опухолей) следует оценивать как нормальные, независимо от количества фолликулов, которые они содержат, и что количество фолликулов всегда следует сообщать, когда экзаменатор является опытным сонографистом, использующим ультразвуковой аппарат высокого разрешения. Конечно, следует помнить, что подсчёт фолликулов может не всегда быть точным, так как порой имеются технические ограничения.
Пониженное количество фолликулов у бессимптомных женщин может указывать либо на использование гормональной контрацепции, либо на снижение функционального резерва яичника, который может быть естественным или ятрогенным (например, после операции на яичнике или химиотерапии). Женщин с уменьшенным количеством фолликулов следует спросить об их желании забеременеть и посоветовать не откладывать попытки забеременеть, поскольку шансы на успешную естественную беременность уменьшаются с увеличением возраста, а женщины с сниженным количеством фолликулов имеют меньшие шансы на успех при использовании вспомогательных репродуктивных технологий.
Большое количество фолликулов может указывать на высокий риск ГА; но что делать, если у женщины, у которой нет признаков ановуляции или гиперандрогении, наблюдается большое количество фолликулов? Важно очень четко пояснить, что мы не знаем клинических последствий этого ультразвукового исследования у женщин с бессимптомным течением, и поэтому мы должны помнить о том, чтобы не ставить клеймо на основании только результатов ультразвукового исследования; что еще более важно, мы не должны сообщать об этих яичниках как о “поликистозных”, что вызовет только ненужную тревогу.
Можно использовать стратификацию морфологии яичников на основе FNPO (таблица 1). Однако важно подчеркнуть, что ни «олигофолликулярный», ни «мультифолликулярный» яичник не следует рассматривать как заболевание.
Ультразвуковая оценка яичников в центрах репродукции
Сонографам следует помнить, что пороговое значение, используемое для диагностики ГА, должно отличаться от того, которое используется для выявления женщин, подверженных риску чрезмерного ответа на контролируемую стимуляцию яичников во время вспомогательной репродукции; с этой целью должен использоваться значительно более низкий порог. Исследования показали, что у женщин с общим числом антральных фолликулов (AFC) (с учетом обоих яичников) > 20 имеют более высокий риск развития синдрома ГСЯ, в то время как женщины с пониженным общим AFC, как известно, подвержены риску плохой реакции яичников на стимуляцию и имеют пониженную вероятность наступления беременности после вспомогательной репродукции. Таким образом, общий AFC часто используется для индивидуализации контролируемой стимуляции яичников. Мы предлагаем вторую систему стратификации, основанную на общем числе антральных фолликулоов, для использования в центрах репродукции (Таблица 1).
Заключение
Термин «поликистоз» не следует использовать при описании морфологии яичников, поскольку он вводит в заблуждение и может привести к ненужной тревоге. Термин СПКЯ также проблематичен и должен быть заменен на гиперандрогенная ановуляция (ГА). Нынешний ультразвуковой критерий для диагностики ГА больше не является адекватным: мы одобряем использование недавно предложенного порога ≥ 25 фолликулов на яичник для этого диагноза.»
Конечно, данная статья — это лишь мнение её авторов, да и сами авторы отмечают, что «необходимы дополнительные доказательства для изучения того, полезны ли эти предложенные системы классификации в клинической практике».
С момента написания статьи в 2014 году медицина не стояла на месте.
В 2018 году Общество изучения Андрогенного Избытка и Синдрома Поликистозных Яичников (AE-PCOS) опубликовало новые клинические рекомендации. Ознакомиться можно по этой ссылке

Вот краткая выдержка, касающаяся УЗ части диагностики СПКЯ:
«Мы одобряем диагностические критерии СПКЯ Роттердамского соглашения (для постановки диагноза необходимы два из трёх критериев: клинический или биохимический гиперандрогенизм, овуляционная дисфункция, поликистоз яичников при УЗИ).
Ультразвук не следует использовать для диагностики СПКЯ у лиц с гинекологическим возрастом <8 лет (<8 лет после менархе) из-за высокой частоты мультифолликулярных яичников на этой стадии жизни.
При использовании влагалищного датчика с частотой 8 МГц, порогом для диагностики поликистозной морфологии яичников следует считать количество фолликулов (диаметром 2-9 мм) в любом яичнике > 20 и / или объем яичника ≥ 10 мл, при этом не должно быть никаких кист, доминантных фолликулов или жёлтого тела.
У пациентов с нерегулярными менструальными циклами и гиперандрогенизмом УЗИ яичников не требуется для диагностики СПКЯ; однако, ультразвук идентифицирует полный фенотип СПКЯ.
Термин «кистозный» является неправильным обозначением по отношению к «застрявшим» на антральной стадии фолликулам (не кисты).
Недостаточно данных для использования других ультразвуковых параметров, включая расположение яичников; максимальное количество фолликулов в одной сонографической плоскости (FSSP); распределение фолликулов по периферии яичника; яркая строма яичника; комбинации возраста, количества фолликулов, объема яичников и уровня тестостерона; или комбинации размера фолликулов и объема яичника для диагностики СПКЯ.
Существует необходимость в обучении тщательному и скрупулёзному подсчету фолликулов в каждом яичнике.»
AE-PCOS, несомненно одно из самых авторитетных обществ, изучающих проблемы СПКЯ, и следует прислушиваться к их рекомендациям. Несмотря на то, что в последних рекомендациях присутствует термин “PCOM” (поликистозная морфология яичника) при ультразвуковом описании, там же указывается, что речь не идёт о кистах, а “термин «кистозный» является неправильным обозначением по отношению к «застрявшим» на антральной стадии фолликулам”. Порогом отсечки для описания эхоструктуры яичников как “мультифолликулярной”, по видимому, на современном этапе следует считать > 20 антральных фолликулов (диаметром 2-9 мм) в любом из яичников.
Источник

Актуальность проблемы поликистоза яичников (ПКЯ) определяется большой распространенностью этой патологии и ведущим ее проявлением – бесплодием. ПКЯ объединяет различные по патогенезу, но сходные по характеру репродуктивных нарушений заболевания, которые на протяжении нескольких десятилетий было принято объединять в одну нозологическую форму – синдром поликистозных яичников (СПКЯ).
С.С. Попова, доцент кафедры эндокринологии и детской эндокринологии Харьковской медицинской академии последипломного образования
тематический номер: ЭНДОКРИНОЛОГИЯ
В настоящее время такой подход считается необоснованным и пересматривается, что требует внесения коррективов как в трактовку понятия «синдром поликистозных яичников», так и в методы его диагностики.
Вот уже 70 лет в многочисленных публикациях обсуждаются механизмы развития ПКЯ и подходы к его диагностике. Однако, несмотря на активные поиски оптимальных методов лечения больных ПКЯ, эта патология по-прежнему занимает лидирующую позицию среди причин женского бесплодия [8, 9].
Проблема ПКЯ чрезвычайно актуальна, поскольку у данной категории больных такие патологии, как ожирение, артериальная гипертензия, гипергликемия и другие проявления метаболического синдрома (МС) манифестируют в молодом возрасте [9].
Патогенез поликистоза яичников
Патогенетической основой ПКЯ является хроническая ановуляция, обусловленная гиперпродукцией андрогенов и повышением их конверсии в эстрогены. Избыточное поступление эстрогенов из экстрагландулярных источников приводит к нарушению цикличности и соотношения гонадотропных гормонов гипофиза, что поддерживает ановуляцию [13, 15].
Хроническая стимуляция яичников лютеинизирующим гормоном (ЛГ) вызывает гиперплазию внутренней тени фолликулов, что сопровождается повышением продукции андрогенов. Возникающая при этом высокая их внутрияичниковая концентрация приводит к ускорению атрезии фолликулов и утолщению капсулы яичников. Процесс кистозной атрезии овариальных фолликулов протекает на фоне атрофии гранулезы, связанной со снижением эффективности влияния фолликулостимулирующего гормона (ФСГ).
Представленные патогенетические основы развития ПКЯ на сегодня являются общепризнанными. Общеизвестным является и тот факт, что ПКЯ обнаруживают при различных по патогенезу и клинической симптоматике заболеваниях. Это явление вполне закономерно с учетом того, что к развитию и поддержанию гиперандрогенного статуса могут привести изменения различных функциональных систем организма женщин.
Наиболее распространенной причиной гиперандрогении надпочечникового происхождения является врожденная дисфункция коры надпочечников (ВДКН), обусловленная генетическими дефектами ферментов, необходимых для нормального стероидогенеза. Развивающееся при этом нарушение синтеза кортизола по принципу отрицательной обратной связи стимулирует секрецию адренокортикотропного гормона (АКТГ), что и служит причиной гиперпродукции андрогенов. Существует также гипотеза о том, что надпочечниковая гиперандрогения может быть связана не с дефицитом определенных ферментов, а напротив, с их патологически увеличенной активностью, что наблюдается при усилении активности цитохрома Р450с17, который регулируется единым универсальным геном СУР 17, локализующимся на 10-й хромосоме [14].
Избыточная продукция андрогенов при патологии гипоталамо-гипофизарной системы обусловлена усилением синтеза АКТГ в передней доле гипофиза и повышением функциональной активности коры надпочечников. При этом наряду с гиперандрогенией наблюдается усиление продукции глюкокортикоидов, что ведет к формированию клинического симптомокомплекса гиперкортицизма.
К типичным для гипоталамо-гипофизарной патологии нарушениям гормонального гомеостаза относится гиперпролактинемия, которая влияет на метаболизм андрогенов путем стимуляции их синтеза в коре надпочечников [2]. Кроме того, в условиях повышенной продукции пролактина уменьшается образование в печени тестостерон-эстрадиолсвязывающего глобулина (ТЭСГ).
При гипотиреозе вследствие снижения уровня ТЭСГ возрастает скорость метаболического клиренса тестостерона, ускоряется превращение андростендиона в тестостерон, а тестостерона – в эстрадиол [13], что согласно механизму отрицательной обратной связи вызывает неадекватную секрецию гонадотропинов, обусловливающую хроническую ановуляцию.
К выраженной гиперандрогении может привести нарушение метаболизма андрогенов в периферических тканях. Важную роль в обмене андрогенов играют кожа и печень, в которых андростендион превращается в тестостерон, а тот, в свою очередь, в дигидротестостерон, обладающий наиболее выраженной андрогенной активностью [4]. У женщин с избыточной массой тела дополнительными факторами развития гиперандрогении является снижение синтеза ТЭСГ и инсулинорезистентность [4].
Можно говорить о большом многообразии причин, с которыми может быть связано развитие ПКЯ, что объясняет значительный полиморфизм СПКЯ. Это обстоятельство подтверждает существование тесной связи составляющих элементов репродуктивной системы между собой, а также с другими органами и системами. Можно считать, что яичникам отведена роль «биологических часов», или «индикатора» нарушений гормонального гомеостаза [3]. По мере прогрессирования этих нарушений функциональные изменения в яичниках сопровождаются их анатомической перестройкой, соответствующей понятию «поликистоз», что является своеобразным маркером неблагополучия эндокринной системы в целом.
Из всего вышеизложенного можно сделать вывод о существовании различных по патогенезу и клинической симптоматике заболеваний, сопровождающихся ПКЯ. Можно констатировать, что эти структурные изменения яичников во многих случаях являются определяющим фактором в формировании клинического симптомокомплекса. Вместе с тем необходимо признать факт существования клинического варианта ПКЯ, полностью соответствующего синдрому Штейна-Левенталя в его первоначальной трактовке [25], когда в развитии гирсутизма и репродуктивных нарушений преимущественную роль играет гиперандрогенная дисфункция кистозно измененных яичников.
Данное положение достаточно четко было сформулировано Б.И. Железновым еще в 1982 году [6]. Автор выделил первичный, истинный ПКЯ, или болезнь ПКЯ (БПКЯ), и вторичный ПКЯ, или СПКЯ, который был назван поликистозоподобным синдромом. Однако такое разделение не нашло своего применения в клинической практике, так что в течение нескольких десятилетий для обозначения различных заболеваний, сопровождающихся ПКЯ, использовали единый термин – «синдром поликистозных яичников».
Синдром поликистоза яичников
До недавнего времени выделяли три клинических формы СПКЯ:
- яичниковую (с преимущественно овариальной гиперандрогенией);
- надпочечниковую, или сочетанную (с яичниковой и надпочечниковой гиперандрогенией);
- центральную, или диэнцефальную (с выраженными проявлениями патологии гипоталамо-гипофизарной системы) [7, 16].
В настоящее время все больше специалистов в области гинекологической эндокринологии отказываются от подобной классификации СПКЯ, признав ее, как считает Т.А. Назаренко, не только патогенетически не обоснованной, но даже вредной, поскольку она препятствует диагностике других состояний [9].
Новые подходы к трактовке понятия «синдром поликистозных яичников» и определению критериев диагностики этого заболевания разработаны в Национальном институте здоровья США и приняты на конференции в 1990 году [18, 23].
Согласно этим представлениям, которые поддерживает все большее количество исследователей, СПКЯ – это диагноз исключения. Для его верификации, кроме наличия гиперандрогении и ановуляции, обязательным является отсутствие таких самостоятельных эндокринных заболеваний, как врожденная дисфункция коры надпочечников, первичная гиперпролактинемия и др. Именно такой «упрощенный» подход к диагностике СПКЯ, по мнению R. Homburg [22], наиболее обоснован и способен объединить результаты проводимых работ, определить круг нерешенных проблем и создать плацдарм для дальнейших исследований. Использование же множества различных дефиниций синдрома затрудняет определение его этиологии, оценки клинических проявлений и подходов к лечению, а также долгосрочных прогнозов течения этого распространенного заболевания.
Таким образом, термины «склерокистоз яичников», «болезнь поликистозных яичников», «вторичные поликистозные яичники» и соответствующие им «надпочечниковая» и «диэнцефальная» формы СПКЯ следует считать устаревшими, поскольку это терминологическое разнообразие во многом способствует различному пониманию патологических основ заболевания. С сожалением приходится констатировать тот факт, что и термин «синдром Штейна-Левенталя» все реже встречается на страницах современных изданий. Признание этого термина устаревшим С.Н. Хейфец [17] обосновывает тем, что описанная Штейном и Левенталем триада (вторичная аменорея – гирсутизм – увеличенные яичники) является слишком ортодоксальной, позволяющей врачам широко ставить диагноз.
В свете вышеизложенной современной трактовки термина «синдром поликистозных яичников» можно отметить его соответствие понятию клинического симптомокомплекса, описанного 70 лет тому назад чикагскими гинекологами [25]. Это соответствие определяется как наличием у больных гиперандрогении (гирсутизма), хронической ановуляции (первичного бесплодия), так и отсутствием признаков эндокринной патологии. Несомненной заслугой Штейна и Левенталя является предложенная ими методика хирургического лечения больных (клиновидная резекция яичников), которая используется до настоящего времени.
Критерии диагностики СПКЯ
Анализ мировой литературы свидетельствует о том, что единые критерии диагностики СПКЯ не разработаны. Однако в современных исследованиях все шире используются рекомендации, принятые на конференции Национального института здоровья США в 1990 г. [9, 23], которые Д.Е. Шилин рассматривает «…единственным документом, хотя бы отчасти регламентирующим процесс обследования и призванным скорее предотвратить гипердиагностику заболевания, чем обеспечить его выявление на ранних стадиях» [18].
Эти критерии можно обобщить следующим образом:
- олиго- и/или аменорея, ановуляция;
- клинические и/или биохимические признаки гиперандрогении;
- поликистозные яичники по данным УЗИ.
Согласно представленным данным основными критериями СПКЯ, рекомендуемыми для клинической практики, являются хроническая ановуляция, а также клинические или биохимические признаки гиперандрогении при исключении других известных заболеваний.
В исследованиях Т.А. Назаренко [9] СПКЯ определен как «…синдром овариальной дисфункции с обязательным наличием олиго-, аменореи, ановуляции и первичного бесплодия в совокупности с характерными ультразвуковыми и/или биохимическими параметрами». Частота клинических и лабораторных признаков представлена автором следующим образом.
- Обязательные (у 100% женщин):
- нарушение менструального цикла по типу олиго-, аменореи;
- ановуляция;
- первичное бесплодие;
- УЗИ-признаки поликистозных яичников.
- Часто встречающиеся (более чем у 50% женщин):
- гирсутизм;
- гиперандрогения (повышение уровня тестостерона);
- повышение уровня ЛГ.
- Наблюдаемые менее чем у 50% женщин:
- акне;
- алопеция;
- ожирение.
При этом было обращено внимание на то, что «…диагноз СПКЯ у фертильных женщин с регулярным овуляторным менструальным циклом представляется необоснованным, даже если у них выявлены гирсутизм, гиперандрогения и кистозные изменения в яичниках».
СПКЯ и метаболический синдром
В настоящее время пристальное внимание исследователей, занимающихся проблемами СПКЯ, занимает оценка этой патологии с позиций ее принадлежности к МС. На большом клиническом материале показано, что СПКЯ часто сопутствуют инсулинорезистентностъ и связанная с ней гиперинсулинемия [20, 21]. Отмечена также важная роль гиперинсулинемии в избыточном образовании андрогенов и развитии ПКЯ. Повышенный уровень инсулина или инсулиноподобных факторов роста, действуя синергично с ЛГ, усиливает функциональную активность тека-клеток яичников. Инсулин может подавлять продукцию ТЭСГ, что приводит к повышению концентрации в крови свободного тестостерона, а также участвует в синтезе и метаболизме андрогенов посредством прямой стимуляции инсулиновых рецепторов в яичниках. При подавлении яичниковой гиперандрогении инсулинорезистентность сохраняется, что подтверждает ее первичность. Снижение уровня андрогенов в условиях, обеспечивающих подавление синтеза инсулина или повышение чувствительности к нему периферических тканей, также служит аргументом в пользу существования взаимосвязи между гиперандрогенией и гиперинсулинемией, а также первичности последней.
Клинической иллюстрацией данного положения является положительный эффект лечения больных с СПКЯ пероральными сахароснижающими препаратами (метформином, розиглитазоном). При этом отмечены нормализация менструального цикла и фертильности, а также уменьшение выраженности клинических проявлений гиперандрогении [24].
Однако в настоящее время все более убедительно звучат данные об отсутствии взаимной обусловленности и причинно-следственной связи в «дуэте», представленном инсулинорезистентностью и гиперандрогенией. Существуют доказательства того, что эти патологические состояния развиваются и существуют параллельно, взаимно осложняя течение друг друга. В основу этих доказательств положены научные открытия последних лет. В частности, установлено, что в состав молекулы инсулинового рецептора и структуры цитохрома Р450с17, регулирующего синтез стероидных гормонов, входит аминокислота серин. В условиях избыточного фосфорилирования серина снижается чувствительность инсулиновых рецепторов, то есть развивается инсулинорезистентность. Вместе с тем повышение активности стероидогенного цитохрома вызывает манифестацию гиперандрогении и связанных с ней репродуктивных нарушений [14, 18].
Механизмы взаимодействия гиперандрогении и инсулинорезистентности при СПКЯ окончательно не изучены. Направления этой дискуссии, по мнению Т.А. Назаренко, «…диаметрально противоположны: от признания инсулинорезистентности и гиперинсулинемии ведущими звеньями в формировании синдрома до утверждений, что гиперинсулинемия – лишь симптом, имеющийся у некоторых больных с СПКЯ» [9]. Очевидно, указанные разногласия связаны с тем, что различные эндокринопатии, сопровождающиеся ПКЯ, в этих исследованиях по-прежнему рассматривают как СПКЯ, т. е. относят к единому заболеванию.
Следует отметить, что, несмотря на активное изучение МС, его единые диагностические критерии до сих пор не определены. Тем не менее для его идентификации у женщин могут быть использованы рекомендации, разработанные в 2005 году. Американской ассоциацией сердца и Национальным институтом сердца, легких и крови – An American Heart Association (National Heart, Lung and Blood Institute Scientific (AHA/NHLBI) [19]:
- абдоминальное ожирение (окружность талии >88 см);
- повышенный уровень триглицеридов: ≥150 мг/дл (1,7 ммоль/л) или уже проводимая терапия по поводу повышенного уровня триглицеридов;
- низкая концентрация холестерина липопротеинов высокой плотности (ХС ЛПВП):
- высокое артериальное давление (АД): систолическое АД≥130 мм рт. ст. или диастолическое АД ≥85 мм рт. ст., или уже проводимая антигипертензивная терапия;
- повышенный уровень глюкозы натощак: ≥100 мг/дл (5,6 ммоль/л) или уже проводимая терапия по поводу повышенного уровня глюкозы в крови.
Для диагностики МС достаточно наличия любых трех из указанных критериев.
Общепринятое до недавнего времени объединение в одно заболевание – СПКЯ – различных эндокринопатий, сопровождающихся кистозными изменениями овариальной ткани, нецелесообразно и уходит в прошлое. Согласно современным представлениям данному синдрому как отдельной нозологической форме патологии соответствует клиническая симптоматика, обусловленная гиперандрогенией яичникового происхождения. Обязательным условием диагностики СПКЯ является исключение самостоятельного эндокринного заболевания, ответственного за формирование хронической ановуляции. Необходимо дальнейшее изучение СПКЯ с позиций его принадлежности к МС.
Следует также отметить, что, несмотря на изменения представлений о СПКЯ, остаются серьезные проблемы, связанные с дифференцированием этого заболевания среди различных гиперандрогенных состояний. На первый взгляд, исключение самостоятельной эндокринной патологии, предусмотренное в современном подходе к диагностике СПКЯ, не представляет особых сложностей. Действительно, клинические проявления и принципы диагностики эндогенного гиперкортицизма, гиперпролактинемии и других вариантов эндокринной патологии общеизвестны и могут быть дополнены современными гормональными и инструментальными исследованиями. Однако это положение распространяется лишь на органические формы заболеваний с манифестными клиническими проявлениями, к которым, в частности, относятся болезнь и синдром Иценко-Кушинга, пролактинома, классическая ВДКН, чаще всего сопровождающиеся атрофией яичников [1, 5]. Морфологические изменения овариальной ткани, соответствующие поликистозу, развиваются, как правило, при эндокринопатиях со стертыми клиническими проявлениями, которые имеют определенное сходство с СПКЯ. Это в первую очередь касается неклассических форм ВДКН, которые по распространенности занимают лидирующую позицию среди гиперандрогенных состояний. Согласно данным современных исследований по клиническим проявлениям нозологические формы ВДКН весьма существенно отличаются от классических вариантов данной патологии [14]. При этом результаты гормональных исследований могут частично совпадать с показателями, присущими здоровым лицам, а их повторяемость является невысокой. Клиническое сходство первичного гиперпролактинемического гипогонадизма с СПКЯ определяется отсутствием манифестной эндокринной симптоматики, незначительной выраженностью андрогенизации, а также наличием избытка массы тела [5]. Общеизвестно, что повышенное содержание пролактина в крови у больных с СПКЯ – достаточно распространенное явление.
Рамки настоящей публикации не позволяют представить современные подходы, обеспечивающие дифференцирование СПКЯ и указанных эндокринных заболеваний (разработке дифференциально-диагностических критериев различных эндокринопатий, сопровождающихся ПКЯ, посвящены и наши собственные исследования [10, 11, 12]). Целесообразно также отметить, что решение этих задач стало возможным благодаря использованию нового для эндокринологов и гинекологов подхода – соматогенетического исследования с синдромологическим анализом.
Источник
