Сепсис синегнойный код мкб

Содержание
- Описание
- Дополнительные факты
- Причины
- Патогенез
- Классификация
- Симптомы
- Возможные осложнения
- Диагностика
- Лечение
- Прогноз
- Профилактика
- Список литературы
Названия
Название: Синегнойная инфекция.
Синегнойная инфекция
Описание
Pseudomonas инфекция. Это инфекционное заболевание, вызванное вторжением Pseudomonas aeruginosa Это ведущая больничная инфекция. Хронические формы характеризуются повреждением дыхательных путей с образованием «биологических пленок», при остром течении – бактериемией и повреждением внутренних органов. Диагноз основан на обнаружении возбудителя в биологических материалах пациента. Лечение включает этиотропную антибактериальную терапию, детоксикационные агенты, жаропонижающие средства и другие симптоматические препараты. В некоторых случаях показано хирургическое лечение.
Дополнительные факты
Pseudomonas aeruginosa был впервые описан в 1850 году французским хирургом Седиллом. В 1882 году французскому военному фармацевту Jessard удалось выделить чистую культуру возбудителя, а в 1916 году была выявлена эпидемиология этого заболевания. Заболевание встречается повсеместно, бактерии встречаются в почве, воде и растениях. Здесь нет явной сезонности. В больницах физиотерапевтическое и реанимационное оборудование считается любимым местом. В группу риска входят недоношенные дети, дети до 3 месяцев, пожилые люди, пациенты в отделениях гемодиализа, химиотерапии, нейрохирургии и реанимации, пациенты с муковисцидозом и иммуносупрессией.

Синегнойная инфекция
Причины
Возбудитель болезни – Pseudomonas aeruginosa (Pseudomonas aeruginosa) и его штаммы – это условно-патогенный микроорганизм, который может вызывать повреждение только при отсутствии адекватного ответа иммунной системы. Источником инфекции являются больные люди и животные, несущие бактерии, преимущественное расположение микроорганизмов – кожа, кишечник. Заражение происходит от капель в воздухе и от пищи. Путь заражения при внутрибольничной инфекции обычно проходит через нестерильные инструменты, руки медицинского персонала и предметы ухода за больными. Бактерия погибает во время кипения, во время автоклава, а также при воздействии 3% перекиси водорода и хлорсодержащих дезинфицирующих средств.
Патогенез
Когда микробы попадают на поврежденную кожу или слизистую оболочку, происходит массивное разрушение тканей из-за воздействия экзотоксинов и веществ, выделяемых бактериями. Как правило, слизистая оболочка тела способна нейтрализовать эффект Pseudomonas aeruginosa благодаря мукоцилиарному клиренсу и механическому барьеру. Привлечение нейтрофилов и активный фагоцитоз усиливают образование многих антибактериальных цитокинов, ферментов и свободных радикалов, служат активаторами системы комплемента и других звеньев гуморального иммунитета.
От 33 до 83% штаммов Pseudomonas aeruginosa имеют эволюционно детерминированный механизм защиты от иммунной системы – образование биопленок, состоящих из кластера пораженных клеток и внеклеточного матрикса, в том числе фибрина, секреторной секреции слизистых оболочек, альгината, полисахариды и липиды. Известно, что бактерии лизируют нейтрофилы, усиливая рост их собственных биопленок.
Классификация
Поражения, вызванные Pseudomonas aeruginosa, можно разделить на локальные и генерализованные (септические) поражения. Некоторые виды, в том числе инфекции центральной нервной системы, сердца и средостения, развиваются в результате распространения возбудителя. В зависимости от топологии очага воспаления выделяют следующие формы инфекции Pseudomonas:
• респираторная инфекция. Пациенты с длительной ИВЛ страдают трахеобронхитом в 30% случаев и пневмонией этиологии Pseudomonas в 24%.
• Инфекция ЛОР-органов. Синусит развивается редко, до 40% хронического среднего отита из-за Pseudomonas aeruginosa. Он проявляется в виде тяжелой диареи, которая часто приводит к летальному исходу у детей до года. Около 16% послеоперационного перитонита связано с возбудителем. Это связано с длительным использованием загрязненных контактных линз и глазных капель, что часто приводит к панофтальмиту.
• Инфекция мочевых путей. Скорее всего, развитие катетер-ассоциированного острого пиелонефрита. До 13% случаев острого простатита связаны с этим возбудителем. Происходит после пребывания в бассейне с пониженной концентрацией дезинфицирующих средств, может поражать ногти, подкожную клетчатку, мышечную фасцию с образованием некроза. На его долю приходится до 10% всех боевых инфекционных осложнений; он вызывает около 30% гнойных процессов при ожоговой болезни. Это считается поддерживающим фактором в формировании трофических язв.
Симптомы
Инкубационный период патологии чрезвычайно изменчив, он может варьироваться от нескольких дней до десятилетий, поскольку микроорганизм является одним из условно-патогенных компонентов микрофлоры человека. Клинические проявления зависят от пораженного органа. У взрослых с инвазией в желудочно-кишечный тракт первыми симптомами являются повышение температуры (не более 38,5 ° С), потеря аппетита, озноб, слабость, тошнота, реже рвота, вздутие живота и болезненность живота, частый жидкий стул с кровью и слизь.
При поражении желудочно-кишечного тракта маленькие дети становятся вялыми, сонливыми, отказываются от еды и питья, срыгивают, возникает гастроэнтероколит с высоким риском кишечного кровотечения. Pseudomonas патология ЛОР-органов проявляется лихорадкой 37,5 ° С и выше, резкими болями в ухе, потерей слуха, желто-зелеными обильными выделениями, иногда с примесью крови. Поражение дыхательных путей происходит в виде пневмонии – при повышении температуры тела свыше 38 ° С, усилении одышки, кашле с обильной слизисто-гнойной мокротой.
Pseudomonas инфекция мочевыделительной системы характеризуется лихорадкой, болью в пояснице, частым болезненным мочеиспусканием, ощущением неполного опорожнения мочевого пузыря, обесцвечиванием и запахом мочи. Глазные симптомы инвазии Pseudomonas aeruginosa чаще выявляются в области одного глазного яблока, начинаются с появления боли, боли, ощущения жжения, инородного тела, слезотечения, фотофобии и слизисто-гнойных выделений. В будущем может произойти снижение и помутнение зрения.
Повреждения кожи проявляются высыпаниями в виде пятен и пустулезных элементов по всему телу, включая сыпь на ладонях рук, подошв и носоглотки, увеличенные лимфатические узлы, постоянные головные боли (так называемая головная боль пловцов), зеленый цвет одной, реже двух ногтевых пластин, образование болезненных уплотнений в подкожно-жировой клетчатке. Раневая инфекция возбудителя сопровождается появлением сине-зеленых гнойных выделений и гнойно-геморрагических корок, увеличением зоны покраснения вокруг раны.
Ассоциированные симптомы: Высокая температура тела. Гематурия. Лейкоцитоз. Лихорадка. Недомогание. Одышка. Озноб. Отсутствие аппетита. Понос (диарея). Привкус во рту. Протеинурия. Рвота. Тошнота. Увеличение СОЭ.
Возможные осложнения
Мультисистемное и клиническое разнообразие симптомов Pseudomonas aeruginosa отражается в количестве осложнений этого состояния. Наиболее распространенные негативные последствия включают генерализацию инфекционного процесса, инфекционно-токсический шок и некротический колит у детей раннего возраста. Высокая вероятность образования абсцесса и гангренозных изменений. Вялое течение инфекции на слизистых оболочках уха, ротоглотки, носа, конъюнктивы и легких приводит к хронизации воспалительного процесса, образованию мезотимпанита, бронхоэктазии, ползучей язве роговицы, частичной или полной глухоте и односторонней слепота.
Диагностика
Диагноз ставится на основании данных, полученных в ходе консультации специалиста по инфекционным заболеваниям. В случае обширных гнойных поражений консультация с хирургом обязательна, по показаниям приглашаются другие специализированные специалисты. Наиболее распространенными диагностическими методами для подтверждения псевдомонадной этиологии заболевания являются следующие инструментальные и лабораторные исследования:
• Физическое обследование. При объективном осмотре обращают внимание на цвет раны, наличие сыпи. Поражение наружного уха, глаза проявляется гиперемией, обильными слизисто-гнойными выделениями. В легких при пневмонии слышно ослабление дыхания, при перкуссии – притупление звука. В случае гастроэнтероколита, болезненности по кишечнику, урчание не обнаружено; визуальная оценка движения кишечника является обязательной.
• Лабораторные исследования. Общий клинический анализ крови указывает на наличие лейкоцитоза, укол слева и ускорение СОЭ. Биохимические показатели показывают увеличение АЛТ, АСТ, СРБ, снижение общего белка и гипоальбуминемию. При общем анализе мочи возможна протеинурия, гематурия. Анализ мокроты подтверждает большое количество бактерий и лейкоцитов. В спинномозговой жидкости с повреждением головного мозга обнаружен нейтрофильный плеоцитоз, диссоциация клеточного белка.
• Идентификация инфекционных агентов. Золотой стандарт – бактериологические исследования, проводимые в современных условиях методом масс-спектрометрии с обязательным определением антибактериальной чувствительности бактерий. Обнаружение возбудителя возможно с помощью ПЦР биологического материала из патологического очага. Серологический диагноз (ИФА) проводится многократно с интервалом не менее 10-14 дней для выявления роста титра антител.
• Инструментальные методы. Рентген органов грудной клетки, реже МРТ или компьютерная томография, проводится для проверки поражений легких, дифференциальной диагностики. УЗИ органов брюшной полости, мочеполовой системы, мягких тканей, костей и забрюшинного пространства позволяет установить основной очаг воспаления. Эхокардиография показана при подозрении на инфекционный эндокардит. Колоноскопия, ФГДС назначают для исключения новообразований пищеварительного тракта.
Дифференциальный диагноз инфекции Pseudomonas затруднен из-за разнообразия клинических форм заболевания. Наиболее распространенные поражения желудочно-кишечного тракта отличаются сальмонеллезом, шигеллезом и псевдомембранозным колитом. Кожные проявления отличаются от гнойно-некротических поражений стрептококковой и стафилококковой этиологии. Инфекции дыхательной системы могут напоминать казеозную пневмонию с туберкулезом, саркоидозом, бактериальной пневмонией. Причинами сепсиса могут быть различные вирусы, бактерии и грибки.
Лечение
Стационарное лечение рекомендуется пациентам с повреждением органов, заболеванием средней и тяжелой степени. Пациенты с нозокомиальной инфекцией Pseudomonas aeruginosa продолжают лечение в отделении, в котором они находились до проявления инфекционного процесса, с обязательным проведением всех противоэпидемических мероприятий и восстановлением оборудования. Постельный режим необходим перед стабильным облегчением лихорадки в течение 3-5 дней, его продолжительность зависит от степени инвазии, наличия осложнений и декомпенсации сопутствующих заболеваний. Специальная диета не разработана, рекомендуется употреблять с достаточным количеством белка, адекватную диету.
Этиотропная терапия Pseudomonas aeruginosa осложняется наличием у микроорганизма естественной резистентности к определенным антибиотикам ряда пенициллина и тетрациклина, триметоприму и частично к цефалоспоринам, карбапенемам и аминогликозидам. Использование антибактериальных агентов разрешено в качестве монотерапии или комбинированной терапии с комбинацией нескольких групп препаратов, назначаемых локально и системно. Основными антибиотиками, используемыми для инактивации Pseudomonas aeruginosa, являются «защищенные» пенициллины, фторхинолоны, цефтазидим, цефепим, имипенем, полимиксин Е, гентамицин, амикацин.
Средство для борьбы с Pseudomonas hyperimmune donor и гамма-глобулин против Pseudomonas считаются средством борьбы с инфекцией. Перечисленные препараты используются реже в связи с возможным развитием сывороточной болезни и показаны для лечения. Медленное воспалительное. Симптоматическое лечение включает детоксикационную терапию, противовоспалительные и жаропонижающие препараты. Хирургическое вмешательство необходимо при локализованных и диффузных гнойных процессах, заключается в вскрытии и дренировании абсцессов, реже – ампутации конечностей. Допускается местное применение раствора перекиси водорода, мазей с антибиотиками.
Прогноз
Прогноз всегда серьезный. Pseudomonas aeruginosa часто вызывает бактерицидные ассоциации – с Candida, Staphylococcus, Klebsiella, что ухудшает течение патологии. Смертность при поражениях органов составляет 18–61%, она увеличивается при проникновении в больницу штамма Pseudomonas aeruginosa Предикторами вероятного летального исхода являются способность патогена продуцировать экзотоксин U, устойчивость ко многим антибиотикам и септический шок.
Профилактика
Специфическая профилактика (поливалентная вакцина) показана для медицинских работников, пациентов с ожогами, пациентов с открытыми переломами и глубокими ранами, людей с иммунодефицитом и пожилых людей. Неспецифические меры сводятся к строгому соблюдению правил обращения с медицинскими инструментами и оборудованием, контролю загрязнения сотрудниками Pseudomonas aeruginosa Важны общие методы укрепления: закаливание, нормальный сон, хорошее питание, ходьба, физическая активность, строгое соблюдение личной гигиены и своевременная санация гнойных вспышек.
Список литературы
1. Pseudomonas aeruginosa: патогенность, патогенез и патология / Лазарева А. В. , Чеботарь И. В. // Клиническая микробиология и антимикробная химиотерапия – 2015 – Т. 17, №3.
2. Инфекционные болезни Национальное руководство/ под ред. Ющука Н. Д. , Венгерова Ю. Я. – 2009.
3. Эпидемиология и профилактика синегнойной инфекции. Федеральные клинические рекомендации / Егорова О. Н. , Брусина Е. Б. И тд; – 2014.
Источник
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Классификация
- Причины
- Патогенез
- Симптомы
- Диагностика
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Названия
Сепсис.
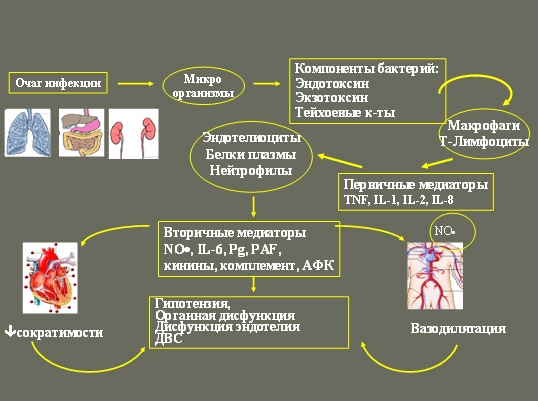
Патогенез сепсиса
Описание
Сепсис- это особая клинико-патогенетическая форма любого инфекционного заболевания, когда либо в связи с тяжелым преморбидным фоном (декомпенсация сахарного диабета, рахит, лекарственная болезнь, иммунодефицит, различные травмы), либо из-за высокой вирулентности или(и) большого количества поступления микроба-возбудителя или необычного пути поступления в органы и ткани макроорганизма, происходит срыв резистентности организма, в результате чего мета прежней локализации патогенной флоры становятся очагами их бурного размножения и источниками повторных генерализаций возбудителя.
Это системная воспалительная ответная реакция организма, которая приводит к развитию септического шока и синдрому полиорганной недостаточности.
Актуальность проблемы сепсиса труднее переоценить. Распространение этой патологии связана с трудностью диагностики на ранних этапах, атипичным стертым течением и склонностью к хронификации.
Классификация
По течению сепсис делится на молниеносный, острый, подострый и хронический (хрониосепсис).
Классификация сепсиса по патогенетическим формам:
1. Септицемия (очагов нет, но размножение возбудителя происходит в макрофагах).
2. Септикопиемия (вторичные множественные очаги в различных органах. В большом количестве поражаются органы ретикулоэндотелиальной системы).
3. Септический эндокардит.
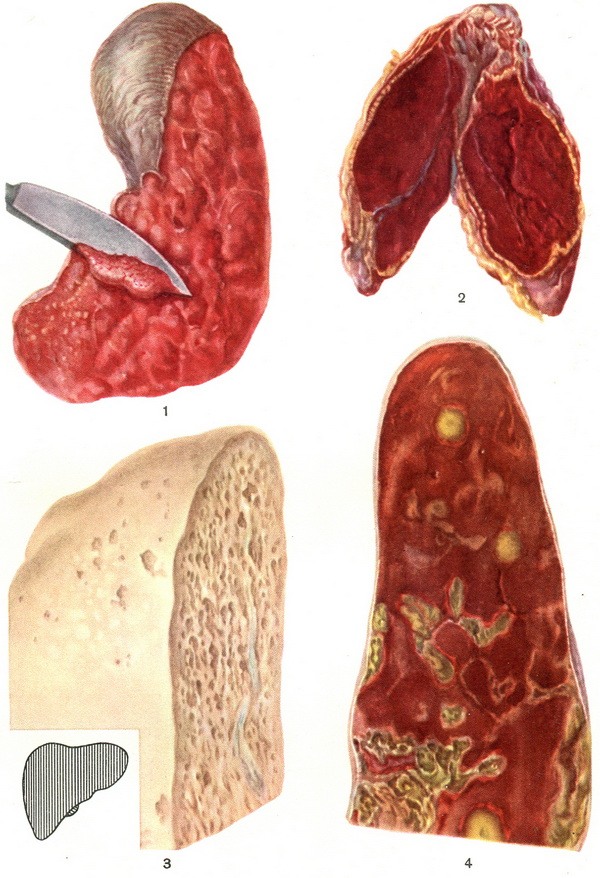
Изменения внутренних органов при сепсисе
Причины
Заболеваемость сепсисом связана к распространением антибиотиков широкого спектра действия, их бесконтрольным назначением, в том числе при самолечении. Установлено, что к условнопатогенным микроорганизмам у человека нет специфической иммунной реакции.
По причине возникновения выделяют следующие формы сепсиса:
- стрептококковый.
- стафилококковый.
- эшерихиозный.
- клебсиеллезный.
- псевдомонадный.
- менингококковый.
- HYP-инфекция (палочка инфлюэнцы).
Патогенез
Патогенез развития сепсиса характеризуется стадийностью.
1. Внедрение возбудителя и формирование первичного очага.
2. Прорыв микроорганизма в кровь (бактериемия).
3. Вследствие выделения токсинов бактериями наблюдается токсинемия.
4. Диссеминация возбудителя во внутренние органы, формирование вторичных очагов в селезенке, миокарде, почках, надпочечников, коже.
5. Активация иммунной системы, но с незавершенными ее функциями. Это приводит к высвобождению противовоспалительных медиаторов, но этот процесс не завершается полностью, и в результате происходит накопление цитокинов.
6. Повреждение клеток тканей, с нарушением перфузии. Данные изменения ведут к шоку.
7. Развитие септического шока. Септический шок – это сепсис с нарушением гемодинамики и развитием синдрома полиорганной недостаточности.
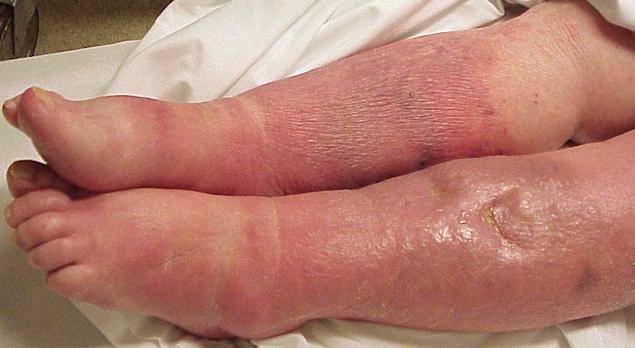
Сепсис у новорожденного
Симптомы
Предвестниками сепсиса является затяжная температурная реакция, температурные «свечи» в течение 2-3 часов, волнообразная лихорадка с периодами апирексии, озноб и познабливание.
Ни одно повышение температуры тела, ни одна необоснованная лихорадочная волна не должна быть оставлена без внимания врача, особенно губительные трафаретные «успокаивающие» диагнозы по типу гриппа или ОРВИ.
Кожа – зеркало сепсиса. Характерна ее бледность, сухость, вначале может быть гиперемия. На коже появляются вторичные гнойничковые элементы. Это мелкие пузырьки размером с булавочную головку с абсолютно прозрачным содержимым. Возможно развитие экзантемы – инфекционно-аллергического дерматита (крапивница, узловая эритема). Характерно поражение суставов в виде полиартрита. Легочная ткань поражается в зависимости от этиологии, при стафилакокковом сепсисе формируются абсцессы легкого, развивается стафилококковый дистресс-синдром, паренхиматозная дыхательная недостаточность). Увеличиваются размеры селезенки и печени.
Возможна диссоциация температурной кривой – снижение температуры на фоне увеличения лейкоцитов.
Как уже упоминалось выше, сепсис может быть вызван различными микроорганизмами – грамотрицательными и грамположительными. В зависимости от этого сепсис имеет некоторые особенности в клинической картине.
При грамположительной этиологии сепсиса наблюдается острая взрывная температурная реакция на фоне отсутствия головной боли. Резко развивается сердечная недостаточность с тахикардией, одышкой. Изменения кожных покровов напоминает сыпь при менингококцемии – обширные участки некроза кожи и вторичные мелкопузырчатые высыпания. Наслаиваются признаки дыхательной недостаточности с формированием абсцессов в легких. Развивается типичный дистресс-синдром и признаки шока.
Сепсис может быть вызван и грамотрицательной флорой, чаще – энтеробактериями. Начало заболевания сопровождается выраженными симптомами интоксикации – головной болью, тошнотой и рвотой. Развивается острая сосудистая недостаточность и инфекционно-токсический шок, падают показатели гемодинамики, снижается АД, повышается частота сердечных сокращений, изменение индекса Альговера (отношение пульса к систолическому давлению, в норме равняется 0,5-0,6). Кожные покровы покрыты пятнами, напоминающими трупные.
Сепсис у новорожденных:
Сепсис в ранний период новорожденности наиболее актуален для недоношенных, ослабленных младенцев. По времени возникновения у новорожденных выделяют ранний и поздний сепсис. Ранний неонатальный сепсис – это развитие сепсиса у детей в первые 3 дня жизни. Ранний сепсис развивается в результате внутриутробного или раннего постнатального инфицирования. Первичным очагом инфекции зачастую выступает внутриутробная пневмония. Источник инфекции в таком случае – это условно-патогенная флора, населяющая родовые пути матери, однако не исключено и трансплацентарный путь инфицировании.
Поздний неонатальный сепсис диагностируется в случае манифеста заболевания в возрасте старше 3-х дней жизни, при этом заражение происходит постнатально. Обнаруживается первичный очаг инфекции. Сепсис протекает с образованием одного или нескольких септикопиемических, метастатических, гнойно-воспалительных очагов, нередко диагностируется септикопиемия. Типичным метастатическим очагом является гнойный менингит.
Ассоциированные симптомы: Билирубинурия. Высокая температура тела. Гипергликемия. Гиперпротеинемия. Глюкозурия. Запор. Истощение. Лейкопения. Лейкоцитоз. Лейкоцитурия. Лимфоцитопения. Нейтрофилез. Низкая температура тела. Одышка. Озноб. Олигурия. Понос (диарея). Потливость. Привкус ацетона во рту. Протеинурия. Субфебрильная температура. Тромбоцитоз. Холодный пот.
Диагностика
Для бактериального исследования берется гемокультура с целью выявления возбудителя. Производится посев крови на сахарный бульон, на МПА и МПБ.
В течение первых двух дней необходимо проводить не менее 5-ти посевов в день. Кровь забирают по 10 мл, посев производят раздельно на 2 колбы. На каждые 5 мл крови используют 50 мл сахарного бульона.
Так же используются урокультура, культуры из доступных гнойных очагов.
В анализе перифирической крови: гиперлейкоцитоз или лейкопения, развитие анемии.
Анализ мочи обнаруживает признаки пиело- и гломерулонефрита.
Лечение
Для лечение сепсиса показана комплексная ранняя терапия, включающая антибактериальную терапию, антикоагуляционные, антиферментные препараты, пассивную и активную иммунизацию, иммуностимуляцию, экстракорпоральные методы очищения крови (гемосорбция, иммуносорбция, плазмоферез, лимфосорбция, лазерное облучение крови, фильтрация через ксеноселезенку).
Показано комбинированное назначение антибиотиков (не менее 2-х, в зависимости от чувствительности): бензилпенициллина натриевая соль 300 – 500 000 ЕД на кг + гентамицин 4-6 гр в сутки. Максимальная доза пенициллина – до 40 млн ЕД; аминогликозиды (амикацин) в комбинации с цефалоспорином 3-4 поколения. Дополнительно – антианаэробные препараты- метронидазол 100 мл внутривенно, клиндамицин; аминогликозиды + амоксициллин+ антианаэробы; аминогликозиды+ ципрофлоксацин+антианаэробы. Выбранную тактику лечения необходимо вести еще в течение 10 дней после нормализации температуры.
Инфузионно проводят дезинтоксикацию. Вводится 5% альбумин до 400 мл, реополюглюкин, реамберин, проводится форсорованный диурез.
Для профилактики ДВС-синдрома ежечасно вводится 1000 ЕД гепарина (суточная доза 24 000 ЕД). При развитии гиперкоагуляции показано сочетание гепарина с ингибиторами протеолиза, при гипокоагляции не следует прекращать введение гепарина, лишь уменьшить его дозировку.
Антистафилококковый иммуноглобулин вводится в дозе 5 мл на 1 кг тела. Курс – 5 инъекций.
Параллельно проводится коррекция кислотно-основного баланса, электролитов, кислородтерапия.
При выраженном септическом шоке – до 1000 мг глюкокортикоидов, при ИТШ – до 800 мг/сутки.
Немаловажную роль играет иммуностимуляция: лизоцим 100-200 мг внутримышечно в течение 10 дней, прием продигиозана повышает лейкопоэз, фагоцитарную активность, его вводят внутримышечно 1 раз в 3 дня в дозе 50 мг, курс состоит из 5-6 инъекций.
Из антисептических средств используется внутривенное введение хлорфиллипта в виде 0,2% спиртового раствора (2 мл хлорфиллипта + 38 мл физ. Раствора).
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
