Синдром бронхиальной обструкции клиническая фармакология
1) Лекарственные средства, тормозящие высвобождение гистамина и других медиаторов аллергии и воспаления.
Препараты: кетотифен, недокромил Na.
Механизм действия: блокирует трансмембранный вход ионов Са⁺⁺ в тучные клетки и прекращают экзоцитоз медиаторов аллергии.
Эти препараты предупреждают, но не купируют приступ бронхоспазма. Длительное применения этих препаратов позволяет значительно уменьшить дозу глюкокортикоидов, можно применять для лечения сезонных ринитов, конъюктивитов.
Фармакокинетика: Недокромил натрия препарат местного действия, используют для ингаляций (спинхалер), биодоступность per os небольшая (9%), ингаляции до 90% – в трахее и крупных бронхах. Максимальный эффект в первые 2 часа и продолжается 5-6ч, применяют также в виде глазных капель и интраназально.
Кетотифен хорошо всасывается в ЖКТ, биодоступность до 50%, эффект длится до 12ч, биотрансформируется в печени, выделяется с мочой и желчью.
Побочное действие: першение в горле, сухость во рту, кашель, осиплость, вялость, сонливость.
Противопоказания: Детям до 2 лет, беременность, кормление грудью, гиперчувствительность.
Взаимодействие: с другими Л.С. Кетотифен нельзя сочетать со средствами, угнетающими ЦНС, препараты этой группы лучше комбинировать со средствами для лечения бронхообструктивного синдрома.
2) Стимуляторы адренергических рецепторов.
Адреналин и эфедрин вызывают сильный побочный эффект назначают при бронхоспазмах в результате анафилактической реакции на фоне отека слизистой, т.к. они стимулируют α-адренорецеторы, что приводит к их спазму и снижению отека.
Стимуляторы β₂- адренорецепторов – сальбутамол, фенотерол, расширяют дистальные отделы бронхиального дерева, уменьшает вязкость мокроты. Ингаляционные формы этих препаратов используют для купирования бронхоспазма.
Пролонгированные β₂- адреностимуляторы (сальметрол, формотерол) используют для предупреждения астмы физической нагрузки и профилактики ночного удушья.
Фармакокинетика: Хорошо всасывается в ЖКТ, биодоступность 40-50%, максимальный эффект через 1,5-3ч, длится до 12ч. Биодоступность ингаляционных форм – до 10%. Действие развивается в течении 3-5мин., максимально через 30-60мин. Выводится с мочой, легкими.
Побочное действие: Тремор рук, гипергликемия, угнетение родовой деятельности у рожениц (все β₂- адреностимуляторы- токолитики, понижают тонус беременной матки, применяют для предупреждения преждевременных родов)
Противопоказания: ИБС, гиперчувствительность, сердечная недостаточность, гипертензия, беременность, кормление грудью, дети до 12лет.
Взаимодействие: с Л.С. других групп. Применять с другими средствами для лечения бронхообструктивного синдрома, но побочные эффекты усиливаются.
3) Блокаторы М-холинорецепторов – атропин, платифиллин.
Расслабляет гладкую мускулатуру внутренних органов, т.е. оказывают системное спазмолитическое действие, но М-холинолитики расширяют только крупные и средние бронхи, но не влияет на бронхиолы. Также уменьшают секрецию желез, что может привести к высушиванию слизистых бронхов. Из-за этих побочных эффектов широкое применение не находят, а используют новые М-холинолитики ипратрориум, тровентол.
Фармакокинетика: Ипратропиум не растворяется в липидах, поэтому практически не всасывается ни с поверхности легких, ни в ЖКТ. Ингаляционно биодоступность 10%, действие носит местный характер. Действие начинается через 5-25мин после ингаляций, максимальный эффект к 180мин, продолжительность действия 6-8ч, выводится с мочой, желчью.
Побочное действие: сухость во рту, першение
Противопоказания: гиперчувствительность, глаукома, беременность.
Взаимодействие: с Л.С. других групп. Синергисты с блокаторами Н₁- гистаминовых рецепторов, β₂- адреномиметиками.
4) Метилксантины
Кофеин, теофиллин, эуфиллин, теобиолонг, теопэк, теотард.
Кофеин использовали издавна как бронходилактирующее средство. В конце 40-х годов был синтезирован теофиллин, широко применяемый при бронхообструктивном синдроме. Теофиллин обладает широким спектром фармакологического действия: устраняет бронхоспазм, стабилизирует тучные клетки, уменьшает секрецию бронхиальных желез, снижает АД за счет расслабления сосудов, оказывает мягкое диуретическое действие, улучшает вентиляцию легких.
Метилксантины per os используют для профилактики приступов бронхиальной астмы. Но действие их непродолжительно, поэтому для профилактики ночных приступов применяют пролонгированные препараты (теобиолонг, теопэк, эуфилонг). Но велик риск побочных эффектов, т.к. широта терапевтического эффекта небольшая.
Эуфиллин – водорастворимая лекарственная форма теофиллина, применяют для купирования приступов бронхиальной астмы и лечения астматического статуса. При в/в введении ампулу целесообразно подогреть до t тела и растворять в изотоническом растворе NaCl, а 5% р-р глюкозы замедляет биотрансформацию в печени и способствует кумуляции препарат в организме.
Фармакокинетика: Метилксантины хорошо всасываются в ЖКТ, биодоступность 90-100%, максимально через 60-90мин. Действие длится 5ч, можно использовать per rectum.
Пролонгированные препараты действуют до 24ч. Эуфиллин при в/м 24% р-ра до 25% выпадает в осадок в месте инъекции, инъекции болезненны. Поэтому целесообразные применять в/в.
Побочное действие: Головная боль, головокружение, сердцебиение, тошнота, тремор, нарушение сна.
При повышении концентрации в плазме крови выше 40 мкг (мл появляется признаки перевозбуждения ЦНС, бред, галлюцинации, судороги, острая сердечная недостаточность, отек легких.
Помощь: прекратить прием лекарства, в/в рибоксин (антагонист), назначение диуретиков (фуросемид, этакриновая кислота), противосудорожные Л.С. (фенобарбитал).
Противопоказания: Гиперчувствительность, инсульт, инфаркт, атеросклероз коронарных артерий, беременность, кормление грудью.
Взаимодействие: с Л.С. других групп. Метилксантины несовместимы с блокаторами Н₂- гистаминовых рецепторов, эритромицином, фторхинолонами, пероральными противозачаточными средствами, эуфиллином, сердечными гликозидами.
5) Гормональные лекарственные средства.
Применяют как ингаляционные, так и неингаляционные. Глюкокортикостероиды ингаляционные : беклометазон, неингаляционные гидрокортизон, дексаметазон, преднизолон, триамцинолон. Влияют на все звенья патогенеза бронхообструктивного синдрома. Они могут быть использованы как для заместительной, так и патогенетической терапии заболевания.
Целью заместительной терапии является восполнение дефицита глюкокортикостероидов из-за недостаточности надпочечников. Для этого используют глюкокотикостероиды в низких дозах.
Для патогенетической терапии дозы выше, но с учетом тяжести заболевания. После достижения терапевтического эффекта дозы необходимо снижать для предупреждения побочных эффектов.
Это самые эффективные препараты при бронхообструктивном синдроме. Но длительное применение вызывает тяжелые системные осложнения (угнетение надпочечников, остеопороз, синдром Иценко-Кушинга и др.). Парентерально применяют для купирования приступа бр. астмы и для лечения астматического заболевания, по достижении эффекта дозы надо уменьшать.
Ингаляционный способ применения глюкокортикостероидов не дает больших побочных действий и терапевтический эффект не высок.
Фармакокинетика: Per os хорошо всасывается, легко проникают через барьеры. Гидрокортизон – естественный глюкокортикостероид. Per os биодоступность 80-90%, действует 4-6ч, в/м действует медленно, при внутрисуставном введении эффект развивается 6-24ч и длится до нескольких недель.
Преднизолон (синтетический препарат) биодоступность per os 95-100%, действует 4-6ч.
Триамцинолон (синт) всасывается в ЖКТ, биодоступность 20-30%, действует 24ч.
Беклометазон (ингаляции) оказывает местное действие.
Побочное действие: кашель, першение, кандидоз ротовой полости, обострение язвенной болезни, желудочное кровотечение, действие на эндокринную систему, гипертензия, психические расстройства, остеопороз, метаболические расстройства, иммунодепрессия, дерматологические и офтальмологические расстройства.
Противопоказания : язвенная болезнь, остеопороз, почечная недостаточность, гипертония, вирусные инфекции, туберкулез, психические болезни, беременность, лактация.
Взаимодействие : с Л.С. других групп. Нельзя комбинировать со снотворными, противосудорожными, антигистаминными, дигитоксином, левомицетином. Нестероидные противовоспалительные средства усиливают ульцерогенный эффект. Целесообразно комбинировать β₂- адреностимуляторами, метилксантинами, м- холинолитиками.
6) Антигистаминные средства (блокаторы Н₁- гистаминных рецепторов).
Гистамин – биологически активное вещество, основная часть его находится в тучных клетках. Высвобождается из тучных клеток в ответ на реакцию антиген- антитело при различных патологических состояниях. Выделившийся гистамин взаимодействует с гистаминовыми (Н) рецепторами. Существует 3 типа Н- рецепторов. Н₁- гистаминовые рецепторы расположены в гладких мышцах, эндотелии сосудов, мозге; Н₂-гистаминовые рецепторы расположены в желудке; Н – гистаминовые рецепторы – в ЦНС.
Способность гистамина вызывать спазм бронхов основной для использования блокаторов Н₁- гистаминовых рецепторов в комплексной терапии бронхообструктивного синдрома.
К антигистаминным препаратам 1 поколения относятся димедрол, супрастин, пипольфен, тавегил; 2 поколения – лоратидин, астемизол, акривастин. Препараты 2 поколения действует длительнее, кроме антигистаминного они оказывают бронходилактирующее действие. Применяют при различных формах аллергии : аллергический ринит, конъюктивит, крапивница, отек Квинке, сывороточная болезнь, поллипозы, для комплексной терапии бронхообструктивного синдрома.
Фармакокинетика: Антигистаминные препараты 1 поколения всасываются их ЖКТ, биодоступность до 45%, действие длится 4-12ч, обладает седативным действием.
Антигистаминные средства 2 поколения хорошо всасываются в ЖКТ, биодоступность до 90%, максимально через 60 мин, действие длится более 24ч.
Побочное действие : 1 поколение: сонливость, слабость, снижение внимания, нарушение координации, сухость во рту, носу.
2 поколение: головокружение, нарушение сна, диспепсия, сухость слизистых,повышение аппетита.
Противопоказания : гиперчувствительность, глаукома, язвенная болезнь, беременность, гипертония.
Взаимодействие : с Л.С. других групп. Усиливают действие наркотических средств, транквилизаторов, снотворных, нейролептиков, средств, угнетающих ЦНС, некоторых антибиотиков.
Тактика фармакотерапии бронхиальной астмы зависит от тяжести заболевания:
· Легкое эпизодическое заболевание
Лечение направлено на предотвращение удушья (интал) в период обострения. Медсестре необходимо рассказать о правилах пользования ингалятором.
ü Энергично встряхнуть ингалятор
ü Сделать неторопливый выдох
ü Поднести баллончик к открытому рту и одновременно с началом вдоха нажать на клапан баллончика (расстояние до рта 2-4см)
ü Вдох медленный и глубокий
ü После вдоха задержать дыхание на 7-14 секунд, выдох- через нос.
ü На 1 ингаляцию не более 2 доз
При отсутствии эффекта через 5мин можно повторить
· Легкое персистирующее течение.
При атопической форме без сопутствующих аллергических состояний интал (кромоглициевая кислота), при атомической форме с сопутствующими аллергическими проявлениями рациональнее использовать кетотифен. При бронхиальной астме неаллергической формы эффективен недокромил натрия (тайлед). Для купирования приступов у пациентов пожилого и старческого возраста комбинированный препарат беродуал.
При неэффективности назначают глюкокортикоиды в малых дозах.
· Среднетяжелое течение заболевания
Препараты, тормозящие выделение гистамина с ингаляционными формами глюкокортикостероидов (беклометазон). Для купирования ночного удушья – М-холинолитик (ипратропиум).
· Тяжелое течение болезни
Высокие дозы ингаляционных глюкокортикостероидов, при недостаточном эффекте применять per os (триамцинолон) дозы подбирают индивидуально. На ночь пролонгированные препараты β₂-адреностимуляторов, М-холиноблокаторы. Применение препаратов под контролем.
Источник
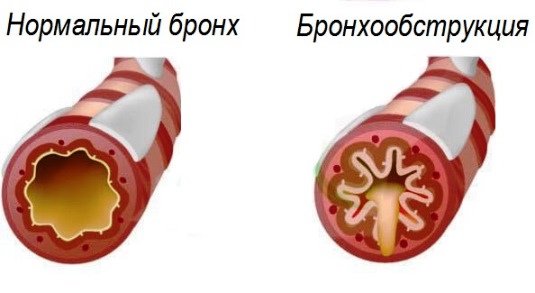
Бронхообструктивный синдром (БОС, бронхоспазм) – клинический симптомокомплекс, обусловленный нарушением проходимости воздуха по бронхам вследствие сужения или окклюзии дыхательных путей с последующим увеличением сопротивления дыхательных путей к вдыхаемому воздушному потоку.

Бронхообструктивный синдром является одним из патофизиологических нарушений, которые способны повлиять на исходы и прогрессирующее течение многих острых и хронических бронхолегочных заболеваний. БОС, не являясь самостоятельной нозологической единицей, может встречаться при различных заболеваниях легких и сердца, приводящих к нарушению проходимости дыхательных путей.
Клинические признаки (симптомы) бронхообструктивного синдрома
Основными клиническими проявлениями БОС являются приступообразный кашель, экспираторная одышка и внезапные приступы удушья. По клиническим проявлениям БОС принято разделять на протекающий латентно и протекающий с выраженной клинической картиной. По течению БОС разделяют на острый (внезапно возникший) и хронический (постоянный).
Функциональные изменения при бронхообструктивном синдроме связаны со снижением основных спирометрических показателей, отражающих степень бронхиальной обструкции (БО) и характер «воздушной ловушки», а именно:
• объем форсированного выдоха за 1-ю секунду (ОФВ1);
• отношение ОФВ1/ФЖЕЛ
Данные показатели являются диагностическим критерием бронхиальной обструкции и служат для определения степени тяжести БОС.
По тяжести клинических и функциональных проявлений БОС разделяют на легкий, средней тяжести и тяжелый.
Основными клиническими проявлениями БОС являются одышка, удушье (относится к угрожающим жизни состояниям), приступообразный кашель, хрипы, шумное дыхание. Симптомы более заметны при физической нагрузке. Другие проявления БОС – повышенная потливость, нарушение сна, головная боль, спутанность сознания, судороги – обнаруживаются при тяжелом течении синдромокомплекса.
Вариантные формы БОС
Спастический – наиболее часто встречаемый вариант БОС (>70% всех случаев), в развитии которого лежит бронхоспазм из-за дисфункции в системах контроля тонуса бронхов.
Воспалительный – механизм обусловлен отеком, инфильтрацией воздухоносных путей, гиперемией оболочки бронхов.
Дискринический – наблюдается при избыточной стимуляции ферментов бокаловидных клеток и желез слоя бронхов, приводящей к ухудшению свойств мокроты, нарушениям функции образования слизи и мукоцилиарного транспорта.
Дискинетический – бронхиальная проходимость нарушена за счет врожденного недоразвития мембранозной части трахеи и бронхов, способствующих закрытию их просвета при вдохе.
Эмфизематозный – сопровождается спадением (коллапсом) мелких бронхов из-за снижения и утраты легкими эластичности.
Гемодинамический – возникает вторично на фоне нарушений гемодинамики малого круга: при гипертензии пре- и посткапилляров, застое в бронхиальных венах и при гипертоническом кризе в малом круге кровообращения.
Гиперосмолярный – наблюдается при уменьшение оводненности слизистых оболочек бронхов (вдыхание холодного воздуха), когда высокая осмотическая концентрация на поверхности клеток вызывает раздражение рецепторов и бронхоспазм.
В основе бронхиальной обструкции лежат обратимые (функциональные) и необратимые (органические) изменения. К функциональным механизмам бронхиальной обструкции относятся спазм гладкой мускулатуры, гиперсекреция слизи и отек слизистой оболочки бронхов. Спазм гладкой мускулатуры и гиперсекреция слизи происходят в результате воздействия раздражающих факторов (поллютанты, инфекционный агент) на слизистую дыхательных путей. В ответ на это выделяются медиаторы воспаления, которые раздражают окончания блуждающего нерва и способствуют выделению ацетилхолина, реализующего свое действие через мускариновые холинорецепторы. Активация этих рецепторов вызывает холинергическую бронхоконстрикцию и гиперсекрецию. В стенке бронхов наблюдается резкое полнокровие сосудов микроциркуляторного русла и повышение их проницаемости. Таким образом, развивается отек слизистой оболочки и подслизистого слоя, инфильтрация их тучными клетками, базофилами, эозинофилами, лимфоидными и плазматическими клетками.
Кашель может быть сухим и продуктивным. Для начального периода воспалительного или отечного процесса характерен сухой кашель. Появление продуктивного кашля свидетельствует о нарушении мукоцилиарного клиренса и дренажа бронхов.
В числе инфекционных агентов, наиболее часто вызывающих обструктивный синдром, находятся респираторно-синцитиальный вирус (около 50%), вирус парагриппа, микоплазма пневмонии, реже – вирусы гриппа и аденовирус.
Лечение бронхообструктивного синдрома
Проявление БОС, независимо от этиологии, требует от врача принятия неотложных мер по ликвидации бронхиальной обструкции посредством воздействия на обратимый ее компонент.
Необходимо отметить, что обратимость бронхиальной обструкции определяется степенью гиперреактивности бронхов (ГРБ). ГРБ определяется как реакция бронхов на различные химические, физические или фармакологические раздражители, когда бронхоспазм развивается в ответ на воздействие, не вызывающее такой реакции у здоровых лиц. Чем выше ГРБ и длительность экспозиции провокационного агента, тем тяжелее и опаснее для жизни пациента протекает БОС.
В современной пульмонологии существуют высокоэффективные способы доставки лекарственных средств непосредственно в бронхи. Такую технологию называют ингаляционной небулайзерной (от латинского nebulae – туман) терапией. Характерной ее чертой является высокая фракция (>80%) частиц размером от 0,5 до 5 мкм, способных легко достигать рецепторной зоны в мелких бронхах и быстро купировать бронхиальную обструкцию.
Неоспоримыми преимуществами ингаляционной терапии в целом являются:
• эффективное создание высоких концентраций медикаментов в дыхательных путях;
• незначительная концентрация препарата в крови;
• быстрое начало действия препаратов;
• возможность коррекции дозы;
• минимум системных побочных эффектов.
Лечебная тактика при БОС достаточна понятна и логична. Для купирования бронхиальной обструкции используют бронхолитики (бронходилататоры). Несмотря на различия в механизме действия различных бронходилататоров, самым важным их свойством является способность устранять спазм мускулатуры бронхов и облегчать прохождение воздуха в легкие. Все современные бронхолитики, используемые для терапии БОС, можно разделить на несколько основных групп:
• b2-агонисты короткого и длительного действия;
• холинолитики короткого и длительного действия;
• комбинированные препараты;
• метилксантины.
Ингаляционные b2-агонисты
Ингаляционные b2-агонисты короткого действия. Эта группа включает два достаточно селективных b2-агониста – фенотерол и сальбутамол. Основными свойствами данной группы препаратов являются:
• расслабление гладкой мускулатуры бронхов;
• снижение гиперреактивности дыхательных путей;
• улучшение мукоцилиарного клиренса бронхов;
• снижение сосудистой проницаемости и экссудации плазмы;
• уменьшение отека слизистой оболочки бронхов;
• стабилизация мембран тучных клеток, уменьшение выброса медиаторов воспаления.
Достоинствами этих препаратов является быстрый (через 3-5 мин) и выраженный бронхолитический эффект. Продолжительность действия препаратов невелика, составляет от 3 до 6 ч, почему их относят к группе короткодействующих b2-агонистов (КДБА). Очевидно, что при необходимости эффективного контроля просвета бронхов в течении 24 ч необходимо совершать от 4 до 8 ингаляций КДБА в сутки.
Однако, как и любые b2-агонисты, препараты этой группы обладают большим количеством побочных эффектов, особенно при частом (более 4 раз в сутки) их использовании.
Одним из серьезных побочных действий b2-агонистов является тремор вследствие прямого действия препарата на b2-адренорецепторы скелетной мускулатуры. Тремор чаще отмечается у пациентов пожилого и старческого возраста. Нередко наблюдается тахикардия – либо в результате прямого действия на b-адренорецепторы предсердий, либо под влиянием рефлекторного ответа вследствие периферической вазодилатации через b2-рецепторы. Особое внимание следует обращать на удлинение интервала Q-T, способное вызвать внезапную смерть у пациентов с кардиоваскулярной патологией. Более редкими и менее выраженными осложнениями являются гипокалиемия, гипоксемия и раздражительность. Кроме того, b2-агонистам короткого действия свойственно явление тахифилаксии – быстрое снижение лечебного эффекта при повторном применении лекарственных препаратов.
Ингаляционные b2-агонисты длительного действия. Препараты данной группы имеют длительность действия от 12 до 24 ч и используются в составе базисной терапии заболеваний, наиболее часто сопровождающихся БОС, например бронхиальной астмы (БА). Наиболее эффективно их назначение в комплексе с противовоспалительными препаратами – ингаляционными глюкокортикостероидами (ИГКС). На сегодняшний день комбинация ДДБА+ ИГКС признается эффективной базисной терапией БА.
Наиболее ярким представителем этой группы является формотерола фумарат (формотерол), который обладает способностью расслаблять гладкую мускулатуру бронхов, усиливать мукоцилиарный клиренс, уменьшать сосудистую проницаемость и высвобождение медиаторов из тучных клеток и базофилов, обеспечивать длительную защиту от воздействия факторов, приводящих к бронхоспазму. Однако нет достаточных доказательств влияния формотерола на персистирующее воспаление при БА; кроме того, в ряде исследований показано, что при длительном его применении выраженность бронхолитического эффекта может cильно изменяться.
Нежелательные эффекты ДДБА не сильно отличаются от таковых у КДБА, развиваются при превышении среднесуточных рекомендуемых доз и проявляются в виде чувства тревоги, тремора скелетных мышц, стимуляции сердечно-сосудистой системы.
Ингаляционные М-холинолитики
Ингаляционные М-холинолитики короткого действия. Основным представителем данной группы – короткодействующие антихолинергические препараты (КДАХ) –
признается ипратропия бромид (ипратропий), обладающий выраженным бронхолитическим эффектом.
Механизм бронхолитического действия обусловлен блокадой мускариновых холинорецепторов, в результате чего подавляется рефлекторное сужение бронхов, вызванное раздражением ирритативных холинергических рецепторов, и снижается тонус блуждающего нерва.
Практически во всех опубликованных руководствах, посвященных БА, холинолитики признаны «препаратами выбора» для лечения данного заболевания, а также в качестве дополнительных бронходилатирующих средств при БОС средней и тяжелой степени у лиц пожилого, старческого и детского возраста.
Неоспоримыми преимуществами М-холинолитиков являются:
• отсутствие кардиотоксического действия, что делает их «препаратами выбора» для пациентов с сердечными и циркуляторными нарушениями, а также у пожилых пациентов;
• отсутствие тахифилаксии при повторном применении;
• стабильная рецепторная активность (количество М-холинорецепторов с возрастом не уменьшается, в отличие от количества и активности b2-адренорецепторов);
• редко встречаемые побочные эффекты (сухость, горький вкус во рту).
Позитивные эффекты холинолитиков многогранны и не ограничиваются только бронходилатационным эффектом. Они выражаются в снижении чувствительности кашлевых рецепторов, изменении секреции вязкой мокроты, уменьшении потребления кислорода дыхательными мышцами. К числу положительных особенностей ипратропия бромида относится большая продолжительность действия – до 8 ч.
Условным недостатком М-холинолитиков короткого действия или короткого действия антихолинергиков (КДАХ) является медленное начало действия (через 30-60 мин) после ингаляции, затрудняющих быстрое купирование проявлений БОС.
Ингаляционные М-холинолитики длительного действия. Основным представителем данной группы – длительно действующие антихолинергические препараты (ДДАХ) – признается тиотропия бромид (тиотропий), обладающий длительным и сильным бронхолитическим эффектом.
Тиотропий целесообразно применять для устранения БОС при «тяжелой рефрактерной БА», когда высокие терапевтические дозы b2-агонистов не дают желаемой бронходилатации и не купируют БОС.
Комбинированные бронхолитики
Ингаляционные комбинированные бронхолитики короткого действия. Основным представителем данной группы – коротко действующие комбинированные бронхолитические препараты (КДКБ) – признается комбинация КДАХ (ипратропий 20 мкг) + КДБА (фенотерол 50 мкг), получившая широкое распространение в современной терапевтической практике под коммерческим названием «Беродуал Н» в форме дозированного аэрозольного ингалятора и «Беродуал» в форме раствора для ингаляций (компания Берингер Ингельхайм, Германия).
Идея комбинирования КДАХ+КДБА не нова и имеет длительную историю. Достаточно сказать и о высоких ожиданиях от сальбутамол + ипратропий, так и не нашедших своего широкого применения. Именно поэтому считаем необходимым отметить ряд особенностей комбинирования фенотерола и ипратропия.
Во-первых, М-холинолитик ипратропий обладает действием преимущественно в проксимальных отделах бронхов, тогда как селективный b2-агонист фенотерол преимущественно действует на дистальные отделы бронхиального дерева. Это приводит к «двойному эффекту» бронходилатации, возможности уменьшения дозы каждого препарата до минимальной терапевтической, устраняет возможность сторонних нежелательных явлений. Во-вторых, оба вещества имеют одинаковое агрегатное состояние (водные растворы) что позволяет создавать высокую респирабильную фракцию в ходе небулайзерной терапии, а значит эффективно купировать БОС.
Обоснованно назначения препарата Беродуал для купирования БОС при БА в следующих случаях:
• наличие у пациентов измененного b2-рецептора (генетическая абнормальность b2-рецептора, заключающаяся в замещении в 16 позиции Gly на Arg с формированием генотипа b2-АРB16 Arg/Arg рецептора, не чувствительного к любым b2-агонистам);
• при уменьшении рецепторной b2-активности;
• при наличии выраженных проявлений сердечно-сосудистых заболеваний;
• при явлениях «ночной астмы» (варианта БА, при котором приступы удушья возникают во второй половине ночи на фоне бронхиальной обструкции, вызванной активностью вагуса);
• при вирусных инфекциях, способных уменьшать экспрессию гена М2 и усиливающих бронхиальную обструкцию.
Интерес представляют рандомизированные клинические исследования, изучающие эффективность комбинированной терапии по сравнению с монотерапией одним из компонентов. Так, в рандомизированном контролируемом перекрестном исследовании N.Gross и соавт., включавшем 863 больных, комбинированная терапия приводила к приросту ОФВ1 на 24% по сравнению с монотерапией сальбутамолом (рВ другом исследовании (мета-анализе двух крупных 3-месячных исследований у 1067 больных (E.J.Weber и соавт., 1999) было продемонстрировано преимущество комбинированной терапии БОС у пациентов хронической обструктивной болезнью легких (ХОБЛ). Установлено, что при монотерапии сальбутамолом частота обострений ХОБЛ (18%) и число дней обострений (770 человеко-дней) были достоверно выше, чем при комбинированной терапии (12% и 554 человеко-дня) (рТаким образом, Беродуал Н рассматривался как препарат, обладающий высоким соотношением стоимость/эффективность. На сегодняшний день фиксированная комбинация b2-агониста короткого действия и ипратропия бромида (Беродуал Н) внесена в международные клинические рекомендации по лечению пациентов с бронхиальной астмой ХОБЛ.
Неоспоримыми доказанными преимуществами Беродуала Н и Беродуал раствор для ингаляций являются:
• быстрый (через 5-10 мин) и достаточно продолжительный (6-8 ч) эффект;
• безопасный клинический профиль (отсутствие кардиотоксического действия);
• отсутвие тахифилаксии;
• отсутствие влияния на смертность пожилых пациентов (в отличие от b2-агонистов);
• умеренное противовоспалительное действие (уменьшение высвобождения медиаторов воспаления);
• более выраженный бронходилатационный ответ в комбинации, чем у каждого препарата в отдельности;
• эффективное купирования острого БОС (при БА) и хронического БОС (при хронической обструктивной болезни легких – ХОБЛ).
Метилксантины
Основным представителем данной группы признается бронхолитическое средство, производное пурина, под названием Теофилли́н (от латинского: theo-чай, phyllin-лист). Теофиллин оказывает слабый бронхорасширяющий эффект, но положительно влияет на дыхательную мускулатуру, улучшает отделение мокроты, стимулирует дыхательный центр. Подобное сочетание положительных свойств наряду с доступностью теофиллина когда-то привело к его широкому использованию.
Применение метилксантинов сопровождается многочисленными побочными эффектами: тошнотой, рвотой, головной болью, возбуждением, гастроэзофагеальным рефлюксом, частым мочеиспусканием, аритмией, тахикардией и т.д. Препараты применяются внутрь или парентерально.
Препараты теофиллина пролонгированного действия отошли на второй план. Их рекомендовано в особых случаях использовать в качестве дополнительного бронхорасширяющего средства при БОС у пациентов БА и ХОБЛ с недостаточным бронходилатационным ответом от современной ингаляционной бронхорасширяющей терапии.
Заключение
Бронхообструктивный синдром сопровождает многие болезни, в особенности заболевания дыхательной системы, такие как бронхиальная астма, ХОБЛ, ОРВИ, пневмонии и др. Все они требуют соответствующей медикаментозной коррекции.
Стандартом лечения БОС можно с уверенностью считать ингаляционные препараты и небулайзерный способ их доставки, позволяющий создать макимальную концетрацию лекарственного вещества в рецепторной зоне и вызывающий максимальный бронходилатационный ответ при отсутствии системного действия лекарства.
В возникновении БОС принимают участие различные отделы нервной системы: симпатический (b-рецепторы) и парасимпатический (М1-2 и М3-рецепторы). Довольно часто клинически трудно определить, что преобладает в механизме бронхообструкции: недостаточная адренергическая стимуляция или чрезмерная вагусная иннервация. В таком случае оптимальным является назначение комбинации b2-агониста короткого действия и М-холинолитика ипратропия бромида (Беродуал Н).
C уверенностью можно сказать, что Беродуал Н в форме дозированного аэрозольного ингалятора и Беродуал раствор для ингаляций через небулайзер показаны для профилактики и симптоматического лечения обструктивных заболеваний дыхательных путей с обратимым бронхоспазмом, таких как острый и хронический обструктивный бронхит, бронхиальная астма, хроническая обструктивная болезнь лекгих.
Источник
