Синдром гиперандрогении у женщин методическое пособие для врачей

Гиперандрогения у женщин – группа эндокринопатий, характеризующихся избыточной секрецией или высокой активностью мужских половых гормонов в женском организме. Проявлениями различных синдромов, схожих по симптоматике, но различных по патогенезу, выступают нарушения обменной, менструальной и репродуктивной функций, андрогенная дермопатия (себорея, акне, гирсутизм, алопеция). Диагноз гиперандрогении у женщин основан на данных осмотра, гормонального скрининга, УЗИ яичников, КТ надпочечников и гипофиза. Коррекцию гиперандрогении у женщин проводят с помощью КОК или кортикостероидов, опухоли удаляют оперативно.
Общие сведения
Гиперандрогения у женщин – понятие, объединяющее патогенетически разнородные синдромы, обусловленные повышенной продукцией андрогенов эндокринной системой или чрезмерной восприимчивостью к ним тканей–мишеней. Значимость гиперандрогении в структуре гинекологической патологии объясняется ее широким распространением среди женщин детородного возраста (4–7,5% у девочек-подростков, 10-20% у пациенток старше 25 лет).
Андрогены – мужские половые гормоны группы стероидов (тестостерон, АСД, ДГЭА-С, ДГТ) синтезируются в организме женщины яичниками и корой надпочечников, меньше – подкожной жировой клетчаткой под контролем гипофизарных гормонов (АКТГ и ЛГ). Андрогены выступают предшественниками глюкокортикоидов, женских половых гормонов – эстрогенов и формируют либидо. В пубертате андрогены являются наиболее значимыми в процессе ростового скачка, созревания трубчатых костей, замыкания диафизаро-эпифизарных хрящевых зон, появления оволосения по женскому типу. Однако избыток андрогенов в женском организме вызывает каскад патологических процессов, нарушающих общее и репродуктивное здоровье.
Гиперандрогения у женщин не только обусловливает возникновение косметических дефектов (себореи, акне, алопеции, гирсутизма, вирилизации), но и становится причиной расстройства метаболических процессов (обмена жиров и углеводов), менструальной и репродуктивной функции (аномалий фолликулогенеза, поликистозной дегенерации яичников, дефицита прогестерона, олигоменореи, ановуляции, невынашивания беременности, бесплодия у женщин). Продолжительная гиперандрогения в сочетании с дисметаболизмом повышает риск развития гиперплазии эндометрия и рака шейки матки, сахарного диабета II типа и сердечно-сосудистой патологии у женщин.
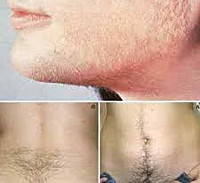
Гиперандрогения у женщин
Причины гиперандрогении у женщин
В гинекологии дифференцируют гиперандрогению яичникового (овариального), надпочечникового (адреналового) и смешанного генеза. Гиперандрогения у женщин может быть первичной и вторичной (при нарушении гипофизарной регуляции), носить наследственный и приобретенный характер. Гиперандрогения бывает абсолютной (с увеличением уровня андрогенов в крови), но чаще – относительной (с нормальным количеством андрогенов, но их усиленным метаболизмом в более активные формы или с повышенной утилизацией в чрезмерно восприимчивых к ним органах-мишенях – яичниках, коже, сальных, потовых железах и волосяных фолликулах).
Гиперандрогения с избыточным синтезом андрогенов у женщин в большинстве случаев определяется при синдроме поликистозных яичников: первичном (синдроме Штейна-Левенталя) и вторичном (на фоне нейроэндокринной формы гипоталамического синдрома, гиперпролактинемии, гипотиреоза), а также при адреногенитальном синдроме (АГС, врожденной гиперплазии надпочечников). При АГС усиленная выработка андрогенов обусловлена дефицитом фермента 21-гидроксилазы и высоким уровнем АКТГ. Стимулятором синтеза андрогенов может выступать избыток пролактина (синдром галактореи-аменореи). К причинам гиперандрогении можно отнести наличие вирилизирующих опухолей яичников (лютеомы, текомы) и надпочечников (андростеромы), стромального текоматоза яичников.
Развитие транспортной формы гиперандрогении у женщин отмечается на фоне недостаточности глобулина, связывающего половые стероиды (ГСПС), блокирующего активность свободной фракции тестостерона (при синдроме Иценко-Кушинга, гипотиреозе, дислипопротеидемии). Компенсаторный гиперинсулизм при патологической инсулинорезистентности клеток-мишеней способствует усилению активации андрогенсекретирующих клеток овариально-адреналового комплекса.
У 70–85% женщин с акне гиперандрогения наблюдается при нормальных показателях андрогенов в крови и повышенной чувствительности к ним сальных желез вследствие увеличения плотности гормональных рецепторов кожи. Основной регулятор пролиферации и липогенеза в сальных железах – дигидротестостерон (ДГТ) – стимулирует гиперсекрецию и изменение физико–химических свойств кожного сала, приводящих к закрытию выводных протоков сальных желез, образованию комедонов, появлению акне и угревой болезни.
Гирсутизм связан с гиперсекрецией андрогенов в 40-80% случаев, в остальных – с усиленным превращением тестостерона в более активный ДГТ, провоцирующий избыточный рост стержневых волос в андрогенчувствительных зонах женского тела или выпадение волос на голове. Кроме этого, у женщин может встречаться ятрогенная гиперандрогения, обусловленная приемом лекарственных препаратов с андрогенной активностью.
Симптомы гиперандрогении у женщин
Клиника гиперандрогении у женщин зависит от степени выраженности нарушений. При гиперандрогении неопухолевого генеза, например, при СПКЯ, клинические признаки медленно прогрессируют в течение нескольких лет. Начальные симптомы манифестируют в период пубертата, клинически проявляясь жирной себореей, вульгарными угрями, нарушением менструального цикла (нерегулярностью, чередованием задержек и олигоменореи, в тяжелых случаях – аменореей), избыточным оволосением лица, рук, ног. В последующем развивается кистозная трансформация структуры яичников, ановуляция, недостаточность прогестерона, относительная гиперэстрогенемия, гиперплазия эндометрия, снижение фертильности и бесплодие. В постменопаузе отмечается выпадение волос сначала в височных областях (битемпоральная алопеция), затем в теменной области (париетальная алопеция). Выраженная андрогенная дерматопатия у многих женщин приводит к развитию невротических и депрессивных состояний.
Гиперандрогения при АГС характеризуется вирилизацией гениталий (женским псевдогермафродитизмом), маскулинизацией, поздним менархе, недоразвитием груди, огрублением голоса, гирсутизмом, угрями. Тяжелая гиперандрогения при нарушении функции гипофиза сопровождается высокой степенью вирилизациии, массивным ожирением по андроидному типу. Высокая активность андрогенов способствует развитию метаболического синдрома (гиперлипопротеинемии, инсулинорезистентности, СД II типа), артериальной гипертензии, атеросклероза, ИБС. При андрогенсекретирующих опухолях надпочечников и яичников симптомы развиваются стремительно и быстро прогрессируют.
Диагностика гиперандрогении у женщин
В целях диагностики патологии проводится тщательный сбор анамнеза и физикальный осмотр с оценкой полового развития, характера менструальных нарушений и оволосения, признаков дермопатии; определяется общий и свободный тестостерон, ДГТ, ДЭА-С, ГСПС в сыворотке крови. Выявление избытка андрогенов требует уточнения его природы – надпочечниковой или яичниковой.
Маркером адреналовой гиперандрогении служит повышенный уровень ДГЭА-С, а яичниковой – увеличение количества тестостерона и АСД. При очень высоком уровне ДГЭА-С >800 мкг/дл или общего тестостерона >200 нг/дл у женщин возникает подозрение на андрогенсинтезирующую опухоль, что требует выполнения КТ или МРТ надпочечников, УЗИ органов малого таза, при сложности визуализации новообразования – селективной катетеризации надпочечниковых и яичниковых вен. УЗ-диагностика позволяет также установить наличие поликистозной деформации яичников.
При овариальной гиперандрогении оценивают показатели гормонального фона женщины: уровни пролактина, ЛГ, ФСГ, эстрадиола в крови; при адреналовой – 17-ОПГ в крови, 17-КС и кортизола в моче. Возможно проведение функциональных проб с АКТГ, проб с дексаметазоном и ХГЧ, выполнение КТ гипофиза. Обязательным является исследование углеводного и жирового обмена (уровней глюкозы, инсулина, HbA1C, общего холестерина и его фракций, глюкозо-толерантного теста). Женщинам с гиперандрогенией показаны консультации эндокринолога, дерматолога, генетика.
Лечение гиперандрогении у женщин
Лечение гиперандрогении длительное, требующее дифференцированного подхода к тактике ведения пациенток. Основным средством коррекции гиперандрогенных состояний у женщин выступают эстроген-гестагенные оральные контрацептивы с антиандрогенным эффектом. Они обеспечивают торможение продукции гонадотропинов и процесса овуляции, подавление секреции овариальных гормонов, в т. ч., тестостерона, подъем уровня ГСПС, блокировку андрогеновых рецепторов. Гиперандрогению при АГС купируют кортикостероидами, их применяют также для подготовки женщины к беременности и в период гестации при данном типе патологии. В случае высокой гиперандрогении курсы антиандрогенных препаратов у женщин продлевают до года и более.
При андрогензависимой дерматопатии клинически эффективна периферическая блокада андрогенных рецепторов. Одновременно проводится патогенетическое лечение субклинического гипотиреоза, гиперпролактинемии и др. нарушений. Для лечения женщин с гиперинсулизмом и ожирением применяются инсулиновые сенситайзеры (метформин), меры по снижению веса (гипокалорийная диета, физические нагрузки). На фоне проводимого лечения осуществляется контроль динамики лабораторных и клинических показателей.
Андрогенсекретирующие опухоли яичников и надпочечников имеют обычно доброкачественную природу, но при их выявлении обязательно хирургическое удаление. Рецидивы маловероятны. При гиперандрогении показано диспансерное наблюдение и медицинское сопровождение женщины для успешного планирования беременности в будущем.
Источник
Заболевание надпочечниковая гиперандрогения, обусловлено повышенным синтезов гормонов андрогенов, что влечет за собой проявление атипичных особенностей для противоположного пола. Заболевание в большей степени характерно для женского пола. Ученые считают, что недуг имеет генетический характер, возникает из-за врожденной патологии надпочечников. В 90% зафиксированных случаев, гиперандрогения развивается на фоне дефицита С21-гидроксилазы.

Общие сведения
Вирилизация (маскулинизация) надпочечникового генеза обуславливается чрезмерным продуцированием надпочечниками гормонов андрогенного типа и приводит к внешним и внутренним изменениям, атипичным для пола пациента. Андрогены необходимы в организме взрослой женщины, поскольку отвечают за важные преобразования организма в процессе полового созревания. В частности, они производят синтез эстрогена, а также способствуют укреплению костной ткани, росту мышц, участвуют в регуляции работы печени и почек и формировании репродуктивной системы. Производятся андрогены в основном надпочечниками и в женском организме яичниками, а в мужском, соответственно, яичками. Существенное превышение нормы содержания этих гормонов у женщин способно значительно расстроить репродуктивную систему и даже спровоцировать бесплодие.
Профилактика
Каких-либо специфических мер профилактики гиперандрогении не существует, поскольку данный синдром развивается на гормональном уровне.
К общим профилактическим мерам относят:
- рациональное питание, включающее в меню продукты, богатые клетчаткой, контроль веса;
- отказ от курения и злоупотребления алкоголем;
- регулярное посещение гинеколога;
- прием лекарственных препаратов и противозачаточных средств только после рекомендации врача;
- своевременное лечение патологий щитовидной железы, заболеваний печени и надпочечников.
Гиперандрогения – это не только проблемы с кожей, волосами и менструальным циклом. Это общее заболевание организма, которое не позволяет женщине вести качественный образ жизни и зачастую лишает ее радостей материнства. Современные методы диагностики и лечения позволяют вовремя выявить патологию и успешно устранять ее проявления.
Причины возникновения надпочечниковой гиперандрогении

Основной причиной накапливания в организме андрогенов является врожденный дефект синтеза ферментов, препятствующий преобразованию стероидов. Чаще всего в роли такого дефекта выступает дефицит С21-гидроксилазы, синтезирующей глюкокортикоиды. Кроме того, гормональный дисбаланс бывает последствием влияния гиперплазии коркового слоя надпочечников или опухолевидных образований (некоторые виды опухолей надпочечников способны продуцировать гормоны). Наиболее часто диагностируется наличие надпочечниковой гиперандрогении врожденного типа. Однако иногда встречаются и случаи развития гиперандрогении вследствие опухолей надпочечников, секретирующих андрогены (болезнь Иценко-Кушинга).
Как распознать недуг?
Самостоятельно диагностировать у себя гиперандрогению невозможно, поскольку такие же симптомы могут быть проявлением других болезней. При проведении диагностики доктор, прежде всего, должен исключить заболевания, сопровождающие эту патологию (синдром Кушинга, новообразования надпочечников, яичников). Немаловажной задачей при установлении гиперандрогении является выявление причин, ее обусловивших. Связано это с тем, что направление лечения, проводимого в дальнейшем, зависит напрямую от того, чем вызвано это заболевание. Терапия будет эффективной только в том случае, когда правильно установлены факторы, вызвавшие патологические процессы. Устанавливают, когда проявились первые симптомы недуга – в пубертатном периоде либо позже. Это во многих случаях поможет установить, патология каких органов обусловила заболевание – яичников или надпочечников.
Чтобы диагностировать заболевание, необходимо выполнить следующие исследования:
- исследования крови и мочи на предмет гормонов. Учитывая, что гормональный фон больных нестабильный, забор крови повторяют трижды с интервалом 30 минут, затем смешивают ее и проводят анализ;
- УЗИ малого таза;
- КТ и УЗИ надпочечников.
В случае необходимости могут быть назначены дополнительные методы диагностики.
Особенности развития адреногенитального синдрома у женщин
Адреногенитальный синдром у женщин приводит к серьезным изменениям в функционировании яичников и нарушениям в репродуктивной системе. Согласно статистическим исследованиям, каждая пятая женщина в той или иной степени страдает гиперандрогенией с различными проявлениями. Причем возраст в данном случае не имеет значения, заболевание проявляется на любом этапе жизненного цикла, начиная с младенчества.
Воздействие гиперандрогении на функцию яичников вызывает следующие проявления:
- угнетение роста и развития фолликулов в ранней фазе фолликулогенеза проявляется аменореей (отсутствием менструаций в течение нескольких циклов);
- замедление роста и развития фолликула и яйцеклетки, не способной к овуляции, способно проявиться ановуляцией (отсутствием овуляции) и олигоменореей (увеличением интервала между менструациями);
- овуляция с дефектным желтым телом, выражается в недостаточности лютеиновой фазы цикла, даже при регулярных менструациях.
В чем опасность заболевания
Наиболее серьезным последствием заболевания является бесплодие, поскольку при повышенной концентрации в сыворотке крови андрогенов фолликулы не могут нормально расти и созревать.
Если беременность все же наступает, то существует значительная вероятность ее прерывания на ранних сроках или замирания развития плода.
Рекомендуем прочитать о синдроме поликистозных яичников. Вы узнаете о причинах и симптомах СПКЯ, возможных осложнениях, УЗИ и других методах диагностики, лечении.
А здесь подробнее о дисфункции яичников.
Симптомы надпочечниковой гиперандрогении

Адреногенитальный синдром имеет первостепенные и второстепенные проявления, в зависимости от фазы развития заболевания и факторов его возникновения. Косвенными признаками наличия надпочечниковой гиперандрогении у женщины бывают частые простудные заболевания, склонность к депрессии, повышенная утомляемость.
Основные симптомы надпочечниковой гиперандрогении:
- повышенный рост волосяного покрова (конечности, живот, молочные железы), вплоть до гирсутизма (рост волос на щеках);
- облысение с формированием залысин (алопеция);
- изъяны кожного покрова (угри, прыщи, шелушение и прочие воспаления);
- атрофия мышц, остеопороз.
Второстепенными симптомами адреногенитального синдрома выступают следующие проявления:
- артериальная гипертензия, проявляющаяся в форме приступов;
- повышенный уровень содержания глюкозы в крови (диабет по второму типу);
- быстрый набор избыточного веса, вплоть до ожирения, нуждающегося в терапии;
- промежуточный тип формирования женских половых органов;
- отсутствие менструации или значительные интервалы между менструациями;
- бесплодие или выкидыш (для благополучного протекания беременности необходимо определенное количество женских гормонов в организме, продуцирование которых практически прекращается в случае возникновения гиперандрогении).
Механизм формирования
Синтез андрогенов (мужских половых гормонов) происходит в яичках и надпочечниках. Этот процесс на начальных этапах идет одинаково в обоих органах и является общим для андрогенов и других стероидов, вырабатываемых надпочечниками: кортизона, кортикостерона и альдостерона. Основными ферментами, которые обслуживают ступени последовательных превращений предшественников тестостерона, являются гидроксилазы и дегидрогеназы.
Казалось бы, раз дело касается мужских половых гормонов, то и патология должна быть присуща только мальчикам, однако это не так, поскольку на начальных этапах биосинтез эстрогенов (женских половых гормонов) ничем не отличается от такового у мужчин, поэтому эти мутации также возможны и у индивида женского пола.
И когда у девочки проявляются черты противоположного пола, принято говорить об адреногенитальном синдроме, который может быть представлен тремя клиническими формами:
- врожденной;
- постнатальной или препубертатной;
- постпубертатной.
Гормональные сдвиги вызывают нарушение половой дифференцировки, которое нередко берет начало еще во внутриутробном периоде, а затем продолжается в постнатальном. Разумеется, если адреногенитальный синдром проявляется уже у новорожденных, то вряд ли можно подвергать сомнению его врожденную наследственную природу. Такую форму гиперандрогении называют классической, и она часто ставит в затруднительное положение неонатологов при определении пола ребенка.
Осложнения

Надпочечниковая гиперандрогения является серьезной патологией, способной привести к значительным осложнениям. При гиперандрогении врожденного типа имеют место аномалии развития половых органов. Расстройства репродуктивной системы способны привести к выкидышу, хронической невозможности выносить плод, бесплодию. При гиперандрогении, возникшей вследствие опухолей надпочечников, существует риск развития злокачественных новообразований и метастазирования.
Диагностические мероприятия
В самом начале врач должен провести дифференциальную диагностику, исключив другие специфические заболевания. Речь идет о следующих патологиях:
- Акромегалия;
- Печеночные недуги;
- Аномальная дифференциация по половому признаку;
- Синдром Кушинга;
- Опухолевые образования надпочечников, способные секретировать андрогены.
Диагноз надпочечниковая гиперандрогения может быть поставлен только после всех надлежащих диагностических процедур. В первую очередь, пациентка назначают следующие анализы:
- Изучение гормонального фона. Современные методы обследования в лаборатории позволяют точно выяснить количество пролактина, свободного и общего тестостерона, уровня ФСГ в крови. Из-за того, что гормональные вещества в течение суток вырабатываются неравномерно, пробы делают трижды на сутки;
- Идентификация кетостероидов в моче;
- Маркеры на ХГ.
Неконтролируемая и не купируемая гипертензия – болезнь надпочечного генеза, поэтому анализы и исследования, традиционные для идентификации патологий ГБ также актуальны. Пациентке в обязательном порядке назначают внутривлагалищное УЗИ обследование; диагностика при помощи МРТ или КТ актуальна в том случае, если особенности организма пациентки нужно изучить предельно подробно. Чтобы точно установить тип и особенности течения заболевания, диагностика ультразвукового типа может проводится несколько раз.
Терапия адреногенитального синдрома
Лечение надпочечниковой гиперандрогении направлено прежде всего на нормализацию гормонального фона и устранение внешних негативных проявлений гормонального дисбаланса. Повышенный уровень андрогенов в организме нейтрализуется с помощью препаратов, способствующих повышению количества гормонов женского типа (например, «Дексаметазон», «Метипрет»).
Гормональная терапия у женщин напрямую зависит от планов пациентки на будущее. Если женщина не планирует зачатия ребенка, то назначаются оральные контрацептивы с антиандрогенным эффектом (например, «Жанин», «Янина»). Для устранения кожных проявлений полезен оральный контрацептив «Диане-35», который назначается в паре с препаратом «Андрокур» для усиления эффекта. Однако результат проявится только через три месяца терапии. В случае планирования беременности назначаются препараты, активирующие выход яйцеклетки. При отсутствии терапевтического эффекта возможно хирургическое вмешательство в виде клиновидной резекции яичников с целью стимуляции выхода яйцеклетки. А также оперативное вмешательство показано при наличии опухолей надпочечников (опухоли должны быть удалены хирургическим путем).
В качестве народных средств регуляции гормонального фона применяются сборы лекарственных трав. Существует масса растений, благотворно влияющих на обменные процессы и способствующих нормализации гормонального баланса (дягиль, клопогон, корень солодки, мята, пион уклоняющийся, прутняк священный и т. д.). Однако использование растительных средств возможно лишь как дополнение врачебной терапии, самостоятельно устранить патологию народными средствами невозможно.
Постановка диагноза
Диагностика патологического состояния включает внешний и гинекологический осмотр пациентки, анализ ее жалоб на общее самочувствие. Обращают внимание на длительность менструального цикла, локализацию избыточного оволосения, индекс массы тела, внешний вид половых органов.
Какие анализы нужно сдать для определения уровня андрогенов?
Врачи (гинеколог, эндокринолог, генетик) назначают следующие исследования:
- определение уровня тестостерона, фолликулярного гормона, пролактина, эстрадиола в крови и кортизола в моче;
- пробы с дексеметазоном для определения причины развития синдрома;
- УЗИ яичников и надпочечников;
- КТ гипофиза;
- исследования уровня глюкозы, инсулина, холестерина.
УЗИ органов малого таза позволит определить возможное наличие поликистоза яичников. Проведение анализов необходимо для установки разновидности заболевания.
Материалы для исследований берут в утренние часы, до приема пищи. Поскольку гормональный фон отличается нестабильностью, для точного диагностирования берут три пробы с перерывами не менее получаса. Желательно сдавать анализы во второй половине менструального цикла, ближе к предполагаемому началу месячных.
Приёмы консервативного лечения
Если врач поставил вам диагноз гиперадрогения, это вовсе не значит, что необходима срочная операция. В большинстве случаев с проблемой можно справиться менее радикальными методами, но это в том случае, если лечение не будет пущено на самотёк . Что может предложить пациентке доктор?
- Пересмотреть собственный рацион. Ведь избыточная масса тела – один из факторов риска. Постарайтесь снизить употребление высококалорийных продуктов, перейдя на гипокалорийную диету.
Постарайтесь снизить употребление высококалорийных продуктов, перейдя на гипокалорийную диету
- Заняться спортом. Если перспектива стать олимпийской чемпионкой вам не нравится, занятиям физической культурой всё равно нужно уделять не меньше одного часа три раза в неделю. Неплохо приобрести абонемент на посещение бассейна или секции аэробики, а также больше ходить и меньше ездить в общественном транспорте.
Источник
