Синдром грейвса что это такое

Что такое болезнь Грейвса?
Болезнь Грейвса — это заболевание, поражающее щитовидную железу и часто кожу и глаза. Щитовидная железа является железой и частью эндокринной системы, сети желез, которые выделяют гормоны, регулирующие химические процессы (обмен веществ), которые влияют на деятельность организма, а также регулируют частоту сердечных сокращений, температуру тела и кровяное давление. Гормоны выделяются непосредственно в кровоток, где они попадают в различные области тела.
Болезнь Грейвса характеризуется аномальным увеличением щитовидной железы (зобом) и повышенной секрецией гормона щитовидной железы (гипертиреоз). Гормоны щитовидной железы участвуют во многих различных системах организма, и, следовательно, конкретные симптомы и признаки болезни Грейвса могут широко варьироваться от одного человека к другому. Общие симптомы включают непреднамеренную потерю веса, непереносимость тепла, мышечную слабость, усталость и выпячивание глазных яблок из их гнезд. Болезнь Грейвса является аутоиммунным заболеванием.
Признаки и симптомы

Появление симптомов, связанных с болезнью Грейвса, обычно происходит постепенно, часто на развитие признаков уходит несколько недель или месяцев. Симптомы могут включать поведенческие изменения, такие как:
- нервозность;
- раздражительность;
- беспокойство;
- проблемы со сном (бессонница).
Дополнительные симптомы включают:
- непреднамеренную потерю веса;
- мышечную слабость;
- ненормальную непереносимость тепла;
- повышенное потоотделение;
- учащенное, нерегулярное сердцебиение (тахикардия);
- усталость.
Болезнь Грейвса часто связана с аномалиями, затрагивающими глаза, которые часто называют офтальмопатией Грейвса. В то время как легкая офтальмопатия присутствует у большинства людей с гипертиреозом Грейвса в какой-то момент их жизни, менее 10% имеют значительное поражение глаз, которое требует терапии. Глазные симптомы могут развиваться до, одновременно или после развития гипертиреоза. В редких случаях у людей с глазными симптомами никогда не развивается гипертиреоз. В некоторых случаях офтальмопатия Грейвса может впервые проявиться или ухудшиться после лечения гипертиреоза Грейвса.
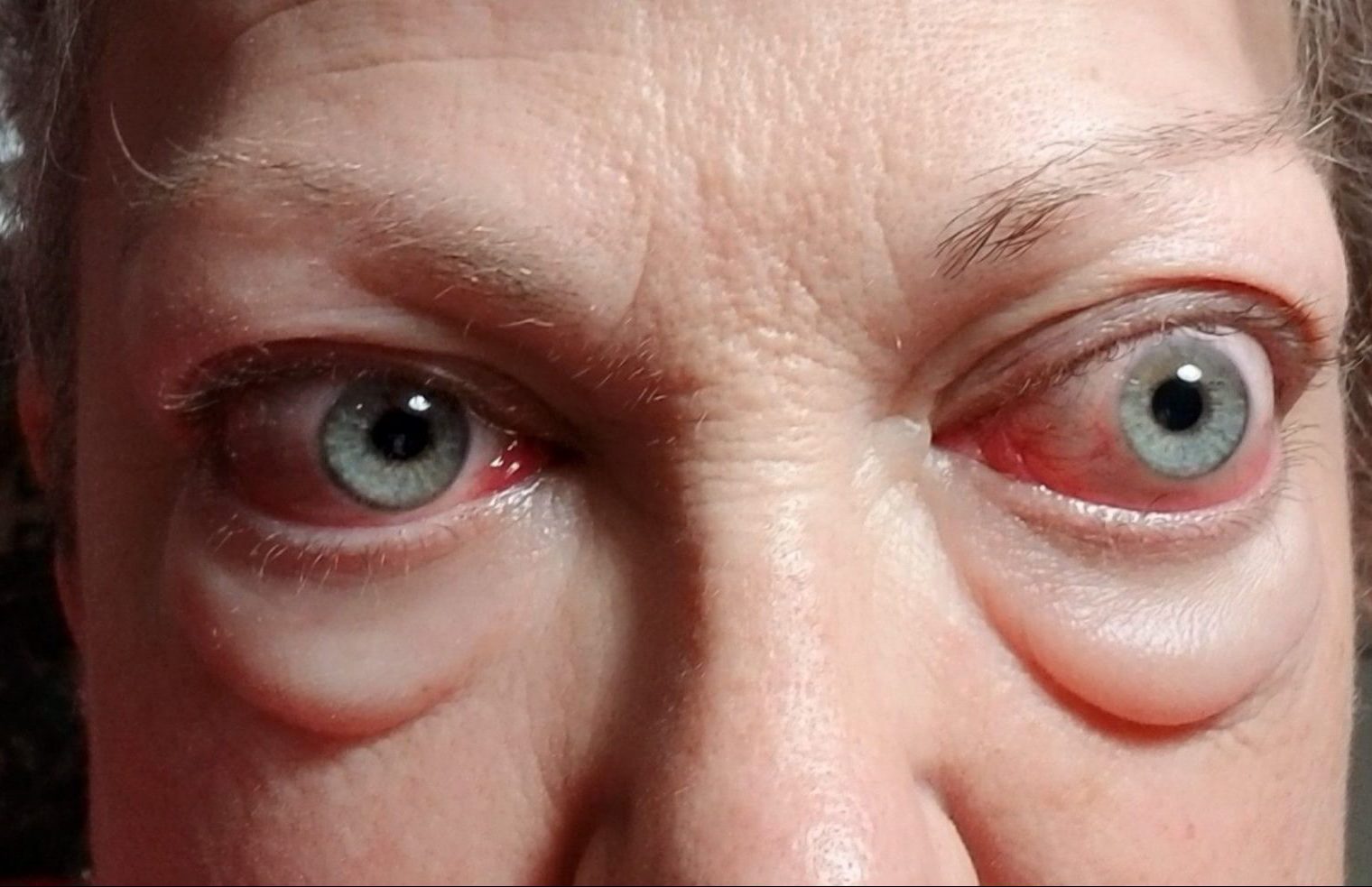
Офтальмопатия Грейвса сильно варьирует от человека к человеку. У некоторых людей она может оставаться неизменной в течение многих лет, в то время как у других она может улучшаться или ухудшаться. Она также может следовать схеме ухудшения (обострения), а затем значительно улучшаться (ремиссия). Большинство людей имеют легкое заболевание без прогрессирования.
Общие аномалии глаза включают отек тканей, окружающих глаз, которые могут вызвать выпячивание глаза из его защитного гнезда (орбиты), состояние, называемое проптозом. Пострадавшие могут также испытывать сухость глаз, опухание веки, ретракцию век, воспаление, покраснение, боль и раздражение глаз. Некоторые больные описывают ощущения песка в глазах. Реже также может наблюдаться помутнение или двойное зрение, чувствительность к свету (светобоязнь) и/или ухудшение зрения.
Очень редко у людей с болезнью Грейвса развивается кожное заболевание, известное как претибиальная дермопатия или микседема. Это состояние характеризуется развитием утолщенной, красноватой кожи на передней части голеней. Она обычно ограничена голенями, но, иногда, может также появится на ногах. Редко возникает отек мягких тканей кистей рук и пальцев рук и ног (акропахия).
Дополнительные симптомы, связанные с болезнью Грейвса, включают учащенное сердцебиение, легкую дрожь рук и/или пальцев, выпадение волос, ломкость ногтей, повышение сегментарных рефлексов (гиперрефлексия), повышение аппетита и увеличение частоты дефекаций. Женщины с болезнью Грейвса могут испытывать изменения в менструальном цикле. Мужчины могут испытывать эректильную дисфункцию. В некоторых случаях болезнь Грейвса может прогрессировать, вызывая застойную сердечную недостаточность или ненормальное истончение и слабость костей (остеопороз), что делает кости ломкими и подверженными повторным переломам.
Причины и факторы риска
Болезнь Грейвса считается аутоиммунным заболеванием, но есть и другие факторы, способствующие его развитию, включая генетические, экологические и/или другие факторы.
Аутоиммунные нарушения возникают, когда иммунная система организма по ошибке атакует здоровые ткани. Иммунная система обычно вырабатывает специализированные белки, называемые антителами. Антитела реагируют на инородные вещества (например, бактерии, вирусы, токсины) в организме, вызывая их разрушение. Антитела могут напрямую убивать микроорганизмы или покрывать их, чтобы они легче разрушались лейкоцитами. Конкретные антитела создаются в ответ на конкретные материалы или вещества. Вещество, которое стимулирует выработку антител, называется антигеном.
При болезни Грейвса иммунная система создает аномальное антитело, называемое иммуноглобулином, стимулирующим щитовидную железу. Это антитело имитирует функцию нормального тиреотропного гормона. Он прикрепляется к поверхности клеток щитовидной железы и включает клетки для выработки гормонов, что приводит к перепроизводству этих гормонов (сверхактивности щитовидной железы). При офтальмопатии Грейвса эти антитела могут также влиять на клетки, окружающие глаза.
Пострадавшие могут нести гены или иметь генетическую предрасположенность к болезни Грейвса. Человек, который генетически предрасположен к расстройству, несет ген (или гены) заболевания, но он не может быть выражен, если он не вызван или «активирован» при определенных обстоятельствах, таких как из-за определенных факторов окружающей среды (многофакторное наследование).
Были идентифицированы различные гены, которые связаны с болезнью Грейвса, включая гены, ослабляющие или модифицирующие реакцию иммунной системы (иммуномодуляторы), такие как CD25, CD40, CD40, CTLA-4, FOXP3 и различные гены HLA, в частности HLA- DR3. Гены, которые напрямую связаны с функцией щитовидной железы, такие как гены тиреоглобулина (Tg) или рецептор гормона, стимулирующего щитовидную железу (TSHR), также связаны с болезнью Грейвса. Ген Tg продуцирует тиреоглобулин — белок, содержащийся только в ткани щитовидной железы и играющий роль в выработке гормонов щитовидной железы. Ген TSHR производит белок, который является рецептором и связывается с гормонами, стимулирующими щитовидную железу. Точная причина, по которой генетические факторы и факторы окружающей среды взаимодействуют, вызывая заболевание, до конца не изучена. Дополнительные генетические факторы, известные как гены-модификаторы, могут играть роль в развитии или выражении болезни Грейвса.
Факторы окружающей среды, которые могут вызвать развитие заболевания, включают экстремальные эмоциональные или физические нагрузки, инфекцию или беременность. Люди, которые курят, подвергаются большему риску развития болезни Грейвса и офтальмопатии Грейвса. Люди с другими расстройствами, вызванными сбоями в работе иммунной системы, такими как диабет 1 типа или ревматоидный артрит, подвержены большему риску развития болезни Грейвса.
Затронутые группы населения
Болезнь Грейвса поражает женщин чаще, чем мужчин, в соотношении 5-10 к 1. Нарушение обычно развивается в среднем возрасте с пиковой заболеваемостью в 40-60 лет, но может также затрагивать детей, подростков и пожилых людей. Заболевание встречается практически в любой части мира. По оценкам, патология поражает 2-3% населения в целом. Болезнь Грейвса является наиболее распространенной причиной гипертиреоза.
Близкие по симптомам расстройства
Люди с болезнью Грейвса часто имеют в анамнезе других членов семьи с проблемами щитовидной железы или аутоиммунными заболеваниями. У некоторых родственников может быть гипертиреоз или недостаточная активность щитовидной железы (гипотиреоз); у других могут быть другие аутоиммунные заболевания, включая преждевременное поседение волос (начиная с 20 лет). Точно так же в семье могут быть проблемы с иммунитетом, в том числе ювенильный диабет, пернициозная анемия (из-за недостатка витамина В12) или безболезненные белые пятна на коже, известные как витилиго.
Болезнь Хашимото, также известная как тиреоидит Хашимото или аутоиммунный тиреоидит, является аутоиммунным заболеванием, подобным болезни Грейвса. Однако антитела при болезни Хашимото либо блокируют, либо разрушают щитовидную железу и вызывают недостаточную секрецию гормонов щитовидной железы (гипотиреоз). Тиреоидит Хашимото может возникать в любом возрасте, но чаще всего встречается в третьем-пятом десятилетиях жизни и чаще встречается у женщин, чем у мужчин. Он характеризуется увеличенной щитовидной железой, которая инфильтрирована лимфоцитами. Со временем щитовидка может быть полностью разрушена. Лечение состоит в замене количества гормона, которое собственная щитовидная железа больше не может вырабатывать, L-тироксином, синтетической формой основного гормона щитовидной железы.
Другие причины гипертиреоза включают токсический узловой или многоузловой зоб, для которого характерны один или несколько узелков или комков в щитовидной железе, постепенно растущих и увеличивающих свою активность, так что общий выброс гормона щитовидной железы в кровь превышает норму. Кроме того, больные могут временно иметь симптомы гипертиреоза, если у них есть состояние, которое называется тиреоидит. Тиреоидит возникает в результате проблем с иммунной системой или вирусной инфекции, в результате которой из железы вытекает накопленный гормон щитовидной железы. Типы тиреоидита включают подострый тиреоидит, тихий тиреоидит, инфекционный тиреоидит, радиационный тиреоидит и послеродовой тиреоидит. В большинстве случаев тиреоидит проходит. Редко, определенные формы рака щитовидной железы и некоторые опухоли, такие как аденомы гипофиза, продуцирующие ТТГ, могут вызывать симптомы, подобные тем, которые наблюдаются при болезни Грейвса. Наконец, симптомы гипертиреоза также могут быть вызваны приемом слишком большого количества гормона щитовидной железы в форме таблеток.
Диагностика
Диагноз болезни Грейвса ставится на основании подробной истории заболеваний пациента и семьи, тщательной клинической оценки, определения характерных признаков и специальных тестов, таких как анализы крови, измеряющих уровни гормонов щитовидной железы и гормонов, стимулирующих работу щитовидной железы. Для подтверждения диагноза могут быть проведены анализы крови на наличие специфических антител, вызывающих болезнь Грейвса, но, как правило, в них нет необходимости.
Стандартные методы лечения
Лечение болезни Грейвса обычно включает один из трех методов:
- Антитиреоидные препараты (тионамиды).
- Использование радиоактивного йода.
- Хирургическое вмешательство.
Конкретная форма рекомендованного лечения может основываться на возрасте больного и степени заболевания.
Наименее инвазивным методом лечения болезни Грейвса является использование препаратов, уменьшающих выброс гормона щитовидной железы (антитиреоидные препараты). Эти препараты особенно предпочтительны для лечения детей младшего возраста и беременных женщин, лиц с легкими случаями гипертиреоза или лиц, которым требуется быстрый контроль гипертиреоза. Наиболее распространенным антитиреоидным препаратом, используемым для лечения болезни Грейвса, является метимазол, который рекомендован Американской ассоциацией щитовидной железы и Американской ассоциацией клинических эндокринологов в качестве исходного метода лечения гипертиреоза у детей и подростков. В России есть аналоги: тирозол, мерказолил. Иногда пропилтиоурацил (пропицил) используется в особых случаях, особенно когда болезнь Грейвса возникает на ранних сроках беременности.
Определенными методами лечения болезни Грейвса являются те, которые разрушают щитовидную железу, что часто приводит к гипотиреозу. Окончательная терапия радиоактивным йодом является наиболее распространенным методом лечения болезни Грейвса. Йод — это химический элемент, используемый щитовидной железой для создания (синтеза) гормонов щитовидной железы. Почти весь йод в организме человека поглощается тканями щитовидной железы. Больным дается раствор, содержащий радиоактивный йод, который будет проходить через кровоток и накапливаться в щитовидке, где он будет повреждать и разрушать ткани щитовидной железы. Это уменьшит щитовидную железу и уменьшит перепроизводство гормонов. Если уровень гормонов щитовидной железы упадет слишком низко, может потребоваться гормональная терапия для восстановления адекватного уровня гормонов щитовидной железы.
Другой окончательной терапией является операция по удалению всей или части щитовидной железы (тиреоидэктомия). Этот метод лечения болезни Грейвса обычно предназначен для лиц, у которых другие формы лечения не были успешными или противопоказаны или при наличии больших желез, или тем, кто заинтересован в скорейшем разрешении гипертиреоза. После операции часто возникает гипотиреоз; однако, эта операция может привести к желаемому результату.
В дополнение к трем вышеупомянутым методам лечения могут быть назначены препараты, блокирующие гормоны щитовидной железы, которые уже циркулируют в крови, для выполнения своих функций (бета-блокаторы). Можно использовать бета-блокаторы, такие как пропранолол, атенолол или метопролол. Когда уровень гормонов щитовидной железы нормализуется, терапию бета-блокаторами можно прекратить.
Во многих случаях необходимы пожизненное наблюдение и лабораторные исследования. В некоторых случаях может потребоваться пожизненная гормонозамещающая терапия.
Легкие случаи офтальмопатии Грейвса (нарушения зрения, связанные с болезнью Грейвса) можно лечить с помощью солнцезащитных очков, мазей, искусственных слез и/или призм, прикрепленных к очкам. Более серьезные случаи офтальмопатии Грейвса можно лечить кортикостероидами, такими как преднизон, чтобы уменьшить отек тканей, окружающих глаза.
Орбитальная декомпрессионная операция и орбитальная лучевая терапия также могут быть необходимы в более тяжелых случаях. Во время операции орбитальной декомпрессии хирург вынимает кость между глазницей (орбитой) и пазухами. Это позволяет глазу вернуться в свое естественное положение внутри глазницы. Эта операция обычно предназначена для лиц, подвергающихся риску потери зрения из-за давления на зрительный нерв или больным, которым другие варианты лечения не помогли. Эти методы лечения требуют лечения у офтальмологов, специализирующихся на лечении офтальмопатии Грейвса.
Прогноз
Многие пациенты остаются здоровыми после одного курса антитиреоидных препаратов, но рецидив может произойти в любое время. Радиоактивный йодид очень эффективен, но часто приводит к гипотиреозу. Хирургия также может вызвать гипотиреоз.
Признаки заболевания, как правило, улучшаются при лечении антитиреоидными препаратами. Тем не менее, некоторый дефекты внешнего вида часто остается.
Источник
Диффузный токсический зоб (болезнь Грейвса, Базедова болезнь, гипертиреоз, болезнь Перри, болезнь Флаяни) — аутоиммунное заболевание, обусловленное избыточной секрецией тиреоидных гормонов диффузной тканью щитовидной железы, которое приводит к отравлению этими гормонами —тиреотоксикозу. Кроме того, сбитая с толку иммунная система пациента начинает проявлять агрессию против собственных клеток.

Диффузный токсический зоб (ДТЗ) относят к опасным для жизни заболеваниям, потому как результатом его оказываются необратимые изменения во всех органах и тканях человеческого организма, особенно в сердце, сосудах, нервной системе и скелете пациента.
Диффузным токсическим зобом заболевают преимущественно в молодом и среднем возрасте женщины (в основном, жительницы крупных городов), и страдают они от этого заболевания в 5-10 раз чаще мужчин. Понятия «тиреотоксикоз» и «диффузный токсический зоб» для многих означают одно и то же, хотя это не соответствует истине. Тиреотоксикоз — это синдром, который может сопутствовать многим заболеваниям и состояниям, в том числе и диффузному токсическому зобу.
Тиреотоксикоз может быть вызван передозировкой L-тироксина и приёмом некоторых лекарственных средств (амиодарона, интерферона). К тому же тиреотоксикоз может возникнуть как симптом заболеваний других органов (к примеру, при опухолях яичников, метастазах рака).
Ещё одно понятие — гипертиреоз — отличается тем, что не является патологическим состоянием. Усиление работы щитовидной железы может проявляться как физиологический процесс при беременности на ранних сроках, при стрессе и прочих кратковременных состояниях.
Говоря профессиональным языком, при диффузном токсическом зобе аутоиммунную агрессию вызывают рецепторы тиреотропного гормона (ТТГ), расположенные на тиреоцитах — белковых структурах, находящихся на поверхности клеток щитовидной железы. При нормальном функционале они соединяются с ТТ-гормоном, который продуцирует и выделяет в кровь гипофиз. Этот тропный гормон является сигналом от центральных эндокринных органов, заставляющий щитовидную железу вырабатывать больше гормонов, в результате чего антитела к рецепторам ТТГ, соединившись с объектом своей агрессии (рецептором), действуют как сам тиреотропный гормон, повышая продукцию тиреоидных гормонов.
Классификация
По-разному можно классифицировать диффузный токсический зоб, степени тяжести которого определяются по размерам зоба и по синдрому тиреотоксикоза.
Для ориентировочного пальпаторного определения размеров щитовидной железы используется несколько дифференциаций.
Наиболее часто продолжает и сегодня использоваться классификация эндемического зоба по О.В. Николаеву.
- 0 степень — щитовидная железа не визуализируется и не пальпируется;
- I степень — железа не визуализируется, но пальпируется и визуализируется перешеек при глотании;
- II степень — щитовидка видна при глотании, пальпируется, но форма шеи не изменена;
- III степень — железа визуализируется и контур шеи утолщен;
- IV степень — зоб большого размера, нарушает контуры шеи;
- V степень — огромный зоб, сдавливающий трахеи и пищевод.
Классификация зоба по ВОЗ (от 1992 года)
- 0 степень — щитовидная железа пальпируется, доли по размерам соответствуют дистальной фаланге пациента;
- I степень — доли железы по размерам больше дистальной фаланги пациента;
- II степень — щитовидная железа визуализируется и пальпируется.
Тиреотоксикоз классифицируется:
Степени тяжести тиреотоксикоза в I варианте:
- Лёгкая степень — при частоте пульса 80-120 ударов в минуту мерцательная аритмия отсутствует, отмечается резкая потеря веса, снижение работоспособности, небольшой тремор верхних конечностей.
- Средняя степень — при частоте пульса 100-120 ударов в минуту наблюдается повышение пульсового давления, отсутствие мерцательной аритмии, снижение веса на 10 кг, упадок сил.
- Тяжелая степень —при частоте пульса более 120 ударов в минуту наблюдается мерцательная аритмия, тиреотоксический психоз, дистрофические изменения паренхиматозных органов, масса тела резко снижена, трудоспособность утрачена.
Степени тяжести тиреотоксикоза во II варианте:
- Лёгкая (субклиническая) степень определяется, в основном, по данным гормонального исследования на фоне стертой клинической картины.
- Средняя (манифестная) степень характеризуется развернутой клинической картиной.
- Тяжелая степень (осложнённая) проявляется сердечной недостаточностью, мерцательной аритмией, тирогенной относительной недостаточностью, дистрофическими трансформациями паренхимных органов, психозом, резкой потерей массы тела.
Осложнения
Вследствие позднего диагностирования диффузного токсического зоба или неадекватного лечения болезнь прогрессирует, проявляя осложнения:
- тиреостатическая миокардиодистрофия, мерцательная аритмия, отек легких;
- токсический гепатоз;
- остеопороз;
- сахарный диабет;
- надпочечниковая недостаточность;
- миопатия (слабость мышц);
- психоз;
- геморрагический синдром (нарушение свертывания крови);
- пернициозная анемия;
- тиреотоксический криз.
Тиреотоксический криз — наиболее тяжелое и опасное для жизни осложнение диффузного токсического зоба, который развивается при внезапно обострившихся симптомах, особенно через несколько часов после частичного оперативного удаления щитовидной железы. Спровоцировать криз могутинфекции, стресс, повышенные физические нагрузки, различные операции и даже удаление зуба.
При развитии тиреотоксического криза происходит мощный выброс неисчислимых активных тиреоидных гормонов, вследствие чего пациенты становятся беспокойными, у них наблюдается значительное повышение артериального давления, затем начинается перевозбуждение, усиливаются все симптомы: тремор, сердцебиение, мышечная слабость, диарея, тошнота, рвота. Дальнейшее возбуждение сменяется ступором, потерей сознания, пациент впадает в кому и погибает.
Прогноз
Прогноз диффузного токсического зоба при адекватном и своевременном лечении— благоприятный, хотя следует учитывать, что послеоперационный период опасен развитием гипотиреоза.
При отсутствии лечения перспектива — неблагоприятная, так как тиреотоксикоз постепенно вызывает сердечно-сосудистую недостаточность, фибрилляцию предсердий, истощение организма.
После лечения тиреотоксикоза и нормализации функции щитовидной железыпрогноз заболевания— благоприятный, большинство пациентов избавляются от кардиомегалии и восстанавливают синусовый ритм сердца.
Профилактика
Профилактические меры при диффузном токсическом зобе предполагают следующее:
- избегать стрессовых ситуаций;
- соблюдать правила гигиены и режим питания;
- отказаться от солнечных ванн и морского купания;
- обеспечивать спокойный отдых и приём витаминов;
- проводить общеукрепляющую терапию;
- привести в соответствие рацион питания;
- своевременно избавляться от хронических очагов инфекции.
И, конечно, при появлении первых симптомов следует немедленно обращаться к эндокринологу.
Причины диффузного токсического зоба
Базедова болезнь (болезнь Грейвса) —мультифакториальное заболевание, так что причины диффузного токсического зоба могут быть следующими:
- генетические особенности иммунного реагирования реализуются на фоне действия психосоциальных факторов и окружающей среды (инфекции, стрессы);
- присутствует этнически ассоциированная генетическая предрасположенность (носительство гаплотипов HLAB8, DR3 и DQA1*0501 у европейцев), а экзогенные факторы (курение, повышающее риск почти в 2 раза, потеря близкого человека) способствуют реализации такой предрасположенности;
- в сочетании с другими аутоиммунными эндокринными заболеваниями (сахарный диабет 1 типа, первичный гипокортицизм) формируется аутоиммунный полигландулярный синдром II типа;
- образование стимулирующих антител к рецептору ТТГ, связавшихся с этим рецептором, активизируют его, запуская внутриклеточные системы, стимулирующие захват щитовидной железой йода, синтез и высвобождение тиреоидных гормонов, пролиферацию тироцитов, что в итоге приводит к синдрому тиреотоксикоза — доминанте в клинической картине Базедовой болезни.
В регионах с нормальным йодным обеспечением болезнь Грейвса является преимущественной причиной стойкого тиреотоксикоза, а в йододефицитных регионах в этиологической структуре токсического зоба это заболевание конкурирует с функциональной автономией щитовидной железы(узловым токсическим зобом).
Предрасположенность к диффузному токсическому зобу передается по наследству, но не у каждого человека с такой наследственностью разовьется это заболевание, нужны факторы-провокаторы (триггеры).
При любых аутоиммунных заболеваниях наиболее мощным триггером является хроническая инфекция в организме, особенно в ЛОР-органах (носу, горле, ушах), потому что эти органы имеют общий со щитовидной железой коллектор лимфатической системы, которая является канализацией человеческого организма.
Все токсины и бактериальные агенты попадают в эту «канализацию», проходя через щитовидную железу, тем самым как бы метят её как зараженную. Затем клетки иммунной системы стремительно направляются в это место и уничтожают всё подряд, не разделяя «своих» и «чужих». Таким путем развивается синдром тиреотоксикоза.
Другими триггерами могут быть:
- стресс (длительные эмоциональные перегрузки или же внезапный шок);
- очаг хронической инфекции (тонзиллит, синусит, аденоиды);
- острая вирусная инфекция (ОРВИ);
- симпатикотония (преобладание тонуса симпатической нервной системы);
- родственники, члены семьи с другими аутоиммунными заболеваниями (сахарный диабет 1 типа,болезнь Аддисона, пернициозная анемия, миастения gravis).
Диффузный токсический зоб нередко совмещается с другими аутоиммунными заболеваниями:
- ревматоидным артритом (поражение суставов);
- гломерулонефритом (поражение почек);
- сахарным диабетом I типа;
- витилиго;
- пернициозной анемией и прочими.
Симптомы диффузного токсического зоба
При таком заболевании, как диффузный токсический зоб, симптомы складываются из признаков аутоиммунной реакции и гиперфункции щитовидной железы. Аутоиммунное поражение проявляется:
- увеличением щитовидной железы;
- поражением надпочечников, глаз, кожи, жировой ткани, мышц;
- визуальным утолщением шеи (безболезненность при пальпировании, эластичность ткань железы);
- отечностью век, слезоточивостью, двоением в глазах, экзофтальмом в 50% случаев;
- пигментными пятнами темного цвета вокруг глаз и на ладонях;
- утолщением кожи на переднем участке голени (не всегда);
- выраженной мышечной слабостью;
- гиперфункцией щитовидной железы, связанной с избытком тиреоидных гормонов (тироксин и трийодтиронина) и проявляющейся повышенным метаболизмом в организме, нарушениями в нервной, сердечно-сосудистой системе, желудочно-кишечном тракте;
- постоянным чувством жара, потливостью, субфебрильной температурой тела;
- потерей массы телапри нормальном или повышенном аппетите до 10% при лёгкой степени тиреотоксикоза, до 20% — при средней степени и более 20% — при тяжелом тиреотоксикозе;
- плаксивостью, возбудимостью, нарушениями сна;
- тремором во всем теле и особенно в руках;
- учащенным сердцебиением, мерцательной аритмией, проявлениями гипертонии;
- иногда болями в животе, учащенным стулом, увеличением печени.
Собственно синдром тиреотоксикоза ещё подразделяют на:
- Синдром нервно-психических нарушений, проявляющийся нервозностью, суетливостью, быстрой сменой настроения, тремором рук, головы или всего тела.
- Синдром обменно-энергетических нарушений, проявляющийся похуданием на фоне нормального или даже повышенного аппетита, слабостью в плечах и бедрах, постоянным ощущением жара и потливости.
- Синдром нарушения сердечно-сосудистой системы, характеризующийся тахикардией, мерцательной аритмией, тиреотоксической миокардиодистрофией.
- Синдром поражения желудочно-кишечного тракта, суть которого в учащенном стуле (до профузных поносов), тиреотоксический гепатоз с переходом в цирроз, возможно увеличение селезёнки.
- Синдром вторичных эндокринных нарушений — менструального цикла, развитие остеопороза, поражение репродуктивной системы, снижение потенции, гинекомастия у мужчин.
- Изменения углеводного обмена — нарушение толерантности к глюкозе и развитие сахарного диабета.
- Недостаточность надпочечников, при которой повышается потребность в гормоне надпочечника — кортизоле, особенно в последней стадии заболевания, когда избыток гормонов щитовидной железы истощает надпочечники.
Главные симптомы тиреотоксикоза:
- симптом Грефе (отставание верхнего века от радужки при взгляде вниз);
- симптом Дельримпля (широкое раскрытие глазных щелей);
- симптом Штельвага (редкое мигание);
- симптом Мебиуса (невозможность фиксировать взгляд на близком расстоянии);
- симптом Кохера (поднятие верхнего века при быстрой перемене взгляда).
Но это не офтальмопатия, а симптомы, которые связаны непосредственно с избытком тиреоидных гормонов. Офтальмопатия наблюдается в 95% случаев заболевания диффузным токсическим зобом.
Клиническая картина тиреотоксикоза
Субклинический тиреотоксикоз, когда симптоматика практически отсутствует. Гормоны: свободный Т3 и свободный Т4—в норме, ТТГ менее 0,2 мМЕ/л при диффузном токсическом зобе встречается редко.
Клинически выраженный тиреотоксикоз, т. е. все симптомы — налицо плюс наличие изменений в гормональном статусе.
Атипичные формы, когда течение болезни происходит нестандартно.
Обнаружили симптомы данного заболевания?
Звоните
Наши специалисты проконсультируют Вас!
Диагностика диффузного токсического зоба
При подозрении на диффузный токсический зобдиагностикаимеет основополагающие методы обследования:
- исследование уровня тиреоидных гормонов и гормона гипофиза — ТТГ (обычно уровень тиреоидных гомонов повышен, а ТТГ — снижен);
- УЗИ (ультразвуковое исследование) щитовидной железы (наблюдается увеличение размеров щитовидной железы, снижение эхогенности ткани и усиление сосудистого рисунка);
- сцинтиграфия — радиоизотопное исследование с изотопами йода (131, 123) и технеция (99m) (пораженная тиреотоксикозом железа быстро и равномерно захватывает радиоактивные элементы);
- МРТ (магнитно-резонансная томография) определит наличие офтальмопатии;
- общеклинические анализы помогут наблюдать работу печени и почек, определить уровень лейкоцитов в крови, что необходимо при назначении дальнейшей терапии;
- анализ крови на присутствие титров специфических антител как более современный метод исследования: выявляет повышенное содержание антител к рецепторам ТТГ, уточняет диагноз ДТЗ и помогает определить продолжительность лечения; проводится также перед решением отмены препарата.
Дифференциальная диагностика проводится с заболеваниями, протекающими с синдромом тиреотоксикоза.
Лечение диффузного токсического зоба
Когда поставлен диагноз диффузный токсический зоб, лечение должно быть направлено на снижение и нормализацию уровня гормонов щитовидной железы в крови, устранение симптоматики тиреотоксикоза и попытки добиться стойкой (желательно пожизненной) ремиссии заболевания.
Сегодня доступными методами лечения диффузного токсического зоба являются:
- Консервативная медикаментозная терапия тиреостатиками (Тиамазол, Мерказолил, Метимазол,Пропицил, Эутирокс в течение полутора лет). Во время беременности —пропилтиоурацил в минимально необходимой дозе и с L-тироксином не сочетают. Глюкокортикоиды — только при тирогенной надпочечниковой недостаточности, оперативных вмешательствах, тиреотоксическом кризе.
- Радиойодтерапия (лечение изотопами радиоактивного йода I131) проводится при определенных условиях:
- послеоперационный рецидив диффузного токсического зоба;
- пожилой возраст;
- сопутствующая патология, исключающая приём тиреостатиков и/или проведение операции;
- отказ пациента от операции.
- Хирургическое лечение (частичное или полное удаление щитовидной железы) проводится после наступления эутиреоза с помощью тиреостатиков и наличии рецидива ДТЗ, а также при
- больших размерахзоба;
- узловых образованиях;
- загрудинном зобе, непереносимости тиреостатиков;
- беременности, тяжелой степени тиреотоксикоза;
- токсической аденоме.
Частота рецидивов после оперативного лечения — не более 10%, но могут быть осложнения — повреждение возвратного нерва с парезом гортани, гипопаратиреоз.
Все вышеперечисленные методы лечения не относятся к патогенетическим, они только помогают устранить те или иные проявления токсического зоба. Метод терапии подбирается индивидуально для каждого пациента, с обязательным учётом существующих показаний и противопоказаний. Немаловажное значение имеет стаж применения каждой методики лечащим эндокринологом, а также его предпочтения при выборе самого оптимального терапевтического метода, хотя основная направленность лечения диффузного токсического зоба должна быть стандартной для всех.
Данная статья размещена исключительно с целью ознакомления в познавательных целях и не является научным материалом
или профессиональным медицинским советом. За диагностикой и лечением обратитесь к врачу.
Источник
