Синдром махейна что это такое

Определение и патогенез
В 1971 г. Велленс (Wellens) описал случай у 8-летнего мальчика с тахикардией с широкими комплексами по типу БЛНПГ, у которого во время синусового ритма отмечались интервал P-R 0,12 с и минимальные признаки предвозбуждения “типа В”. Было принято, что в основе этой формы предвозбуждения находится нодовентрикулярный тракт Махайма. Впоследствии было продемонстрировано, что ДПП у этих пациентов обычно состоит из правостороннего патологического узла в свободной стенке, который продолжается в добавочную систему Гиса-Пуркинье, в дистальной части врастающий в нормальную правую ножку пучка Гиса или напрямую в миокард ПЖ.
Термин “физиология Махайма” ошибочно используют для наименования этого состояния, поскольку Махайм описал нодовентрикулярные и фасцикуловентрикулярные соединения, а в нашем случае мы имеет дело с атриофасцикулярными или шунтирующими АВ-трактами. Данная форма предвозбуждения наблюдается менее чем в 1% случаев пациентов с ДПП, обследованных в электрофизиологических лабораториях, и более часто встречается у пациентов с аномалией Эбштейна, и также чаще у женщин, чем у мужчин.
Диагностика
Предсердная стимуляция с нарастающей частотой приводит к нарастающему предвозбуждению желудочков, в конечном итоге воспроизводящему морфологию комплекса QRS, наблюдаемую во время тахикардии. Поскольку проксимальная часть ДПП находится в ПП, максимальное предвозбуждение достигается при стимуляции ПП на меньших частотах, чем ЛП. Предвозбуждение может исчезать при стимуляции левопредсердного коронарного синуса. Степень предвозбуждения комплекса QRS прогрессивно нарастает, а АВ-проведение постепенно замедляется после предсердной ЭС, тем самым указывая на декрементные свойства проведения АВ-шунта.
Имеют место два вида ЭКГ-картины данной формы предвозбуждения на синусовом ритме: одна с “неявным предвозбуждением”, а другая с нормальным интервалом P-R и картиной БЛНПГ с маленькой Δ-волной, искажающей начальную часть комплекса QRS (см. рис. 1). Тахикардия у всех этих пациентов является антидромной АВРТ с медленным и избирательным проводением по ДПП в АВ-направлении и ретроградным ВА-проведением по пучку Гиса и АВ-узлу, или может возникать вследствие сосуществующей АВУРТ с использованием декрементно проводящего ДПП в качестве антероградного “свидетеля”.
В крайне редких случаях АВРТ может использовать декрементно проводящий ДПП в антероградном направлении и другой обычный аномальный АВ-путь в ретроградном направлении. Данные антидромные АВРТ имеют длину цикла в пределах 220-450 мс, ось комплекса QRS от 0 ° до -75 °, ширину комплекса QRS ≤ 150 мс, зубцы R в отведении I, зубцы rS (или QS) в отведении V1 и смещение переходной зоны влево (см. рис. 1). У пациентов с данным синдромом также может развиваться ФП, при которой обычно происходит проведение через ДПП с максимально предвозбужденными комплексами QRS.

Рис. 1. Правые атриофасцикулярные ДПП с “механизмами Махайма”.
А и Б – у двух различных пациентов представлены “неочевидное” (А) и “атипичное” (Б) предвозбуждение во время синусового ритма. ЭКГ в отведении V5 увеличено справа, при этом видно, что интервал P-R на ЭКГ (А) равен 0,24 с, а комплекс QRS узкий. На ЭКГ (Б) интервал P-R равен 0,12 с, а комплекс QRS представляет неполную БЛНПГ с искажением начальной части комплекса (см. фрагмент V5 справа). В обоих случаев у пациентов развивалась тахикардия с широкими комплексами QRS по типу БЛНПГ и отклонением оси влево.
Ретроградное проведение по ДПП обычно отсутствует, хотя был отмечен случай, при котором правосторонний медленно декрементно проводящий ДПП привел к развитию типичной антидромной АВРТ с типичной конфигурацией БЛНПГ и узкой ортодромной АВРТ, а время ВА проведения было удлиненным. Наиболее ранний участок ретроградной активации предсердий при ортодромной АВРТ имел ту же локализацию, где атриофасцикулярный ДПП потенциал был зарегистрирован при синусовом ритме, РЧА в этой области привела к прекращению индукции обеих тахикардий.
Место наиболее ранней активации желудочков при правожелудочковом картировании обычно находится в апикальной трети правой части МЖП. На различном расстоянии от данного очага и по направлению к правостороннему АВ-кольцу на свободной стенке возможно зарегистрировать быстрые “Пуркинье-подобные” отклонения (известные так же как потенциалы Махайма), предшествующие началу комплекса QRS. Картирование проксимального конца ДПП с предсердной стороны ТК может привести к индуцированной катетером блокаде аномального пучка, которая может персистировать в течение нескольких часов даже после инфузии изопреналина.
Лечение
Методом выбора у данных пациентов является РЧА в месте индукции механической блокады ДПП или, что лучше, в локализациях, где зарегистрированы “потенциалы Махайма”. Сегменты ДПП, близкие к его желудочковому выходу, вероятно, ветвятся и являются неподходящими целями для РЧА, так как достигается только временный успех. Воздействие на предсердные концы ДПП часто провоцирует длительно существующий механический блок, что делает процедуру абляции более сложной. Абляцию участков, где “потенциалы Махайма” предшествуют началу максимально предвозбужденного комплекса QRS на ≥ 20 мс, стоит проводить, избегая наиболее проксимальных участков, которые могут быть обрамлены “щитом” из соединительной ткани, и более дистальных, потенциально ветвящихся частей. Абляция данных участков перманентно блокирует ДПП без индукции БПНПГ.
Jerónimo Farré, Hein J.J. Wellens, José M. Rubio и Juan Benezet
Наджелудочковая тахикардия
Опубликовал Константин Моканов
Источник
Преждевременное возбуждение осуществляется по волокнам Махейма, при этом ЭКГ может быть нормальной или изменяться (короткий интервал Р—R или различные аномалии комплекса QRS).
а. Нодожелудочковые волокна: эти пути соединяют АВ область (зоны переходных клеток или компактного узла) с миокардом межжелудочковой перегородки, они образованы специализированной тканью.
б. Гисовые или пучковожелудочковые волокна: они идут от дистальных отделов проводящей системы (пучок Гиса или ножки пучка Гиса) к миокарду желудочков. Эти пути сформированы из специализированной ткани и соответствуют, хотя и не полностью, волокнам, описанным Махеймом, поскольку волокна Махейма соединяют СА узел с желудочком (см. выше). Эти волокна встречаются довольно часто, особенно дистальные, из чего можно заключить, что их функциональное значение зависит не только от их наличия, но и от многочисленных других факторов.
Пучковожелудочковые волокна. Интервал Р—R: в отдельных случаях нормальный, но поскольку он часто взаимосвязан с ускорением АВ проводимости (у 2 из 4 больных в исследовании Garcia-Civera и у всех 6 больных в исследовании Gallagher), интервал Р—R может быть укорочен. По этой причине часто развивается картина, напоминающая классический синдром ВПУ.
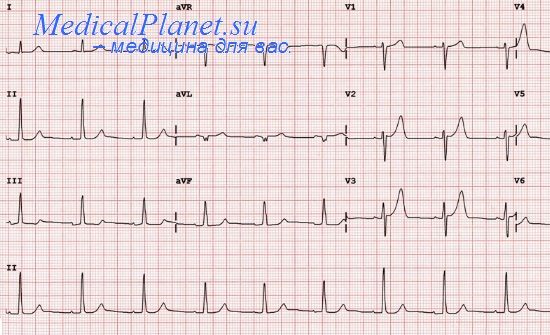
Комплекс QRS: предвозбуждение обычно минимальное (маленькие сигма волны) и комплекс QRS обычно < 0,12 с. Может иметь место блокада правой ножки пучка Гиса или картина неполной блокады левой ножки пучка Гиса, на которую не влияет изменение частоты сердечных сокращений.
Реполяризация обычно меняется мало, потому что степень преждевременного возбуждения обычно невелика.
Преждевременное возбуждение типа Махейма встречается значительно реже, чем классический синдром ВПУ. Прогноз при данном состоянии намного лучше: сообщений о внезапной смерти не обнаружено, хотя у двоих больных с пучковожелудочковыми волокнами в исследовании Gallagher возникала фибрилляция желудочков, возможно, в связи с ускорением АВ проведения. Больные с нодожелудочковыми волокнами могут страдать приступами пароксизмальной тахикардии, что нехарактерно для больных с пучковожелудочковыми волокнами. В противоположность этому у последних иногда встречается трепетание или фибрилляция желудочков вследствие ускорения АВ проводимости. Сообщалось, что нодожелудочковые волокна часто ассоциируются с болезнью Эбштейна (в 3 из 6 случаев в исследовании Gallagher).
Пятьдесят лет тому назад Gere, Levy и Critesco описали электрокардиографическую картину укорочения интервала Р—R при сохранении нормального комплекса QRS. Позже Lown, Ganong и Levine в 1957 г. описали взаимосвязь между коротким интервалом Р—R и наджелудочковой аритмией (синдром LGL). Только электрофизиологическое подтверждение наличия ускорения АВ проводимости делает правомерным диагноз преждевременного возбуждения.
Некоторые случаи преждевременного возбуждения могут быть объяснены наличием вспомогательного предсердногисового пучка типа, описанного Brechenmacher. Эти пути соединяют миокард межпредсердной перегородки с пучком Гиса и образованы сократительными мышечными волокнами. Они встречаются нечасто, и хотя, как было показано, обнаруживаются в некоторых случаях преждевременного возбуждения по типу короткого интервала Р—R, такие предсердногисовые пучки, видимо, не участвуют в генезе аритмий, которые возникают при синдроме LGL.
Учебное видео ЭКГ при синдроме WPW (Вольфа-Паркинсона-Уайта)
– Читать далее “ЭКГ при преждевременном возбуждении желудочков. Ишемическая болезнь сердца”
Оглавление темы “Диагностика синдрома ВПУ и ишемии миокарда”:
1. Реполяризация при преждевременном возбуждении желудочков. Типы преждевременного возбуждения желудочков
2. Дифференциация преждевременного возбуждения желудочков. Спонтанно возникающие изменения конфигурации ЭКГ
3. Взаимосвязь синдрома ВПУ с нарушениями ритма. Синдром ВПУ
4. Прогноз при синдроме Вольфа-Паркинсона-Уайта. Тактика при синдроме ВПУ
5. Характеристика волокон Махейма. Диагностика преждевременного возбуждения желудочков
6. ЭКГ при преждевременном возбуждении желудочков. Ишемическая болезнь сердца
7. ЭКГ при ишемии миокарда. Проявления ишемии на ЭКГ
8. ЭКГ субэндокардиальной ишемии миокарда. Дифференциация ишемии миокарда
9. Субэпикардиальная ишемия миокарда. Диагностика субэпикардиальной ишемии
10. Дифференциация ишемия миокарда. Состояния с признаками ишемии миокарда
Источник
ШИХЕНА СИНДРОМ (H. L. Sheehan, английский эндокринолог и патолог, родился в 1900 году; синоним: болезнь Шихена, послеродовой гипопитуитаризм) — заболевание, развивающееся у женщин после родов, осложнившихся массивным кровотечением, и характеризующееся снижением функции эндокринных желез.
Впервые описан в 1913 году польским патологом Глинским (L. К. Glinski). Подробную характеристику заболевания дал в 1937 году Шихен.
Частота Шихена синдрома, по данным Л. С. Ланецкой и сотрудники (1968), составляет примерно один случай на 28 178 родов. По данным Аарскога (D. Т. Aarskog, 1957), на 10 000 кровотечений во время родов развиваются два клинически выраженных и семь латентных случаев Шихена синдрома. Чаще возникает у многорожавших женщин.
Этиология и патогенез
Возникновение Шихена синдрома связано с ишемическим некрозом передней доли гипофиза (аденогипофиза), развившимся после родов, осложнившихся массивным кровотечением, коллапсом, а у некоторых женщин и сепсисом. Известны случаи Шихена синдрома, возникшего после аборта, сопровождающегося большой кровопотерей.
По мнению Шихена и Мердока (R. Murdoch), во время родов уменьшается поступление крови к функционально-гипертрофированному гипофизу. При выраженных циркуляторных расстройствах, обусловленных острой массивной кровопотерей, наступает спазм или тромбоз сосудов передней доли гипофиза с развитием в ней некроза. Наряду с выраженностью кровопотери для возникновения заболевания имеет значение и преморбидный фон (позднее начало менструаций, небольшие размеры турецкого седла, поздний токсикоз беременных). Так, по данным Д. Ф. Чеботарева, капилляроспазм, имеющий место при позднем токсикозе беременных, приводит к нарушению кровообращения, увеличению проницаемости стенок капилляров, недостаточности питания, уплотнению аргирофильного вещества и некротическим изменениям в тканях печени, почек и особенно в передней доле гипофиза. В настоящее время большое значение в развитии некроза передней доли гипофиза придают внутрисосудистому диссеминированному свертыванию крови (см. Геморрагические диатезы).
По мнению Плаута (A. Plaut), важную роль в развитии Шихена синдрома играет функциональное состояние клеток передней доли гипофиза во время беременности, а именно их повышенная чувствительность к недостатку кислорода и воздействию промежуточных продуктов обмена. Фасбендер (H. Fasbender) придает значение несоответствию между повышенным обменом веществ в передней доле гипофиза во время беременности и родов и недостаточным снабжением ее кислородом из-за массивной кровопотери. Таким образом, условия, предрасполагающие к возникновению нарушения питания передней доли гипофиза, возникают еще во время беременности, а массивная кровопотеря во время родов, аборта или в раннем послеродовом периоде является разрешающим фактором. Имеются сообщения о неблагоприятном влиянии на переднюю долю гипофиза алкалоидов спорыньи и питуитрина, которые применяют для борьбы с маточными кровотечениями. Эти соединения вызывают спазм сосудов гипофиза, что может привести к развитию в нем некроза.
По данным многих исследователей, выраженная клин, картина заболевания развивается в случае поражения более 80% ткани передней доли гипофиза. При меньшем объеме поражения заболевание протекает в стертой (латентной) форме или не возникает совсем, так как неповрежденная часть железы полностью компенсирует функцию органа.
Патологическая анатомия
В ранней стадии обнаруживают ишемические некрозы и тромбы в сосудах, позже — рубцовые изменения и атрофию значительной части передней доли гипофиза. В сохранившихся участках ее паренхимы преобладают базофильные клетки. В задней доле гипофиза отмечается резко выраженное полнокровие. Определяются также полнокровие и отек мягкой оболочки и вещества мозга. Преимущественно в диэнцефальной области наблюдаются резкие циркуляторные расстройства (стаз, отек, периваскулярные кровоизлияния), выраженные дистрофические изменения нервных клеток, очаговая пролиферация клеток глии. Морфологические изменения в периферических органах зависят от тяжести заболевания. Отмечается атрофия яичников, матки, маточных труб, влагалища и наружных половых органов. Щитовидная железа уменьшена в размерах, плотная, на разрезе видны тяжи белесоватой волокнистой ткани. Эпителий фолликулов щитовидной железы уплощен, фолликулы атрофированы, заполнены слабоэозинофильным коллоидом, отмечается разрастание и лимфоидно-клеточная инфильтрация грубоволокнистой соединительной ткани. В надпочечниках также резко выражены явления атрофии, кора их истончена, клетки содержат мало липидов. Поджелудочная железа уменьшена, микроскопически в ней выявляется атрофия островков Лангерганса. Отмечается уменьшение и других органов (сердца, печени, селезенки, почек).
Клиническая картина
Клиническая картина характеризуется симптомами, которые наблюдаются при гипопитуитаризме, возникающем в результате других причин (см. Апитуитаризм, Гипопитуитаризм). Одним из первых симптомов является нарушение лактации — агалактия, реже гиполактия, обусловленное уменьшением и прекращением выделения пролактина (см. Лактация). Наблюдается слабость, сонливость, похудание, выпадение волос. Отмечается атрофия молочных желез, наружных и внутренних половых органов, аменорея (см.), реже — гипоменорея. Развивается гипотиреоз (см.). Прекращение выделения АКТ Г приводит к частичной атрофии коры надпочечников, снижению выработки ею гормонов, главным образом глюкокортикоидов, в результате которого может развиться острая надпочечниковая недостаточность (см. Надпочечники).
Опасным осложнением Шихена синдрома является гипопитуитарная кома (см.), которая может возникнуть на ранних стадиях заболевания. Причины комы при Шихена синдроме окончательно не установлены. По-видимому, основное значение имеет некроз передней доли гипофиза, а также биохимические изменения в клетках центральной нервной системы, мозговая аноксия, гипогликемия. Провоцирующими факторами могут стать оперативные вмешательства и инфекции. Коме могут предшествовать сонливость, адинамия, рвота, озноб, профузный пот, судороги. При гипопитуитарной коме отмечается замедление пульса, резкое снижение АД, и чаще всего она заканчивается гибелью больной.
Диагноз
Несмотря на характерную клиническую картину, появляющуюся вскоре после родов, Шихена синдром диагностируется, как правило, через несколько месяцев, а иногда через несколько лет после начала заболевания, когда появляются тяжелые симптомы болезни, связанные с недостаточностью функции щитовидной железы, надпочечников и половых желез. Так, по данным С. Б. Ханиной и сотр. (1967), в 90% наблюдений диагноз ставится не ранее чем через два года, а в 70% — через пять лет и более от начала заболевания. Важное значение для диагностики Шихена синдрома имеют указания на острую массивную кровопотерю во время родоразрешения. При лабораторном исследовании отмечается снижение экскреции гонадотропинов и половых стероидов, а также 17-кетостероидов (17-КС) и 17-оксикортико-стероидов (17-ОКС), уменьшается поглощение радиоактивного йода щитовидной железой (см.). Большое значение при диагностике придается определению функционального состояния гипофиза с помощью пробы с метопироном (см.). При лаб. исследовании определяется гипохромная анемия, ускорение РОЭ, лейкопения, нейтрофилез, снижение уровня сахара в крови. На ЭКГ определяются признаки диффузной гипоксии миокарда (снижение вольтажа, сглаженность зубца Т). Данные электроэнцефалографического исследования свидетельствуют о преобладании процессов торможения в коре головного мозга. Для выявления атрофии матки производят гистеросальпингографию (см. Метросальпингография), пневмопельвиографию и ультразвуковое сканирование.
Дифференциальную диагностику чаще проводят с опухолью гипофиза (см. Гипофиз), первичным гипотиреозом (см.), аддисоновой болезнью (см.). Об опухоли гипофиза свидетельствует отсутствие указаний на кровотечения в родах, данные рентгенологического исследования и появление нейроофтальмологических нарушений. При первичном гипотиреозе отсутствуют признаки поражения других эндокринных органов, отмечается улучшение при лечении тиреоидными гормонами. При дифференциальной диагностике Шихена синдрома с аддисоновой болезнью учитывают анамнестические данные (отсутствие кровотечений в родах), усиленную гиперпигментацию кожи и слизистых оболочек.
Лечение
Лечение включает заместительную терапию и проводится в течение всей жизни больных. Назначают кортикостероиды (кортизон, гидрокортизон, преднизолон, дексаметазон) повторными прерывистыми курсами с интервалами в 3—4 месяца и дополнительно в периоды эпидемий гриппа, повышенной нервной и физической нагрузки; половые гормоны (эстрогены и гестагены), по показаниям — тиреоидин. При гипопитуитарной коме внутривенно вводят 100—300 мг гидрокортизона гемисукцината (или 100—200 мг преднизолона гемисукцината), 500—1000 мл изотонического раствора хлорида натрия, по показаниям — мезатон, норадреналин, применяют гипербарическую оксигенацию (см.).
Прогноз
Своевременно начатая рациональная терапия позволяет в ряде случаев восстановить трудоспособность (чаще — не полностью), а иногда и репродуктивную функцию. Поздняя диагностика и несвоевременно начатое лечение приводят к утрате трудоспособности и инвалидности. Больные могут погибнуть от гипопитуитарной комы и острой надпочечниковой недостаточности, а также от осложнений, присоединяющихся вследствие резкого снижения сопротивляемости организма к инфекции.
Профилактика
Профилактика сводится к своевременному лечению генитального инфантилизма и нормализации менструального цикла, предупреждению кровотечений во время родов и раннем послеродовом периоде (восстановление коагуляционных свойств крови, повышение сократительной способности матки во время родов); к своевременному и адекватному возмещению острой массивной кровопотери (лучше свежестабилизированной кровью), восстановлению реологических свойств крови, своевременному выведению больной из коллаптоидного состояния, а также к предупреждению и интенсивному лечению инфекционных осложнений в послеродовом периоде.
См. также Гипофизарная кахексия.
Библиогр.: Кантер X. и Гросс Ю.,Синдром Шихена, Клин, мед., т. 43, № 6, с. 21, 1965; Ланецкая Л. С., Толстых А. С. и Степанова Н. М.. Некоторые вопросы клиники и лечения синдрома Шихена, Пробл. эндокрин., т. 14, № 1, с. 12, 1968; Лихт Л. Л. и Неймарк Е. 3. Клиника и патологическая анатомия синдрома Шихена, Клин, мед., т. 43, Кя6, с. 143, 1965; Паша С. П. Этиология и патогенез синдрома Шихана, Акуш. и гинек., № 5, с. 20, 1972; Плешков А. М. и Успенская К. Ф. К вопросу о послеродовом гипопитуитаризме или болезни Шихена, Тер. арх., т. 40, № 6, с. 112, 1968; Серов В. Н. Послеродовые нейроэндокринные заболевания, М., 1978; Ханина С. Б., Чудиновских А. Я. и Мельникова А. Е. О клинике и лечении ранней стадии синдрома Шихана, Тер. арх., т. 39, № 4,с. 100, 1967; Chryssikopulos А., а. о. Sheehan-Syndrom und Graviditat, Geburtsh. u. Frauenheilk., Bd 34, S. 121, 1974; G-r i m e s H. G. a. Brooks М. H. Pregnancy in Sheehan’s syndrome, Obstet, gynec. Surv., v. 35, p. 481, 1980; Husslein H. u. Stoger H. Klinik und Therapie des Sheehan-Synd-roms, Wien. klin. Wschr., S. 489, 1974; Shanmanesh M. a. o. Pituitary function tests in Sheehan’s syndrome, Clin. Endocr., v. 12, p. 303, 1980; S h e e-h a n H. L. The repair of post-partum necrosis of the anterior lobe of the pituitary gland, Acta endocr, (Kbh.), v. 48, p. 40, 1965.
В. П. Баскаков.
Источник
