Синдром нарушения внутрисердечной гемодинамики это
Выраженная ГЛЖ и уменьшение размеров его полости
Выброс снижается,а приток нормальный.
Диастолическая дисфункция ЛЖ
– Возрастание КДД в ЛЖ
– Повышение давления в ЛП и венах МК КО
– Расширение ЛП
– Застой крови в МК КО, дилатация
Классификация клинических вариантов.
ХСН (левожелудочковая) одышка
Гипоксия головного мозга- головокружение ,обмороки
Нарушения ритма и проводимости
Стенокардия- гипертрофия,увеличение потребности в кислороде
Внезапная сердечная смерть
Осложнения.аритмии, диастолическая сердечная недостаточность, тромбоэмболии при фибрилляции предсердий, инфаркт миокарда, инсульт, внезапная смерть
Диагностика и дифференциальный диагноз.
Шум более на верхушке,может иррадиировать в подмыш.обл
ЭКГ(гипертрофия лев.желуд),ЭХО(гипертрофия,степень выраженности,наличие обструкции)
ДИФ,с пороками сердца, сопровождающимися систолическим шумом, обструктивную форму ГКМП. У больных с очаговыми и ишемическими изменениями на ЭКГ и (или) ангинозной болью первостепенной задачей является дифференциальная диагностика с ИБС.
Лечение.
Ограничение физических нагрузок
Верапамил(120-360мг.сут)-уменьшают чсс и удлиняют диастолу
Aнтикоагулянты
Хирургические методы (миоэктомия, протезирование митрального клапана, имплантация ЭКС )
Прогноз.Перход в дилатационную. Осложнение инф.эндокардитом.
Дилатационная кардиомиопатия
-первичное поражение сердца,характеризующееся расширением его полостей и нарушением сократительной функции
Патогенез нарушений внутрисердечной гемодинамики.
Под действием экзогенных факторов,уменьшается количество полноценных функциониров.кардиомиоцитов—-расширение камер—дисфункция обоих желудочков—ХСН
Уменьшается минутный и ударный объем,увеличивается КДД в ЛЖ,происходит дальнейшее расширение полости.Возникает относительная недостаточность митр.и трехстворч.клапана из-за расширения желудочков и колец. Гипертрофия,тромбы
Клиника.
ХСН (левожелудочковая или бивентрикулярная недостаточность)-одышка,слабость,утомляемость,сердцебиение,периф.отёки
Нарушения ритма и проводимости(парокс.мерц.аритмия,фибрилляция предсердий)
Тромбоэмболии артерий БК КО и ТЭЛА
Диагностика. ЭКГ
ЭХО-КС(дилятация с уменьшением выброса ЛЖ)
Рентгенография (увеличение разсеров сердца,гидроперикард)
Коронарография(исключает стенозирующие поражения артерий)
Вентрикулография
Дифференциальный диагноз.
ИБС,АГ,микседема,системные заболевания
Лечение.
Малосолевая диета
Ингибиторы АПФ
Диуретики
Сердечные гликозиды(дигоксин 0,25-0,3мг.сут)
Антиагреганты(аспирин)
Трансплантация сердца
Прогноз.(неблагоприятный)
ХСН 4 ФК
КДР больше 7,6 см
Фракция Выброса менее 35%
Возникновение полной блокады ЛНПГ
Наличие желудочковых аритмий 3 класса и выше по Лауну
Постоянная форма МА
Миокардиты.
это очаговое или диффузное воспаление сердечной мышцы, сопровождающееся ее дисфункцией
Этиология.
Инфекционные (инфекционно-токсические Стрептококки,вирусы)
Аутоиммунные (иммунопатологические,СКВ,ЛС,трансплантации)
Токсико-аллергические(алкоголь,наркотики)
Патогенез.Воспалит.реакция—инфильтрация лекоцитами,отложение Ig,комплемента,повреждение эндотелия капилляров,возможна дистрофия.
Классификация.
Распространенность (очаговый, диффузный)
Клиническое течение (острый, подострый, латентный, рецидивирующий)
Характер воспаления
n Альтеративный (дистрофически-некробиотический)
n Экссудативно-пролиферативный (интерстициальный)
Клинические синдромы.
Болевой синдром
Сердечная недостаточность(одышка,слабость,сердцебиение)
Интоксикация
Нарушение ритма и проводимости
Диагностические критерии.
Анамнестическая хронологическая связь с предполагаемым этиологическим фактором
Общевоспалительный синдром
Лабораторные признаки повреждения кардиомиоцитов
Нарушение функций сердца
Изменения на ЭКГ
Кардиалгия
Признаки воспаления миокарда (биопсия, МРТ, РИТ)
Дифференциальный диагноз.
При выраженной кардиомегалии и ХСН с ДКМП
При болях, локализующихся за грудиной и повышении КФК-МВ и Тропонина с острым инфарктом миокарда
Лечение.
Ограничение физ.нагрузки
При выявлении этиологии(При инфекционных невирусных миокардитах – антибиотики. )
НПВС, ГК?
Лечение сердечной недостаточности, нарушений ритма сердца и проводимости, тромбоэмболических осложнений
Прогноз.Самостоятельно проходит при легком течении,или переходит в хроническую форму,блокады
Перикардит.
это инфекционное или асептическое воспаление висцерального и париетального листков перикарда.
Классификация
I. Клиническая классификация
А. Острые перикардиты (менее 6 нед)
1. Фибринозный (сухой)
2. Выпотной (или геморрагический) Б. Подострые перикардиты (от 6 нед до 6 мес)
1. Констриктивный (сдавливающий)
2. Констриктивно-выпотной
В. Хронические перикардиты (более 6 мес)
1. Констриктивный
2. Выпотной
3. Адгезивный (неконстриктивный) слипчивый
II. Этиологическая классификация
А. Инфекционные перикардиты
Б. Неинфекционные перикардиты (ИМ,опухоль,метастазы,травма,ревматоид.артрит,СКВ)
Клинические синдромы.
Боли в области сердца
Постоянный, однообразный характер
Связь с положением тела
n Связь с дыханием и кашлем
n Отсутствие эффекта от нитратов
Воспалительный синдром
Шум трения перикарда
n Выслушивается в зоне абсолютной тупости
n Непостоянный
n Усиливается при наклоне вперед, на выдохе
Диагностика.Эхо(жидкость в полости перикарда),рентген(кардиомегалия),исследование перикардиальной жидкости(опухоль,бактерии,белок)
Дифференциальный диагноз.
Лечение.Госпитализация и динамическое наблюдение за гемодинамикой
Ограничение физической активности
НПВС(преднизолон 60мг.сут в теч.5-7 дней
ГКС (при интенсивном болевом синдроме, аутоиммунном характере)
Перикардиоцентез(при неэффективности)
Субтотальная перикардэктомия (при констриктивном перикардите)
14)Врожденные пороки:
Дефект межпредсердной перегородки-наличие сообщения между левым и правым предсердиями,приводящее к патологическому сбросу(шунтированию) крови из одной камеры сердца в другую.
Сброс крови из ЛП в ПП, Объемная перегрузка ПП и ПЖ……Легочная гипертензия
Жалобы:одышка, сердцебиение, быстрая утомляемость при физической нагрузке, отставание в физическом развитии, частые инфекции
Осмотр:цианоз,барабанные палочки,часовые стеклышки(сброс справа на лево)
Пальпация:пульсация легочной артерии(при лег.гипертензии) во 2м межреберье слева от грудины.
Аускультация:2й тон расщеплен,шум над трехстворчатым
ЭКГ: нарушение ритма в виденаджелудочковых аритмий,фибрилляции предсердий
Рентген,ЭХО:дилятация правого предсердия и правого желудочка
Лечение: при выраженной легочной гипертензии-пластика. При СН-серд.гликозиды,диуретики,иАПФ
Показания к хир.лечению:
– отношение Qp/Qs составляет 1,5 и более,
– дефекты типа ostium primum,
– крупные дефекты типа ostium secundum,
сопутствующие гемодинамически значимые аномалии (аномальный дренаж лёгочных вен, митральный стеноз и пр.).
При своевременной операции благоприятный
Дефект межжелудочковой перегородки-наличие сообщения между левым и правым желудочками,приводящие к сбросу из одной камеры в другую.
При сбросе слева направо и отношении лёгочного минутного объёма кровотока к системному (Qp/Qs) менее 1,5:1 лёгочный кровоток возрастает незначительно, и повышения ОЛСС не происходит
По мере увеличения ОЛСС возможно изменение направления сброса крови — он начинает происходить справа налево.
Без лечения развиваются правожелудочковая и левожелудочковая недостаточность и необратимые изменения лёгочных сосудов (синдром Айзенменгера)
Жалобы = ДМПП
Объективно:
Бледность кожных покровов
Усиление верхушечного толчка, дрожание в области левого нижнего края грудины
Патологическое расщепление II тона в результате удлинения периода изгнания правого желудочка
Грубый пансистолический шум у левого нижнего края грудины
ЭХО-КС:
Гипертрофия и дилатация левых отделов, а при лёгочной гипертензии — и правых
Визуализация ДМЖП в допплеровском и В-режиме
Определяют систолическое давление в правом желудочке, степень сброса крови и Qp/Qs
Взрослым проводят чреспищеводную ЭхоКГ
Рентген: При лёгочной гипертензии — выбухание дуги лёгочной артерии
Показания:
– При бессимптомном течении — если к 3–5 годам жизни не происходит самопроизвольного закрытия дефекта, хотя лучших результатов достигают при оперативном лечении в возрасте до 1 года
– Сердечная недостаточность или лёгочная гипертензия у детей младшего возраста
– У взрослых отношение Qp/Qs составляет 1,5 и более.
Рекомендуемые страницы:
Воспользуйтесь поиском по сайту:
Источник
Нарушения гемодинамики при пороках сердца и физической нагрузке
а) Изменения гемодинамики при физической нагрузке у больных с пороками клапанов сердца. При физической нагрузке большое количество венозной крови поступает к сердцу из периферических сосудов. Следовательно, все патологические сдвиги гемодинамики, которые характерны для разных типов поражения клапанов, усиливаются многократно. Даже нетяжелые пороки, которые никак не проявляются в состоянии покоя, при физической нагрузке приводят к развитию выраженной симптоматики. Например, у больных с поражением аортальных клапанов физическая нагрузка может вызвать острую недостаточность левого желудочка с последующим отеком легких. У больных с митральным пороком физическая нагрузка может вызвать тяжелый застой крови в легких, в результате в течение 10 мин может развиться смертельный отек легких.
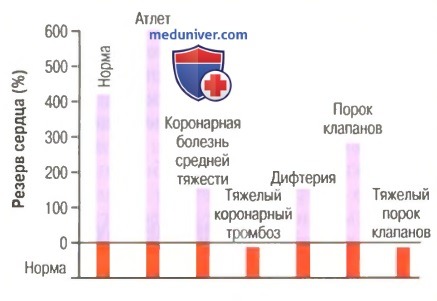
Даже умеренная степень того или иного повреждения клапана приводит к уменьшению резерва сердца пропорционально тяжести дисфункции клапанной системы. Это значит, что сердечный выброс не может увеличиваться в той мере, в какой требуется для выполнения физической нагрузки. Утомление развивается слишком быстро, т.к. скелетные мышцы страдают от недостаточного кровоснабжения.

Резерв сердца в различных условиях (в двух случаях резерв сердца меньше нуля)
б) Нарушения гемодинамики при врожденных пороках сердца. В процессе внутриутробного развития может нарушиться правильное формирование сердца и связанных с ним сосудов. Подобные дефекты называют врожденными аномалиями, или врожденными пороками сердца. Встречаются три основных типа врожденных пороков сердца и крупных сосудов:
(1) стеноз тех или иных путей кровотока в сердце или в крупных сосудах;
(2) аномалии, которые допускают ток крови из левых отделов сердца или аорты в правые отделы сердца или легочную артерию, что приводит к недостаточности системного кровообращения (так называемый сброс слева направо);
(3) аномалии, которые допускают ток крови прямо из правых отделов сердца в левые отделы сердца, что приводит к недостаточности легочного кровообращения (так называемый сброс справа налево).
Изменения гемодинамики, возникшие в результате стеноза той или иной локализации, понять довольно легко. Например, врожденный стеноз аортальных клапанов приводит к тем же изменениям, что и приобретенный стеноз, а именно к развитию отека легких и уменьшению сердечного выброса.
Другим примером врожденного стеноза является коарктация аорты, которая часто локализуется на уровне диафрагмы. При этом артериальное давление в верхней части туловища (выше уровня коарктации) становится гораздо выше, чем давление в нижней части туловища. Причиной этого является высокое сопротивление кровотоку в области коарктации; кроме того, часть крови должна протекать по мелким коллатеральным сосудам, минуя место сужения.
– Также рекомендуем “Открытый артериальный проток. Гемодинамика при открытом Боталловом протоке”
Оглавление темы “Пороки сердца. Циркуляторный шок”:
1. Недостаточность левого желудочка. Гемодинамика при митральном стенозе и митральной недостаточности
2. Нарушения гемодинамики при пороках сердца и физической нагрузке
3. Открытый артериальный проток. Гемодинамика при открытом Боталловом протоке
4. Тетрада Фалло. Гемодинамика при тетраде Фалло
5. Искусственное кровообращение. Гипертрофия миокарда при врожденных пороках
6. Циркуляторный шок. Причины циркуляторного шока
7. Стадии шока. Гиповолемический шок
8. Геморрагический шок. Непрогрессирующий геморрагический шок
9. Прогрессирующий геморрагический шок. Порочный круг прогрессирующего шока
10. Генерализованное поражение клеток при шоке. Ацидоз при шоке и некрозы тканей
Источник
Рассмотрим теперь, какие изменения миокарда и внутрисердечной гемодинамики приводят к развитию синдрома ХСН.
Ранее мы уже упоминали мнение нашего учителя A. Л. Мясникова, который не сомневался, что главнейшей причиной СН является снижение сократительной способности миокарда. Такая же точка зрения высказывалась на страницах учебников и руководств по диагностике, принадлежащих перу других отечественных клиницистов.
Строго говоря, всегда признавалось существование такого варианта ХСН, когда в ее основе лежит первичное нарушение диастолической функции желудочков сердца. Однако это считалось возможным при относительно редко встречающейся патологии, когда способность сердечных камер расширяться и вмещать в себя необходимое количество крови резко ограничивается или избыточной гипертрофией миокарда (аортальные пороки сердца, гипертрофическая кардиомиопатия), или давлением снаружи (экссудативный или констриктивный перикардит), или уменьшением объема желудочка за счет реетриктивного процесса (рестриктивные кардиомиопатии). Что же касается основной массы сердечных заболеваний (ИБС, артериальная гипертензия, дилатационная кардиомиопатия), то оказалась непреложной ведущая роль снижения систолической функции ЛЖ в патогенезе ХСН, вызываемой ими.
Но сегодня СН не может больше определяться как болезнь недостаточного выброса крови желудочками. В большей степени она должна пониматься как следствие процесса прогрессирующих изменений структуры и объема желудочков, клеточных изменений их стенок и структуры сосудов, в которые осуществляется выброс крови.
Создание новых методов исследования, позволяющих достоверно прижизненно судить о состоянии систолической и диастолической функций ЛЖ (прежде всего, ЭхоКГ, допплеровской ЭхоКГ, радионуклидной вентрикулографии), в корне изменило прежние представления. Ныне нарушению диастолического наполнения сердца отводится не меньшая, а возможно, даже большая роль в патогенезе ХСН, чем систолическим расстройством опорожнения желудочков.
В 1983 г. Echeverria и соавт. установили, что у 40 % из 50 больных с ХСН ФВ ЛЖ — наиболее популярный, высокоточный и хорошо воспроизводимый показатель его сократительной (систолической) функции — оказалась нормальной. Близкие данные о частоте нормальной систолической функции ЛЖ (36 % из 188 и 42 % из 74 наблюдавшихся) у больных с клиническими признаками ХСН получили вскоре Douqerhy и Soufer. В последующие годы (1988—2000) было проведено более 20 аналогичных исследований, в которых частота нормальной ФВ колебалась от 13 до 100 %, а средняя ее частота, по данным обследования более 5 тыс. больных с ХСН, составила 37 %. Таким образом, по крайней мере от 25 до 30 % больных с ХСН страдают диастолической дисфункцией при сохранной систолической функции сердца.
Напомним, что диастолической дисфункцией называется неспособность желудочка заполниться во время диастолы объемом крови, достаточным для поддержания адекватного СВ при нормальном среднем давлении в легочных венах, т. е. < 12 мм рт. ст. Как известно, диастолическое наполнение ЛЖ протекает в две фазы: фазу быстрого (активного) наполнения и фазу медленного (пассивного) наполнения, которая заканчивается систолой предсердий. Вклад систолы предсердий в СВ при нормальном синусовом ритме и отсутствии нарушений диастолического расслабления желудочков составляет не более 25 % и не считается в нормальных условиях очень значительным.
Расслабление миокарда в раннюю фазу происходит за счет актин-миозиновой диссоциации (ее активная, энергозависимая часть) и растяжения эластических структур, сжатых во время систолы. Актин-миозиновая диссоциация обеспечивается работой трансмембранного и саркоплазматического кальциевого насоса (Са2+— АТФаза) и требует значительного количества свободных макроэргических фосфатов. Это обстоятельство делает раннюю диастолу наиболее «уязвимой мишенью при любом заболевании, сопровождающемся энергодефицитом, особенно при ишемии миокарда». Считается поэтому, что нарушение диастолической функции при миокардиальных поражениях сердца обычно предшествует нарушению систолической функции и на ранних доклинических стадиях ХСН сочетается с нормальной сократительной функцией. Ю. Н. Беленков и соавт. полагают, что «если диастолическая дисфункция может существовать без видимых систолических расстройств, то систолическая дисфункция всегда возникает на фоне нарушенной диастолической функции».
В фазу медленного (пассивного) наполнения поступление крови в желудочек определяется прежде всего жесткостью его камеры, податливостью его стенок к растяжению и зависит от гипертрофии миокарда, степени его фиброзирования и ишемизации, а при артериальной гипертензии — также от возрастания постнагрузки на желудочек.
В эволюции ХСН можно условно выделить три стадии. На I стадии нарушение процессов активного расслабления и раннего наполнения желудочка компенсировано активностью предсердия и не приводит к появлению признаков СН. При прогрессировании заболевания, дальнейшем повышении жесткости миокарда повышается давление в предсердии и легочных венах, что снижает толерантность к нагрузкам. Появляются начальные признаки ХСН, обычно выявляемые нагрузочными тестами. Наконец, в III стадии уже наблюдается критическое уменьшение притока крови в желудочек. При этом возникает застой крови в легких, одышка при небольших нагрузках, снижается СВ. Таким образом, первоначально бессимптомная диастолическая дисфункция эволюционирует в застойную ХСН.
Изолированная диастолическая ХСН при сохранной систолической функции сердца чаще наблюдается у женщин пожилого возраста (старше 65—70 лет) с относительно небольшой кардиомегалией, обычно страдающих артериальной гипертензией. Предрасполагающими к ее развитию факторами считаются сахарный диабет, выраженное ожирение, аортальные пороки сердца, ХПН.
Систолическая и диастолическая дисфункции желудочка имеют, по современным представлениям, несколько разное значение. Так, систолическая дисфункция и ее ЭхоКГ-маркер — ФВ ЛЖ — играют роль независимого предиктора прогноза больных ХСН, могут быть использованы для оценки эффективности лечения. Кроме того, ФВ — надежный маркер повреждения миокарда и используется для оценки сократимости при определении риска оперативного вмешательства на сердце. В то же время, как установлено, именно диастолические расстройства ответственны за тяжесть декомпенсации сердечной деятельности и выраженность клинических проявлений ХСН. Диастолические маркеры точнее и надежнее систолических в оценке функционального резерва миокарда, качества жизни и эффективности терапевтических мероприятий. Используются они и при определении прогноза ХСН. К. Weber и С. Brilla показали, что в нормальном миокарде контрактильные клетки-миоциты составляют лишь 1/3 от общего числа клеточных структур, хотя и занимают до 70 % объема миокардиального пространства. Остальные же 2/3 несократимых клеток миокарда представлены фибробластами, гладкомышечными клетками сосудов, клетками эндотелия и свободными клетками соединительной ткани. Кроме самих клеток, массу миокарда в определенной степени определяют внеклеточные субстанции, среди которых выделяют коллаген, эластин и др. Наши исследования, показавшие практическую независимость сократительной функции миокарда (которая может страдать в результате гибели миокардиоцитов) от диастолической, определяющейся выраженностью разрастания несократимых клеток сердца и неклеточных структур, позволяют сделать заключение, что общая группа больных с ХСН оказывается разнообразной по характеру изменений внутрисердечной гемодинамики. В настоящее время вполне реально подразделять больных, имеющих клиническую симптоматику ХСН, на подгруппы с сохранной ФВ — диастолическую СН, и нарушенной ФВ (среди них могут быть лица как с нарушенной диастолической функцией, так и с нормальными ее параметрами).
Определенную роль в развитии ХСН наряду с перечислявшимися механизмами, вызывающими развитие тех или иных клинических проявлений, играет генетическая предрасположенность. Полагают, что в то время как гемодинамические и нейрогормональные факторы играют главную роль в определении прогноза течения заболевания, генетические факторы особенно важны при определении исхода заболевания. Высказываются надежды на то, что в будущем на основании изучения специфического фенотипа больного будет идентифицироваться возможность внезапной смерти. Основанием для этого стало открытие полиморфизма β-адрено-рецепторов, при котором различие структуры рецептора лишь на одну аминокислоту может существенно изменять благоприятный прогноз на неблагоприятный.
Мы полагаем, что выделение ведущего патогенетического фактора станет в ближайшем будущем одним из принципов классифицирования СН.
Источник
