Синдром острой токсической печеночной недостаточности
ОТВЕТЫ ПО КЛИНИЧЕСКОЙ ПАТФИЗИОЛОГИИ
Респираторный дистресс-синдром у взрослых.
РДСВ (пример острой дыхательной недостаточности) – полиэтилогическое состояние, характеризующееся острым началом, выраженной гипоксемией (не устраняемой оксигенотерапией), интерстициальным отеком и диффузной инфильтрацией легких.
Этиологическими факторами РДСВ являются: шоковые состояния, множественные травмы (включая ожоговые), ДВС-синдром (синдром диссеминированного внутрисосудистого свертывания крови), сепсис, аспирация желудочным содержимым при утоплении и вдыхании токсических газов (включая чистый кислород), острые заболевания и повреждения легких (тотальная пневмония, контузии), атипичная пневмония, острый панкреатит, перитонит, инфаркт миокарда и др. Многообразие этиологических факторов РДСВ отражается во множестве синонимов: синдром шокового легкого, синдром влажных легких, травматическое легкое, синдром легочных нарушений у взрослых, синдром перфузионного легкого и др.
В развитии РДС выделяют несколько стадий:
I стадия — повреждение эндотелия. При различных критических состояниях (шок, эндотоксинемия, ДВС-синдром) происходит нарушение микроциркуляции в легких, повышение концентрации биологически-активных веществ, с развитием массивного диффузного повреждения эндотелия и базальной мембраны капилляров легких и увеличением проницаемости сосудистой стенки.
Клинические проявления в этой стадии, как правило, отсутствуют. Продолжительность стадии — до 6 часов.
II стадия — интерстициальный отек. В условиях повышения проницаемости эндотелия в интерстициальное пространство перемещается вода, электролиты, белки и форменные элементы крови даже без существенных изменений гидростатического и коллоидно-осмотического давления.
Клиническая картина характеризуется появлением одышки (>20 в мин), тахикардии; аускультативно в легких выслушивается жесткое дыхание, сухие хрипы; начинает снижаться рО2 (<50 мм рт. ст.) параллельно с развитием гипокапнии. Алкалоз, характерный для начальной стадии РДС купируется, но на фоне гипоксии развивается внутриклеточный метаболический ацидоз.
III стадия — повреждение клеток альвеолярного эпителия. Вначале происходит повреждение клеток альвеолярного эпителия, более чувствительных к гипоксии — пневмоцитов 1 порядка. Более устойчивые пневмоциты 2 порядка не разрушаются, а пролиферируют и частично замешают клетки 1 порядка. Нарушается синтез сурфактанта в легких.
В клинике нарастают явления дыхательной недостаточности: одышка, гиперпноэ, тахикардия, цианоз, бронхиальное дыхание и влажные хрипы в легких. Мокрота скудная или вообще отсутствует, в отличие от «сердечного» отека легких. В этой стадии развивается респираторный и метаболический ацидоз, повышается РаСО2.
IV стадия — альвеолярный отек. При дальнейшем нарушении проницаемости транссудат проникает в альвеолы и затопляет их. Кроме воды отечная жидкость содержит фибриноген, форменные элементы крови, разрушенные пневмоциты.
Синдром острой токсической печеночной недостаточности.
Гепатотоксические вещества-ксенобиотики:
• промышленные яды (производные бензола, свинца, ртути, толуола, фосфорорганические соединения, хлороформ, четыреххлористый углерод, кислоты, нитрокраски, щелочи и др.);
• лекарственные препараты (антибиотики, сульфаниламиды, наркотические, снотворные и противовоспалительные средства – бруфен, индометацин, парацетамол и др.);
• грибной яд – фаллоидин, фаллоин, содержащийся в бледной поганке;
• афлатоксины (плесневые грибы);
• красители, бытовые химические вещества;
Механизм повреждения гепатоцитов токсическими агентами.Токсические агенты могут оказывать прямое повреждающее действие на печень, в результате чего развиваются дистрофические изменения вплоть до необратимого некроза (яд бледной поганки). Ряд ксенобиотиков сами не вызывают некроза гепатоцитов, но в организме могут подвергаться биотрансформации с образованием метаболитов, оказывающих повреждающий эффект (тетрациклин, салицилаты, этанол). Так, основным метаболитом этанола является ацетальдегид (85% этанола превращается в ацетальдегид под влиянием цитозольного фермента алкогольдегидрогеназы).
Ацетальдегид – химически активная молекула, способная связываться с альбумином, гемоглобином, тубулином, актином и др., формируя таким образом соединения, которые способны сохраняться в ткани печени длительный период даже после завершения метаболизма этанола. Связь ацетальдегида с белками цитоскелета может приводить к необратимым клеточным повреждениям, нарушая секрецию белка и способствуя формированию баллонной дистрофии гепатоцитов (задержка белков и воды).
Кроме того, в механизме повреждения гепатоцитов под влиянием этанола выделяют следующие основные эффекты:
1. Усиление перекисного окисления липидов вызывает повреждение клеточных мембран, приводящее к повышению их проницаемости и как следствие нарушению трансмембранного транспорта, клеточных рецепторов, мембраносвязанных ферментов.
2. Нарушение функций митохондрий (хроническое употребление алкоголя снижает активность митохондриальных ферментов, возникает разобщение окисления и фосфорилирования, что сопровождается снижением синтеза АТФ).
3. Подавление репарации ДНК в клетках и активация апоптоза.
4. Активация системы комплемента и стимуляция продукции супероксида нейтрофилами и т.д.
В ряде случаев играют роль иммунные механизмы, которые включаются в том случае, если лекарства или метаболиты, выступая в качестве гаптенов, превращают белки гепатоцита в иммуногены.
При истинной печеночно-клеточной недостаточности развиваются следующие синдромы:
1) синдром нарушенного питания (ухудшение аппетита, тошнота, боли в животе, неустойчивый стул, похудание, появление анемии). В основе этого синдрома лежат нарушения обменных процессов;
2) синдром лихорадки (до 38 °С и даже до 40 °С) с ядерным сдвигом лейкоцитарной формулы влево. Этот синдром связан с некрозами гепатоцитов, поступлением токсических продуктов в кровь, бактериемией (возможно поступление микроорганизмов в кровь из кишечника);
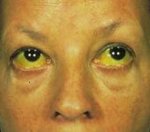
3) синдром желтухи;
4) синдром эндокринных расстройств. Отмечаются снижение либидо, атрофия яичек, бесплодие, гинекомастия, атрофия молочных желез, матки, нарушение менструального цикла. Возможно развитие сахарного диабета и вторичного альдостеронизма;
5) синдром нарушенной гемодинамики – накопление гистаминоподобных и других вазоактивных веществ, приводящее к вазодилатации (компенсаторное повышение сердечного выброса в сочетании с гипотензией). Снижение синтеза альбуминов и падение онкотического давления, а также развитие вторичного гиперальдостеронизма обусловливают отечно-асцитический синдром (см. раздел 18.1.3);
6) специфический печеночный запах (fetor hepaticis) связан с выделением метилмеркаптана. Это вещество образуется из метионина, который накапливается в связи с нарушением в печени процессов деметилирования и может содержаться в выдыхаемом воздухе;
7) «печеночные знаки» – телеангиэктазии и пальмарная эритема;
8) синдром геморрагического диатеза – снижение синтеза факторов свертывания крови и частые кровотечения обусловливают возможность развития ДВС-синдрома.
Печеночную недостаточность характеризуют следующие лабораторные показатели: в сыворотке крови уменьшается содержание альбумина (чрезвычайно важный показатель!) и факторов свертывания, снижается уровень холестерина, нарастает содержание билирубина, отмечается накопление фенола, аммиака и повышение активности аминотрансфераз.
Печеночная недостаточность может привести к развитию печеночной энцефалопатии и печеночным комам.
Интенсивная терапия при явлениях печеночной недостаточности должна быть направлена на устранение этиологического фактора, восстановления функции печеночных клеток, снижения активности кишечной флоры.
1. Диета. Ограничение жиров, белков. Потребности организма в энергии удовлетворяют за счет углеводов.
2. Восстановление обменных процессов в гепатоците достигается путем:
· оксигенотерапии;
· повышения уровня гликогена в гепатоцитах в/в введением 10-40% раствора глюкозы с инсулином (1ЕД на 4 гр глюкозы), в дозе 4-6 гр/кг/сут;
· стабилизации клеточных мембран применением гепатопротекторов (эссенциале), ингибиторов протеолетических ферментов (контрикал 100 тыс ЕД/сут);
· применения антиоксидантов : аскорбиновая кислота 5% 5мл в/в 3-4 раза в день, токоферола ацетат 1-2 мл в/м, унитиол 10-20 мл в/в; рибоксин 2% 10 мл в/в;
· применения антигипоксантов: ГОМК 20% – 50-60 мг/кг в/в, пирацетам по 10 мл в/в 3-4 раза в сутки, цитохром С 5мл в/м, дроперидол 0,25% 5-10 мг в/в, реланиум 0,5% – 10-20 мг в/м или в/в.
· ликвидации отека гепатоцитов: лазикс 1-2 мг/кг стартовая разовая доза, при неэффективности увеличить, эуфиллин 2,4% -0,6 мг/кг/час.
3. Улучшение обменных процессов в печени осуществляется введением витаминов группы В, витамина Д, К, никотиновой, липолиевой кислоты.
4. Угнетение процессов гниения в кишечнике и нейтрализации аммиака достигается проведением деконтаминации кишечника (неомицин, олеандомицин по 2 гр перорально), очищением кишечника (солевые слабительные, высокие сифонные клизмы), в/в введением глютаминовой кислоты 1% раствора 50 мл.
5. Искусственная детоксикация: энтеросорбция, плазмоферез, плазмосорбция, гемодиализ.
6. При развитии генерализованного кровотечения проведение гемостатической терапии (криопреципитат 5-6 доз, свежезамороженная плазма 500 мл, аминокапроновая кислота 100 мл 3 раза, дицинон, этамзилат 2-4 мл в/в 4раза в сутки). При необходимости проведение гемотрансфузии, предпочтительнее использовать свежую донорскую кровь, что позволяет обеспечить больного максимальным количеством факторов свертывания.
7. С целью дезинтоксикации, улучшения кровоснабжения печени иногда бужируют пупочную вену и вводят 250 мл свежезаготовленной оксигенированной крови, 400-600 мл 5% раствора глюкозы с витаминами, спазмолитики (2-3 мл 2% раствора папаверина, 5-10 мл 2,4% раствора эуфиллина.)
Источник

Острая печеночная недостаточность – патологический симптомокомплекс, развивающийся при изменениях паренхимы печени и сопровождающийся нарушением ее функций. Острая печеночная недостаточность характеризуется признаками печеночной энцефалопатии (немотивированной слабостью, сонливостью, адинамией, возбуждением), диспепсическими расстройствами, появлением и нарастанием желтухи, отеков, асцита, геморрагического диатеза; в тяжелых случаях – развитием печеночной комы. Диагностика острой печеночной недостаточности основывается на клинических данных, результатах исследования печеночных проб, КЩС, ЭЭГ. Лечение острой печеночной недостаточности требует проведения инфузионной терапии, витаминотерапии, гормонотерапии, плазмафереза, гемодиализа, гемосорбции, лимфосорбции, кислородных ингаляций, гипербарической оксигенации.
Общие сведения
Острая печеночная недостаточность – тяжелый синдром, в результате которого развиваются грубые метаболические нарушения, интоксикация организма продуктами белкового обмена, геморрагический синдром, нарушения деятельности ЦНС, печеночная кома. В гастроэнтерологии и гепатологии острой печеночной недостаточностью могут осложняться различные заболевания и патологические состояния. Смертность пациентов от печеночной недостаточности составляет 50-80%.
Причины острой печеночной недостаточности
Острая печеночная недостаточность является исходом целого ряда патологических процессов, приводящих к обширным дистрофическим, фиброзным или некротическим изменениям паренхимы печени. Она может развиваться при тяжелом течении гепатитов различной этиологии (вирусных, лекарственных, аутоиммунных), циррозе, гепатозе, обтурации желчных протоков, отравлениях гепатотропными токсичными веществами и ядами (соединениями фосфора, мышьяка, несъедобными грибами, фармакологическими препаратами), при инфузии крови, не совпадающей по групповой принадлежности и др. Иногда острая печеночная недостаточность возникает как следствие нарушения печеночного кровообращения, которое встречается при ожогах, сепсисе, массивном кровотечении, тромбозе воротной вены и т. д.
Непосредственными пусковыми факторами развития острой печеночной недостаточности могут выступать прием алкоголя или лекарственных препаратов с гепатотоксическим действием, наркоз при операциях, хирургические вмешательства (например, портокавальное шунтирование, лапароцентез при асците), желудочно-кишечное кровотечение, избыток белка в пище, почечная недостаточность, поносы. У пациентов с имеющимся поражением печени (гепатит, цирроз) острая печеночная недостаточность может быть спровоцирована интеркуррентными инфекциями, перитонитом, тромбофлебитом воротной вены и др. состояниями.
Патологические сдвиги, развивающиеся в организме при острой печеночной недостаточности, обусловлены накоплением в крови соединений (аммиака, аминокислот, фенолов), оказывающих церебротоксическое действие, нарушением водно-электролитного и кислотно-щелочного баланса, расстройствами кровообращения и др. факторами. При острой печеночной недостаточности в наибольшей степени нарушается детоксикационная функция печени, а также снижается участие печени в различных обменных процессах (белковом, углеводном, жировом, витаминном, электролитном и т. д.).
Классификация острой печеночной недостаточности
Выделяют три формы острой печеночной недостаточности: эндогенную (спонтанную), экзогенную (индуцированную) и смешанную. Функциональная недостаточность, развивающаяся при непосредственном поражении паренхимы печени, расценивается как эндогенная. В основе экзогенно обусловленной печеночной недостаточности лежит расстройство кровообращения в печени, что приводит к сбросу крови, насыщенной токсинами (в первую очередь, аммиаком), в общий круг кровообращения. При смешанной печеночной недостаточности имеют место оба патологических механизма – эндогенный и экзогенный.
По выраженности функциональных нарушений печени различают три степени гепатопатии. При гепатопатии легкой степени клинические проявления поражения печени отсутствуют. С помощью лабораторных тестов выявляются умеренные функциональные нарушения (повышение ферментов, билирубинемия, увеличение уровня трансаминаз и др.).
Гепатопатия средней степени характеризуется появлением клинических симптомов: гепатомегалии, болезненности печени, приступов печеночной колики, желтушности кожных покровов и склер, явлений геморрагического диатеза. В крови нарастает гипербилирубинемия, гипопротеинемия, диспротеинемия.
Тяжелая гепатопатия соответствует стадии острой печеночной недостаточности. К вышеназванным проявлениям присоединяются симптомы печеночной энцефалопатии и печеночной комы, развивающиеся на фоне грубого нарушения функций печени.
Симптомы острой печеночной недостаточности
Клиническая стадия острой печеночной недостаточности (печеночная энцефалопатия) характеризуется сонливостью, которая может сменяться возбуждением, адинамией, прогрессирующей слабостью. Отмечаются диспепсические расстройства: тошнота, потеря аппетита, рвота, поносы. Нарастают отеки, явления геморрагического диатеза, желтухи, интоксикации, асцита, лихорадка.
В прекоматозном периоде развиваются нервно-психические нарушения: головокружение, замедление речи и мышления, расстройства сна, слуховые и зрительные галлюцинации, спутанность сознания, тремор пальцев, двигательное возбуждение. Могут отмечаться кровотечения из носа, десен, варикозно-расширенных вен пищевода.
Предвестниками приближающееся печеночной комы служат боли в подреберье, появление «печеночного» запаха изо рта, уменьшение печени в размерах. Собственно печеночная кома характеризуется утратой сознания; судорогами, гипотермией, аритмией, появлением патологических рефлексов, полиорганной недостаточностью.
Диагностика острой печеночной недостаточности
Распознавание острой печеночной недостаточности проводится с учетом симптоматики, результатов исследования биохимических показателей (в т. ч. печеночных проб), КЩС, инструментальных исследований (электроэнцефалографии).
Лабораторными признаками острой печеночной недостаточности служат анемия, тромбоцитопения, гипербилирубинемия (уровень билирубина может повышаться в 5 и более раз), увеличение активности сывороточных трансаминаз. В терминальной стадии острой печеночной недостаточности выражены гипохолестеринемия, гипоальбуминемия, снижение ПТИ и др. факторов свертывания, гипогликемия, гипокалиемия, отмечается нарушение кислотно-основного состояния.
Исследование ЭЭГ в зависимости от стадии острой печеночной недостаточности выявляет нарушение (неравномерность, замедление или исчезновение) альфа-ритма, доминирование тета- и дельта-волн.
Лечение острой печеночной недостаточности
Центральное место в лечении острой печеночной недостаточности занимает инфузионная терапия, направленная на дезинтоксикацию, улучшение микроциркуляции, метаболизма, коррекцию электролитных нарушений, восстановление кислотно-щелочного равновесия. При острой печеночной недостаточности показано внутривенное введение растворов глюкозы, альбумина, декстрана, реополиглюкина, сорбита, маннита и др. При введении большого объема жидкости для профилактики отека головного мозга и легких применяются диуретики.
Производится назначение витаминов (аскорбиновой кислоты, тиамина, рибофлавина, пиридоксина гидрохлорида, цианокобаламина, никотинамида). При геморрагическом синдроме показано введение растворов викасола, аминокапроновой кислоты, этамзилата натрия; при дефиците факторов свертывания и признаках ДВС-синдрома осуществляется трансфузия больших объемов плазмы. Прогрессирование острой печеночной недостаточности требует применения глюкокортикоидных гормонов (преднизолона), антибиотиков (аминогликозидов, цефалоспоринов).
С дезинтоксикационной целью используют плазмаферез, гемосорбцию, лимфосорбцию, гемодиализ. Для стимуляции иммунологической активности применяют УФО крови, для борьбы с гипоксией – гипербарическую оксигенацию, кислородные ингаляции.
Прогноз и профилактика острой печеночной недостаточности
Своевременная интенсивная терапия острой печеночной недостаточности существенно улучшает прогноз. При глубокой печеночной коме развиваются необратимые изменения, приводящие к гибели пациента.
Профилактика острой печеночной недостаточности требует адекватного лечения первичных заболеваний печени, исключения действия гепатотоксических или церебротоксических веществ, провоцирующих факторов.
Источник
