Синдром рикошета при бронхиальной астме
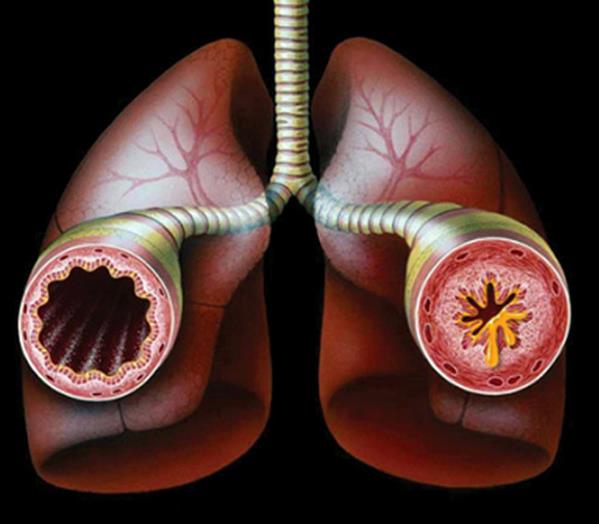
Приступ удушья
Бронхоспазм — спазм гладкой мускулатуры бронхов и бронхиол. Бронхоспазм может быть проявлением тяжелого приступа бронхиальной астмы, аллергической или анафилактической реакции на лекарства, следствием вдыхания токсических веществ, реакцией на травму при недостаточном наркозе во время операции, при выходе из наркоза после операции или бронхоскопии с применением жесткого бронхоскопа.
Приступ удушья сопровождается острой дыхательной недостаточностью. Во время приступа брохоспазма возникает обструкция дыхательных путей, которая характеризуется несоответствием соотношения вентиляции и кровотока, результатом которого являются альвеолярная гиповентиляция, гипоксемия, гиперкапния, дыхательный ацидоз.
Увеличение сопротивления в дыхательных путях и задержка воздуха в легких во время выдоха вызывают усиленную работу дыхательных мышц, которая в условиях артериальной гипоксии сопровождается накоплением молочной кислоты в дыхательных мышцах вследствие чего развивается комбинированный дыхательный и метаболический ацидоз.
Астматический статус, или «статус астматикус» — крайняя степень бронхоспазма c отеком и закупоркой мелких бронхов и бронхиол вязкой мокротой.
При тотальном бронхоспазме вовлечены все мелкие бронхи и бронхиолы. При таком состоянии перестают прослушиваться дыхание и хрипы, наступает «остановка легких», асфиксия, приводящая к терминальному отеку легких, остановке сердца и смерти больного.
Лечение внезапного приступа бронхоспазма
Купирование внезапного приступа бронхоспазма начинают с внутривенного введения эуфиллина, который, помимо бронхоспастического эффекта, уменьшает легочное сосудистое сопротивление, оказывает положительное инотропное и умеренное диуретическое действие. Для подбора оптимальной и нетоксичной дозы эуфиллина необходимо определить его концентрацию в сыворотке крови, поскольку высокие дозы эуфиллина способны усилить тахикардию, вызвать аритмию, возбуждение центральной нервной системы и даже судороги.
Интенсивная терапия тяжелого приступа бронхоспазма заключается в немедленном внутривенном введении кортикостероидных гормонов (преднизолона, гидрокортизона), холинолитиков (атропина или метацина), бета2-агонистов (сальбутамола) антигистаминных препаратов (супрастина, пипольфена).
Важно!!! Адреномиметики (адреналин, изадрин, новодрин, изупрел, алупент) следует применять с особой осторожностью, поскольку одновременно с бронхолитическим эффектом они оказывают стимулирующее действие на сердце и могут резко усугубить гипоксию миокарда.
Важно!!! В лечебной тактике бронхоспазма необходимо исключить применение морфина и его производных, которые могут способствовать усилению бронхоспазма, возбуждая парасимпатическую систему и высвобождая в кровь гистамин.
Важно!!! Реланиум и другие транквилизаторы должны вводиться только в тех случаях, когда решается вопрос о переводе больного на аппаратное дыхание.
Купирование приступа бронхоспазма завершается небулайзерной терапией
- Бронхолитики: холинолитик атровента (ипратропиум бромида), препараты группы бета2-адреномиметиков (сальбутамол, беротек и др) или комбинированный препарат беродуал .
- Муколитики (бизолвон, лазолван) показаны больным когда затруднено отхождение густой и вязкой мокроты.
- Кортикостероидный препарат пульмикорт (будесонит) для ингаляций оказывает выраженный противовоспалительный эффект и восстанавливает проходимость мелких бронхов.
Лечение приступа бронхоспазма во время торакальной операции
Бронхоспазм, возникший во время торакальной операции, проявляется в виде острого вздутия легкого или его доли. При этом ригидность вздутой доли легкого может сочетаться с коллапсом другой доли легкого, а после ее раздувания не удается обеспечить спадение легкого при активном выдохе во время наркоза и проведения искусственной легочной вентиляции. В такой критической ситуации, когда во время наркоза не обеспечивается адекватный газообмен, необходимо безотлагательно прибегнуть к прямому массажу легкого. Прямой массаж легкого ручным способом сочетается с нагнетанием в легкие гипероксической смеси из наркозно-дыхательного аппарата. При этом вдох осуществляется с помощью меха наркозного аппарата анестезиологом, а выдох — сдавления легкого руками хирурга.
Остро развившийся приступ бронхоспазма может быть купирован фторотановым или эфирным наркозом масочным способом.
Астматический статус
Астматический статус — критическое состояние, обусловленное не только броноспазмом, но главным образом закупоркой мелких бронхов и бронхиол вязкой мокротой и их воспалительным отеком.
Можно условно выделить три стадии астматического статуса.
I стадия — относительная компенсация. Наблюдается «эффект рикошета», когда после начального улучшения бронхиальной проходимости под влиянием бета-адреностимуляторов при развивающейся блокаде бета-адренорецепторов увеличивается бронхиальное сопротивление, возникают отек слизистой бронхов и бронхиол, гиперсекреция, бронхообтурация вязкой мокротой и рефлекторно усугубляется бронхоспазм.
II стадия — декомпенсация. Прогрессирование легочной недостаточности в связи с увеличивающейся бронхиальной обструкцией густой слизью и появлением «немых зон» в легких, вплоть до полностью «молчащих легких». Усиливаются цианоз и тахипноэ, резко нарастают гипоксемия и гиперкапния, развивается респираторный и метаболический ацидоз. Аускультативно выявляются «зоны молчания» в легких, сухие свистящие хрипы выслушиваются на ограниченных участках легких. Рентгенологически и кардиологически определяются признаки легочного сердца. Быстро прогрессирует правожелудочковая недостаточность.
III стадия — гипоксическая кома, которая характеризуется нарушением деятельности центральной нервной системы в результате тяжелых респираторных и метаболических расстройств. Кома может быть финальной стадией астматического статуса. В конце ее нередко возникает фибрилляция желудочков и асистолия.
Лечение астматического статуса
В начальной стадии астматического статуса следует стремиться купировать бронхоспазм внутривенным введением эуфиллина, сальбутамола, а при необходимости и адреналина или его производных. Отсутствие положительного эффекта от симпатомиметиков означает, что уже возникла блокада бета-адренорецепторов и возможна извращенная реакция на них («синдром рикошета»). Поэтому дальнейшее лечение симпатомиметиками становится бесполезным и даже опасным.
Важно!!! Больным, находящимся в астматическом статусе, назначать холинолитики (атропин или метацин) не следует в связи с их неэффективностью и свойством высушивать слизистую оболочку бронхов, способствуя сгущению мокроты и образованию пробок.
С целью повышения и восстановления чувствительности бета-адренорецепторов к катехоламинам осуществляют массивную кортикостероидную терапию и коррекцию кислотно-щелочного состояния.
Кортикостероидные гормоны назначают большие дозы (например, 90-120 мг преднизолона) внутривенно. Введение может быть повторено в зависимости от получения эффекта. Коррекцию кислотно-щелочного состояния проводят инфузией натрия бикарбоната и проводят гипергидратацию введением раствора Рингера, реополиглюкина, 5% глюкозы (до 2,5-3 л в сутки) под контролем диуреза, гематокрита, электролитов и кислотно-щелочного состояния. Наряду с гидратацией, необходимой для разжижения мокроты, и применением муколитика (бизолвон) могут быть использованы диуретики (лазикс или альдактон) для уменьшения отека слизистой бронхом и предупреждения гипоксической энцефалопатии и отека мозга.
С целью улучшения реологических свойств крови и профилактики тромбоэмболических осложнений следует назначать антикоагулянты (гепарин до 25000-30000 ЕД в сутки).
Легочная гипертензия может поддерживать бронхоспастическое состояние и поэтому целесообразно применять ганглиоблокаторы (25-50мг пентамина) под контролем гемодинамики.
При неэффективности медикаментозной терапии, дальнейшем нарастании легочной обструкции, вызванной чрезмерной продукцией и ретенцией бронхиального секрета, показан бронхоальвеолярный лаваж по Сандерсу в модификации Г.И.Лукомского и Л.А.Вайсберга. Лаваж проводят под наркозом с помощью жесткого оптического бронхоскопа инжекционным способом, бронхи промывают теплым содовым или физиологическим раствором с фурагином и тщательно отсасывают бронхиальное содержимое, и сгустки в виде слепков бронхов. Если состояние больного позволяет, то бронхоальвеолярный лаваж одного из легких осуществляют до получения в мокроте многочисленных пробок и слепков мелких бронхов, в этом случае процедура бывает эффективной. Поскольку лаваж небезопасен из-за возможности усугубления бронхиолоспазма, в целях создания более благоприятных и надежных условий поддержания газообмена его следует осуществлять после интубации двухпросветной трубкой Карленса. При этом, не прерывая искусственной вентиляции одного легкого, осуществляеют бронхоальвеолярный лаваж другого легкого, что позволяет проводить процедуру для обоих легких поочередно через небольшой промежуток времени.
При нарастании легочно-сердечной недостаточности и переходе больного в кому показана механическая искусственная вентиляция легких. После интубации трахеи (возможно большим размером интубационной трубки) подключают больного к наркозно-дыхательному аппарату и проводят искусственную легочную вентиляцию с большим вентилируемым объемом и высокой минутной легочной вентиляцией, периодически отсасывать мокроту из дыхательных путей. При этом необходимо увлажнять воздушно-кислородную смесь и устранять возбуждение больного внутривенным введением реланиума или дроперидола. Иногда приходится прибегать к мышечным релаксантам для полного выключения спонтанного дыхания больного при искусственной вентиляции легких.
Важно!!! Введение морфина для подавления спонтанного дыхания и обезболивания недопустимо, поскольку он оказывает парасимпатомиметическое действие и не показан при бронхоспазме.
Источник
Не для самолечения. Проконсультируйтесь с врачом.
Астматический статус.
Крайним проявлением
бронхиальной астмы является астматическое состояние (астматический статус). Причины развития
астматического статуса многообразны, но основными из них являются:
– передозировка симпатомиметиков (бесконтрольный их прием более 6 раз в
сутки);
– внезапное прекращение приема глюкокортикоидов;
– контакт с аллергеном (особенно с большой его концентрацией);
– обострение воспалительного процесса (особенно бронхолегочного);
– нервно-психическое или физическое перенапряжение;
– климато-погодные факторы (изменение барометрического давления, сырая,
влажная и холодная погода, большая концентрация пыли и др.);
– неправильное проведение специфической гипосенсибилизации и др.
Иногда причину развития астматического статуса не удается установить.
А. Г. Чучалин рассматривает астматический
статус как “качественно новое состояние, основными патогенетическими
механизмами которого являются наряду с выраженным бронхоспазмом, отеком
слизистой оболочки бронхов и гиперсекрецией слизи- полная блокада -адренорецепторов
бронхиального дерева, выраженные гиперкапния, гипоксия, аноксия
тканей, полицитемия и синдром острого легочного сердца”.
Основными клиническими критериями
астматического состояния являются: возрастающая резистентность к терапии
бронхолитиками симпатомиметического действия, развитие синдромов “рикошета”
и “запирания” от их применения, выраженное кардиотоксическое действие
симпатомиметиков (сердцебиения, боли в области сердца, аритмия, повышение АД);
плохая переносимость ранее хорошо воспринимаемого эуфиллина (диспепсические
расстройства, головные боли, боли в области сердца).
Важно отметить, что выраженность приступа удушья, его продолжительность не
могут быть признаками, определяющими астматическое состояние, поэтому
неправомочно ставить знак равенства между затяжным или тяжелым приступом удушья
и астматическим статусом. Прогрессирующая блокада β2-адренорецепторов приводит
к нарушению функции мукоцилиарного аппарата с продукцией вязкого стекловидного
секрета, закрывающего воздухоносные пути. Одновременно с этим усугубляется
отек слизистой оболочки бронхов, усиливается спазм бронхиальной гладкой
мускулатуры. Дополнительным фактором нарушения проходимости дыхательных путей
является экспираторный коллапс мелких и средних бронхов в результате повышения
внутригрудного давления на выдохе.
Выделяют две формы
астматического статуса – анафилактическую и метаболическую.
При анафилактической форме ведущим
механизмом нарастающей бронхиальной обструкции является спазм гладкой
мускулатуры, развивающийся очень быстро и быстро приводящий к картине острой
дыхательной недостаточности. Метаболическая форма астматического статуса
формируется постепенно и характеризуется медленно прогрессирующим нарастанием
обструкции, в основе которой чаще лежит отек слизистой оболочки бронхов и дискриния.
Анафилактическая форма статуса чаще развивается в результате аллергической
реакции на медикаменты, а метаболическая – при развитии синдрома
“рикошета” или “запирания”. Синдром “рикошета”
возникает при использовании неселективных симпатомиметиков, когда на фоне
блокады β2-адренорецепторов преобладает эффект α-адреностимуляции, выражающийся
в тотальном спазме гладкой мускулатуры бронхов. Чрезмерное использование
селективных адреномиметиков (стимуляция β2-адренорецепторов) приводит к
значительной вазодилатации бронхиальных сосудов, замедлению кровотока,
пропотеванию плазмы с развитием отека слизистой оболочки бронхиального дерева
и нарушению проходимости бронхов – их “запиранию”.
В течение астматического
статуса выделяют три стадии.
I стадия – стадия относительной
компенсации. Она характеризуется нарастающей бронхиальной обструкцией с
повышением вязкости секрета, гиповолемией. В клинической картине обращает внимание
усиление кашля с резким уменьшением количества мокроты, нарастание удушья, при
котором характерно усиление интенсивности дистанционно определяемых хрипов при
уменьшении их количества в легких при аускультации. Положение больных
вынужденное – сидя с фиксированным плечевым поясом и включением вспомогательной
дыхательной мускулатуры. Отмечается бледный цианоз, выраженная тахикардия,
иногда – аритмия, нередко – повышение АД, снижение диуреза.
II стадия – декомпенсации или
“немого” легкого, проявляется выраженным несоответствием между
шумным, свистящим дыханием и почти полным отсутствием хрипов в легких, резким
ослаблением дыхания или отсутствием его в некоторых участках легкого. Кожные
покровы у больных бледно-серые, влажные, тахикардия свыше 120 ударов в минуту,
аритмия, резкое повышение АД (может быть и значительное снижение АД после
повышения его в I стадии). Отмечается возбуждение больного, которое может
сменяться апатией.
III стадия – стадия гиперкапнической
(гипоксемической) комы. Она характеризуется тяжелой артериальной гипоксемией
(РаО2 40 – 55 мм рт. ст.) и резко выраженной гиперкапнией
(РаСО2 80-90 мм рт. ст. и выше). В клинике этой стадии превалирует
нервно-психическая симптоматика – психоз с дезориентацией во времени и месте,
бредовое состояние или глубокая заторможенность и утрата сознания. Нередко
отмечается диффузный “красный цианоз”, резкая потливость,
слюнотечение. Дыхание становится все более поверхностным, урежается, при
аускультации резко ослаблено, сухие хрипы не выслушиваются. Нередко
наблюдается расстройство сердечного ритма, нарастает артериальная гипотония
вплоть до коллапса, могут быть судороги.
При астматическом статусе развивается
гиповолемия и экстрацеллюлярная дегидратация, на высоте астматического
состояния развивается синдром диссеминированного внутрисосудистого свертывания
(ДВС). Факторами риска ДВС-синдрома при бронхиальной астме являются
длительность и тяжесть астматического статуса, гормональная зависимость,
присоединение инфекции, особенно гнойной.
Лечение астматического статуса строится на
следующих основных принципах:
– минимум лекарственных средств, только жизненно необходимые на данный
момент медикаменты;
– полная отмена препаратов симпатомиметического действия (если они
использовались в лечении), отказ от их применения как средств для оказания
первой помощи;
– обязательное назначение глюкокортикостероидов.
Медикаментозная терапия складывается из
следующего:
– глюкокортикоиды,
– борьба с
обезвоживанием,
– устранение
бронхоспазма,
– коррекция
кислотно-щелочного состояния,
– оксигенотерапия.
Глюкокортикоиды применяются одновременно парентерально (внутривенно) и
внутрь. Доза КС для парентерального применения определяется клинической
картиной. Однократная начальная доза КС (в пересчете на преднизолон) для
внутривенного введения при I стадии астматического статуса – 60 – 90 мг, при
II стадии – 90 – 120 мг, при III стадии – 120 – 150 мг.
При отсутствии или недостаточности эффекта (сохранение бронхоспазма) через
0,5 – 1 час преднизолон вводится повторно в вену в той же дозе или в большей.
Терапия КС проводится до полного купирования астматического статуса. Так как
при парентеральном введении происходит обязательное связывание КС с белками
крови, что как минимум наполовину снижает клинический эффект, то необходимо
одновременно назначать КС перорально в суточной дозе 40 – 60 мг и более (в
зависимости от тяжести течения астмы, предшествующего приема гормонов и др.).
Целесообразно при сочетании путей введения использовать разные группы КС.
Выход больного из астматического статуса является показанием для снижения
дозы КС. Тактика отмены (снижения) дозы КС такова:
ежедневное в течение 3-5 дней уменьшение дозы внутривенно вводимого
гормона наполовину с полной отменой. После этого также в течение 3-5 дней
отменяется пероральный прием гормонов. Если уменьшение дозы КС сопровождается
появлением признаков заболевания – переходят к подбору поддерживающей дозы
препарата для дальнейшего лечения.
Для борьбы с
обезвоживанием, с целью усиления бронхиальной экссудации и улучшения тканевого обмена
назначается введение достаточного количества жидкости – регидратация тканей.
Лучше использовать 5%-ный раствор глюкозы и физиологический раствор. В течение
первых суток лечения вводится 3-4 литра жидкости. Для улучшения
микроциркуляции и предотвращения развития ДВС-синдрома вводимые растворы
гепаринизируют из расчета 5000 ЕД гепарина на 1 литр жидкости. При появлении
эффективного кашля (с хорошим отхождением мокроты) и устранении бронхиальной
обструкции регидратация прекращается.
Ликвидация бронхиальной
обструкции при астматическом статусе достигается применением препаратов
метилксантинового ряда -эуфиллина. Начальная доза внутривенно струйно 5-6
мг/кг. После этого проводится внутривенное капельное введение
препарата в дозе 0,9 мг/кг/час до улучшения состояния, а затем в той же дозе в
течение 6-8 часов. Суточная доза эуфиллина может достигать 2 г (но не более).
При сочетании астматического статуса с артериальной гипертезией могут быть
рекомендованы ганглиотики (5%-ный раствор пентамина по 0,3 – 0,5 мл п/к или
в/в).
Появление резко выраженного токсического эффекта при применении эуфиллина
(головная боль, тошнота, рвота, боли в области сердца) может быть основанием
для назначения глюкозо-новокаиновой смеси (5%-ный раствор глюкозы 150-200 мл +
0,25%-0,5%-ный раствор новокаина 30-50 мл) для внутривенного применения.
Разжижение мокроты при астматическом
статусе лучше всего достигается назначением йодистого калия (3%-ный раствор
внутрь или 10%-ный раствор в/в – 5-10 мл). Отхаркивающие средства
муколитического действия при астматическом статусе противопоказаны.
Для астматического статуса
свойственно развитие дыхательного и метаболического ацидоза. Поэтому необходим
контроль за рН крови (должная величина не менее 7,3). Устранение ацидоза
достигается назначением щелочных растворов, парентеральное применение которых
возможно только под контролем рН, так как алкалоз значительно более губителен
для клеток организма, чем ацидоз. При невозможности динамического контроля за
рН крови уменьшения ацидоза можно добиться или приемом щелочных растворов
внутрь, или введением их в клизме (особенно у больных в бессознательном
состоянии).
Оксигенотерапия – важный фактор в
лечении астматического статуса, но следует помнить, что эффект ее будет
зависеть от состояния бронхиальной проходимости.
Лечение больных с III стадией астматического статуса должно
проводиться в условиях реанимационного отделения, так как в этих случаях
необходим чаще всего перевод больного на искусственную вентиляцию легких,
промывание (лаваж) бронхов с отсасыванием бронхиальной слизи, нередко –
длительная перидуральная блокада, фторотановый наркоз.
Источник
