Синдром шарко мари тута днк диагностика
Первое описание НМСН, известное в мировой литературе, было сделано французскими невропатологами Шарко и Мари в 1886 г., в статье «Относительно специфической формы прогрессирующей мышечной атрофии, часто семейной, начинающейся с поражения ступней и ног, и поздним поражением рук». Одновременно с ними заболевание описал Говард Тут в диссертации «Перонеальный тип прогрессирующей мышечной атрофии», который впервые сделал правильное предположение о связи заболевания с дефектами в периферических нервах. В России невропатолог, Давиденков Сергей Николаевич, впервые в 1934 году описал вариант невральной амиотрофии с усилением мышечной слабости при охлаждении.
Болезнь Шарко-Мари-Тута (ШМТ), или невральная амиотрофия Шарко-Мари, известная и как наследственная моторно-сенсорная невропатия (НМСН), – обширная группа генетически гетерогенных заболеваний периферических нервов, характеризующаяся симптомами прогрессирующей полинейропатии с преимущественным поражением мышц дистальных отделов конечностей. НМСН являются не только самым частым среди наследственных заболеваний периферической нервной системы, но и одним из самых частых наследственных заболеваний человека. Частота всех форм НМСН варьирует от 10 до 40:100000 в различных популяциях.
Клинико-генетическая гетерогенность невральной амиотрофии Шарко-Мари, явилась основанием для поиска локусов, сцепленных с данными заболеваниями. К настоящему времени картировано более 40 локусов, отвечающих за наследственные моторно-сенсорные нейропатии, идентифицировано более двадцати генов, мутации в которых приводят к развитию клинического фенотипа НМСН. Описаны все типы наследования НМСН: аутосомно-доминантный, аутосомно-рецессивный и Х-сцепленный. Наиболее часто встречается аутосомно-доминантное наследование.
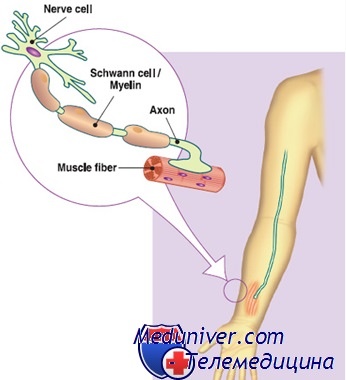
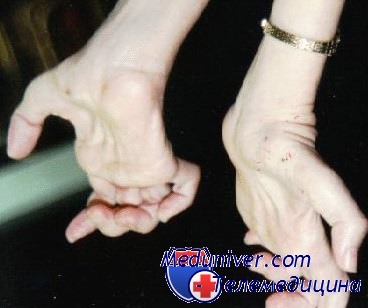
Первичное поражение нерва приводит к вторичной слабости и атрофии мышц. В наибольшей степени страдают толстые «быстрые» нервные волокна, покрытые миелиновой оболочкой («мякотные» волокна) – такие волокна иннервируют скелетные мышцы. Длинные волокна повреждаются сильнее, поэтому в первую очередь нарушается иннервация наиболее дистальных (удаленных) мышц, испытывающих большую физическую нагрузку – это мышцы стоп и голеней, в меньшей степени – мышцы кистей рук и предплечий. Поражение чувствительных нервов приводит к нарушению болевой, тактильной и температурной чувствительности в стопах, голенях и кистях рук. В среднем заболевание начинается в возрасте 10-20 лет. Первыми симптомами являются слабость в ногах, изменение походки (штампующая, «петушиная» походка, или «степпаж»), подворачивание голеней, иногда возникают несильные преходящие боли в нижней части ног. В дальнейшем прогрессируют слабость мышц, происходит атрофия мышц голеней, ноги приобретают вид «перевернутых бутылок», часто происходит деформация стоп (стопы приобретают высокий свод, затем формируется так называемая «полая» стопа), в процесс вовлекаются мышцы кистей рук и предплечий. При осмотре врачом-невропатологом выявляется снижение или утрата сухожильных рефлексов (ахилловых, карпорадиальных, реже – коленных), сенсорные нарушения.
Все моторно-сенсорные нейропатии в настоящее время по электронейромиографическим (ЭНМГ) и морфологическим признакам принято разделять на три основных типа: 1) демиелинизирующий (НМСНI), характеризующийся снижением скорости проведения импульса (СПИ) по срединному нерву, 2) аксональный вариант (НМСНII), характеризующийся нормальной или несколько сниженной СПИ по срединному нерву, 3) промежуточный вариант (intermedia) со СПИ по срединному нерву от 25 до 45 м/с. Величина СПИ, равная 38 м/с, определяемая по двигательной компоненте срединного нерва, считается условной границей между НМСНI (СПИ<38м/с) и НМСНII (СПИ>38м/с). Таким образом, ЭНМГ исследование приобретает особый смысл для ДНК-диагностики, поскольку позволяет выделить наиболее оптимальный алгоритм генетического обследования для каждой семьи.
Возраст начала заболевания, его тяжесть и прогрессирование зависят от типа нейропатии, но могут сильно варьировать даже в пределах одной семьи. Наиболее часто встречается форма болезни НМСНIА – от 50% до 70 % всех случаев НМСН 1 типа в различных популяциях. В 10% случаев выявляются Х-сцепленные формы НМСН, среди которых преобладает форма с доминантным типом наследования – НМСНIX, составляющая 90% от всех Х-сцепленных полинейропатий. Среди НМСН II типа наиболее часто встречается доминантная форма – НМСНIIA – в 33% всех случаев (табл. 1).
Наследственные моторно-сенсорные нейропатии с аутосомно-рецессивным типом наследования сравнительно редки, но клинически не отличимы от НМСН с аутосомно-доминантным типом наследования. НМСН 4D(Lom), 4С, 4H и 4J являются одними из таких болезней. Примечательно, что в генах NDRG1 и SH3TC2 локализованы частые мутации, характерные для цыган.
В ООО «Центр Молекулярной Генетики» разработан и проводится поиск наиболее частых мутаций цыганского происхождения, ответственных за развитие НМСН 4D(Lom) (Arg148X) и 4C (Arg1109X). Так же в ООО «Центр Молекулярной Генетики» разработана система поиска повторяющихся мутаций в генах GDAP1 (Leu239Phe), SH3TC2 (Arg954X и Arg659Cys), FIG4 (Ile41Thr) и FGD4 (Met298Arg и Met298Thr), ответственных за аутосомно-рецессивные типы НМСН.
Таблица 1. Гены, ответственные за развитие различных форм НМСН. (Синим цветом выделены гены, анализ которых проводится в ООО “Центр Молекулярной Генетики”)
Ген | Локус | Тип заболевания | Тип наследования |
|---|---|---|---|
| PMP22 | 17p11 | CMT 1A Dejerine-Sottas | АД АД |
| MPZ (P0) | 1q22 | CMT 1B CMT 1E CMT 2I CMT 2J CMT-DI3 Dejerine-Sottas | АД АД АД АД АД (intermedia) АД/АР |
| LITAF | 16p13 | CMT 1C | АД |
| EGR2 | 10q21 | CMT 1D CMT 4E Dejerine-Sottas | АД/АР АД/АР АД/АР |
| NEFL | 8p21 | CMT 1F CMT 2E | АД АД |
| GJB1 | Xq13 | CMT 1X | ХД-сцепленное |
| PRPS1 | Xq22.3 | CMT 5X | ХР-сцепленное |
| MFN2 | 1p36 | CMT 2A CMT 6 | АД АД |
| DNM2 | 19p12 | CMT 2 CMT-DIB | АД АД |
| YARS | 1p34 | CMT-DIC | АД |
| GDAP1 | 8q21 | CMT 4A CMT 2K CMT 2H | АР АР АР |
| HSPB1 | 7q11 | CMT 2H Distal HMN | АД/АР АД/АР |
| KIF1B | 1p36 | CMT 2A1 | АД |
| LMNA A/C | 1q21 | CMT 2A1 | АР |
| GARS | 7p15 | CMT 2D | АД |
| HSPB8 | 12q24 | CMT 2L | АД |
| IGHMBP2 | 11q13.3 | CMT 2S | АР |
| MTMR2 | 11q23 | CMT 4B | АР |
| SBF2 | 11p15 | CMT 4B2 | АР |
| SH3TC2 (KIAA1985) | 5q32 | CMT 4C | АР |
| NDRG1 | 8q24 | CMT 4D (Lom) | АР |
| Periaxin | 19q13 | CMT 4F | АР |
| FGD4 | 12q12 | CMT4H | АР |
| FIG4 | 6q21 | CMT4J | АР |
В ООО «Центр Молекулярной Генетики» разработана и проводится диагностика НМСН I, II и промежуточного типов с аутосомно-доминантным (АД), аутосомно-рецессивным (АР) и Х-сцепленным наследованием.
Нами разработан набор для регистрации дупликаций в локусе гена PMP22 при болезни НМСН 1А с использованием двух микросателлитных повторов методом ПЦР. Набор предназначен для использования в диагностических лабораториях молекулярно-генетического профиля.
При проведении пренатальной (дородовой) ДНК-диагностики в отношении конкретного заболевания, имеет смысл на уже имеющемся плодном материале провести диагностику частых анеуплоидий (синдромы Дауна, Эдвардса, Шерешевского-Тернера и др), пункт 54.1. Актуальность данного исследования обусловлена высокой суммарной частотой анеуплоидий – около 1 на 300 новорожденных, и отсутствием необходимости повторного забора плодного материала.
Публикации по теме раздела
Наследственная моторно-сенсорная нейропатия (Шарко-Мари-Тута)
Источник
Болезнь Шарко (в литературе еще встречается как «Болезнь Шарко-Мари», «Болезнь Шарко-Мари-Тута», код по МКБ- G60) –генетически обусловленное хроническое заболевание нервной системы, которое характеризуется развитием постоянно прогрессирующей периферической полинейропатией.
Частота диагностирования болезни Шарко-Мари-Тута согласно статистическим данным где-то один случай на две с половиною тысячи пациентов. Первые симптомы появляются в молодом возрасте. Выраженность симптомов и скорость прогрессирования болезни Шарко-Мари разная у каждого пациента. Процент инвалидизации при заболевании очень высок.

Причины заболевания болезнью Шарко:
- Мутация гена PMP22;
- Мутация MPZ;
- Мутация GJB1;
- Мутация MFN и др.
Пути наследования:
- аутосомно-доминантный (чаще всего);
- аутосомно-рецессивный;
- Х-сцепленный.
Заболевание имеет много форм, вызванные разным видом мутаций. Качество жизни и возможности работоспособности при болезни Шарко-Мари-Тута значительно ухудшаются, но на продолжительности жизни обычно это не сказывается.
Симптомы болезни Шарко связанные с поражением моторных и сенсорных нервных волокон. Диагностика болезни Шарко-Мари заключается в исключении диагнозов, которые могут давать подобную клиническую картину, и в проведении ДНК-диагностики, но учитывая, что не все виды мутаций известны, она не всегда информативна.
Лечение болезни Шарко-Мари-Тута заключается в симптоматической терапии. Специфическое лечение на данный момент все еще находится в стадии разработки.
Юсуповская больница – одно из лучших медицинских учреждений, где лечатся пациенты с болезнью Шарко-Мари-Тута. Несмотря на то, что терапия направлена только на купирование симптомов, неврология стремительно развивается и питается найти способы лечения многих заболеваний, в том числе и болезни Шарко. Ведение пациентов изданной патологией достаточно сложное, ведь клиническая картина разнообразна, симптомы выражены в неодинаковой степени и п.т. Опыт работы специалистов Юсуповской больницы позволяет оказывать качественную и эффективную медицинскую помощь. Доктора следят за клиническими исследованиями, новыми разработками, препаратами, изучают их эффективность. В случае необходимости, диагностика проводится быстро и с использованием нового оборудования. Персонал работает на благо пациента.
Симптомы болезни Шарко
Симптомы болезни Шарка-Мари появляются в молодом возрасте, чаще всего до двадцати лет. Прогрессирует заболевание постепенно, пациенты долгое время сохраняют работоспособность и возможность самообслуживания. Причинами, которые ускоряют развитие заболевания, могут стать вирусные и бактериальные инфекции, воздействия неблагоприятных факторов среды, травматизм, недостаток витаминов и т.п.
По МКБ-10 болезнь Шарко-Мари-Тута кодируется как «G60 Наследственная моторная и сенсорная невропатия», что связано в какой-то мере с клинической картиной.
В начале заболевания беспокоит чрезмерная усталость, невозможность долго стоять на одном месте, чувство онемения, «беганье мурашек», а дальше присоединяется атрофическое поражение мышц стоп, которое чаще носит симметричный характер. При обследовании выявляют выпадение сухожильных рефлексов. Стопа деформируется на столько, что больные не могут ходить, опираясь на пятки. Прогрессируя, атрофический процесс поражает голени и бедра.
Дальнейшее развитие заболевания болезни Шарко-Мари-Тута приводит к втягиванию в процесс и кистей, далее – предплечий. Мышцы шеи, туловища и плечевого пояса не атрофируются. Мышцы проксимальных отделов компенсаторно увеличиваются.
Все виды чувствительности нарушаются, но больше всего страдает поверхностная, особенно температурная.
Диагностика болезни Шарко
Диагностика включает:
- Осмотр неврологом;
- Лабораторные исследования;
- Инструментальные исследования;
- ДНК-исследования.
Полное обследование необходимо для исключения заболеваний, в которых клиническая картина сходна. К ним относят: боковой амиосклероз, миотония, метаболическая невропатия. Для исключения хронических полинейропатий проводят биопсию мышц.
Лечение болезни Шарко
Все способы лечения болезни Шарко-Мари-Тута не радикальны. Симптоматическое лечение включает медикаментозную терапию, физиотерапию, лечение у ортопеда и т.п.
Физиотерапевтическое лечение болезни Шарко-Мари-Тута включает ЛФК, массаж, электрофорез, диадинамотерапию, терапию лечебными грязями, разные виды ванн и др.
Медикаментозная терапия направлена на улучшение питания мышечных волокон. С этой целью назначают кокарбоксилазу, глюкозу, аденозинтрифосфат и др. Так же широко применяют антиоксидантные средства, препараты, улучшающие микроциркуляцию, и витамины. Хорошо зарекомендовали себя препараты, которые тормозят активность ацетилхолинэстеразы и повышают уровень ацетилхолина, например, прозерин, галантамин.
Дальнейшие разработки новых препаратов, направленные на радикальные меры – это мир без болезни Шарко-Мари-Тута. Прогрессирование болезни Шарко-Мари-Тута не отражается на том, сколько живут пациенты.
В Юсуповской больнице специалисты долгие годы помогают пациентам держать болезнь под контролем. Минимальная выраженность симптомов и медленное прогрессирование – результат работы врачей. В комфортных палатах, на новых тренажерах, в хорошо оснащенных кабинетах – вот где проходит лечение болезни Шарко-Мари-Тута. Не затягивайте с лечением, запишитесь на консультацию.
Источник
Болезнь Шарко-Мари-Тута 1А типа: причины, диагностика, лечениеЭтиология и встречаемость болезни Шарко-Мари-Тута. Болезнь Шарко-Мари-Тута — генетически разнородная группа наследственных нейропатий, характеризующихся хронической моторной и сенсорной полинейропатией. Данное заболевание подразделяют согласно типам наследования, неврологическим изменениям и клиническим симптомам. По определению, болезнь Шарко-Мари-Тута 1-го типа — аутосомно-доминантная демиелинизирующая нейропатия; ее распространенность приблизительно 15 на 100 000, она также генетически разнородна. Болезнь Шарко-Мари-Тута 1А типа, представляющая 70-80% всех случаев патологии, вызывается повышенной дозой белка PMP22 из-за дупликации гена PMP22 в хромосоме 17. Новые дупликации составляют 20-33% случаев болезни Шарко-Мари-Тута 1А типа; более 90% этих мутаций возникает в ходе мужского мейоза. Патогенез болезни Шарко-Мари-ТутаБелок PMP22 — внутримембранный гликопротеид. В периферической нервной системе PMP22 обнаруживают в только в компактном миелине. Функция PMP22 объяснена не полностью, но имеются подтверждения, что он играет ключевую роль в уплотнении миелина. Доминантные мутации с утратой функции в гене PMP22 и увеличение дозы PMP22 вызывают демиелинизирующую периферическую полинейропатию. Увеличение дозы белка PMP22 возникает при тандемной дупликации участка р11.2 в хромосоме 17. Этот участок размером 1,5 мегабазы ограничен повторяющимися последовательностями ДНК, идентичными почти на 98%. Нарушение спаривания фланговых повторяющихся элементов в ходе мейоза может приводить к неравному кроссинговеру и образованию одной хроматиды с дупликацией региона в 1,5 мегабазы и другой с реципрокной делецией. [Реципрокная делеция вызывает наследственную нейропатию с параличами сдавливания]. Индивидуум, унаследовавший хроматиду с дупликацией, будет иметь три копии нормального гена PMP22 и, таким образом, избыточную экспрессию белка PMP22. Избыточная экспрессия белка PMP22 или экспрессия его доминантных отрицательных форм приводит к невозможности формирования и поддержки компактного миелина. Образцы биопсии нервов от сильно пораженных детей демонстрируют рассеянную скудность миелина, в биоптатах нервов пациентов при меньшей степени поражения видны участки демиелинизации и гипертрофии миелиновой оболочки. Механизм образования данных изменений при избыточной экспрессии белка PMP22 остается неясным. Слабость и атрофия мышц при болезни Шарко-Мари-Тута 1-го типа происходят в результате их денервации, вызванной дегенерацией аксонов. Длительные наблюдения за больными показывают возраст-зависимое уменьшение плотности нервных волокон, согласующееся с развитием симптомов болезни. Кроме того, исследования на мышиных моделях указывают, что миелин необходим для функционирования цитоскелета аксонов. Как демиелинизация изменяет цитоскелет аксонов и влияет на их дегенерацию, полностью не объяснено.
Фенотип и развитие болезни Шарко-Мари-ТутаБолезнь Шарко-Мари-Тута 1А типа имеет почти полную пенетрантность, хотя тяжесть, возраст начала и течение болезни заметно изменяются внутри семей и между семьями. Большинство больных не обращаются за медицинской помощью, или не замечая симптомов, или поскольку эти симптомы легко переносятся. С другой стороны, многие имеют тяжелую болезнь, обнаруживаемую в раннем детстве. Симптомы болезни обычно появляются в первые два десятилетия жизни; начало после 30 лет бывает редко. Обычно симптомы начинаются с незаметной медленно прогрессирующей слабости и атрофии дистальных мышц ног и легкого сенсорного ухудшения. Слабость в стопах приводит к аномалии походки, хлопающей стопе и, в конечном счете, изменению формы стопы (полая стопа молокообразные пальцы стоп) и утрате равновесия; но это редко приводит к утрате способности ходить. Слабость важных мышц рук обычно появляется в конце болезни и, в серьезных случаях, вызывает аномалию кисти в виде сжатого кулака из-за дисбаланса между мышечной силой сгибателей и разгибателей кисти. Другие связанные симптомы — снижение или отсутствие рефлексов, атаксия и тремор верхних конечностей, сколиоз и пальпаторно утолщенные поверхностные нервы. Иногда также поражаются диафрагмальный и автономный нервы. При электрофизиологических исследованиях патогномоничный признак болезни Шарко-Мари-Тута 1А типа — равномерное снижение скорости проведения во всех нервах и нервных сегментах в результате демиелинизации. Выраженное снижение скорости проведения обычно присутствует уже к 2-5 годам жизни, хотя клинически явные симптомы могут не обнаруживаться в течение многих лет. Особенности фенотипических проявлений болезни Шарко-Мари-Тута:
Лечение болезни Шарко-Мари-ТутаХотя болезнь Шарко-Мари-Тута 1-го типа можно заподозрить на основе клинических, электрофизиологических и патогистологических признаков, окончательный диагноз часто зависит от обнаружения мутации. Воспалительные периферические нейропатии часто трудно отличить от болезни Шарко-Мари-Тута 1-го типа и наследственной нейропатии с параличами сдавливания, и ранее, до появления молекулярной диагностики, многих больных с унаследованной нейропатией лечили иммуносупрессорами, в итоге получая повышенную смертность без улучшения нейропатии. Лечение симптоматическое, поскольку радикальной терапии к настоящему времени не разработано. Параллельно развитию болезни терапия обычно состоит из трех этапов: укрепляющие и растягивающие упражнения для поддержания ходьбы и других двигательных функций, использование ортопедической обуви и специальных шин и ортопедическая хирургия. При дальнейшем ухудшении могут понадобиться передвижные опоры, такие как костыли, ходунки или, в редких тяжелых случаях, инвалидное кресло. Всем больным необходимо рекомендовать избегать воздействия нейротоксичных медикаментов и химических веществ. Риски наследования болезни Шарко-Мари-ТутаПоскольку дупликация и большинство точковых мутаций в гене PMP22 аутосомно-доминантные и полностью пенетрантные, каждый ребенок больного родителя имеет 50% шанс развития болезни Шарко-Мари-Тута 1А типа. Тем не менее переменная экспрессивность дупликации и мутаций в гене PMP22 делает невозможным прогноз тяжести болезни. Пример болезни Шарко-Мари-Тута. В течение нескольких последних лет 18-летняя женщина обращала внимание на прогрессирующую слабость, снижение выносливости и способности бегать и ходить. Она также жаловалась на частые судороги ног, усиливающиеся при охлаждении, и появившиеся затруднения при перешагивании через предметы или подъеме по ступенькам. Она не помнила предшествующих болезней или жалоб, напоминающих воспалительный процесс, например мышечных болей, лихорадки, или ночных потов. Ни у кого из других членов семьи не было аналогичных проблем или нервно-мышечных заболеваний. При обследовании у пациентки обнаружены худые атрофичные ноги, больше в дистальных отделах, небольшая слабость при сгибании и разгибании стопы, отсутствие рефлексов стопы, снижение коленных рефлексов, «хлопающая» походка и утолщение перонеальных нервов. Ей трудно ходить на пальцах ног и невозможно ходить на каблуках. В остальном результаты обследования оказались нормальными. Как часть обследования, невролог запросил несколько анализов, включая скорость проведения по нервам. Скорость проведения по нервам оказалась аномальной; средний показатель составил 25 м/с (в норме >43 м/с). Результаты последующей биопсии нерва показали сегментарную демиелинизацию, гипертрофию миелиновой оболочки (избыток шванновских клеток вокруг нервных волокон) и никаких признаков воспаления. Невролог заключил, что эти результаты сильно напоминают демиелинизирующую нейропа-тию, например болезнь Шарко-Мари-Тута 1-го типа, также известную как наследственная мотосенсорная нейропатия 1-го типа. Объяснив, что наиболее частая причина болезни Шарко-Мари-Тута — дупликация в гене периферического миелинового белка 22 (PMP22), невролог предложил анализ на эту дупликацию. Тест подтвердил, что пациентка имела удвоение аллеля PMP22 и болезнь Шарко-Мари-Тута 1А типа. – Также рекомендуем “Синдром CHARGE: причины, диагностика, лечение” Оглавление темы “Наследственные болезни”:
|
Источник