Синдром склерокистозных яичников штейна левенталя
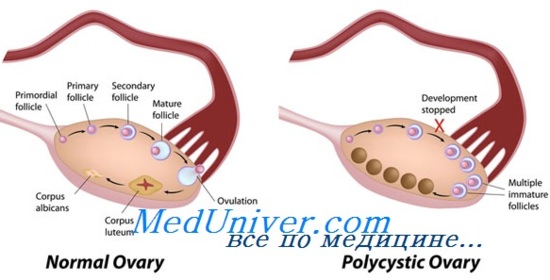
Синдром склерокистозных яичников (Штейна — Левенталя)
Этот синдром принято называть синдромом Штейна — Левенталя, так как эти авторы весьма детально описали в 1935 г. клинико-морфологические особенности склерокистозно-измененных яичников у 7 больных, а также сообщили об успешном лечении таких больных путем двусторонней клиновидной резекции яичников [Stein, Leventhal]. Однако в отечественной литературе на 20 лет раньше [Хачкурузов Я. К.] было опубликовано сообщение с описанием двустороннего увеличения в 2—3 раза яичников у 5 молодых женщин с расстройством менструального цикла (аменорея 2—3 мес). Ограниченное число наблюдений не дало возможности отечественным авторам подробно описать клиническую картину при поликистозных яичниках.
В настоящее время представление о синдроме склерокистозных яичников настолько расширилось, что некоторые авторы включают в этот синдром и другие заболевания яичников, а также болезни коры надпочечника и гипоталамо-гипофизарной системы.
В то же время при наличии типичного синдрома Штейна—Левенталя у половины больных обнаруживается и надпочечниковая гиперандрогения [Петухова Л. В., Givens]. Имеется также указание, что склерокистозные яичники встречаются в 10 раз чаще, чем, маскулинизирующие опухоли яичника (Scully).
Морфологические особенности. Размеры склерокистозных яичников большей частью бывают 6х5х3 см, а размеры нормальных—3,8х2х1,2 см [Тонков В. Н.]. Происходит гиперплазия клеток thecae interna [Tillinger, Westman, Jones, Toth]. Интенсивность склероза может быть различной при одинаковой клинической картине заболевания [Gyves]. Чрезмерное разрастание фиброзной соединительной ткани при склерокистозных яичниках ведет к утолщению коркового и мозгового слоев яичников, что наряду с увеличением кистозно-атрезирующихся фолликулов обусловливает их увеличение. Raj и соавт. считают, что морфологические изменения в яичниках при синдроме Штейна—Левенталя формируются вторично вследствие нарушения в них стероидогенеза и избыточного образования андрогенов.
Если морфологические изменения в яичнике ограничиваются только мелкокистозным их перерождением — degeneratio nicrocystica ovarii, это обусловливает гиперэстерогенизм и часто наблюдается при миомах матки и ановуляторных кровотечениях. Отождествление мелкокистозных яичников с поликистозными при синдроме Штейна — Левенталя [Шушания П. Г.] вносит путаницу в понятие синдрома Штейна—Левенталя или синдрома склерокистозных яичников.
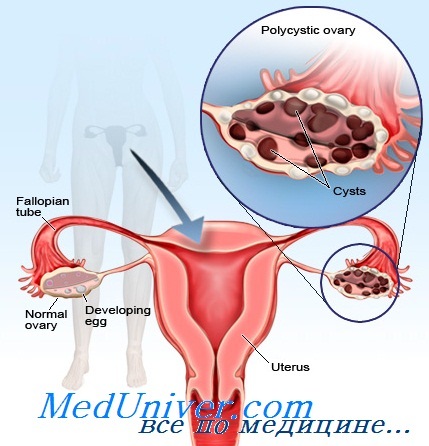
Отсутствие увеличения яичников при гипертекозе и часто сочетающаяся гиперплазия коры надпочечника с гипертекозом [Benedict et al.] заставляют многих считать гипертекоз отдельной формой заболевания.
Патогенез поликистозных яичников до сих пор остается окончательно невыясненным. Существующие многочисленные теории их возникновения в конечном счете сводятся к тому, что в основе их развития лежат гормональные нарушения. Однако одни авторы объясняют развитие поликистозных яичников нарушением функции гипоталамо-гипофизарной системы, другие — нарушением функции коры надпочечника, третьи— патологией яичников.
Теория гипофизарного генеза поликистозных яичников. В литературе имеется много сообщений относительно гиперсекреции гонадотропных гормонов при поликистозных яичниках. Одни авторы считают, что поликистозные яичники развиваются в результате избыточного выделения ФСГ гипофиза, а другие объясняют возникновение этой патологии избыточным выделением ЛГ гипофиза [Givens].
По мнению П. Г. Шушания, Mohesh и Greenblatt, избыток ФСГ гипофиза вызывает поликистозное перерождение яичников.
Теория избыточного выделения ФСГ гипофизом как причины развития поликистозных яичников основывается на том, что в эксперименте введение ФСГ гипофиза ведет к резкому (в 5 раз) увеличению яичников и повышению секреции ДНА, андростерона и этиохоланолона яичником [Mahesh, Greenblatt].
При вскрытии у 7 из 12 женщин с синдромом поликистозных яичников, умерших от случайных причин, было обнаружено увеличение базофильных клеток в передней доле гипофиза, секретирующих ФСГ и АКТГ [Sommers, Wadman]. Наряду с этим Gemzell и др. установили, что после введения ФСГ гипофиза больным с поликистозными яичниками появляется овуляция; у 2 женщин наступила беременность, закончившаяся родами двойней. Вместе с тем, по данным Morris и Scully, в эксперименте на обезьянах при введении ФСГ не возникло типичных поликистозных яичников с утолщением их белочной оболочки и склерозированием стромы.
Гормональные исследования не обнаруживают повышения уровня гонадотропинов в моче при поликистозных яичниках, поэтому мы согласны с Leventhal, что роль ФСГ гипофиза в формировании поликистозных яичников еще не доказана. Теория избыточного выделения ЛГ гипофизом как причины развития поликистозных яичников основывается на том, что некоторые авторы [Fisher, Riley, Traymor, Barnard, Givens] обнаружили повышение выделения ЛГ у 50% больных с поликистозными яичниками, а также в большинстве случаев лютеинизацию клеток thecae internae. Ingersoll и McArthur обследовали 6 больных с поликистозными яичниками и выявили у них значительные колебания ЛГ гипофиза: каждый 4-й день содержание ЛГ достигало высокого уровня с последующим падением. У 13 женщин с нормальным менструальным циклом уровень ЛГ повышался только перед овуляцией и в лютеиновой фазе цикла.
Sterba и Sturma показали, что при центральном, а также при периферическом происхождении поликистозных яичников происходит избыточное выделение ЛГ гипофизом. Эти авторы считают, что при центральном происхождении поликистозных яичников избыточное выделение ЛГ гипофизом наступает вследствие нарушения гипоталамо-гипофизарных отношений, при периферическом происхождении поликистозных яичников повышение уровня ЛГ происходит вследствие нарушения биосинтеза прогестерона из прегненолона, обусловленного недостатком энзима Зb-ол-дегидрогеназы. Недостаточное количество прогестерона в яичнике поддерживает длительное и повышенное выделение ЛГ гипофизом. Sterba и Sturma успешно лечили больных с синдромом поликистозных яичников большими дозами прогестерона: в процессе лечения снижался уровень ЛГ и уменьшалась выработка андрогенов яичником.
Givens в 1979 г. предложил пробу с синтетическими прогестинами (норэтнинондрон 2 мг и местранол 0,1 мг) для выявления яичниковой гиперандрогении, обусловленной избыточным выделением ЛГ. Эта проба оценивается как положительная, если после применения синтетических прогестинов в течение 16—20 дней происходит снижение содержания андростендиона, тестостерона и ЛГ в плазме.
Leventhal, Soffer и соавт. также считают, что избыточное выделение ЛГ гипофизом ведет к развитию поликистозных яичников. Однако у некоторых больных не было обнаружено постоянного повышения ЛГ [Богданова Е. А., Evans, Riley]. Ingersoll и McArthur нашли значительные колебания в выделении ЛГ в течение менструального цикла (резкое падение каждый 3—4-й день). Эти данные свидетельствуют о том, что при синдроме Штейна — Левенталя нарушается выделение ЛГ гипофизом: оно периодически то повышается, то снижается.
– Также рекомендуем “Теория надпочечникового генеза поликистозных яичников”
Оглавление темы “Вирильный синдром. Поликистоз яичников”:
- Дифференциация болезни и синдрома Иценко-Кушинга
- Лечение вирильного синдрома и аномалий наружных половых органов
- Эффекты длительного лечения глюкокортикоидами. Терапия адреногенитального синдрома
- Синдром склерокистозных яичников (Штейна — Левенталя)
- Теория надпочечникового генеза поликистозных яичников
- Теория морфологических и функциональных нарушений яичников при поликистозе
- Клиника и проявления синдрома Штейна—Левенталя
- Диагностика синдрома Штейна—Левенталя. Гормональные нарушения при поликистозе яичников
- Лечение синдрома Штейна—Левенталя. Операция при поликистозе яичников
- Маскулинизирующие опухоли яичников. Арренобластома
Источник
Поликистоз яичников. Синдром Штейна — Левенталя
Поликистозное перерождение или склерокистозная дегенерация яичников впервые была описана в 1935 г. американскими исследователями Штейном и Левенталем. Впоследствии этот клинический синдром стали называть именем этих авторов. Но этиология и патогенез этого заболевания яичников до настоящего времени еще недостаточно изучены. Одним из основных и ведущих клинических проявлений данного заболевания являются выраженные симптомы вирилизма.
Наряду с этим признаком имеется еще ряд других различных неспецифических клинических проявлений этого синдрома.
В яичниках больных при синдроме Штейна — Левенталя основным морфологическим признаком является выраженный поликистоз при отсутствии каких бы то ни было опухолевых изменений. Причиной этого заболевания яичников являются, по-видимому, глубокие нарушения регуляторной связи между гонадотропными функциями передней доли гипофиза и жепскими половыми железами.
В яичниках нарушается процесс образования желтых тел, прекращается продукция прогестерона, сопровождающаяся стойким нарушением овариально-менструального цикла. Как указывают Н. А. Шерешевский, Е. А. Васюкова, Е. И. Кватер и М. Л. Крымская, следует строго разграничивать кистозные поражения яичников, возникшие на почве различных воспалительных процессов, при которых редко развиваются явления вирилизма, от поликистозной дегенерации женских половых желез, вызванной нарушением коррелятивных связей между некоторыми органами эндокринной системы.

При синдроме Штейна — Левенталя степень и характер возникающих изменений в яичниках разнообразны и не всегда постоянны. Такие яичники увеличены иногда в 5—10 раз по сравнепию со здоровыми. Чаще при этом синдроме наблюдается симметричное увеличение яичников, однако встречаются случаи и одностороннего увеличения. Поверхность яичников слегка бугристая и в отличие от неизмененных имеет перламутровый оттенок.
Яичники при синдроме Штейна—Левенталя характеризуются повышенной плотностью. Снаружи яичник покрыт утолщенной склеротически измененной капсулой белесоватого или перламутрового оттенка, через которую нередко просвечивают резко инъецированные кровеносные сосуды. Иногда на поверхности яичников можно обнаружить небольшие единичные или множественные выпячивания, соответствующие разросшимся фолликулярным кистам.
На разрезе в корковом веществе яичника чаще обнаруживаются множественные, реже единичные кистозные полости с гладкими, блестящими сероватого оттенка стенками. Подобные кисты при синдроме Штейна — Левенталя выполнены желтоватой, слегка опалесцирующей жидкостью. Кистозно расширенные же фолликулы, возникшие на почве воспалительного процесса, содержат серозно-геморрагический экссудат красновато-коричневого цвета.
Обнаруживаемые в яичниках кисты при синдроме Штейна — Левенталя обычно локализуются в корковом веществе этого органа, имеющем эластическую консистенцию и серовато-розовый цвет. Однако следует отметить, что при синдроме Штейна — Левенталя не всегда в корковом веществе яичников обнаруживаются кисты. Этот признак не постоянный и не обязателен.
– Также рекомендуем “Гистология яичников при поликистозе. Текаклеточная реакция”
Оглавление темы “Патология яичек и яичников”:
- Гормональноактивные опухоли яичка – лейдигомы
- Злокачественные новообразования яичка. Андробластома яичка
- Поликистоз яичников. Синдром Штейна — Левенталя
- Гистология яичников при поликистозе. Текаклеточная реакция
- Гормональноактивные опухоли яичников. Фолликулома
- Цитобластомы яичников. Текаклеточная опухоль – текома
- Арренобластома яичника – гистология, патологическая анатомия
- Дисгерминома или семинома яичников. Липоидноклеточные вирилизирующие опухоли яичника
- Менструальный цикл. Менструация
- Влияние гипофиза на менструальный цикл. Гонадотропины – ФСГ и ЛГ
Источник
ШТЕЙНА — ЛЕВЕНТАЛЯ СИНДРОМ (J. F. Stein, американский гинеколог, родился в 1887 году; М. L. Leventhal, американский гинеколог, родился в 1901 году; синоним: синдром склерокистозных яичников, болезнь склерокистозных яичников, болезнь поликистозных яичников, поликистоз яичников, поликистозные яичники) — синдром, характеризующийся двусторонним увеличением и склерокистозньши изменениями яичников и проявляющийся различными нарушениями менструального цикла на фоне ановуляции, бесплодием, избыточным оволосением,, ожирением.
В 1915 году Я. К. Хачкурузов, а в 1928 году С. К. Лесной наблюдали подобное заболевание и предложили его оперативное лечение. В 1935 году Штейн и Левенталь детально описали клиническую и патоморфологическую картину синдрома, характеризующегося яичниковой гииерандрогенией.
В настоящее время под названием синдрома Штейна — Левенталя объединяют различные по патогенезу состояния, проявляющиеся гипер-андрогенией и склерокистозными или поликистозными изменениями яичников.
Этиология и патогенез
Этиология не известна. Предполагается роль генетических факторов, а также патогенных (гормональных или инфекционных) воздействий в эмбриональном периоде на гипоталамус или яичники плода. Психические травмы, стрессовые ситуации, смена климатогеографической зоны, особенно в пубертатном периоде, могут способствовать развитию Штейна— Левенталя синдрома.
В соответствии с патогенетическими особенностями выделяют три основные формы заболевания: типичную (описанную Штейном и Левенталем), смешанную и центральную. Типичная форма Штейна— Левенталя синдрома характеризуется гиперандрогенией яичникового генеза. В основе ее развития лежит первичный генетически обусловленный энзимный дефект в яичниках на уровне 19-гидроксилазы и (или) 3-бета-ол-дегидрогеназы, в результате чего нарушается биосинтез стероидов в яичниках и повышается уровень андрогенов в организме. При смешанной форме наблюдается гиперандрогения надпочечникового и яичникового происхождения, что обусловлено первичным нарушением функции надпочечников (см.) с вторичным вовлечением в патологический процесс яичников (см.), формированием в них склерокистозных изменений и повышенной секрецией ими андрогенов (см.). Развитие центральной (гипоталамо-гипофизарной) формы Штейна— Левенталя синдрома связано с первичным расстройством функции гипоталамо-гипофизарной системы (см.) вследствие врожденного ее дефекта, острой или хронической инфекции, интоксикации в препубертатном или пубертатном периоде и нарушением секреции гонадотропных гормонов (см.) и моноаминов, особенно дофамина (см. Катехоламины) и серотонина (см.).
В формировании Штейна— Левенталя синдрома гипоталамо-гипофизарная система играет роль пускового механизма (при центральной форме) и (или) поддерживающего (при других формах синдрома). Для Штейна— Левенталя синдрома характерно повышение уровня секреции лютеинизирующего гормона (см.), причем соотношение содержания лютеинизирующего гормона и фолликулостимулирующего гормона (см.), в норме равное 0,5 и обеспечивающее рост и созревание фолликулов, при Штейна— Левенталя синдроме повышается до 1 и более. При подобном нарушении секреции гонадотропных гормонов происходит неадекватная стимуляция функции яичников, нарушение развития в них фолликулов, снижение количества зреющих фолликулов, нарушение синтеза стероидных гормонов (см.),что приводит к ановуляции (см. Ановуляторный цикл). В яичниках происходит гиперплазия мозгового вещества, текаклеток и хидусных клеток, в которых в избытке продуцируются андрогены. В организме увеличивается количество андрогенов (тестостерона, андростендиона), возрастает уровень эстрогенов (см.), синтезируемых из предшественников андрогенов. Между секрецией андрогенов, эстрогенов, пролактина, дофамина и серотонина существует сложная взаимосвязь. Дофамин влияет на циклическую секрецию лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ) гипофиза, действуя непосредственно на люлиберин (см. Гипоталамические нейрогормоны), и подавляет высвобождение пролактина (см.). Серотонин оказывает преимущественно угнетающее действие на высвобождение гонадотропных гормонов гипофиза, что приводит к блокаде овуляции (см.), а также стимулирует продукцию пролактина. Таким образом, дефицит моноаминов (дофамина, серотонина) или нарушение их метаболизма в структурах центральной нервной системы играют существенную роль в патогенезе Штейна— Левенталя синдрома.
Патологическая анатомия
Яичники увеличены, сероватого цвета, гладкие, плотные; на разрезе видны кистозные полости (атретические фолликулы). Микроскопически отмечаются значительное утолщение белочной оболочки, дистрофические и атрофические изменения фолликулов, уменьшение числа примордиальных и увеличение количества кистозно-атретических фолликулов, отсутствие зрелых фолликулов и желтых тел, выявляются фолликулы различной степени зрелости. Выражены склеротические изменения в корковом, мозговом веществе и сосудах яичников, гиперплазия клеток внутренней оболочки фолликулов. В каждом из яичников типичные для Штейна— Левенталя синдрома изменения могут быть неоднородными. При Штейна— Левенталя синдроме размеры матки несколько меньше нормы, в эндометрии отмечаются различные изменения — от атрофии до гиперпластических процессов.
Клиническая картина
Синдром нередко вначале протекает скрыто и клинически проявляется в возрасте 16—30 лет, часто лишь при определенных условиях (хронические инфекции, оперативные вмешательства, начало половой жизни и др.). Иногда симптомы появляются только после беременности и родов.
Основными симптомами являются: бесплодие (см.); нарушения менструального цикла (см.), проявляющиеся либо удлинением продолжительности менструации (полименорея) либо ее укорочением (олигоменорея), либо отсутствием менструации (см. Аменорея), реже кровотечениями во время менструаций (менометроррагия), гирсутизм (см.), ожирение (см.). Наблюдаются также (чаще при центральной форме заболевания) вегето-сосудистые, трофические и обменные расстройства, иногда — расстройства психики в виде депрессии (см. Депрессивные синдромы), агрессивности.
Для типичной формы Штейна— Левенталя синдрома более характерно своевременное наступление первой менструации, нерегулярность менструаций, олигоил и аменорея, реже — ациклические кровотечения (см. Маточные кровотечения), первичное бесплодие. Гирсутизм и ожирение умеренно выражены. Наружные половые органы развиты правильно, матка обычных размеров, яичники увеличены. С помощью тестов функциональной диагностики выявляются признаки ановуляции — однофазная базальная температура, положительный симптом «зрачка», и др. (см. Ановуляторный цикл). Содержание ЛГ в крови увеличено в 1,5—5 раз, ФСГ — в пределах, нормы или ниже ее, соотношение ЛГ и ФСГ равно 1,5—5. Секреция пролактина, дофамина и серотонина не отличается от нормы. Экскреция 17-кетостероидов (см.) и эстрогенов — в пределах нормы или несколько превышает ее. Уровень андростерона, тестостерона (см.), этиохоланолона выше нормы. Проба со стимуляцией яичников хорионическим гонадотропином на фоне торможения функции надпочечников дексаметазоном вызывает повышение уровня андрогенов в организме.
Смешанная форма Штейна— Левенталя синдрома характеризуется более поздним (в 16—18 лет) наступлением первой менструации, нарушениями менструального цикла по типу вторичной аменореи (реже — олигоменореи), первичным бесплодием. Гирсутизм значительно выражен; телосложение приближается к интерсексуальному; подкожный жировой слой развит умеренно и равномерно. Молочные железы и наружные половые органы часто несколько недоразвиты, клитор незначительно увеличен. Матка, как правило, меньше нормы, яичники увеличены. С помощью тестов функциональной диагностики (см. Яичники) выявляют ановуляцию и низкую эстрогенную насыщенность (см. Влагалище). У половины больных отмечается изменение толерантности к глюкозе, у 1/3 больных — увеличение размеров турецкого седла, остеопороз костей черепа, изменения ЭЭГ. Гиперандрогения более выражена — отмечается увеличение экскреции 17-кетостероидов, андростерона, этиохоланолона, дегидроэпиандростерона. Экскреция эстрогенов с мочой снижена. Повышение содержания ЛГ в плазме крови менее выражено, содержание ФСГ снижено, соотношение ЛГ и ФСГ приблизительно 3,2; содержание пролактина в пределах нормы, содержание в крови дофамина и серотонина повышено.
Для центральной формы Штейна— Левенталя синдрома характерны позднее (в 16—20 лет) наступление первой менструации, нарушения менструального цикла но типу олигоменореи или аменореи, реже — ациклических кровотечений, бесплодие, а также вегетососудистые, обменные и трофические расстройства. У больных отмечается чрезмерное отложение жира на груди, животе, бедрах. Наблюдается гипоплазия наружных половых органов, умеренное увеличение яичников, уменьшение размеров матки. На ЭЭГ обнаруживают изменения, свидетельствующие о вовлечении в патологический процесс диэнцефальной области. Содержание ЛГ колеблется в широких пределах (от небольшого повышения до значительного), содержание ФСГ в пределах нормы, соотношение этих гормонов в несколько раз превышает нормальные показатели. Уровень пролактина в пределах или выше нормы, содержание дофамина в организме снижено, серотонина — превышает норму. Гиперандрогения менее выражена. Экскреция 17-кетостероидов и дегидроэпиандростерона в пределах нормы или несколько повышена, экскреция эстрогенов снижена.
Течение и тяжесть патологического процесса определяются выраженностью ферментных нарушений в яичниках, степенью дистрофических изменений в их фолликулярном аппарате, нарушениями в центральных корригирующих системах, компенсаторными возможностями организма.
Для Штейна— Левенталя синдрома характерно развитие гиперпластических процессов в эндометрии, чаще при центральной форме заболевания (аденоматозные полипы эндометрия и рак эндометрия регистрируют в 14—30% случаев). В случаях наступления беременности последняя часто осложняется невынашиванием (см. Невынашивание беременности), поздним токсикозом (см. Токсикозы беременных), внутриутробной гибелью плода (см. Внутриутробная смерть), слабостью родовой деятельности (см. Роды) и кровотечением в родах.
Диагноз
Диагноз основывается на данных анамнеза, клинической картине, данных осмотра, биохимических исследований крови и мочи и инструментального исследования.
При сборе анамнеза следует обратить внимание на нарушения репродуктивной функции у родственников, пожилой возраст родителей, на перенесенные матерью больной во время беременности заболевания, такие как эпидемический паротит, корь, краснуха, а также обострения хронических болезней, например ревматизма, туберкулеза и др.; прием лекарственных средств, в частности синтетических эстрогенгестагенных препаратов, андрогенов, неполноценное или недостаточное питание, воздействие ионизирующего излучения и других неблагоприятных факторов во время беременности.
При осмотре, как правило, отмечается увеличение обоих, редко одного яичника; в ранних стадиях заболевания яичники могут быть нормальных размеров или даже несколько уменьшены — малые склерокистозные яичники. Степень увеличения яичников определяют с помощью пельвиграфии (см.) и ультразвукового сканирования (см. Ультразвуковая диагностика). Ценным диагностическим методом является лапароскопия (см. Перитонеоскопия) с обязательной биопсией (см.) яичников. При постановке диагноза Штейна— Левенталя синдрома определяют количество гонадотропных гормонов в плазме крови, соотношение ЛГ и ФСГ, содержание тестостерона и других андрогенов (д4-андростендиона, дигидротестостерона — ДЭА-сульфата), а также пролактина в крови, характер жирового и углеводного обмена, проводят рентгенологическое исследование черепа и турецкого седла (см. Краниография), электроэнцефалографию (см.). Определение в моче 17-кетостероидов имеет меньшее диагностическое значение, так как они не являются активными андрогенами. Для диагностики Штейна— Левенталя синдрома и уточнения источника гиперандрогении используют функциональные пробы с дексаметазоном (см. Дексаметазоновая проба), прогестинами и преднизолоном, АКТГ и хорионическим гонадотропином.
Дифференциальную диагностику Штейна— Левенталя синдроме проводят с адреногенитальным синдромом (см.), болезнью Иценко — Кушинга (см. Иценко — Кушинга болезнь), гипертекозом (см. Липидоклеточные опухоли), андрогенопродуцирующими опухолями яичников (см.), функциональными или органическими поражениями гипоталамо-гипофизарной системы (см.), с туберкулезом половых органов (см. Туберкулез внелегочный). Для адреногенитального синдрома характерен быстрый рост в детском возрасте, первичная аменорея, мужской тип телосложения, значительно развитый гирсутизм, выраженная гипертрофия клитора, повышение уровня 17-кетостероидов, положительная проба с дексаметазоном. При адреногенитальном синдроме опухолевого генеза учитывают быстрое прогрессирование вирилизации, наличие артериальной гипертензии, обменных нарушений, а также данные оксисупраренографии или компьютерной томографии (см. Томография компьютерная).
При болезни Иценко — Кушинга отмечается повышение уровня АКТГ, кортизола в крови, оксикортикостероидов в крови и моче.
Гипертекоз характеризуется более выраженным гирсутизмом, гиперплазией и лютеинизацией стромы яичника, накоплением в ней липидов, отсутствием кистозно-атретических фолликулов и утолщения белочной оболочки; лечение кломифенцитратом при гипертекозе в отличие от Штейна— Левенталя синдрома неэффективно.
При андрогенопродуцирующей опухоли яичника отмечается поражение, как правило, одного яичника, гипотрофия молочных желез и матки; учитывают также данные, полученные при лапароскопии.
При органических или функциональных поражениях гипоталамо-гипофизарной системы отмечаются нарушения обмена веществ (ожирение), вегетососудистые расстройства, нарушение толерантности к глюкозе, изменения в области турецкого седла, повышение секреции кортизона и его производных.
Туберкулез половых органов подтверждается данными анамнеза, гистеросальпингог рафии (см. Метросальпингография), лапароскопии.
Лечение
Лечение в начальных стадиях, а также при легком течении Штейна— Левенталя синдрома консервативное. Применяют синтетические прогестины, кломифенцитрат, гонадотропины при смешанной форме синдрома кломифенцитрат назначают в сочетании с преднизолоном или дексаметазоном. При центральной форме с целью восстановления функций гипотал амогипофизарной системы назначают также седативные средства, синтетические эстрогенгестагенные препараты в малых дозах (прерывистыми курсами), проводят диетотерапию. При выраженном гирсутизме применяют верошпирон, антиандрогены.
При отсутствии в течение 6—12 месяцев положительного результата от консервативной терапии показано оперативное лечение (исключение составляют больные с центральной формой Штейна— Левенталя синдрома). Задержка оперативного вмешательства нецелесообразна в связи с прогрессированием дистрофических процессов в яичниках, а также опасностью развития опухолевых процессов в эндометрии. Больных лучше оперировать в возрасте до 20 лет; при этом восстановление менструального цикла отмечается в 90—95% случаев, наступление беременности — в 60—65% случаев. Если операция производится в период от 21 до 35 лет, эти цифры соответственно равны 70 и 40%. Перед операцией независимо от формы Штейна— Левенталя синдрома следует произвести выскабливание слизистой оболочки матки (см. Выскабливание) с последующим гистологическим исследованием полученного материала для исключения предракового состояния или рака эндометрия.
Наиболее распространена расширенная клиновидная резекция обоих яичников (см. Яичники, операции), иногда производят их частичную демедулляцию (удаление мозгового слоя яичника). Чаще удаляют 2/3—3/4 объема ткани яичников, в последнее время применяют субтотальную резекцию с максимальным удалением гиперплазированной стромы и щажением коркового вещества. Предполагают, что эффект операции обусловлен уменьшением объема стероидопродуцирующей ткани яичников, в результате чего происходит снижение уровня андрогенов в организме, а также рефлекторным воздействием резецированных яичников на функцию гипоталамуса и гонадотропную функцию гипофиза. Результаты клиновидной резекции яичников зависят от состояния фолликулярного аппарата яичников: количества примордиальных фолликулов, наличия зреющих фолликулов, степени дистрофических изменений в фолликулах, а также от полноты удаления измененной ткани. После операции за больными осуществляют строгое наблюдение. В случае отсутствия эффекта от операции с целью восстановления менструальной и репродуктивной функции назначают заместительную терапию (эстрогены, прогестерон), с целью стимуляции овуляции — гонадотропины, Штейна— Левенталя синдрома, при недостаточности секреторной фазы цикла (во второй фазе цикла) — синтетические прогестины, при смешанной форме Штейна— Левенталя синдрома — преднизолон или дексаметазон в сочетании с кломифенцитратом. При сочетании Штейна— Левенталя синдрома с другими эндокринными заболеваниями проводят комплексное лечение. Больные с Штейна— Левенталя синдромом нуждаются в систематическом наблюдении в связи с опасностью развития у них рака эндометрия.
Прогноз и Профилактика
Прогноз в плане восстановления менструальной и репродуктивной функции при своевременно начатом и правильно проводимом лечении благоприятен.
Профилактика заключается в исключении вредных воздействий во время беременности, в предупреждении стрессовых ситуаций и заболеваний в детском возрасте и пубертатном периоде. Необходимо раннее лечение гиперандрогении яичникового и надпочечникового генеза, а также коррекция нарушений функций гипоталамо-гипофизарной системы.
Библиогр.: Бадоева Ф. С. О восстановлении репродуктивной функции после клиновидной резекции склерокистозных яичников, Акуш. и гинек., № 9, с. 26,1980; Бескровная Н. И. Прогноз у больных с синдромом склерокистозных яичников и тактика их ведения после хирургического лечения, там же, № 10, с. 14, 1982; Б о х м а н Я. В. и др. Онкологические аспекты синдрома склерокистозных яичников, там же, № 2, с. 19; Гинекологическая эндокринология, под ред. К. Н. Жмакина, М., 1980; Ж е-лезнов Б. И. Спорные и неясные вопросы терминологии, морфологии, диагностики и лечения склерокистозных яичников, Акуш. и гинек., № 2, с. 10, 1982; Коренева Г. II., Шикаева Ф. В. и Ефименко Н. Ф. К патогенезу синдрома склерокистозных яичников, там же, с. 21; Крымская М. JI. Синдром склерокистозных яичников, там же, № 9, с. 53, 1980; Савельева Г. М. и Б о г и н с к а я JI. Н. Значение лапароскопии в диагностике склерокистозных яичников, там же, № 10, с. 17, 1982; Савельева Г. М. и Серов В. Н. Предрак эндометрия, М., 1980; Baird D. Т. а. о. Pituitary-ovarian relationships in polycystic ovary syndrome, J. clin. Endocr., v. 45, p. 798, 1977; Buvat J. et Buvat-Her-b a u t M- Traitement du syndrome des ovaries polykystiques, Nouv. Presse med., t. 10, p. 2019, 1981; Goldzieher J. W. Polycystic ovarian disease, Fertil. and Steril., v. 35, p. 371, 1981; Judd H. L. Endocrinology of polycystic ovarian disease, Clin. Obstet. Gynec., v. 21, p. 99, 1978; Lindsay A. N., Voorhess M. L. a. Me Giiliv-r а у М. H. Multicystic ovaries detected by sonography, Amer. J. Dis. Child., v. 134, p. 588, 1980; Quigley М. E., Rakoff J. S. a. Yen S. S. Increased luteinizing hormone sensitivity to dopamine inhibition in polycystic ovary syndrome, J. clin. Endocr., v. 52, p. 231, 1981; Stein I. E. a. Leventhal M. L. Amenorrhea associated with bilateral polycystic ovaries, Amer. J. Obstet. Gynec., v. 29, p. 481, 1935; Wortsman J., Singh К. B. a. Murphy j. Evidence for the hypothalamic origin of the polycystic ovary syndrome, Obstet, and Gynec., v. 58, p. 137, 1981; Yen S. S. The polycystic ovary syndrome, Clin. Endocr., v. 12, p. 177, 1980.
В. И. Алипов.
Источник
