Статьи о синдроме диабетической стопы
Дата обновления: 2019-05-14

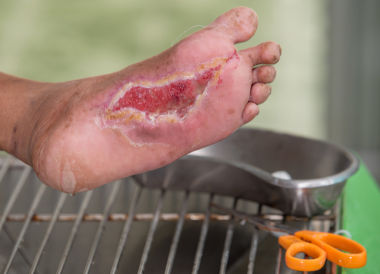
Диабетическая стопа (синдром диабетической стопы, англ. diabeticfoot) — это общее понятие группы поздних осложнений декомпенсированного сахарного диабета, когда происходят микроциркуляторные и нейротрофические изменения в дистальных отделах нижних конечностей, ведущих к гнойно-язвенно-некротическим процессам кожи, мягких тканей и костно-суставным поражениям. В Международном соглашении по диабетической стопе в 2000 году было принято определение «синдрома диабетической стопы» как комплекса анатомо-функциональных изменений стопы у больного сахарным диабетом, связанного с диабетической нейропатией, ангиопатией, остеоартропатией, переходящих в гнойно-некротические процессы.

При сахарном диабете возможны нарушения нормального кровоснабжения и нервной регуляции ног, что предопределено сбоями функционирования сосудистой (поражения артерий нижних конечностей, склероз Менкеберга) и нервной (нейропатии) систем. Процесс бывает отягощенным из-за воздействия какой-либо инфекции. Из этих составляющих и складывается основа синдрома диабетической стопы. Тяжелое течение данного заболевания может закончиться гангреной и ампутацией конечностей. Чаще всего синдром развивается после 15-20 лет заболевания сахарным диабетом у 10% пациентов, 40-50% больных диабетом находятся в группе риска с угрозой лишиться ног, до 90% пациентов, имеющих диабетическую стопу, больны сахарным диабетом второго типа.
Классификация форм диабетической стопы
В зависимости от тяжести течения синдрома диабетической стопы определяют стадии:
- 0 — высокий риск развития диабетической стопы при наличии её деформации, мозолей, гиперкератоза и отсутствия язвенных дефектов;
- 1 — стадия поверхностной язвы в пределах кожных покровов;
- 2 — стадия глубокой язвы на коже с вовлечением подкожно-жировой клетчатки, мышечной ткани, сухожилий и без поражения костей;
- 3 — стадия глубокой язвы с поражением костных тканей;
- 4 — стадия ограниченной гангрены;
- 5 — стадия обширной гангрены.
Отталкиваясь от преимущественного наличия какого-либо из патологических компонентов, определяют ишемическую (5-10%), нейропатическую (60-75%) и смешанную — нейро-ишемическую (20-30%) форму диабетической стопы:
Ишемическая (нейроишемическая) форма диабетической стопы развивается на фоне диабетической ангиопатии и характеризуется нарушением кровоснабжения конечностей в связи с поражениями крупных и мелких сосудов атеросклерозом, развивающимся у больных сахарным диабетом намного быстрее, чем других людей. Течение ишемической формы подчеркивается стойким отёком, перемежающей хромотой, постоянными болями и усталостью в ногах, посинением кожи конечностей. Стопы и голени холодеют, при запущенности заболевания появляются язвы, некроз края пятки или пальцев стопы.
Нейропатическая форма диабетической стопы имеет три вида:
- нейропатическая язва;
- остеоартропатия (сустав Шарко);
- нейропатический отёк.
Нейропатическая форма развивается при поражении нервного аппарата дистальных отделов конечностей на фоне диабетической полиневропатии. Первые сигналы заболевания появляются в местах наибольшего нажима на стопу при нагрузках. Впоследствии при длительном течении нейропатии стопа деформируется, и точка опоры переносится на определённые её участки, где кожа утолщается, а позже образовывается язва.
При таких обстоятельствах больной ощущает частичное онемение конечности, жжение и «мурашки». Через какое-то время чувствительность ноги снижается настолько, что человек не ощущает появление язвы. По той же причине нечувствительности человек не в состоянии отреагировать на травмирующие термические или механические факторы, что сильнее усугубляет разрушительный процесс, к которому легко присоединяется инфекция.
Предрасположенность больных сахарным диабетом к переломам костей и другим костным изменениям часто ведёт к развитию остеоартропатической формы или сустава Шарко, поражающего, как правило, коленный сустав. Возникает остеоартропатия в результате малозначительных травм, получение которых пациент не ощущает, затем сустав опухает и с течением времени деформируется.
При нейропатической форме синдрома развивается нейропатический отёк (накопление жидкости в подкожных тканях), который осложняет нездоровые процессы стоп.
Классификация диабетической остеоартропатии:
- стадия 1 — наличие отёка стопы, гипертермии и гиперемии;
- стадия 2 — развитие деформации стопы (под рентгеном видны костные изменения — остеопороз, костная деструкция, фрагментация костных структур);
- стадия 3 — чёткая выраженность деформации стопы, спонтанных переломов и вывихов;
- стадия 4 — образование язв, при инфицировании опасность быстрого развития гангрены.
Смешанная форма диабетической стопы в равной степени отражает признаки ишемической и нейропатической формы.
Прогноз и профилактика диабетической стопы
Профилактические меры для предотвращения развития диабетической стопы:
- тщательное соблюдение правил ухода за ногами и ежедневный осмотр стоп с целью обнаружения изменений;
- регулярный контроль уровня глюкозы в крови в домашних условиях;
- постоянное наблюдение у диабетолога и подиатра;
- соблюдение диеты и схемы приема лекарств;
- отказ от тесной обуви в пользу ортопедических стелек и обуви;
- упражнений для стоп;
- опаска травмирования ног.
Для составления прогноза должен учитываться целый комплекс факторов, включая адекватность лечения, стаж заболевания диабетом и сопутствующие недуги.
Причины развития диабетической стопы
Основными элементами патогенеза синдрома диабетической стопы выступают ангиопатия, нейропатия и инфекция.
Некорригируемая гипергликемия на протяжении длительного периода при сахарном диабете приводит к специфическимизменениям сосудов (диабетической макроангиопатии и микроангиопатии) и периферических нервов (диабетической нейропатии).
Ангиопатии вызывают снижение эластичности и проходимости кровеносных сосудов, повышение вязкости крови, что нарушает иннервацию и нормальную трофику тканей, а также ведёт к потере чувствительности нервных окончаний ног.
Повышенное гликозилирование пептидов снижает подвижность суставов, это объединяется с деформацией костей конечности и вызывает нарушение нормальной биомеханической нагрузки на стопу (диабетическая остеоартропатия или стопа Шарко). При измененном кровообращении, снижении чувствительности и защитной функции тканей каждая незначительная травма стопы (ушиб, потертость, трещинка, микропорез) превращается в длительно незаживающие трофические язвы, которые нередко инфицируются стафилококками, колибактериями, стрептококками, анаэробной микрофлорой.
Различные бактериальные группы ферментов разрыхляют окружающие ткани, распространяя инфекцию и некротизацию на подкожно-жировую клетчатку, мышечную ткань, костно-связочный аппарат и повышая риск развития абсцесса, флегмоны и гангрены конечности.
Невзирая на то, что потенциальная угроза формирования диабетической стопы существует у всех больных сахарным диабетом, к группе наибольшего риска относятся пациенты с:
- периферической полинейропатией;
- атеросклерозом сосудов;
- аномальным содержанием липидов в крови;
- ишемической болезнью сердца;
- артериальной гипертензией;
- лица, злоупотребляющие алкоголем и курением.
Повышенным риском развития диабетической стопы при сахарном диабете угрожают очаговые изменения тканей стоп:
- вросший ноготь;
- грибковые поражения ногтей;
- микозы кожи;
- натоптыши и мозоли;
- трещины пяток;
- недостаточная гигиена ног.
Причиной появления вышеуказанных дефектов может быть неправильно подобранная обувь — слишком тесная, узкая или сильно разношенная, не плотно сидящая на ногах. Потеря чувствительности конечностей не позволяет больному ощутить, что неподходящая обувь травмирует стопу.
Симптомы диабетической стопы
У такого заболевания, как диабетическая стопа, симптомы зависят от причины синдрома (нарушение кровоснабжения или повреждение нервов).
При поражении нервов конечностей:
- язвы, образующиеся в местах повышенного давления на стопу (подошва, пальцы) безболезненны и сопровождаются выраженным утолщением эпидермиса стопы (омозолелостью);
- снижение вибрационной, болевой и температурной чувствительности стоп;
- розовость и теплота кожи стоп;
- пульсация на артериях конечностей сохранена.
При преимущественном поражении костей и суставов:
- покраснение и отёк стопы;
- позднее —деформация костей стопы, плоскостопие;
- частые спонтанные переломы костей ног.
При сочетанном поражении артерий и нервов:
- выраженные постоянные боли в области пораженной стопы, уменьшающиеся при свешивании ног с постели;
- сухость, бледность или синюшность, холодность кожи ног;
- язва в области кончиков пальцев, пяток при тяжелом нарушении кровообращения.
Признаки нейропатической стопы:
- сухость кожи конечностей;
- гиперкератозы (ороговение эпидермиса);
- ангидроз конечностей;
- снижение всех видов чувствительности (тепловой, болевой, тактильной и прочих);
- деформации костей стопы;
- плоскостопие;
- спонтанные переломы.
Любые из вышеперечисленных симптомов обязывают больного сахарным диабетом срочно обратиться к врачу-эндокринологу. Промедление может привести к ампутации ноги или летальному исходу.
Обнаружили симптомы данного заболевания?
Звоните
Наши специалисты проконсультируют Вас!
Диагностика диабетической стопы
Диагностировать синдром диабетической стопы следует обязательно. Пациенты с высоким риском развития диабетической стопы должны наблюдаться не только у эндокринолога-диабетолога, но также врача-подолога, сосудистого хирурга, ортопеда. Важна роль самообследования по обнаружению изменений, характерных для диабетической стопы: изменение цвета кожи, появление сухости, отечности и боли, искривления пальцев, грибковых поражений и пр.
Диагностика диабетической стопы предполагает сбор анамнеза с уточнением стажа заболевания сахарным диабетом, осмотр стоп, определение лодыжечно-плечевого индекса и рефлексов, оценку всех видов чувствительности.
Применяются методы диагностики:
- неврологическое исследование чувствительности (вибрационной, температурной);
- УЗИ с доплерографией, с измерением артериального давления в артериях голени для оценки кровотока в стопе;
- ангиография — для исследования состояния сосудов стопы;
- периферическая КТ-артериография;
- УЗДГ сосудов нижних конечностей;
- Транскутанная оксиметрия — для определения состояния тканевого кровоснабжения;
- денситометрия (вид рентгенологического исследования) для определения наличия остеопороза и минеральной плотности костной ткани;
- гликемический профиль — для определения суточного уровня сахара в крови, гликолизированного гемоглобина, холестерина, липопротеидов;
- анализ мочи на сахар и кетоновые тела;
- рентгенография стоп в двух проекциях;v
- ультразвуковое сканирование кости для выявления переломов при большой отечности;
- общий анализ крови;
- бактериологический посев крови;
- тщательное изучение содержимого дна, краев язв и его бактериологический посев на микрофлору.
Изучив результаты диагностики при диагнозе «диабетическая стопа», врач назначает адекватное лечение.
Лечение диабетической стопы
Подход к терапии больных с диабетической стопой должен быть мультидисциплинарным и объединять специалистов различных профилей: эндокринолога-диабетолога, хирурга (сосудистая и гнойная хирургия), ортопеда-подиатра, психолога, терапевта, анестезиолога—реаниматолога совместно с подготовленным средним медицинским персоналом.
Лечение диабетической стопы имеет основную тактику:
- коррекция углеводного обмена и артериального давления;
- разгрузка пораженной конечности;
- местная обработка ран/язв;
- системная медикаментозная терапия;
- при неэффективности консервативной терапии — хирургическое лечение.
С целью оптимизации уровня гликемии при сахарном диабете 1 типа производится корректировка дозы инсулина; при диабете 2 типа — перевод пациента на инсулинотерапию.
Для нормализации артериального давления применяются β—блокаторы, ингибиторы АПФ, антагонисты кальция, диуретики.
При гнойно-некротических поражениях (особенно при нейропатической форме синдрома) следует обеспечить разгрузку пораженной конечности, ограничив её движения применение костылей или кресла-каталки, специальных ортопедических приспособлений, стелек или обуви.
При диагнозе «диабетическая стопа» лечение язвенных поражений необходимо производить систематически, обрабатывая раны, иссекая некротизированные ткани, делая перевязки с использованием антибактериальных и антисептических средств. Также язву необходимо освобождать от окружающих мозолей, натоптышей, участков гиперкератозов для снижения нагрузки на пораженный участок.
Терапия антибиотиками широкого спектра противомикробного действия при синдроме диабетической стопы проводится системно.
Консервативная терапия диабетической стопы предусматривает применение препаратовa—липоевой кислоты, спазмолитиков (дротаверина, папаверина), актовегина, инфузии растворов.
При тяжелых поражениях нижних конечностей, когда консервативное лечение бессильно помочь, требуется хирургическое лечение.
При ишемической форме диабетической стопы применяется:
- эндоваскулярная дилатация и стентирование периферических артерий;
- тромбоэмболэктомия;
- пластическое закрытие больших раневых повреждений —аутодермопластика;
- аутовенозное шунтирование;
- артериализация вен стопы, стентирование артерий нижних конечностей и др.
При необходимости применяется дренирование глубоких гнойных очагов —абсцессов, флегмон. При гангрене и остеомиелите высок риск ампутации/экзартикуляции пальцев или стопы.
Данная статья размещена исключительно с целью ознакомления в познавательных целях и не является научным материалом
или профессиональным медицинским советом. За диагностикой и лечением обратитесь к врачу.
Источник
 Для цитирования. Кисляков В.А., Оболенский В.Н., Юсупов И.А. Синдром диабетической стопы: комплексный подход к лечению // РМЖ. 2015. No 12. С. 768–770.
Для цитирования. Кисляков В.А., Оболенский В.Н., Юсупов И.А. Синдром диабетической стопы: комплексный подход к лечению // РМЖ. 2015. No 12. С. 768–770.
Распространенность и экономические аспекты
В XXI в. сахарный диабет (СД) стал ведущим неинфекционным заболеванием. Каждые 10 с в мире становится на 2 больных СД больше – это 7 млн в год. По мнению экспертов Всемирной организации здравоохранения, СД занимает 1-е место среди заболеваний, приводящих к инвалидности, и 3-е – по смертности [1–4].
Согласно исследованиям Эндокринологического научного центра (ЭНЦ), в России распространенность СД достигает 10–12 млн человек (7–8% населения страны). Наиболее высокая распространенность СД среди взрослого населения крупных городов. При этом соотношение мужчин и женщин – 1:3. В половине случаев СД 2-го типа выявляется на 5–7-м году от начала заболевания, и у 20–30% выявляются специфические осложнения: катаракта, ретинопатия, нефропатия, нейропатия, синдром диабетической стопы (СДС), ишемическая болезнь сердца, артериальная гипертония и др. [5–8].
СДС приводит к гнойно-некротическим поражениям стоп с последующей потерей нижних конечностей – к самой высокой инвалидизации. Окончательные цифры распространенности СДС в настоящее время неизвестны. Тем не менее установлено, что у 15% больных СД развиваются патологические изменения в стопах или голеностопном суставе [9–13].
В последние годы широко обсуждаются не только клинические, но и экономические, социальные аспекты профилактики и лечения СДС, методы клинико-экономического анализа и, прежде всего, учет всех затрат, связанных с лечением СДС [1, 14].
На 18-м конгрессе Международной федерации диабета (МФД) были представлены, в частности, данные о распространенности язвенных дефектов при СДС в странах Балканского региона – 7,5%. Диагноз СД впервые ставится во время хирургического вмешательства у 15–19% больных, подвергающихся ампутации. Специалисты МФД считают, что вероятная частота ампутаций при СД составляет 5–24 на 100 000 населения в год, или 6–8 на 1000 больных в год, а в эпидемиологически неблагоприятных регионах достигает 24 на 1000 больных в год. В России, согласно данным государственного регистра, эти показатели колеблются от 0,76 до 18,2 и в среднем составляют 6,4 случая на 1000 больных [3, 4, 11, 15].
Расходы на лечение СДС в развитых странах составляют около 12–15% от всех затрат на лечение СД, в развивающихся странах они могут составлять до 40% от общего объема финансовых ресурсов, выделяемых на СД. Подсчитано, что на проведение одной ампутации в зарубежных странах тратится более 10 000 долл. Общие затраты на лечение СДС в среднем составляют 13 179 долл. и меняются в зависимости от степени тяжести по классификации Wagner в пределах от 1892 долл. при I степени до 27 721 долл. при IV–V степени тяжести. Лечение СДС на фоне хронической артериальной недостаточности нижних конечностей обходится в 4,5 раза дороже, чем при сохранном периферическом кровотоке. Ежегодная стоимость лечения язвенных поражений стоп при СДС в США составляет 5 млрд долл. прямых медицинских затрат и 400 млн долл. косвенных медицинских затрат. Кроме того, в США зафиксировали, что 77% людей старше 75 лет после ампутации не способны вернуться в собственный дом и им нужна дополнительная помощь и поддержка социальных групп [8, 16–18].
Анализ работы отделения диабетической стопы ЭНЦ показал, что при своевременно начатой адекватной терапии СДС понижается риск хирургических вмешательств и тяжелых осложнений: у 98% больных с нейропатической инфицированной формой СДС можно избежать хирургического вмешательства; у 60% с нейроишемической формой – проведения ампутаций на уровне голени и бедра; у 25% с критической ишемией – предотвратить высокие ампутации на уровне бедра; на 50% уменьшить частоту образования язв стоп в группе высокого риска [4, 5, 13].
Летальность среди больных СД, перенесших высокую ампутацию конечности по поводу гангрены, в течение последующих 5 лет достигает 68%, в ближайшие 3 нед. – 22%, в течение года – 11–41%, через 3 года – 20–50%, через 5 лет – от 39–68%. Частота ипсилатеральных ампутаций через год после первой ампутации – до 24%, через 2 года – 30%, через 5 лет – 49% и контралатеральных ампутаций через год после первой ампутации – до 12%, через 2 года – 23%, через 5 лет – 28-51%. Рецидивы язв на стопах через 1, 3, 5 лет составили 44, 61, 70% соответственно. Рецидивирующие деструктивные поражения ухудшают проблемы лечения, реабилитации, социальной помощи, увеличивая экономические затраты [19–23].
Если распространенность СД, а соответственно и СДС будет увеличиваться с той же скоростью, что и сейчас, то к 2025 г. экономический ущерб составит от 213 до 396 млрд долл. в год. 75% прироста заболевания придутся на развивающиеся страны. По данным немецких исследователей, общая стоимость лечения больных СД в Германии составляет приблизительно 5 млрд. евро, а средняя стоимость лечения 1 пациента – 5000 евро в год. Ежегодные общие затраты в России на лечение нейроишемической формы СДС составляют 56,2 млн долл., при этом затраты на ампутации достигают 14,4 млн долл. [2, 5, 17].
По оценке главного экономиста Morgan Stanley Эльги Бартш, сочетание двух факторов – СД и ожирения – снизит среднегодовые темпы роста валового внутреннего продукта (ВВП) в странах Организации экономического сотрудничества и развития (ОЭСР) в 2015–2035 гг. с 2,3 до 1,8%, в странах БРИКС (Бразилия, Россия, Индия, Китай, Южно-Африканская Республика) – с 4,5 до 4,2%. Согласно прогнозам ОЭСР, среднегодовые темпы роста ВВП России составят 2,8%. При сохранении нынешнего уровня потребления сахара гражданами страны этот показатель снизится до 2%. Согласно результатам исследования, проведенного фармацевтической компанией «Ново Нордиск», «Инвестиции в лечение сахарного диабета в России», ежегодные прямые затраты, связанные с СД в России, составляют 12,5 млрд долл. США. При этом 42% объема этих средств расходуется на лечение осложнений, которые выявляются у 40–50% людей в момент постановки диагноза. Соответственно диагностика заболевания на ранних стадиях позволит российскому обществу сэкономить более 1,5 млрд долл. США из средств, выделяемых на здравоохранение [13].
Принципы терапии
По мнению большинства авторов, в лечении пациентов с синдромом диабетической стопы должны участвовать квалифицированные эндокринолог, гнойный хирург, сосудистый хирург, ортопед, специально обученный средний медицинский персонал, а комплексное лечение должно включать общие и местные методы (рис. 1) [24–26].
Тактика комплексного лечения зависит от формы заболевания [14, 15, 18, 19, 21, 27]. Мы, как и ряд специалистов, выделяем следующие клинические формы СДС.
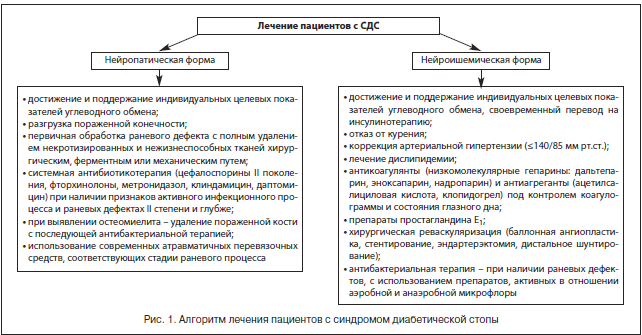
1. Нейропатическая форма:
– без остеоартропатии;
– с остеоартропатией – «сустав Шарко».
2. Нейроишемическая форма с учетом других характеристик.
К общим принципам терапии пациентов с СДС относятся коррекция факторов риска, компенсация углеводного обмена и поддержание целевых показателей углеводного обмена, компенсация сопутствующих заболеваний, системная антибактериальная, антитромботическая, вазопротекторная терапия в сочетании с адекватным обезболиванием.
К местным принципам лечения относятся: обеспечение полной разгрузки пораженной области с помощью разгрузочного полубашмака, индивидуальной разгрузочной повязки, костыля, сложной ортопедической обуви, кресла-каталки; контроль раневой инфекции, заключающийся в первичной обработке раны и местном лечении раны с правильным выбором повязки в зависимости от фазы течения раневого процесса; хирургическое лечение гнойно-некротического очага стопы с закрытием ран и/или формированием культи пораженной стопы при помощи реконструктивных и пластических операций; восстановление магистрального артериального кровотока в сосудах нижних конечностей.
Перспективным является применение L-лизина эсцината в комплексном лечении язвенных и гнойно-некротических поражений при СДС. Эффективность препарата объясняется его противоотечным действием, связанным со снижением проницаемости сосудистой стенки и улучшением венозного оттока. L-лизина эсцинат обладает стабилизирующим действием на мембраны клеток, снижает активность лизосомальных ферментов, принимающих непосредственное участие в воспалительном процессе. Кроме того, препарат блокирует эффекты фосфолипазы А2, которая является ключевым веществом в развитии воспалительной реакции, связанной с повреждением мембран клеток различными факторами при ишемии, инфекции и травме. Стабилизация фосфолипазы А2 способствует снижению активности простагландинов, что также приводит к уменьшению воспалительного ответа. Доказано также влияние L-лизина эсцината на такие медиаторы воспаления, как гистамин, серотонин, которые выделяются из тромбоцитов, тучных клеток и создают основу для классической воспалительной реакции. Комплексный эффект препарата L-лизина эсцината апробирован в нейрохирургической, неврологической, травматологической практике, ангиологии и флебологии [26–31].
Мы регулярно применяем L-лизина эсцинат по 10 мл в разведении на 50 мл физиологического (0,9%) раствора внутривенно капельно в течение 10 дней у пациентов с нейропатической формой СДС в послеоперационном периоде, с трофическими язвами на фоне нейропатических отеков и у больных с язвами на фоне венозной недостаточности (СЕАР 2-3). Отмечаем благоприятное течение послеоперационного периода, более раннее уменьшение отеков, снижение болевого синдрома, нейропатических болей, заживление язв. Рекомендуем применение L-лизина эсцината для лечения язвенных и гнойно-некротических поражений при СДС в амбулаторной и стационарной практике.
Заключение
СД является серьезным заболеванием, способным привести к тяжелым социально-экономическим и демографическим последствиям. Вопрос о влиянии СДС на качество жизни остается малоизученным. Неизвестны долговременные затраты, связанные с лечением рецидивов язв, проведением повторных ампутаций и увеличением расходов на социальное обслуживание. Кроме того, неучтенными остаются непрямые затраты вследствие утраты человеком из-за болезни профессиональных и социальных функций, что наносит обществу материальный и духовный ущерб.
Опыт других стран, например США, показал, что мультидисциплинарный подход, ранняя диагностика и обучение больных позволяют снизить количество язв стопы и ампутаций на 49–85% и существенно уменьшить расходы государства. Использование программ по профилактике осложнений и обучению больных СД приводит к уменьшению количества ампутаций почти в 2 раза, а экономический эффект от внедрения программ обучения составил 10 млн долл. [2, 5, 9, 11, 13, 21].
Учитывая вышеизложенное, 20 апреля 2015 г. в Кремле Президент РФ Владимир Путин подписал Закон о ратификации соглашения о сотрудничестве стран СНГ в борьбе с ростом заболеваемости сахарным диабетом [18], что в сочетании с грамотным ведением пациентов с СДС может улучшить прогноз как для этих пациентов, так и для больных СД в целом.
Источник
