Танатоформная дисплазия код мкб

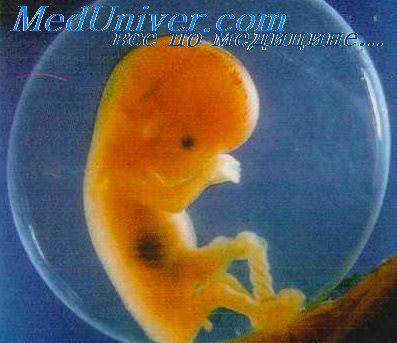
Танатофорная дисплазия. Диагностика и прогноз танатоформной дисплазииТанатофорная дисплазия является летальной формой хондродисплазии, которая характеризуется укорочением конечностей и подразделяется на два типа. Синонимы. Танатофорный нанизм.
Этиология. Возможно, аутосомно-доминантное наследование. Однако большинство случаев возникает в результате новых мутаций гена FGFR3. Диагностика. Эхографический диагноз может устанавливаться на основании обнаружения нанизма, обусловленного короткими конечностями, гипоплазии грудной клетки, формы черепа в виде «трилистника», выступающего лба и поперечной («обезьяньей») складки ладони. Искривление бедренных костей, узкая грудная клетка, относительно большой размер головы, даже без вентрикуломегалии, и впечатление избыточности мягких тканей являются признаками, которые становятся более заметными по мере роста и развития плода, но могут еще отсутствовать во втором триместре беременности. В 70% случаев танатофорная дисплазия сочетается с многоводием, которое может быть значительно выражено и приводить к преждевременным родам. Маловероятно, что заболевание влияет на двигательную активность плода, однако имеются сообщения о снижении его шевелений в третьем триместре. Уменьшение сжимательных движений кисти, возможно, обусловливает развитие поперечной складки ладони. При отсутствии формы черепа в виде «трилистника» заболевание должно предполагаться на основании выявления тяжелой формы ризомелического нанизма и узкой грудной клетки. Измерение длины бедренной кости у плода с помощью эхографии, особенно с оценкой отношения ее длины к бипариетальному размеру, является надежным методом идентификации некоторых форм скелетных дисплазий, сопровождающихся укорочением конечностей, а также танатофорной дисплазий. Сочетанные аномалии. Форма черепа в виде «трилистника» (обнаруживается только при типе II), подковообразная почка, гидронефроз, дефекты межпредсердной перегородки, аномалии развития трикуспидального клапана, неперфорированный анус, локтелучевой синостоз. Дифференциальный диагноз. Хондроэктодермальная дисплазия (синдром Эллис-ван-Кревельда (Ellis-van-Creveld)), асфиксическая дисплазия грудной клетки, синдромы коротких ребр – полидактилии, а также гомозиготная ахондроплазия. Следует рассматривать все виды нанизма с короткими конечностями. При подозрении на наличие II типа необходимо исключить состояния, сопровождающиеся краниосиностозами и формой черепа в виде «трилистника» (синдрома Апера (Apert), Крузона (Crouzon), Пфайффера (Pfieiffer), Карпентара (Carpenter) и Kleeblattschadel). Прогноз. Данное заболевание неизменно летально, и новорожденные умирают вскоре после рождения. Причиной гибели является дыхательная недостаточность вследствие гипоплазии легких. Видео ЭхоКГ при дисплазии трикуспидального клапана у плода– Также рекомендуем “Синдромы тромбоцитопении. Синдром аплазии лучевой кости” Оглавление темы “Врожденные синдромы плода”: |
Источник
Thanatophoric dysplasia (thanatophoric dwarfism) is a severe skeletal disorder characterized by a disproportionately small ribcage, extremely short limbs and folds of extra skin on the arms and legs.
Symptoms[edit]
Infants with this condition have disproportionately short arms and legs with extra folds of skin. Other signs of the disorder include a narrow chest, small ribs, underdeveloped lungs, and an enlarged head with a large forehead and prominent, wide-spaced eyes.
Thanatophoric dysplasia is a lethal skeletal dysplasia divided into two subtypes. Type I is characterized by extreme rhizomelia, bowed long bones, narrow thorax, a relatively large head, normal trunk length and absent cloverleaf skull. The spine shows platyspondyly, the cranium has a short base, and, frequently, the foramen magnum is decreased in size. The forehead is prominent, and hypertelorism and a saddle nose may be present. Hands and feet are normal, but fingers are short. Type II is characterized by short, straight long bones and cloverleaf skull.[1]
It presents with typical telephone-handle shaped long bones and H-shaped vertebrae.[citation needed]
Causes[edit]
It can be associated with missense mutations in fibroblast growth factor receptor-3. It is inherited in an autosomal dominant manner.[2][3]
Diagnosis[edit]
Classification[edit]
Infants with type 1 thanatophoric dysplasia also have curved thigh bones, flattened bones of the spine (platyspondyly) and shortened thoracic ribs. Note: Prenatal ultra-sound images of the ribs sometimes appear asymmetrical when in fact they are not. In certain cases, this has caused a misdiagnosis of Osteogenisis Imperfecta (OI) type II.
An unusual head shape called kleeblattschädel (“cloverleaf skull”) can be seen with type 2 thanatophoric dysplasia.[4]
Prognosis[edit]
The term thanatophoric is Greek for “death bearing”. Children with this condition are usually stillborn or die shortly after birth from respiratory failure. A small number have survived into childhood, and a very few beyond. Survivors have difficulty breathing on their own and require respiratory support such as high flow oxygen through a canula or ventilator support via tracheostomy. There may also be evidence of spinal stenosis and seizures.
The oldest known living TD survivor as of 2013 was a 29-year-old woman.[5] One man lived to be 26 years old. Another man lived to age 20. It was reported in 1998 that a 21 year old man with the condition lives in the United States, while two children with TD aged 10 and 12, a boy and a girl, were known in Germany. There was also a 6-year-old boy living with TD and two 1-year old boys.[6] As of 2020 Christopher Álvarez, 23, is a Colombian living with TD in New York City.[7]
Incidence[edit]
This condition affects about 1 in 60,000 births.[8][failed verification]
References[edit]
- ^ Norris, Cheryl D., George Tiller, Philippe Jeanty, Srini Malini (2008-12-12). “Thanatophoric dysplasia in monozygotic twins”. TheFetus.net. Archived from the original on December 12, 2008. Retrieved 2016-03-01.
- ^ Bonaventure J, Gibbs L, Horne WC, Baron R (2007). “The localization of FGFR3 mutations causing thanatophoric dysplasia type I differentially affects phosphorylation, processing and ubiquitylation of the receptor”. FEBS J. 274 (12): 3078–93. doi:10.1111/j.1742-4658.2007.05835.x. PMID 17509076.
- ^ Lievens PM, Liboi E (2003). “The thanatophoric dysplasia type II mutation hampers complete maturation of fibroblast growth factor receptor 3 (FGFR3), which activates signal transducer and activator of transcription 1 (STAT1) from the endoplasmic reticulum”. J. Biol. Chem. 278 (19): 17344–9. doi:10.1074/jbc.M212710200. PMID 12624096.
- ^ Norman AM, Rimmer S, Landy S, Donnai D (1992). “Thanatophoric dysplasia of the straight-bone type (type 2)”. Clin. Dysmorphol. 1 (2): 115–20. doi:10.1097/00019605-199204000-00008. PMID 1345514.
- ^ Nikkel, Sarah M.; Major, Nathalie; King, W. James (2013-12-01). “Growth and development in thanatophoric dysplasia – an update 25 years later”. Clinical Case Reports. 1 (2): 75–78. doi:10.1002/ccr3.29. ISSN 2050-0904. PMC 4184754. PMID 25356217.
- ^ Baker, K. M.; Olson, D. S.; Harding, C. O.; Pauli, R. M. (1997). “Long-term survival in typical thanatophoric dysplasia type 1”. American Journal of Medical Genetics. 70 (4): 427–436. doi:10.1002/(SICI)1096-8628(19970627)70:4<427::AID-AJMG18>3.0.CO;2-J. PMID 9182787.
- ^ “TheyWantca Instagram”. www.instagram.com. December 30, 2020.
- ^ Vajo, Zoltan; Francomano CA; Wilkin DJ (2000). “The molecular and genetic basis of fibroblast growth factor receptor 3 disorders: the achondroplasia family of skeletal dysplasias, Muenke craniosynostosis, and Crouzon syndrome with acanthosis nigricans”. Endocr. Rev. 21 (1): 23–39. doi:10.1210/er.21.1.23. PMID 10696568.
External links[edit]
- GeneReview/NCBI/NIH/UW entry on Thanatophoric Dysplasia
- Thanatophoric dysplasia at NLM Genetics Home Reference
Источник
Танатофорная дисплазия у плода. Причины и частота танатоформной дисплазии
P.L. Tavormina et al. обнаружили новую миссенс-мутацию гена FGFR3 у четырех пациентов со скелетными дисплазиями, не состоящих в родстве, которая по тяжести клинических проявлений приближалась к танатофорной дисплазии I типа. У трех из них начиная с раннего детства отмечалось появление областей выраженной гиперпигментации кожи, характерной для черного акантоза (acanthosis nigricans).
Все они страдали тяжелыми неврологическими нарушениями и начиная с периода позднего детства обходились без длительного применения средств для жизнеобеспечения. При мутации гена FGFR3 (А1949Т : Lys650Met) происходит замена нуклеотида, расположенного рядом с тем нуклеотидом, замена которого возникает при танатофорной дисплазии II типа (A1948G : Lys650Glu) и вызывает изменения в аминокислотной последовательности белка, когда лизин в позиции 650 заменяется двумя разными аминокислотами.
Авторы обозначили фенотип, вызываемый мутацией (A1948G : Lys650Met), как «тяжелая ахондроплазия, связанная с задержкой развития и черным акантозом», поскольку данное состояние имело значительные отличия от фенотипов при других известных мутациях FGFR3.
Это состояние сопровождается тяжелыми нарушениями энхондрального окостенения, которые в значительной степени аналогичны тем, которые наблюдаются при танатофорной дисплазии I типа. Кроме этого отмечаются редко встречающиеся деформации костей, такие как искривление бедренной кости с обратным расположением ее оси (то есть с формированием заднего апекса), искривления больше- и малоберцовых костей и искривление ключицы в виде «бараньего рога» (ram’s horn).

В дополнение к скелетным аномалиям у выживших пациентов с данным заболеванием присутствуют прогрессирующий черный акантоз, аномалии центральной нервной системы, судороги и тяжелое отставание в развитии. Однако при этом состоянии не наблюдается форма черепа в виде «трилистника» (cloverleaf) или краниосиностозы.
Танатофорная дисплазия является наиболее часто встречающейся летальной скелетной дисплазией у плодов и новорожденных. Она характеризуется выраженной ризомелией конечностей в сочетании с нормальной длиной туловища, узкой грудной клеткой и большой головой с выступающим лбом.
Частота ее распространенности составляет от 0,24 до 0,69 на 10 000 родов. Существует два типа данной патологии: тип I – с типично искривленными бедренными костями в виде «телефонной трубки» (telephone receiver) без «черепа-трилистника»; и тип II – с выраженным «черепом-трилистником» и короткими, не искривленными длинными трубчатыми костями. Однако умеренно выраженные признаки «черепа-трилистника» были описаны и при I типе танатофорной дисплазии.
Каждый из этих типов вызывается различными мутациями гена FGFR3. Дифференциальный диагноз между этими типами дисплазии проводится на основании рентгенологических и гистологических данных. Относительно характера наследования этой патологии существуют противоречивые мнения. Все случаи танатофорной дисплазии I типа и большинство наблюдений при II типе возникают спорадически. Имеются описания только нескольких случаев семейной формы заболевания для танатофорной дисплазии II типа.
– Также рекомендуем “УЗИ при танатофорной дисплазии. Пренатальная диагностика танатофорной дисплазии”
Оглавление темы “Скелетные дисплазии у плода”:
1. Оценка кривизны позвоночника плода. Обследование внутренних органов плода
2. Значение УЗИ в диагностике скелетных дисплазии. Признаки скелетных дисплазий у плода
3. Остеохондродисплазии у плода. Антенатальная диагностика остеохондродисплазий
4. Танатофорная дисплазия у плода. Причины и частота танатоформной дисплазии
5. УЗИ при танатофорной дисплазии. Пренатальная диагностика танатофорной дисплазии
6. Фиброхондрогенез и ателостеогенез. Ахондрогенез или аностеогенез
7. Классификация ахондрогенеза плода. Диагностика ахондрогенеза
8. Несовершенный остеогенез плода. Причины и диагностика несовершенного остеогенеза
9. Гипофосфатазия у плода. Диастрофическая дисплазия
10. Пренатальная диагностика диасторофической дисплазии. Синдром Книста у плода
Источник
Содержание
- Описание
- Дополнительные факты
- Причины
- Симптомы
- Диагностика
- Лечение
Названия
Название: Q78,5 Метафизарная дисплазия.
Q78.5 Метафизарная дисплазия
Описание
Краниометафизарная дисплазия. Наследственное состояние из группы остеохондродисплазий, характеризующееся аномалиями развития черепа и метафизов костей конечностей. Симптомами данного заболевания являются гипертелоризм, пороки развития лица, нередко уродующие больного, аномальное формирование носовых ходов с нарушением их проходимости, иногда головные боли и искривления конечностей. Диагностика краниометафизарной дисплазии осуществляется на основании изучения настоящего статуса пациента, рентгенологических данных и результатов молекулярно-генетических исследований. Специфического лечения данной патологии не существует, используют симптоматическую терапию, в некоторых случаях проводят хирургические вмешательства для облегчения дыхания пациента и улучшения его внешнего вида.
Дополнительные факты
Краниометафизарная дисплазия – группа наследственных заболеваний, которые приводят к порокам развития костей лицевого и мозгового отделов черепа различной степени выраженности в сочетании с аномалией метафизов длинных трубчатых костей и другими нарушениями. Ранее это состояние относили в одну группу с болезнью Пайла (множественная метафизарная дисплазия, краниометафизарная дисплазия Пайла), однако в настоящее время его выделяют в отдельную нозологическую единицу. Это связано с тем, что при данном заболевании превалирующими являются именно аномалии строения черепа (деформации, гиперостозы и склерозы костей), тогда как патологии иных отделов скелета выражены слабо. Существуют две основные формы краниометафизарной дисплазии, отличающиеся между собой механизмом наследования (аутосомно-доминантный и аутосомно-рецессивный типы), клиническими проявлениями и выраженностью нарушений. За счет наследования посредством аутосом патология с равной долей вероятности поражает как мужчин, так и женщин. Встречаемость краниометафизарной дисплазии точно не установлена, доминантный тип регистрируется во много раз чаще рецессивного.

Q78.5 Метафизарная дисплазия
Причины
Основной причиной более частой, но более легкой аутосомно-доминантной формы краниометафизарной дисплазии становятся мутации в гене ANKH, располагающемся на 5-й хромосоме. Ген кодирует белок, который является мембранным переносчиком пирофосфата, участвующего в угнетении процессов обызвествления костной ткани и ее резорбции. В результате генетического дефекта у белка-переносчика изменяется структура, и он становится неспособным полноценно выполнять свои функции, что приводит к краниометафизарной дисплазии. На клеточном уровне это проявляется аномальным изменением активности остеокластов, развитием склероза и гиперостоза главным образом костей черепа. Также может нарушаться конфигурация основных отверстий основания черепа, что становится причиной компрессии некоторых сосудов и нервов и во многом определяет остальные симптомы краниометафизарной дисплазии (нарушения слуха, головные боли, поражения тройничного и лицевого нервов). В генетике известны и другие заболевания, обусловленные поражением гена ANKH, в частности – наследственная псевдоподагра или семейный хондрокальциноз.
Намного более редкая аутосомно-рецессивная форма краниометафизарной дисплазии обусловлена дефектом гена GJA1, локализованного на 7-й хромосоме. Продуктом его экспрессии является белок под названием коннексин 43, принимающий активное участие в формировании межклеточных (межщелевых) контактов во многих тканях, что позволяет клеткам обмениваться низкомолекулярными соединениями. Патогенез развития краниометафизарной дисплазии при миссенс-мутации c716GA неизвестен, основная проблема сводится к выявлению причин изолированного поражения костей черепа и метафизов костей при относительном отсутствии патологий других органов. Учитывая, что наибольшее количество коннексина 43 у человека находится в сердечной ткани, вопрос отсутствия патологий сердца при данной мутации на сегодняшний день представляет собой загадку для большинства врачей-генетиков. Так же, как и в случае аутосомно-доминантной формы краниометафизарной дисплазии, при этом типе заболевания наблюдаются многочисленные вторичные нарушения, обусловленные воздействием измененных костей и отверстий на нервные структуры.
Симптомы
Аутосомно-доминантный тип краниометафизарной дисплазии характеризуется более легким течением, нередко при рождении ребенка никаких симптомов заболевания не выявляется. Лишь к первому году жизни возникает гипертелоризм с расширением переносицы вследствие гиперостоза носовых костей. В дальнейшем краниометафизарная дисплазия приводит к сужению носовых ходов и нарушению их проходимости, поэтому у больных нередко приоткрыт рот из-за нарушенного носового дыхания. К 6-7 годам может начать определяться увеличение метафизов длинных трубчатых костей, что внешне проявляется увеличением размеров коленных и локтевых суставов. Примерно у половины больных краниометафизарной дисплазией развиваются нарушения слуха различной выраженности вплоть до полной глухоты – чаще всего это обусловлено компрессией слухового нерва в костном канале. Из-за сдавления нервов возникают и другие неврологические нарушения, возможны расстройства чувствительности на лице, невралгия тройничного нерва и головные боли.
Диагностика
Диагностика краниометафизарной дисплазии основывается на данных осмотра пациента, изучении его наследственного анамнеза, результатах рентгенологических исследований и молекулярно-генетических анализов. При осмотре определяются различные по выраженности аномалии развития костей черепа, что отражается на чертах лица больного. При этом аутосомно-доминантная форма, особенно у маленьких детей, довольно слабо проявляет себя в отношении этого симптома. При обоих типах краниометафизарной дисплазии практически всегда присутствуют гипертелоризм, расширение переносицы за счет разрастания носовых костей по направлению к скулам, сужение или непроходимость носовых ходов. В рамках физикального осмотра и дополнительных исследований могут быть также выявлены неврологические нарушения: снижение или отсутствие слуха, снижение зрения, симптомы со стороны тройничного и лицевого нервов.
Намного больше информации при краниометафизарной дисплазии дают рентгенологические методы исследования скелета. На рентгенограммах черепа при аутосомно-доминантной форме заболевания определяются уплотнение костной ткани в области затылочной кости, склероз основания черепа, пониженная пневматизация синусов и ячеек височной кости. В ряде случаев может выявляться склероз межкостных швов и расширение метафизов трубчатых костей. При аутосомно-рецессивном типе краниометафизарной дисплазии на рентгенограммах обнаруживаются схожие, но намного более выраженные нарушения, например – полное отсутствие околоносовых пазух, резкое сужение и иногда заполнение костной тканью отверстий черепно-мозговых нервов. Кроме того, наблюдается склероз не только основания, но и свода черепа, в ряде случаев определяются значительные деформации костей лицевого отдела. Немного сильнее, чем при доминантном типе, выражены расширение и склероз метафизов трубчатых костей.
Изучение наследственного анамнеза и генетическая диагностика также активно используются для определения краниометафизарной дисплазии. При этом можно сначала установить тип наследования заболевания, что позволяет скорректировать молекулярно-генетический анализ для поиска мутаций в конкретном гене. Для этого применяют метод прямого секвенирования генов ANKH и GJA1.
Лечение
Специфического лечения краниометафизарной дисплазии не существует, назначают симптоматическую терапию с привлечением разнообразных хирургических техник. Последние, в частности, могут улучшить проходимость носовых ходов для облегчения дыхания. Уменьшить выраженность неврологической симптоматики можно путем расширения отверстий соответствующих черепно-мозговых нервов. Кроме того, пластические хирурги способны минимизировать выраженность эстетических дефектов при краниометафизарной дисплазии. Для улучшения слуха используют слуховые аппараты.
Источник