Ведение пациентов с болевыми синдромами
Комментарии
Опубликовано в журнале:
CONSILIUM MEDICUM »» ТОМ 12 № 9, С. 111-114
А.В.Наумов, П.А.Семенов, А.Л.Верткин
ГОУ ВПО Московский государственный медико-стоматологический университет
Боль занимает лидирующие позиции по частоте обращений за медицинской помощью. Боль можно рассматривать и как самостоятельную болезнь, и как симптом. Однако очевидно, что боль сама по себе является целым каскадом патологических изменений как в остром периоде, так и в хронической форме.
Известно, что болевой синдром является причиной не только неприятных ощущений и эмоций (как следует из определения боли, IASP, 1992), но и сопровождается клинически значимым ответом практически со всех органов и систем организма. К примеру, болевой синдром, активируя симпатическую нервную систему, повышает число сердечных сокращений, артериальное давление, сердечный выброс, что в свою очередь провоцирует развитие ишемии миокарда. У больных с имеющейся кардиоваскулярной патологией это сопровождается дестабилизацией ишемической болезни сердца (ИБС), артериальной гипертензии (АГ) и т.д. Описаны случаи развития гипостатических и инфекционных пневмоний у пациентов с хроническим болевым синдромом, в первую очередь за счет снижения объема выдоха и жизненной емкости легких. Снижение венозного оттока и кровотока в конечностях при остром болевом синдроме является частой причиной тромбозов и тромбоэмболий. Симпатическая активация также способствует повышению активности мочевых сфинктеров, что является причиной острой задержки мочеиспускания при острых и хронических болевых синдромах.
Описанные выше ответы на болевой синдром со стороны систем организма в совокупности с долгосрочной «болевой памятью» мозга – основная причина хронизации боли, что является основополагающей проблемой обезболивания в соматической практике.
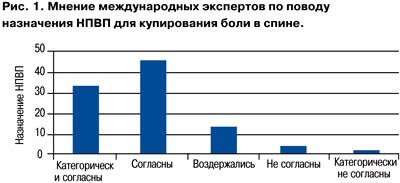
Исходя из практических рекомендаций по ведению хронической боли (An Updated Report by the American Society of Anesthesiologists Task Force on Chronic Pain Management and the American Society of Regional Anesthesia and Pain Medicine Anesthesiology 2010; 112: 81033), большинство международных экспертов считают необходимым назначение нестероидных противовоспалительных препаратов (НПВП) для купирования боли в спине (рис. 1).
Таким образом, выбор НПВП должен быть обдуманным и взвешенным, с оценкой соотношения риска и пользы конкретного препарата.
Следует отметить, что у пациентов с соматическими заболеваниями безопасность применения лекарственного препарата должна быть предпочтительным критерием выбора.
Однако анальгетическая активность не может оставаться в тени, поскольку адекватное обезболивание является решением проблемы хронизации и пролонгации как неприятных ощущений и эмоций, так и патологических изменений в системах организма.
Механизм обезболивающего эффекта НПВП обусловлен блокадой синтеза изоферментов циклооксигеназы (ЦОГ), в частности ЦОГ-2, которая ответственна за синтез провоспалительных цитокинов – триггерных факторов активации болевых рецепторов. Отметим, что блокада изофермента ЦОГ-1 большинством неселективных НПВП определяет сумму побочных эффектов этих препаратов. При этом, как правило, практический врач забывает, что блокада синтеза этого изофермента (ЦОГ-1) является причиной резкого снижения синтеза лейкотриенов, которые стимулируют синтез эндогенных опиоидов. Но отсутствие снижения концентрации динорфина и b-эндорфина в крови и тканях могло бы служить поводом к увеличению анальгетической активности. Из известных неселективных НПВП только лорноксикам шунтирует синтез арахидоновой кислоты до лейкотриенов без участия ЦОГ-1, что, соответственно, сохраняет синтез эндогенных опиоидов и повышает анальгетическую активность лорноксикама. Что и было доказано в большинстве рандомизированных клинических исследований (РКИ).
Метаанализ, включающий три исследования, проведенных на 673 пациентах, сравнивающий эффективность кеторолака, ацетилсалициловой кислоты и лорноксикама, продемонстрировал, что для всех доз лорноксикама, превышающих 2 мг, доверительный интервал не включал нулевую величину. Полученные данные свидетельствуют о том, что дозы, равные или превышающие 4 мг, являются достоверно более эффективными при обезболивающем лечении, чем плацебо. Эффективность ацетилсалициловой кислоты 1650 мг соответствует эффективности 4 мг лорноксикама, а эффективность кеторолака 10 мг аналогична эффективности лорноксикама при величине дозы между 8 и 16 мг.
Сопоставимую анальгетическую активность лорноксикам продемонстрировал и с наркотическими анальгетиками в исследованиях, моделью острой боли в которых явились болевые синдромы после удаления моляров.
Описанная в литературе индивидуальная чувствительность к разным НПВП зачастую определяет в РКИ результативную эффективность препарата. Индивидуальная чувствительность определяется влиянием полиморфизма цитохрома Р-450 на фармакокинетику препарата. Так, для метамизола натрия зарегистрировано лишь 2-4% «нечувствительных» пациентов, для диклофенака натрия до 25%.
В исследовании, оценивающем влияние полиморфизма Р-450 на фармакокинетику лорноксикама, было обнаружено, что кинетика лорноксикама и 5′-гидроксилорноксикама одинакова как у лиц, медленно метаболизирующих спартеин/дебризохин или мефенитоин, так и у лиц, быстро метаболизирующих эти вещества, что снижает процент не чувствительных к лорноксикаму пациентов до 2%.
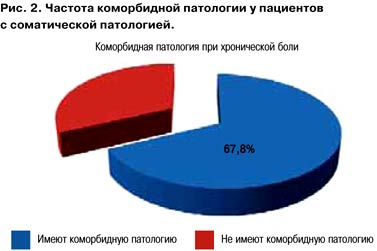
Чем же можно определить сегодня безопасность терапии? Естественный клинический ответ будет лежать в области коморбидности пациентов. Это неслучайно. При собственном многоцентровом анализе пациентов, страдающих хроническим болевым синдромом (n=950), установлено, что 67,8% пациентов имеют сочетанную соматическую патологию (рис. 2).
Литература, посвященная болевым синдромам, сегодня позиционирует боль не как симптом, а как болезнь, требующую комплексного подхода к ведению пациентов. Неслучайно в англоязычной медицинской литературе термин treatment (лечение) заменен на management (ведение) of acute pain (острой боли).
В условиях коморбидности этот вопрос приобретает иную актуальность в связи c изменением профиля безопасности лекарств при сочетании нескольких заболеваний и полипрагмазии.
К примеру, риск поражения слизистой оболочки гастродуоденальной зоны (в том числе и НПВП-гастропатия) имеет место у большинства пациентов отделений неотложной кардиологии, госпитализированных в многопрофильный стационар скорой медицинской помощи.
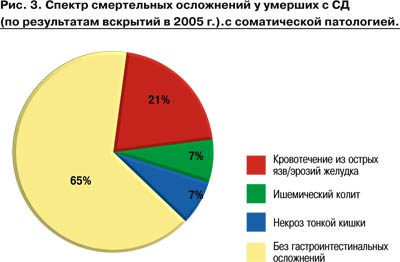
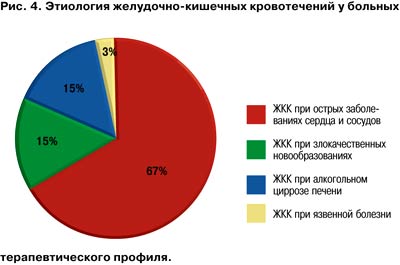
Например, желудочно-кишечные кровотечения (ЖКК) составляют около 20% (рис. 3, 4) среди всех смертельных осложнений – непосредственных причин летального исхода пациентов с сахарным диабетом (СД).
Кроме того, на практике эти больные нередко не получают адекватного лечения АГ и СД, не имеют доступа к оперативной реваскуляризации сердца.
Повсеместно риск ЖКК у этих пациентов не стратифицируется, и они не получают адекватной антисекреторной терапии ни в целях профилактики желудочных кровотечений в амбулаторных условиях, ни на фоне обострения ИБС в стационаре. В этих условиях активная и профилактическая антиагрегантная терапия при остром коронарном синдроме также является рискованной.
Таким образом, одной из основных задач ведения болевого синдрома является сокращение доз и сроков назначения НПВП.
Наиболее перспективными направлениями в лечении боли следует считать применение средств, действие которых затрагивает и патогенетические механизмы, и клинические проявления.
Понятно, что речь идет о других лекарственных препаратах, которые потенциально могли бы также обладать анальгетическим потенциалом и их клиническая эффективность была бы связана c ключевыми звеньями патогенеза.
Поскольку подобной направленностью действия обладают нейротропные витамины группы B, препаратами выбора для лечения боли разного генеза можно считать именно их. Традиционно к нейротропным относят три витамина группы B: тиамин (B1), пиридоксин (В6), цианокобаламин (B12). Объединяет их высокая значимость для нормального функционирования нервной ткани.
К примеру, тиамин в активной коферментной форме представляет собой тиаминпирофосфат или кокарбоксилазу и играет ключевую роль в энергетическом метаболизме, в частности в цикле Кребса. Дополнительно к функциям кофактора углеводного обмена тиамин является модулятором нейромышечной передачи, связываясь с n-холинергическими рецепторами. Опосредованно он участвует в метаболизме нейротрансмиттеров – серотонина и g-аминомасляной кислоты, которые играют важную роль в подавлении боли; участвует в обмене глютатиона, проявляя тем самым антиоксидантную активность.
Таблица 1. Характеристика пациентов
| Характеристика | 1-я группа, n=30 | 2-я группа, n=30 | 3-я группа, n=30 |
| Средний возраст, годы | 67,4±4,1 | 68,2±4,6 | 66,4±3,8 |
| Пол, м/ж | 13/17 | 11/19 | 12/18 |
| ИМТ, кг/м | 29,3±2,4 | 28,7±3,1 | 28,4±4,2 |
| Формы ИБС | 7 (23,3%) | 5 (16,7%) | 7 (23,3%) |
| АГ | 100% | 100% | 100% |
| СД типа 2 | 12(40%) | 10(33,3%) | 8(26,7%) |
| Прочие | 4(13,3%) | 5(16,7%) | 3(10%) |
В нескольких исследованиях указано, что как комбинация, так и отдельное назначение витаминов B1, В6 и В12 обладает анальгетическим потенциалом. В экспериментальной работе по изучению эффектов комбинации витаминов В1, В6 и В12 при болях показано ингибирование ноцицептивных ответов, вызванных формальдегидом, не меняющееся после введения налоксона. Выдвинуто предположение, что антиноцицептивный эффект комбинированного витаминного комплекса может быть обусловлен ингибированием синтеза и/или блокированием действия воспалительных медиаторов. В другой работе показано, что комплекс витаминов группы В усиливает действие норадреналина и серотонина – главных «антиноцицептивных» нейромедиаторов.
Пиридоксин (витамин В6) – групповое название трех производных пиримидина: пиридоксина, пиридоксаля и пиридоксамина. Активной формой В6 является пиридоксаль-5-фосфат (PLP) – важнейшая простатическая группа метаболизма аминокислот. PLP выступает в роли кофермента более чем в 100 ферментативных реакциях. Так, он служит кофактором для аминокислотных декарбоксилаз и трансаминаз, регулирующих белковый обмен, и тесно связан с процессами синтеза и разрушения катехоламинов, гистамина, дофамина, g-аминомасляной кислоты, превращения триптофана в никотиновую кислоту и серотонин.
Пиридоксин является составной частью системы, отвечающей за синтез аминолевулиновой кислоты, первичного звена в синтезе веществ, составляющих гем. PLP влияет на процессы свертывания крови и агрегации тромбоцитов. Его действие связано с обменом холина и незаменимых ненасыщенных жирных кислот. Он непосредственно участвует в метаболизме белков, синтезе и транспортировке аминокислот, в обмене липидов, выработке энергии в организме; стимулирует синтез гемоглобина в эритроцитах; участвует в синтезе нейромедиаторов центральной и периферической нервной системы, а также в биосинтезе миелиновой оболочки нервов.
Цианокобаламин (витамин В12) – комплексное соединение, имеющее в основе цикл коррина и содержащее координационно связанный ион кобальта. Витамин В12 играет важную роль в аминокислотном обмене, биосинтезе ацетилхолина, а также в процессах миелинизации нервных волокон. Известно, что высокие дозы цианокобаламина улучшают проведение возбуждения по периферическим нервам и их структурно-функциональную регенерацию.
Таблица 2. Фармакотерапия в группах
| Группа | Фармакотерапия |
| 1-я | Лорноксикам: 1, 2, 3-и сутки – 16 мг внутримышечно, внутривенно; далее – по потребности Нейробион: 3 таблетки в день в течение 2 нед; далее по 2 таблетке 2 раза в день на протяжении 2 нед |
| 2-я | Лорноксикам: 1, 2, 3-и сутки – 16 мг; далее – по потребности |
| 3-я | Диклофенак натрия: 1, 2, 3-и сутки – 100 мг внутримышечно; далее – по потребности |

Цианокобаламин необходим для синтеза двух коферментов: метилкобаламина и 5-дезоксиаденозилцианокобаламина. Они принимают участие в двух типах реакций. Первой является реакция трансметилирования, в которой метилкобаламин выполняет роль промежуточного переносчика метильной группы (синтез метионина и ацетата). Синтез метионина происходит из гомоцистеина, поэтому недостаток В12 вызывает повышение уровня гомоцистеина.
В основе второй группы реакций лежит перенос водорода и образование новой углеводородной связи: глутаматмутазная реакция (взаимопревращение глутаминовой и b-метиласпарагиновой кислот), реакция восстановления рибонуклеотидов до дезоксирибонуклеотидов, реакция синтеза липотропного фактора – холина (превращение метилмалоновой кислоты в янтарную, входящую в состав миелина), реакции дезаминирования и трансаминирования и др.
Биологические свойства витамина В12 достаточно многообразны и изучены относительно подробно. Цианокобаламин оказывает гемопоэтическое, эритропоэтическое, противоанемическое, метаболическое действие; участвует в углеводном, белковом, липидном обмене; повышает регенерацию тканей; нормализует кроветворную функцию печени, функционирование нервной системы; регулирует свертывающую систему крови; снижает содержание холестерина и гомоцистеина в крови.
Во многих исследованиях подчеркивается, что при лечении боли комбинация витаминов В1, В6 и В12 более эффективна, чем монотерапия каким-либо из них. Также продемонстрировано, что длительность терапии болевых вертебральных синдромов может быть уменьшена за счет применения комбинации витаминов В1, В6, В12 и НПВП вместо проведения монотерапии НПВП.
Одной из актуальных лекарственных форм витаминов группы В является препарат Нейробион.
Под нашим наблюдением находились 90 пациентов, которые обратились за медицинской помощью по поводу боли в нижней части спины. На основании проведенного дифференициального диагноза у всех пациентов были исключены такие причины боли в нижней части спины, как аневризма брюшного отдела аорты, остеопоротические переломы, метастатические поражения тел позвонков, инфекционные процессы и туберкулез. Ни у одного пациента не было выявлено грыжи межпозвоночного диска.
Причиной боли в спине явились дегенеративно-дистрофические изменения позвоночника.
Пациенты были рандомизированы на три группы по 30 пациентов в зависимости от назначенной терапии. Характеристика пациентов представлена в табл. 1.
Как видно, из табл. 1, группы были сопоставимы по полу, возрасту и индексу массы тела (ИМТ). Видно, что все пациенты имели коморбидную соматическую патологию, что являлось ключевым для проведения нашего исследования.
Статистически достоверной разницы между интенсивностью боли по визуальной аналоговой шкале (ВАШ) в момент обращения к врачу в группах не было. Во всех группах была констатирована хроническая боль, а настоящий рецидив боли – как минимум 4 в анамнезе.
Фармакотерапия в группах представлена в табл. 2
В качестве оценки эффективности мы использовали оценку уровня интенсивности боли в момент обращения пациента и в конце 1, 2, 3-х суток терапии. Интенсивность боли оценивали по ВАШ.
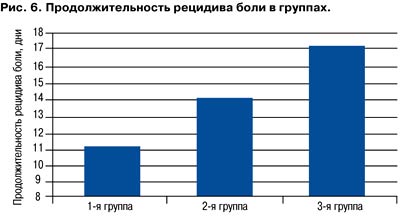
Также мы оценили продолжительность рецидива боли. Принималось к учету количество дней от начала боли до полного купирования.
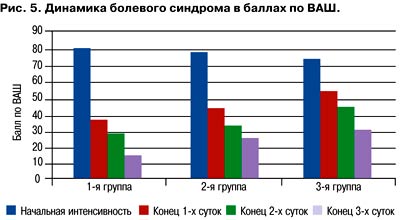
Во всех группах терапии к концу 1-х суток удалось достичь достоверного регресса болевого синдрома. К концу 3-х суток во всех группах отмечалась достоверная динамика нивелирования боли (рис. 5).
Однако у пациентов 1-й группы уже к концу 1-х суток терапии интенсивность боли была достоверна меньше в сравнении c другими группами. Схожая тенденция сохранилась и к концу 3-х суток (р<0,05 в сравнении со 2 и 3-й группами).
Оценивая время рецидива болевого синдрома мы также установили, что наименьшая его продолжительность была в 1-й группе (рис. 6), составив 11,4±2,3 дня, а в 3-й – 17,2±5,3 (р<0,05).
Таким образом, наше наблюдение продемонстрировало, что включение препарата Нейробион в комплексную терапию пациентов c болью в нижней части спины приводит к более выраженному анальгетическому эффекту и сокращению длительности рецидива боли.
Данная стратегия ведения пациентов позволит сократить время назначения НПВП, что сопровождается лучшим профилем безопасности купирования болевых синдромов.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник

Цель данной публикации — стремление четко изложить проблемы, возникающие перед специалистами по лечению хронической боли: какие материально-технические и физические затраты ожидают администраторов здравоохранения и практических врачей, каковы экономические и моральные приобретения. Подчеркиваем: речь пойдет о хроническом болевом синдроме, о боли-болезни, а не об острой боли-симптоме, с которым анестезиологи-реаниматологи в настоящее время справляются довольно успешно.
Потребности общества и понимание важности проблемы боли способствовали появлению в некоторых развитых странах специализированных “клиник боли”, профильных отделений в медицинских центрах и университетских клиниках.
Проводимое в этих клиниках лечение пациентов с хроническими болевыми синдромами позволяет оказывать им значительно более эффективную и грамотно построенную специализированную помощь, существенно повышает положительный эффект от лечения, способствует скорейшему восстановлению трудоспособности пациентов или их социальной адаптации.
К сожалению, проблема хронической боли абсолютно игнорируется российскими страховыми компаниями и здравоохранением как несуществующая. У нас все еще нет официальной статистики на этот счет, хотя исходя из пропорций населения совсем несложно подсчитать, что в России страдают миллионы людей от различных видов хронической или часто рецидивирующей боли. А учитывая нынешнее состояние экономики государства, по-видимому, в обозримом будущем не следует надеяться на сколь-нибудь существенное бюджетное финансирование для решения этой проблемы.
Согласно статистическим данным служб здравоохранения и ведущих специалистов по проблеме боли, хроническими болевыми синдромами страдает огромное множество людей. Например,
в США эта цифра достигает
20 млн. человек, что ежегодно обходится высокотехнологичному американскому здравоохранению и страховым компаниям в десятки миллиардов долларов в год.
В Германии 7 млн. больных, ведение которых также требует серьезных материальных расходов
Мультидисциплинарный научный центр “Интегративная медицина” создан при РНЦХ РАМН на базе научно-консультативного отделения (поликлиника) и отделения терапии болевых синдромов в 1993 году. Цель создания центра — предоставить возможность пациентам, страдающим различными видами болевого синдрома, сопутствующей патологией и функциональными нарушениями, получить специализированную медицинскую помощь, а медицинским работникам на вполне законном основании иметь дополнительный заработок.
Организационно-правовая форма нового структурного подразделения РНЦХ — закрытое акционерное общество, где единственный его учредитель — государственное учреждение, владеющее 51% акций. Остальные акции распределены среди сотрудников РНЦХ и не могут передаваться (продаваться) сторонним физическим или юридическим лицам. Вся финансово-хозяйственная деятельность контролируется и определяется общим собранием. Прибыль от коммерческой деятельности в основном идет на закупку медикаментов, оборудования и расходных материалов для исследований; конкретные статьи расходов утверждаются на ежегодном общем собрании акционеров.
Центр “Интегративная медицина” имеет лицензию практически на все виды медицинской деятельности (от врачебно-контрольной комиссии и всех видов лечебно-диагностической практики до испытаний и разработки новой медицинской техники), что в значительной степени обусловливает успех финансово-хозяйственной деятельности в нынешних экономических условиях.
Как результат длительного научного исследования проблемы диагностики и лечения хронической боли и практических достижений в этой области в Центре сформировался следующий состав специалистов, работающих в соответствующих лабораториях:
- основные специалисты: анестезиологи, невропатологи, психоневролог, ортопедтравматолог, физиотерапевты, рефлексотерапевты, мануальный терапевт, врач ЛФК, массажисты, медицинские сестры и младший медицинский персонал;
- консультанты: нейрохирург, микрохирург, сосудистый, торакальный и других профилей хирурги, терапевты (кардиолог, гастроэнтеролог и др.), уролог, гинеколог, ЛОР, офтальмолог, эндокринолог, дерматолог, специалисты по функциональной диагностике;
- диагностические лаборатории: экспресс-диагностики, клинической, функциональной, иммунологии, радиоизотопной, ультразвуковой, эндоскопической, рентгенодиагностики и компьютерной томографии, термокартирования, профилактики и лечения инфекций.
В центре применяются новейшие диагностические и лечебные методики (табл. 1 и 2). Конечно, такой подбор специалистов, с широким спектром диагностических и лечебных методов, под силу лишь достаточно крупным научно-исследовательским центрам и многопрофильным клиническим больницам. В практической же медицине поначалу вполне можно обойтись 25-33% указанного перечня специалистов и методов, а по мере приобретения навыков, опыта работы, соответствующей аппаратуры и оснащения можно расширять и объем помощи. Минимально достаточным следует считать следующий состав специалистов: два анестезиолога (один из них должен иметь подготовку по выполнению лечебных блокад, а второй владеть методами рефлексотерапии в объеме, необходимом для лечения боли, в том числе элементами мануальной терапии), психоневролог (или невропатолог и психиатр) и физиотерапевт. Эти специалисты ex consilio определяют стратегию и тактику лечения каждого пациента, а также необходимость дополнительных исследований и консультаций. Чаще приходится прибегать к консультациям специалистов, имеющихся в каждой поликлинике или больнице (хирурга, гинеколога, стоматолога и т. д.).
| Специфические | Компьютеризированная визуальная аналоговая шкала боли Модернизированный опросник боли Mc’Gill в той или иной модификации Оценка состояния триггерных точек Определение болевых порогов на электрораздражение Компьютерная пульсометрия Omura-тест Метод Ryodorraky Электропунктурная аурикулярная и корпоральная диагностика и др. |
| Общепринятые | Рентгенография и рентгеноскопия Компьютерная и ЯМР-томография Ультразвуковая диагностика сосудов, сердца, органов брюшной полости и др. Электромиография и электрокардиография Эндоскопия Термография, в том числе компьютерное термокартирование, и другие методы |
Следует специально отметить, что в настоящее время (приказы МЗ РФ №364 и 365 от 10.12.1997) рефлексотерапия и мануальная терапия впервые получили статус официально существующих в России специальностей. Средний медперсонал привлекают по мере необходимости для выполнения конкретной работы (массажа, физиопроцедур, манипуляций, блокад и т. п.). Медрегистратор вполне справляется с функцией кассира.
Организацию работы противоболевого центра, как показал опыт, с успехом берут на себя анестезиологи, будучи наиболее инициативными, информированными о стационарной и амбулаторной деятельности больницы людьми, которые, как правило, хорошо ладят с руководством, коллегами и персоналом. Если в вашем лечебном учреждении имеются все вышеперечисленные предпосылки, то группа единомышленников может выступить с инициативой организации противоболевого центра с целью обеспечения дополнительным ЛЕГАЛЬНЫМ заработком ВСЕХ специалистов больницы или поликлиники. Дальнейшие организационные действия не представляют больших проблем. Руководство лечебного учреждения или инициативная группа выносит на общее собрание сотрудников вопрос о создании закрытого акционерного общества (или другой более удобной для коллектива структуры), принимается устав и производится регистрация нового юридического лица, заключается договор, по которому учреждение передает противоболевому центру в пользование необходимые площади или же рабочие места и необходимое оборудование. Остается выполнить одно условие — ввести единственную штатную должность — бухгалтера, а также приобрести и зарегистрировать кассовый аппарат.
В настоящее время уже имеются нормативные акты о ценообразовании медицинских услуг. Все сотрудники, чья консультативная и лечебная деятельность будет пользоваться спросом у населения, работают в центре по договору подряда в свободное от основной деятельности время. Процент отчислений от общего объема поступающих денежных средств на заработную плату, равно как и на развитие, определяет общее собрание акционеров с учетом налогов и проч.
| Немедикаментозные | Классическая корпоральная акупунктура Аурикулярная акупунктура Микроиглотерапия и поверхностная иглотерапия ECIWO и Су-Джок-терапия Электроакупунктура и электропунктура Чрескожная электронейростимуляция Резонансная электропунктурная аналгезия и терапия Свето-, термо-, лазеропунктура КВЧ-терапия и микромагнитотерапия Гирудо- и апитерапия Вакуумный, точечный и классический массаж, вибрационная рефлексотерапия ЛФК и мануальная терапия в разных вариантах Звуко-, арома- и музыкотерапия Аутотренинг с биологической обратной связью и др. методы |
| Фармакотерапевтические | Блокады различного типа (эпидуральные, эпиплевральные, проводниковые и др.) Фармакопунктура (мезопунктура) Фармакотерапия аналгетиками, седативными, противовоспалительными, релаксирующими и прочими препаратами |
| Гомеопатические, фитотерапевтические и другие нестандартные методы | |
Противоболевой центр должен строить свою работу, ориентируясь в основном на амбулаторных больных, что, однако, не исключает при необходимости госпитализации для более детального обследования и лечения, а также возможность обслуживания коллективов предприятий на договорной основе.
Объем услуг зависит от уровня профессиональных навыков у персонала. Исходя из принципа минимальной достаточности, экономическая рентабельность может быть достигнута при наличии в перечне медицинских услуг следующих позиций:
- классическая акупунктура;
- мануальная терапия;
- лечебные блокады и фармакопунктура;
- лечебные массажи: вакуумный, сегментарный, точечный;
- интегративные методы воздействия (ЧЭНС, КВЧ и др.);
- комбинированная рефлексотерапия с психотропными средствами;
- физиотерапевтические процедуры.
Приведенный перечень воздействия может быть освоен и применен любым специалистом противоболевого центра — обучение этим методам сегодня в России ведется во многих специализированных учреждениях.
Несколько особняком стоит группа пациентов с хронической болью онкологического происхождения, то есть больные, входящие в компетенцию паллиативной и хосписной службы онкодиспансера. По современным критериям перечисленные выше методы приравнены к физиотерапевтическим процедурам, а поэтому неприменимы в онкологии, хотя имеются результаты исследований, проведенных во многих университетских клиниках мира, показывающие эффективность методов интегративной медицины в купировании онкологической боли. Вместе с тем, по нашему мнению, любой способ, облегчающий боль в терминальной стадии онкологического заболевания, заслуживает самого внимательного отношения и изучения.
В Центр обращаются пациенты с различными состояниями и заболеваниями. Болевые синдромы представлены в табл. 3 в уменьшающейся прогрессии.
Как было сказано выше, все методы воздействия мы подразделяем на инвазивные и неинвазивные, фармакотерапевтические и немедикаментозные. Выбор оптимальных комплексных методов лечения и их интеграция основывались на применении более 150 классических традиционных и современных лечебных методик.
На каждом этапе лечения выбор и последовательность применения методик определялись индивидуально, в зависимости от этиологических и симптоматических проявлений болевого синдрома и степени выраженности сопровождающих его функциональных расстройств.
|
Обычно пациенты приходили к нам уже после прохождения лечения во многих инстанциях, но с прежними жалобами, поэтому чаще всего нам приходилось начинать лечение с купирования болевого синдрома следующими фармакотерапевтическими методами.
- При резко выраженном мучительном болевом синдроме, обусловленном злокачественными новообразованиями органов брюшной полости и малого таза, фантомными и каузалгическими болями, использовали эпидуральную анальгезию. Пункцию и катетеризацию эпидурального пространства проводили в соответствии с общепринятыми рекомендациями. Анальгезию осуществляли введением наркотического анальгетика морфина (0,1 — 0,3 мл 1%-ного раствора в 10 мл физиологического раствора) один раз в сутки. Преимущества данного методического решения состоят в том, что достигается хороший аналгетический эффект при минимальном введении препарата, нет необходимости в частых повторных введениях, что снижает риск инфицирования эпидурального пространства. Метод использовали как в стационарных, так и в амбулаторных условиях. Побочных эффектов, таких как гипотония, ортостатический коллапс, депрессия дыхания, не наблюдалось.
- Метод регионарной анальгезии применялся для лечения практически всех видов болевых синдромов. Анальгезию осуществляли введением 0,75—1%-ных растворов местноанестезирующих средств (бупивокаин, лидокаин). Для верхних конечностей использовалась блокада по Куленкампфу, блокада аксиллярного нерва с наложением жгута; для нижних конечностей — блокада бедренного, седалищного, наружного кожного, запирательного нервов. Лечебные сеансы назначались по мере необходимости, но не чаще чем один раз в два дня, как в стационарных, так и в амбулаторных условиях.
- Суть методики фармакопунктуры состоит в введении микродоз современных фармацевтических препаратов в точки классической акупунктуры. Метод применялся для лечения всех видов болевых синдромов, сопутствующей патологии и функциональных расстройств, таких как бронхиальная астма, нарушение моторики кишечника, нарушение мочеиспускания, кожный зуд, невралгии, в том числе герпетические, невропатии, невриты. Вводились ненаркотические анальгетики (трамал, бутарфанолтартрат, анальгин, баралгин) и местные анестетики. В комплексе с ними в зависимости от причины, вызвавшей болевой синдром, назначались гормоны и другие противовоспалительные препараты и антигистаминные средства, витамины группы В. Препараты вводили в классические точки акупунктуры по индивидуально подобранному рецепту, исходя из наиболее болезненных (триггерных) зон. Оптимальным можно считать введение препаратов с помощью оригинальных наборов разовых шприцов, имеющих в тубусе две-три последовательно расположенные емкости, содержащие местный анестетик, витамины группы В и гормональные средства. Введение препаратов осуществляется посредством одной инъекции, что уменьшает травматичность, повышает точность введения и оптимизирует дозирование лекарств. Мы также использовали последовательную насадку на одну инъекционную иглу двух-трех шприцев, содержащих препараты, подобранные по индивидуальному рецепту. Обе методики могут выполняться по принципу политопного введения препаратов.
Выбор интегративных методов рефлексотерапии для лечения пациентов с хроническим болевым синдромом основан на тяжести его проявлений, то есть интенсивности и длительности, психоэмоциональной истощенности пациентов, связанной с низкой эффективностью длительного использования традиционных анальгетических средств (наркотических и ненаркотических). Мы исходили также из того, что травматичность интегративных методов клинической рефлексотерапии не должна превышать тяжесть проявлений болевого синдрома и должна быть субъективно не тягостной для пациента.
Объективная характеристика эффективности интегративных методик рефлексотерапии, основанных на воздействии на биологически активные точки и зоны, выполнена на основе анализа результатов компьютерного термокартирования и расчета потребляемого количества анальгетиков до и на фоне лечения. Хорошая субъективная переносимость больными этих методик подтверждается исследованием гемодинамических показателей и циклических нуклеотидов до и после воздействия. Все использованные нами методы рефлексотерапии снижают адренергическую стимуляцию, благодаря чему ликвидируется артериолоспазм и улучшается микроциркуляция тканей.
Результаты внедрения в практику клиник боли интегративных методов клинической рефлексотерапии при лечении тяжелых болевых синдромов от травматичных хирургических (разрушение передней доли гипофиза и френотомия) и лучевых методов свидетельствуют в пользу интегративной рефлексотерапии.
Источник
