Аномалия развития головного мозга код мкб
Содержание
- Описание
- Дополнительные факты
- Симптомы
- Дифференциальная диагностика
- Причины
- Диагностика
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Другие названия и синонимы
Пороки развития головного мозга.
Названия
Название: Аномалии развития головного мозга.
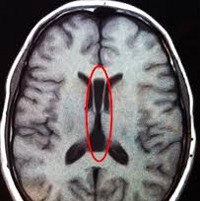
Аномалии развития головного мозга
Описание
Аномалии развития головного мозга. Результат происходящих во внутриутробном периоде нарушений формирования отдельных церебральных структур или головного мозга в целом. Зачастую имеют неспецифическую клиническую симптоматику: преимущественно эпилептический синдром, задержку психического и умственного развития. Тяжесть клиники напрямую коррелирует со степенью поражения головного мозга. Диагностируются антенатально при проведении акушерского УЗИ, после рождения — при помощи ЭЭГ, нейросонографии и МРТ головного мозга. Лечение симптоматическое: противоэпилептическое, дегидратационное, метаболическое, психокоррегирующее.
Дополнительные факты
Аномалии развития головного мозга — пороки, заключающиеся в аномальных изменениях анатомического строения церебральных структур. Выраженность неврологической симптоматики, сопровождающей церебральные аномалии, значительно варьирует. В тяжелых случаях пороки являются причиной антенатальной гибели плода, они составляют до 75% случаев внутриутробной смерти. Кроме того, тяжелые церебральные аномалии обуславливают около 40% случаев гибели новорожденного. Сроки манифестации клинических симптомов могут быть различны. В большинстве случаев церебральные аномалии проявляются в первые месяцы после рождения ребенка. Но, поскольку формирование головного мозга длится до 8-летнего возраста, целый ряд пороков дебютируют клинически после 1-го года жизни. Более чем в половине случаев церебральные пороки сочетаются с пороками соматических органов: врожденными пороками сердца, сращением почек, поликистозом почек, атрезией пищевода и пр. Пренатальное выявление церебральных аномалий является актуальной задачей практической гинекологии и акушерства, а их постнатальная диагностика и лечение — приоритетными вопросами современной неврологии, неонатологии, педиатрии и нейрохирургии.
Построение нервной системы плода начинается буквально с первой недели беременности. Уже к 23-му дню гестации заканчивается образование нервной трубки, неполное заращение переднего конца которой влечет за собой серьезные церебральные аномалии. Примерно к 28-му дню беременности образуется передний мозговой пузырь, в последующем разделяющийся на 2 боковых, которые ложатся в основу полушарий мозга. Далее образуется кора головного мозга, его извилины, мозолистое тело, базальные структуры.

Аномалии развития головного мозга
Симптомы
Ассоциированные симптомы: Слабость мышц (парез). Судороги.
Дифференциальная диагностика
Дифференцировка нейробластов (зародышевых нервных клеток) приводит к образованию нейронов, формирующих серое вещество, и глиальных клеток, составляющих белое вещество. Серое вещество отвечает за высшие процессы нервной деятельности. В белом веществе проходят различные проводящие пути, связывающие церебральные структуры в единый функционирующий механизм. Рожденный в срок новорожденный имеет такое же число нейронов, как и взрослый человек. Но развитие его мозга продолжается, особенно интенсивно в первые 3 мес. Жизни. Происходит увеличение глиальных клеток, разветвление нейрональных отростков и их миелинизация.
Причины
Сбои могут произойти на различных этапах формирования головного мозга. Если они возникают в первые 6 мес. Беременности, то способны приводить к снижению числа сформированных нейронов, различным нарушениям в дифференцировке, гипоплазии различных отделов мозга. В более поздние сроки может возникать поражение и гибель нормально сформировавшегося церебрального вещества. Наиболее весомой причиной подобных сбоев является влияние на организм беременной и на плод, различных вредоносных факторов, обладающих тератогенным действием. Возникновение аномалии в результате моногенного наследования встречается лишь в 1% случаев.
Наиболее влиятельной причиной пороков головного мозга считается экзогенный фактор. Тератогенным эффектом обладают многие активные химические соединения, радиоактивное загрязнение, отдельные биологические факторы. Немаловажное значение здесь имеет проблема загрязнения среды обитания людей, обуславливающая поступление в организм беременной токсических химических веществ. Кроме того, различные эмбриотоксические воздействия могут быть связаны с образом жизни самой беременной: например, с курением, алкоголизмом, наркоманией. Дисметаболические нарушения у беременной, такие как сахарный диабет, гипертиреоз и пр. , могут также стать причиной церебральных аномалий плода. Тератогенным действием обладают и многие медикаменты, которые может принимать женщина в ранние сроки беременность, не подозревая о происходящих в ее организме процессах. Мощный тератогенный эффект оказывают инфекции, перенесенные беременной, или внутриутробные инфекции плода. Наиболее опасны цитомегалия, листериоз, краснуха, токсоплазмоз.
Диагностика
Тяжелые аномалии развития головного мозга зачастую могут быть диагностированы при визуальном осмотре. В остальных случаях заподозрить церебральную аномалию позволяет ЗПР, гипотония мышц в неонатальном периоде, возникновение судорожного синдрома у детей первого года жизни. Исключить травматический или гипоксический характер поражения головного мозга можно при отсутствии в анамнезе данных о родовой травме новорожденного, гипоксии плода или асфиксии новорожденного. Пренатальная диагностика пороков развития плода осуществляется путем скринингового УЗИ при беременности. УЗИ в I триместре беременности позволяет предупредить рождение ребенка с тяжелой церебральной аномалией.
Одним из методов выявления пороков головного мозга у грудничков является нейросонография через родничок. Намного более точные данные у детей любого возраста и у взрослых получают при помощи МРТ головного мозга. МРТ позволяет определить характер и локализацию аномалии, размеры кист, гетеротопий и других аномальных участков, провести дифференциальную диагностику с гипоксическими, травматическими, опухолевыми, инфекционными поражениями мозга. Диагностика судорожного синдрома и подбор антиконвульсантной терапии осуществляется при помощи ЭЭГ, а также пролонгированного ЭЭГ-видеомониторинга. При наличии семейных случаев церебральных аномалий может быть полезна консультация генетика с проведением генеалогического исследования и ДНК-анализа. С целью выявления сочетанных аномалий проводится обследование соматических органов: УЗИ сердца, УЗИ брюшной полости, рентгенография органов грудной полости, УЗИ почек и пр.
Лечение
Терапия пороков развития головного мозга преимущественно симптоматическая, осуществляется детским неврологом, неонатологом, педиатром, эпилептологом. При наличии судорожного синдрома проводится антиконвульсантная терапия (карбамазепин, леветирацетам, вальпроаты, нитразепам, ламотриджин и тд ). Поскольку эпилепсия у детей, сопровождающая аномалии развития головного мозга, обычно резистентна к противосудорожной монотерапии, назначают комбинацию из 2 препаратов (например, леветирацетам с ламотриджином). При гидроцефалии осуществляют дегидратационную терапию, по показаниям прибегают к шунтирующим операциям. С целью улучшения метаболизма нормально функционирующих мозговых тканей, в какой-то степени компенсирующих имеющийся врожденный дефект, возможно проведение курсового нейрометаболического лечения с назначением глицина, витаминов гр. В и пр. Ноотропные препараты используются в лечении только при отсутствии эписиндрома.
При умеренных и относительно легких церебральных аномалиях рекомендована нейропсихологическая коррекция, занятия ребенка с психологом, комплексное психологическое сопровождение ребенка, детская арт-терапия, обучение детей старшего возраста в специализированных школах. Указанные методики помогают привить навыки самообслуживания, уменьшить степень выраженности олигофрении и по возможности социально адаптировать детей с церебральными пороками.
Прогноз во многом определяется тяжестью церебральной аномалии. Неблагоприятным симптомом выступает ранее начало эпилепсии и ее резистентность к осуществляемой терапии. Осложняет прогноз наличие сочетанной врожденной соматической патологии.
Основные медуслуги по стандартам лечения | ||
Клиники для лечения с лучшими ценами
|
Источник
Последствиями патологии являются разрывы сосудистой стенки с кровоизлияниями, ишемия, аневризмы. Лечение только хирургическое, направленное на удаление, эмболизацию или облитерацию мальформации.
Что это такое
В норме вены с артериями соединяются обширной сетью мелких капилляров. Функция последних – перенос питательных веществ из крови в ткани органов. Диффузия возможна за счет однослойного строения стенки капилляров. При мальформации часть капиллярной сети заменяется более крупными извитыми сосудами. Чаще всего этот клубок представляет собой комбинацию вен с артериями – в этом случае речь идет об артериальновенозной мальформации сосудов головного мозга (сокращенно АВМ). Иногда наблюдаются аномалии только одного типа.
Чем опасна данная патология? При небольшом размере конгломерата он может продолжительное время не проявлять себя, однако крупные образования очень опасны. Прежде всего риском разрыва, так как сосудистая стенка мальформации деформированная, истонченная. Вероятность такого исхода составляет до 4% в год, при этом повторное кровоизлияние наступает в 2 раза чаще. Летальный исход в случае разрыва – 1 случай из десяти, а стойкая инвалидизация наступает в половине из них. Если же помимо мальформации имеются аневризмы, смертность повышается.
Еще одно вероятное последствие – ишемия тканей мозга. Сброс крови напрямую из артерий в вены приводит к тому, что участки мозгового вещества, расположенные ниже по направлению тока крови, лишаются кислорода с питательными веществами. Результатом продолжительного «голодания» становятся дисфункция и отмирание тканей по типу ишемического инсульта.
Несмотря на то что заболевание достаточно редкое – 2 случая на 100 000 – из-за негативных последствий и высокой летальности ему уделяется особое внимание в неврологии.
Классификация
Сосудистая мальформация, находящаяся в головном мозге, может состоять только из вен, артерий либо быть комбинированной. Последний вариант – артериальновенозный – встречается чаще всего.
По типу строения церебральные АВМ подразделяются на:
- Рацемозные (составляют ¾ от общего количества) – разветвленный сосудистый конгломерат.
- Фистулезная – представляет собой массивный шунт между крупными сосудами.
- Кавернозная – скопление тонкостенных полостей, внешне напоминающее ягоды шелковицы (диагностируется в 11% случаев АВМ).
- Микромальформация – небольшое по размерам образование.
Среди изолированных выделяют венозную мальформацию, артериальную, телеангиоэктазию. Аномалии различают также по размеру. Диаметр малых не превышает 30 мм, средних – 60 мм, а крупные – это клубки больше 6 см. Для диагностики и лечения имеет значение локализация дефекта: в легких случаях они расположены вне функционально значимых зон, к которым относятся мозговой ствол, височные и затылочные доли, таламус, сенсомоторная кора, речевая область, центр Брока. Важен также характер дренирования, то есть наличие выхода в крупные вены.
Перечисленные параметры классификации важны для определения риска в случае операции. Каждый из них (локализация, тип дренирования, размер) оценивается по трехбалльной шкале, и в зависимости от суммы набранных баллов определяется операционный риск. Низкий – это 1, а пятерка означает повышенную техническую сложность вмешательства, высокую вероятность инвалидизации или летального исхода.
Причины
В большинстве случаев артериовенозная мальформация головного мозга – следствие нарушения формирования церебральной сосудистой сети во внутриутробном периоде. Генетический фактор не доказан, поэтому наследственность роли, предположительно, не играет. Негативное влияние на развитие системы мозгового кровообращения у плода оказывают хронические заболевания будущей матери, внутриутробные инфекции, повышение радиационного фона. Тератогенный эффект дают также прием некоторых препаратов, интоксикации, наличие у беременной вредных привычек (алкоголизм, наркомания, курение).
Частота кровоизлияний у детей с цереброваскулярной патологией данного типа невелика. Обычно заболевание впервые проявляется после достижения 20-летнего возраста. По мере взросления пациента риск разрыва образования возрастает. Приобретенные мальформации встречаются очень редко, манифестируя к 50 годам. Среди причин развития болезни выделяют атеросклеротические, склеротические изменения сосудистой стенки, а также черепно-мозговые травмы.
Симптомы
Симптоматика заболевания зависит от типа его протекания. Первый, геморрагический, наблюдается более чем в половине случаев (по статистике, до 70%). Он характерен для сосудистых мальформаций небольших размеров. Второй вариант клинических проявлений – торпидный – встречается при крупных и средних образованиях.
Геморрагическое течение патологии
Мелкие конгломераты, характерные для этого типа протекания, могут не проявляться годами. Часто первым признаком заболевания становится разрыв дефектной стенки сосуда с последующим кровоизлиянием. Если артериовенозная аномалия дислоцируется в задней черепной ямке и имеет дренирующие вены, появляется такой клинический симптом, как артериальная гипертензия. В случае разрыва развивается симптоматика геморрагического инсульта:
- интенсивная головная боль;
- тошнота с приступами рвоты;
- парестезии, параличи, мышечная слабость;
- спутанность и потеря сознания;
- расстройства мозговой деятельности (координации, зрения, речи).
Перечисленные признаки свойственны субарахноидальному кровоизлиянию (кровотечение происходит между мозговыми оболочками). На его долю приходится почти половина от общего числа случаев. В остальных кровь изливается непосредственно в мозг с образованием гематом различной локализации. Наиболее опасны из них внутрижелудочковые. К общей симптоматике при внутримозговом кровоизлиянии присоединяются специфические симптомы, по которым можно определить пораженную область мозга.
Торпидное течение патологии
В отличие от геморрагического, о наличии сосудистой мальформации можно судить еще до ее разрыва. Крупные и средние по размеру аномалии проявляются регулярными кластерными головными болями. Приступы могут длиться на протяжении 3 часов, на их фоне нередко развивается судорожный синдром. Еще одним характерным признаком может стать неврологический дефицит, свойственный для опухолей мозга.
В этом случае развиваются общемозговые симптомы: диффузные головные боли распирающего характера, расстройства психики и зрения, рвота, эпиприступы. По характеру эпилептических припадков и предшествующей им ауры можно достаточно достоверно установить местоположение мальформации. Когда она оказывает давление на близлежащие ткани и отдаленные структуры, к общемозговой симптоматике присоединяется очаговая. В зависимости от локализации могут наблюдаться нарушения когнитивных функций, парезы лицевых нервов, параличи конечностей и другие неврологические расстройства.
АВМ вены Галена
Отдельный вид врожденной цереброваскулярной патологии у детей, характеризующийся комплексом дефектов развития большой мозговой вены, включая шунтирование. Встречается достаточно редко, однако в большинстве случаев приводит к летальному исходу.
Единственный вид лечения – нейрохирургическая операция в первый год жизни. Основные симптомы определяются сразу после рождения у половины младенцев с данным типом АВМ: сердечная недостаточность, гидроцефалия. В последующем наблюдается отставание в психическом и физическом развитии.
Диагностика
До разрыва сосудистая мальформация геморрагического типа часто никак не проявляется и может быть обнаружена случайным образом. При торпидном течении заболевания поводом для обращения к неврологу служат головные боли, появление судорожного синдрома, очаговых признаков. На основании жалоб врач назначает консультацию нейрохирурга, который проводит комплексное обследование:
- электроэнцефалографию;
- эхоэнцефалографию;
- реоэнцефалографию;
- КТ и МРТ;
- церебральную ангиографию.
Компьютерная и магнитно-резонансная томография в случае патологии торпидного типа может оказаться неинформативной. Для подтверждения диагноза предпочтительна ангиография с использованием контрастного вещества. При разрыве весь комплекс диагностических мероприятий проводится экстренно, наибольшей информативностью при этом обладает МРТ.
Как лечится мальформация
Лечение аномалии до ее разрыва сводится к исключению конгломерата из кровотока. Выполняется эта задача одним из трех методов: эмболизацией АВМ головного мозга, транскраниальным или радиохирургическим удалением. Методика подбирается с учетом всех операционных рисков, величины и локализации образования.
Операция проводится по показаниям также после разрыва, когда состояние пациента стабилизируется. На остром этапе возможно только удаление гематомы. Комбинированное вмешательство (экстракция сгустка и иссечение АВМ) показано при небольших размерах образования.
Хирургическое удаление
Выполняется транскраниально после трепанации черепа, если объем сосудистой мальформации не превышает 100 мл. Применяется при неглубоком залегании конгломерата вне функционально значимых областей мозга. В ходе операции приводящие сосуды перекрываются методом коагуляции, конгломерат выделяется, отводящие вены перевязываются, АВМ иссекается полностью.
Классическое удаление в большинстве случаев гарантирует полное выздоровление, однако требуется прием ноотропов с ангиопротекторами в восстановительном периоде. Обязательно систематическое наблюдение у врача, поскольку вероятны осложнения – инсульты.
Эмболизация АВМ
Менее травматичная методика лечения, направленная не на удаление, а на окклюзию цереброваскулярной аномалии. С помощью микрокатетера, введенного в разрез бедренной артерии, в мальформацию вводят специальный сополимер, склеивающий сосуды. Данный способ используется только в том случае, когда имеются приводящие сосуды, доступные для катетеризации.
Кроме того, эмболизация проводится в несколько этапов, а полной окклюзии удается добиться только у трети пациентов. Поэтому часто эта манипуляция проводится в качестве подготовительной перед хирургическим иссечением. Предварительное склеивание части сосудов уменьшает риск операционных кровотечений и осложнений в послеоперационном периоде.
Радиохирургический метод
Как и классическая хирургическая операция, позволяет полностью удалить аномалию (однако размер ее не должен превышать 3 см). Этот способ используется, когда транскраниальный доступ к сосудистой мальформации мозга затруднен, а также нет возможности провести эмболизацию. Операция представляет собой часовое облучение пораженной зоны узконаправленным излучением. После этого происходит постепенное склерозирование АВМ в течение нескольких лет.
Недостатком радиохирургического лечения является долго ожидание полного закрытия сосудов, поскольку сохраняется вероятность разрыва. Поэтому современные методики чаще всего состоят из разных типов операций. Например, сначала делается частичная эмболизация, а затем АВМ удаляется хирургически.
Последствия и прогнозы
Наиболее вероятный исход мальформации – это ее разрыв со всеми специфическими симптомами и последствиями геморрагического инсульта. Степень инвалидизации, вероятность летального исхода зависят от объема и локализации кровоизлияния. Повторные разрывы повышают процент смертности. Однако есть возможность дожить до преклонных лет без хирургического вмешательства, что наблюдается примерно в половине случаев АВМ.
Если появляются характерные мозговые симптомы в виде головных болей, эпиприступов, обращение к неврологу и начало лечения помогут избежать осложнений. Каков процент выздоровления после операции? Радиохирургическое и классическое удаление – 85%, эмболизация – около 30%. В комбинации эти методики более эффективны и дают почти стопроцентный результат. Из послеоперационных осложнений наиболее вероятным является инсульт.
Источник
