Антифосфолипидный синдром при беременности реферат
Статья посвящена особенностям течения антифосфолипидного синдрома у беременных и вариантам терапии
Беременность существенным образом влияет на иммунную систему матери: депрессия клеточного звена иммунитета, повышенная секреция иммуноглобулинов, снижение функции лимфоцитов вследствие экспрессии особых белков PSP (pregnancy-specific proteins). Все эти преобразования направлены на выживание плода. Процессы изменения цитокинового профиля Т-хелперов 2 типа являются доминирующими в поддержании «иммунотолерантности» при беременности и могут влиять на различные аутоиммунные заболевания. Существует ряд феноменов, с помощью которых можно увидеть влияние ревматической патологии на беременность, и наоборот. Процессы эти носят разнонаправленный характер: с одной стороны, может отмечаться как дебют системного аутоиммунного заболевания (САЗ), так и обострение существующей патологии (например, вспышка люпус-нефрита), с другой стороны, описаны многочисленные случаи ремиссии, индуцированной беременностью, у пациенток с ревматоидным артритом. Кроме того, аутоиммунная дисфункция, характерная для САЗ, наличие антифосфолипидных антител (АФА) могут привести к повышению риска выкидыша, гибели плода и преэклампсии. Трансплацентарный транспорт патологических макромолекул, особенно анти-Ro/La или SS-A, SS-B антител, напрямую влияет на плод и повышает вероятность развития неонатальной волчанки. Наконец, высокая иммуновоспалительная активность, поражение внутренних органов в рамках САЗ могут оказать существенное влияние на показатели материнской и фетальной смертности.
Беременность вызывает множество физиологических изменений в организме матери помимо дисфункции иммунной системы. Так, отмечается значительное увеличение объема циркулирующей крови (до 40–45%), что может усугубить течение заболеваний почек или сердечно-сосудистой системы. Скорость клубочковой фильтрации (СКФ) увеличивается примерно на 50% при нормальном течении беременности, поэтому у пациентки с предшествующей протеинурией почти наверняка будет отмечаться некоторое увеличение количества белка в моче. В результате изменений коагуляционного звена гемостаза, активности тромбоцитов, фибринолиза, венозного стаза, компрессии сосудов беременной маткой, вынужденного постельного режима повышается вероятность тромботических осложнений. Отмечаются отек и кровоточивость десен, желудочно-пищеводный рефлюкс, значительные потери костной массы из-за беременности, лактации, а также возможного применения глюкокортикостероидов (ГКС). Таким образом, даже нормальная беременность может усугубить течение САЗ.
Физиологические или патологические изменения, в т. ч. вызванная беременностью гипертензия, могут также имитировать активность САЗ, что представляет собой определенные трудности при проведении дифференциального диагноза. Например, покраснение или гиперпигментацию лица легко спутать с центробежной скуловой сыпью по типу «бабочки». Ладонная эритема у беременных может выглядеть, как кожный васкулит. Физиологический лейкоцитоз, анемия и низкий уровень тромбоцитов вследствие гемодилюции, распространенной у беременных, могут имитировать гематологические проявления САЗ. В результате повышения уровня фибриногена, анемии может отмечаться ускорение скорости оседания эритроцитов, и данный параметр не может быть объективным маркером активности заболевания. Многие женщины предъявляют жалобы на диффузные артралгии, боли в мышцах и костях, особенно во время первой беременности. Гипертензия, протеинурия, почечная недостаточность и отеки, связанные с гестозом, могут имитировать различные заболевания или их обострение, включая волчаночный нефрит, острую склеродермическую нефропатию, рецидив васкулита, некротизирующего гломерулонефрита. HELLP-синдром – вариант преэклампсии, характеризующийся низким количеством тромбоцитов, повышенным уровнем печеночных ферментов, гемолизом, болью в животе, может имитировать системную красную волчанку (СКВ) или обострение системного васкулита. Наконец, эклампсию, которая включает в себя судорожный синдром или нарушение мозгового кровообращения, можно спутать с поражением центральной нервной системы при СКВ или нейроваскулитом.
Антифосфолипидный синдром
В начале 1950-х гг. антифосфолипидный синдром (АФС) был описан как вариант СКВ или волчаночноподобного синдрома. Однако очень скоро было установлено, что связь между гиперпродукцией АФА и тромботическими нарушениями наблюдается в отсутствие достоверных клинических и серологических признаков СКВ или какого-либо другого ведущего заболевания. Для определения этой новой нозологической формы был предложен термин «первичный антифосфолипидный синдром».
Разработка методов радиоиммунологического (1983) и иммуноферментного анализа для определения антител к кардиолипину способствовала расширению исследований, касающихся роли АФА при заболеваниях человека. Оказалось, что эти антитела являются серологическим маркером своеобразного симптомокомплекса, включающего венозные и/или артериальные тромбозы, различные формы акушерской патологии (в первую очередь привычное невынашивание беременности), тромбоцитопению, а также другие разнообразные неврологические, кожные, сердечно-сосудистые, гематологические нарушения. В 1986 г. G. Hughes et al. предложили обозначать этот симптомокомплекс как АФС. В 1994 г. на VI международном симпозиуме, посвященном изучению АФА, было предложено называть АФС синдромом Hughes – по имени английского ревматолога, впервые описавшего его и внесшего наибольший вклад в разработку этой проблемы.
В 2006 г. в Сиднее произошел последний пересмотр критериев этого заболевания. Несколько изменена была трактовка клинических проявлений, в лабораторные критерии добавлены антитела к бета-2 гликопротеину I (АБ2ГП) (табл. 1). На основе австралийских критериев в настоящее время строится практическая диагностика АФС.
![Таблица 1. Дополненные критерии антифосфолипидного синдрома (Сидней, 2006) [1] Таблица 1. Дополненные критерии антифосфолипидного синдрома (Сидней, 2006) [1]](https://www.rmj.ru/upload/medialibrary/f85/f85acd6d40c7dfd5904308d4df8c6b29.png)
Клинический спектр проявлений, которые связывают с АФС, достаточно широк: мигрень, артриты/артралгии, легочная гипертензия, livedo reticularis, язвы ног и др. Хотя большинство из них не были включены в итоговые критерии диагностики АФС от 2006 г., место этих феноменов активно обсуждается в литературе.
Потеря беременности является частым осложнением АФС в акушерской практике, кроме того, обращает на себя внимание тот факт, что преэклампсия и эклампсия часто встречаются при сочетании АФС и СКВ. HELLP-синдром в сочетании с циркуляцией АКЛА протекает тяжелее и часто встречается во II, а не III триместре. Риск развития инфаркта печени у пациентов с HELLP-синдромом, ассоциированным с АКЛА, увеличивается в 30 раз по сравнению с таковым при серонегативном варианте HELLP-синдрома [2]. Кроме того, при АФС часто развиваются другие множественные тромботические осложнения, которые требуют более агрессивного лечения, чем у пациентов с традиционным течением HELLP-синдрома. Сама по себе беременность является фактором риска развития гиперкоагуляции, и при появлении АФС вероятность тромбозов у матери существенно увеличивается. В редких случаях во время беременности может формироваться катастрофический АФС: в проанализированных работах было выявлено 15 случаев, характерной особенностью которых явился тот факт, что почти половина пациенток до этого имела в анамнезе латентно протекающий АФС [3]. Пациентки могут иметь и другие гематологические осложнения АФС, такие как выраженная тромбоцитопения во II и III триместрах беременности.
Наиболее распространенными нежелательными явлениями, связанными с АФС у беременных, являются преждевременные роды и задержка внутриутробного развития. Преждевременные роды наиболее часто встречаются у пациенток, у которых есть сочетание АФС и СКВ, а заболеваемость колеблется от 10 до 40%. В одном исследовании авторы попытались определить причины неблагоприятных неонатальных исходов (преждевременные роды, задержка внутриутробного развития, низкая оценка по шкале Апгар). Такими факторами явились присутствие ВАК, АКЛА, АБ2ГП антител, наличие в анамнезе сосудистых тромбозов перед беременностью. При отсутствии этих факторов (даже при наличии предшествующего отягощенного акушерского анамнеза) отмечался более благоприятный неонатальный исход [4].
В редких случаях у плода или новорожденного формируются тромбозы вследствие трансплацентарного транспорта АФА. В таких случаях речь может идти о наличии неонатального АФС [5]. Риск тромбозов в данной когорте пациентов уменьшается вместе со снижением концентрации материнских АФА, однако в дальнейшем отмечаются затруднение обучаемости, снижение памяти и других когнитивных функций. В настоящее время существуют регистры (European registry to babies born to mothers with antiphospholipid syndromе) по наблюдению за отдаленными нейропсихическими последствиями неонатального АФС [6].
ВАК, по-видимому, является наиболее важным фактором риска неблагоприятного исхода беременности, в т. ч. ее потери. В настоящее время способы определения концентрации ВАК являются нестандартизованными в отличие от тестов, связанных с определением антикардиолипинов и бета-2 гликопротеина I. В настоящее время завершается многоцентровое проспективное наблюдательное исследование PROMISSE, основная цель которого – наблюдение за АФС-позитивными и СКВ-ассоциированными беременными женщинами. Недавний анализ промежуточных данных установил, что только уровень ВАК является единственным лабораторным маркером АФС, связанным с такими неблагоприятными исходами беременности, как интранатальная гибель плода, задержка внутриутробного развития и преждевременные роды [7]. С другой стороны, появляются данные о том, что только совокупность ВАК, АКЛА и АБ2ГП у конкретной пациентки является предиктором интранатальной гибели плода [8]. Эта информация несколько обнадеживает тех пациенток, которые имеют низкий или умеренный титр АКЛА, АБ2ГП. Для своевременной оценки риска тромбозов у пациенток с АФС необходимо проводить тщательный скрининг на наличие маркеров наследственной тромбофилии (гены фибринолиза: PAI-I, PLAT; гены тромбоцитарных рецепторов: ITGA2, ITGB3, Gplba; гены системы свертывания крови: Fl, F2, F5, F7), наличие гипергомоцистеинемии [8–10]. В последнее время появляются данные о взаимосвязи изменения уровня комплемента в сыворотке во время беременности и неблагоприятных исходов. Интерпретация этого феномена представляется весьма затруднительной: при эклампсии и первичном АФС возможно повышение титра, а при СКВ и вторичном АФС – гипокомплементемия. Комплемент является важным прогностическим фактором неблагоприятного исхода беременности и смертности в мышиной модели АФС [11], представляется вероятным, что активация системы комплемента играет такую же негативную роль и в человеческой популяции.
Рекомендации по ведению беременных женщин с АФС
Своевременное становление лечения акушерского АФС относится к 1980–1985 гг., когда пациентки с наличием АКЛА, ВАК и акушерскими неудачами стали получать ГКС (преднизолон) и ацетилсалициловую кислоту (АСК) в небольших дозах. Более того, дозу ГКС постепенно увеличивали вплоть до достижения ВАК или другими маркерами АФС приемлемых уровней. В 1990-х гг. исследования показали, что низкие дозы гепарина в сочетании с малыми дозами АСК оказались столь же эффективными, как ГКС, но с гораздо меньшим количеством побочных эффектов. На сегодняшний момент комбинация антитромбоцитарных препаратов и прямых антикоагулянтов является стандартной: дозировка низкомолекулярного гепарина (НМГ) обычно – 40 мг эноксапарина ежедневно, некоторые специалисты используют 30 мг 2 р./сут, доза для нефракционированного гепарина (НФГ) обычно – 5000 ЕД 2 р./сут [12].
Исследования показывают, что сочетание низких доз гепарина и низких доз АСК более эффективно, чем монотерапия АСК [13], с успешностью около 75% против 40%. Не получено принципиальных отличий между малыми и высокими дозами антикоагулянтов, а также НФГ и НМГ гепарина [14, 15]. Такой вид терапии относится к первой линии и является наиболее эффективным в плане профилактики потери беременности на ранних сроках [16].
Терапия второй линии включает в себя применение внутривенного человеческого иммуноглобулина (ВВИГ). Некоторые эксперты на этом этапе рекомендуют увеличение дозы гепарина до общетерапевтических доз. В единственном контролируемом исследовании с использованием ВВИГ не было получено достоверного улучшения исходов беременности. Однако существует значительное количество неконтролируемых исследований, опубликованных клинических случаев с блестящим эффектом при комбинированном применении ВВИГ, низких доз АСК и НМГ. При дальнейшем повышении уровня АКЛА, ВАК с успехом может применяться плазмаферез. Наиболее перспективными методами лечения АФС в будущем являются ингибирование комплемента [11], а также применение средств генно-инженерной биологической терапии [17].
Лечение средними/высокими дозами ГКС в настоящее время практически не применяется из-за отсутствия доказательств их эффективности и негативного воздействия на организм как матери, так и плода. Применение ГКС оправданно, только если АФС развивается на фоне какого-то заболевания (СКВ, болезни Шегрена и др.). Использование ГКС в этих случаях направлено на лечение не АФС, а основного заболевания.
В послеродовом периоде антикоагулянтная терапия должна быть продолжена на срок от 6 до 8 нед. даже у пациенток без тромбозов в анамнезе.
Тактика ведения беременных с АФС, режим дозирования во многом зависят от предшествующего анамнеза (наличия/отсутствия неплацентарных тромбозов, количества спонтанных абортов, предшествующей терапии). В связи с этим можно выделить следующие подгруппы:
1. Пациентки только с серологическими маркерами АФС (без предшествующей беременности, с одним эпизодом необъяснимого спонтанного аборта до 10 нед. гестации), без тромбозов в анамнезе.
Тактика ведения этой категории женщин заключается в применении малых доз АСК, которая назначается на весь период беременности и в течение 6 мес. после родоразрешения.
При наличии у беременных высокопозитивных АКЛА (более 65 ЕД GPL) целесообразно назначение НМГ. Риск развития тромботических осложнений высок не только во время беременности, но и в послеродовом периоде (в течение 6 мес. после родов). При родоразрешении естественным путем целесообразно возобновление лечения НМГ в послеродовом периоде. В случае проведения кесарева сечения введение НМГ отменяется за 2—3 дня и возобновляется в послеродовом периоде с последующим переходом на прием непрямых антикоагулянтов.
2. Пациентки с АФС без неплацентарных тромбозов в анамнезе и женщины с серологическими маркерами АФС и двумя или более необъяснимыми спонтанными абортами (до 10 нед. гестации) в анамнезе.
Тактика ведения данной категории беременных заключается в сочетанном применении малых доз АСК (50–150 мг/сут) с момента зачатия до родоразрешения и НФГ (эноксапарина и др.) или НФГ (5000–10 000 ЕД каждые 12 ч) с момента документированной беременности и до родов. Через 12 ч после родов необходимо возобновить лечение НМГ, НФГ (или варфарином).
Длительная терапия гепарином у беременных женщин может приводить к развитию остеопороза. Вследствие этого все беременные, получающие гепаринотерапию, обязательно должны принимать препараты кальция (1500 мг/сут) и витамина D3 (не менее 1000 МЕ/сут).
3. Пациентки с АФС и неплацентарными тромбозами в анамнезе (получавшие варфарин до беременности).
Необходимо до 6 нед. беременности отменить варфарин. В последующем беременная принимает АСК в низких дозах в сочетании с НФГ.
4. При неэффективности стандартной терапии в период следующей беременности применяют иммуноглобулин в/в 0,4 г/кг в течение 5 сут каждый месяц беременности.
Источник
Всего лишь сорок лет назад врачи даже не подозревали о существовании антифосфолипидного синдрома. Открытие принадлежит врачу Грэму Хьюзу, который практиковал в Лондоне. Он подробно описал его симптомы и причины возникновения, поэтому иногда АФС еще называют синдромом Хьюза.
При развитии антифосфолипидного синдрома в крови появляются антифосфолипидные антитела (АФЛА), способствующие усиленному образованию тромбов в просветах сосудов. Они могут стать причиной осложнения беременности и даже вызвать ее прерывание. Чаще всего АФС диагностируют у женщин в возрасте 20-40 лет.
Содержание:
- Патогенез развития антифосфолипидного синдрома
- Особенности диагностики АФС
- Причины развития АФС
- Виды АФС
- Опасность антифосфолипидного синдрома
- Осложнения АФС
- Антифосфолипидный синдром во время беременности
- Как обнаружить АФС во время беременности
- Какие системы организма страдают при АФС, симптомы нарушений
- Лечение АФС
- Антифосфолипидные антитела в крови – норма или патология?
Патогенез развития антифосфолипидного синдрома
В крови человека на фоне антифосфолипидного синдрома начинают циркулировать антитела, которые разрушают фосфолипиды, находящиеся в мембранах клеток тканей организма. Фосфолипиды присутствуют в тромбоцитах, в нервных клетках, в клетках эндотелия.
Фосфолипиды могут быть нейтральными и отрицательно заряженными. В последнем случае их называют анионными. Именно эти два вида фосфолипидов встречаются в крови чаще остальных.
Так как фосфолипиды могут быть разными, то и антитела к ним вырабатываются разные. Они способны вступать в реакцию как с нейтральными, так и с анионными фосфолипидами.
Определяют антифосфолипидный синдром по иммуноглобулинам, которые появляются в крови при развитии заболевания.
Среди них различают:
Волчаночные иммуноглобулины lgG, lgM. Впервые эти антитела были выявлены у пациентов с системой красной волчанкой. При этом удалось обнаружить у них повышенную склонность к тромбозам.
Антитела к кардиолипиновому антигену. Этот компонент теста позволяет обнаружить у человека сифилис. При этом в его крови будут циркулировать антитела класса A, G, M.
Антитела, которые представлены сочетанием кардиолипина, фосфатадилхолина и холестерина. Они способны давать положительный результат при проведении реакции Вассермана (диагностика сифилиса), но этот результат бывает ложным.
Суммарные иммуноглобулины классов A, G, M (бета-2-гликопротеин-1-кофакторзависимые антитела к фосфолипидам). Так как бета-2-гликопротеин-1 являются фосфолипидами-антикоагулянтами, то появление к крови антител, направленных на их уничтожение, приводит к усиленному формированию тромбов.
Обнаружение антител к фосфолипидам позволяет диагностировать антифосфолипидный синдром, выявление которого сопряжено с рядом трудностей.
Особенности диагностики АФС

Антифосфолипидный синдром дает ряд патологических симптомов, которые наталкивают на мысль о данном нарушении. Однако, чтобы выставить верный диагноз, потребуется провести лабораторные исследования. Причем их будет немалое количество. Сюда входит сдача крови на общий и биохимический анализ, а также проведение серологических тестов, дающих возможность обнаружить антитела к фосфолипидам.
Применение одного метода исследования недостаточно. Часто пациентам назначают анализ на реакцию Вассермана, который способен давать положительный результат не только при антифосфолипидном синдроме, но и при иных заболеваниях. Это приводит к постановке неверного диагноза.
Чтобы минимизировать вероятность врачебно-диагностической ошибки, следует назначать пациенту с симптомами АФС комплексное обследование, которое должно включать в себя:
Обнаружение волчаночных антител – это анализ, который при подозрении на АФС выполняют в первую очередь.
Обнаружение антител к кардиолипиновому антигену (реакция Вассермана). При АФС анализ будет положительным.
Тест на бета-2-гликопротеин-1-кофакторозависимые антитела к фосфолипидам. Показатели этих антител будут превышать допустимые границы нормы.
Если антитела в крови появились ранее, чем за 12 недель до манифестации первых симптомов АФС, то их нельзя считать достоверными. Также на их основании не подтверждают диагноз АФС, если анализы стали положительными лишь спустя 5 дней от дебюта болезни. Итак, чтобы подтвердить диагноз «антифосфолипидный синдром», требуется наличие симптомов нарушения и положительный тест на антитела (положительную реакцию должно дать хотя бы одно исследование).
Дополнительные методы диагностики, которые может назначить врач:
Анализ ложноположительной реакции Вассермана.
Проведение пробы Кумбаса.
Обнаружение в крови ревматоидного фактора и антинуклеарного фактора.
Определение криоглобулинов и титра антител к ДНК.
Иногда врачи, при подозрении на АФС, ограничиваются забором крови на обнаружение волчаночного антикоагулянта, но в 50% случаев это приводит к тому, что нарушение остается неустановленным. Поэтому при наличии симптомов патологии, следует проводить максимально полное исследование. Это позволит вовремя обнаружить АФС и начать терапию. Кстати, современные медицинские лаборатории имеют тесты, которые дают возможность провести именно комплексную диагностику, так как они оснащены всеми необходимыми реагентами. Между прочим, в некоторых таких системах в качестве вспомогательных компонентов используется змеиный яд.
Причины развития АФС

Антифосфолипидный синдром чаще всего манифестируется на фоне таких патологий, как:
Системная красная волчанка.
Системная склеродермия, ревматоидный артрит, синдром Шегрена.
Раковые опухоли в организме.
Лимфопролиферативные заболевания.
Аутоиммунная тромбоцитопеническая пурпура, которая может быть спровоцирована системой красной волчанкой, склеродермией или ревматоидным артритом. Наличие пурпуры в разы повышает риск развития антифосфолипидного синдрома.
ВИЧ-инфекция, мононуклеоз, гепатит С, эндокардит, малярия. АФС может развиваться при вирусных, бактериальных и паразитарных инфекциях.
Заболевания, поражающие ЦНС.
Период вынашивания ребенка, роды.
К АФС может иметься наследственная предрасположенность. При этом в фенотипе крови человека будут иметься специфичности DR4, DR7, DRw53.
Прием некоторых лекарственных препаратов, например, психотропных, противозачаточных и оральных контрацептивов.
Чем дольше в крови присутствуют антифосфолипидные антитела, тем быстрее у человека разовьется АФС. Причем причина их появления не имеет значения.
Виды АФС
Различают следующие виды АФС:
Первичный антифосфолипидный синдром, который развивается сам по себе, то есть его началу не предшествует какое-либо заболевание.
Вторичный антифосфолипидный синдром, который развивается на фоне аутоиммунной патологии, например, при системной красной волчанке.
Катастрофический антифосфолипидный синдром, который диагностируют редко, но при этом данная форма патологии является крайне опасной. Развивается заболевание стремительно и приводит к формированию тромбов по всем сосудам организма. Часто такой синдром становится причиной летального исхода.
АФЛА-негативный синдром, который сложно обнаружить. При этой форме болезни в крови отсутствуют волчаночные антитела и антитела к кардиолипину.
Синдром Снеддона – это заболевание, которое развивается на фоне АФС. При этом у человека случаются эпизоды тромбоза сосудов головного мозга. Симптомами нарушения являются синюшные кожные покровы и повышенное артериальное давление. Синдром Снеддона относят к одному из возможных вариантов течения болезни.
Опасность антифосфолипидного синдрома
Антитела к фосфолипидам, которые появляются при АФС, нарушают нормальное функционирование системы гемостаза. Это приводит к тому, что в сосудах начинают формироваться тромбы, у человека развивается тромбоз.
При АФС страдают не только капилляры, но и крупные сосуды. В целом, тромбы могут образовываться в любой вене или артерии, которые несут кровь к разным органам. Поэтому симптомы данного нарушения весьма разнообразны.
Осложнения АФС
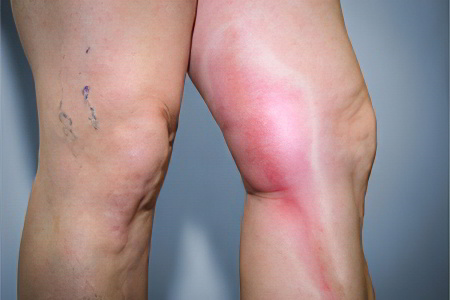
Антифосфолипидный синдром провоцирует формирование тромбов в сосудах. Чаще всего от тромбоза страдают вены нижних конечностей. Если тромб отрывается, то с током крови он попадает в сосуды, питающие легочную ткань. Это влечет за собой развитие опасного состояния, которое называется тромбоэмболия легочной артерии. Если тромб перекрывает магистральный сосуд легкого, то происходит его инфаркт, прекращается сердечная деятельности. Часто ТЭЛА заканчивается гибелью больного, причем летальный исход может наступить очень быстро.
Когда тромб перекрывает мелкие сосуды, у человека имеется шанс на восстановление, но при этом он должен быть экстренно доставлен в медицинское учреждение. Даже в этом случае вероятность возникновения тяжелых последствий для здоровья крайне высока.
Тромбы при АФС могут образовываться в почечных артериях. На фоне таких тромбозов развиваются тяжелые почечные патологи, например, синдром Бадда-Киари.
Реже тромбы формируются в капиллярах сетчатки глаза, в подключичных венах, в центральных венах надпочечников, что ведет к развитию недостаточности этих органов. Также на фоне тромбоза возможно развитие синдрома нижней или верхней полой вены.
Тромбоз с закупоркой артерий различной локализации может приводить к инфаркту, гангрене, некрозу головки бедра.
Антифосфолипидный синдром во время беременности

Развитие антифосфолипидного синдрома во время беременности может приводить к таким серьезным последствиям, как:
Прерывание беременности.
Выкидыш на ранних сроках беременности. Риск самопроизвольного аборта тем выше, чем больше в крови женщины циркулирует антител к кардиолипиновому антигену.
Развитие фетоплацентарной недостаточности, которая ведет к гипоксии плода с задержкой его развития. При неоказании медицинской помощи сохраняется высокий риск внутриутробной гибели ребенка.
Развитие гестоза с эклампсией и преэклампсией.
Развитие хореи.
Формирование тромбов.
Повышение артериального давления.
Развитие HELLP-синдрома с гемолизом, поражением паренхимы печени и с тромбоцитопенией.
Преждевременная отслойка плаценты.
Ранние роды.
На фоне АФС попытки зачать ребенка методом экстракорпорального оплодотворения могут заканчиваться неудачно.
Как обнаружить АФС во время беременности
Женщины, которые находятся в группе риска по развитию АФС, должны быть у врача на особом контроле.
По показаниям, им могут быть назначены следующие диагностические процедуры:
Регулярное выполнение гемостазиограммы.
Внеплановое УЗИ плода с допплерографией маточно-плацентарного кровотока.
УЗИ сосудов ног, головы, шеи, почек, глаз.
ЭхоКГ для проверки работы сердечных клапанов.
Это позволит своевременно обнаружить развитие серьезных осложнений беременности, таких как: ДВС-синдром, пурпура, ГУС.
Кроме врача-гинеколога беременной женщине с диагностированным антифосфолипидным синдромом может потребоваться консультация иных узких специалистов, например, ревматолога, кардиолога, невролога и пр.
Лечение сводится к приему глюкокортикостероидов и препаратов-антиагрегантов. Дозу должен подбирать врач. Также могут быть назначены гепарины и иммуноглобулины. Эти препараты вводят на фоне контроля картины крови.
Ели женщина уже страдает от АФС, но не планирует беременность, то для контрацепции ей не следует использовать гормональные препараты. В противном случае можно усугубить течение болезни.
Какие системы организма страдают при АФС, симптомы нарушений

Антифосфолипидный синдром сопряжен с риском развития различных заболеваний. Причем пострадать могут любые органы и системы, даже головной мозг. При поражении его сосудов возможно развитие транзиторной ишемической атаки или инфаркта.
Это сопровождается такими симптомами, как:
Появление судорог.
Слабоумие, которое постоянно прогрессирует.
Нарушения психики.
Также АФС может проявляться следующими неврологическими симптомами:
Выраженные головные боли, протекающие по типу мигрени.
Неконтролируемая дрожь конечностей.
Симптомы, характерные для поперечного миелита. Они возникают по той причине, что при АФС страдает спинной мозг.
Самым грозным осложнением при поражении сердца является инфаркт. Он развивается при условии, что тромбы формируются в коронарных артериях. Если задействованы их мелкие ответвления, то инфаркту будет предшествовать нарушения сокращения сердца. Также АФС может привести к развитию порока сердца, к формированию внутрисердечного тромба. Такие косвенные признаки антифосфолипидного синдрома способны затруднять диагностику причины болезни.
Симптомы АФС в зависимости от того, какой именно орган оказался поражен тромбозом, будут следующими:
Повышение артериального давления наблюдается при тромбозе почечных артерий.
При закупорке тромбом легочной артерии развивается ТЭЛА, что ведет к резкому ухудшению самочувствия человека. Иногда гибель больного может наступить мгновенно.
Кровотечение в желудочно-кишечном тракте.
Инфаркт селезенки.
Появление подкожных кровоизлияний, некроз кожи, язвы на ногах – все эти симптомы развиваются при поражении дермы.
Клиника АФС разнообразна. Точные симптомы описать невозможно, так как в патологический процесс могут быть вовлечены любые органы и системы.
Лечение АФС

Лечение АФС должно быть комплексным. Основная его направленность – это предотвращение осложнений тромбозов.
Больной обязательно должен соблюдать следующие рекомендации:
Отказаться от непосильных физических нагрузок.
Нельзя долгое время оставаться без движения.
Отказ от травматических видов спорта.
Отказ от перелетов.
Медикаментозная терапия сводится к назначению следующих препаратов:
Варфарин – препарат из группы непрямых антикоагулянтов.
Гепарин, Надропарин кальция, Эноксапарин натрия – препараты, относящиеся к прямым антикоагулянтам.
Аспирин, Дипиридамол, Пентоксифиллин – препараты-антиагреганты.
Ели больной находится в тяжелом состоянии, то ему вводят высокие дозы глюкокортикостероидов, выполняют переливание плазмы.
Прием антикоагулянтов и антиагрегантов должен быть длительным. Иногда эти препараты назначают пожизненно.
АФС – это не приговор. Если заболевание диагностировано на начальном этапе его развития, то прогноз благоприятный. При этом пациент должен соблюдать все рекомендации врача, принимать препараты, которые он ему назначает. Женщины имеют высокие шансы на зачатие и рождение здорового ребенка.
Осложняет течение болезни системная красная волчанка, тромбоцитопения, стойкое повышение артериального давления, высокий уровень антител к кардиолипиновому антигену с тенденцией к их росту.
В обязательном порядке пациент с диагностированным АФС должен наблюдаться у ревматолога. Ему потребуется регулярно сдавать кровь на анализ, а также проходить иные диагностические и лечебные процедуры.
Антифосфолипидные антитела в крови – норма или патология?
Иногда уровень антифосфолипидных антител может быть повышен у здорового человека. У 12% людей эти антитела присутствуют в крови, но заболевания при этом у них не развивается. Чем старше человек, тем выше могут быть показатели патологических иммуноглобулинов. Также имеется вероятность возникновения ложноположительной реакции Вассермана, к чему пациент должен быть готов. Главное не впадать в панику и пройти комплексную диагностику.
Видео: АФС и другие тромбофилии в акушерстве:
Автор статьи: Волков Дмитрий Сергеевич | к. м. н. врач-хирург, флеболог
Образование:
Московский государственный медико-стоматологический университет (1996 г.). В 2003 году получил диплом учебно-научного медицинского центра управления делами президента Российской Федерации.
Наши авторы
Источник
