Гиперэозинофильный синдром что это такое
Гиперэозинофильный синдром (ГЭС) – причины, механизмы развития эозинофилииГиперэозинофильный синдром (ГЭС) — это гетерогенная группа заболеваний, для которых характерны повышенный уровень эозинофилов в крови и повреждение внутренних органов. Первое упоминание о злокачественной эозинофилии принадлежит Stillman, который в 1912 г. описал группу больных с выраженной эозинофилией в крови и тяжелым течением заболевания. Выделяют три основные группы заболеваний, протекающих с эозинофилией:
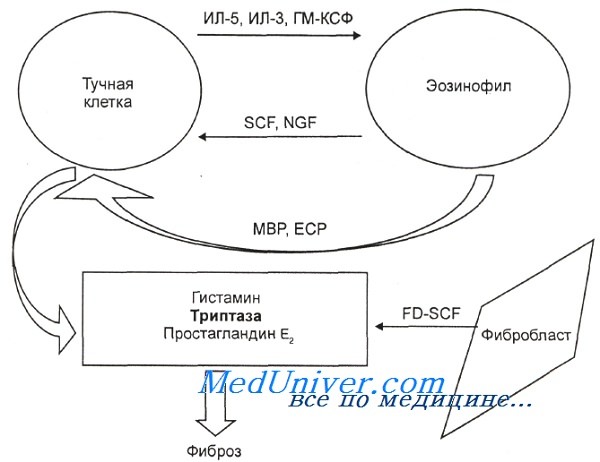
Эозинофилии 1-й группы неклонального генеза (симптоматические, реактивные) наблюдаются при следующих заболеваниях: При аллергических состояниях и инфекциях активируются Th2-клетки, продуцирующие ИЛ-5. Кроме того, активированные эозинофилы способны к аутокринной стимуляции путем секреции ИЛ-1, ИЛ-5, TGFa и PAF.
Вторую большую группу эозинофилии представляют эозинофилии, сопровождающие клональные заболевания кроветворной ткани. При гемобластозах эозинофилы могут быть частью злокачественного клона: например, эозинофилы при Ph-позитивном хроническом миелолейкозе. В других случаях лейкозные клетки могут продуцировать цитокины, стимулирующие пролиферацию нормальных эозинофилов. Dombret назвал такие эозинофилии параклональными. В современной классификации опухолей гемопоэтической и лимфоидной тканей ВОЗ (2001) выделены хронический эозинофильный лейкоз (ХЭЛ)/гиперэозинофильный синдром (ГЭС), относящийся к группе миелопролиферативных заболеваний, и острый миеломонобластный лейкоз (ОММЛ) с увеличенным количеством эозинофилов костного мозга с inv(16)(p13;q22) или t(16;16)(p13;q22) (CBFb/MYH11). Кроме этих двух заболеваний, эозинофилии могут сопровождать еще ряд гемобластозов:
Тем не менее у многих больных даже после тщательного поиска не удается найти какой-либо известной причины эозинофилии. В этих случаях может быть диагностирован идиопатический ГЭС. Этиология гиперэозинофильного синдрома до сих пор полностью не ясна. Предполагают, что гиперэозинофильный синдром является гетерогенной группой заболеваний, в основе которой лежит либо вторичная эозинофилия, вызванная гиперпродукцией эозинофилотропных цитокинов клональной популяцией лимфоцитов, либо это первичное миелопролиферативное заболевание. Признаки клональности удается обнаружить не всегда даже с помощью современных методов диагностики. Многие авторы высказывают предположение, что в основе гиперэозинофильного синдрома лежит увеличенная пролиферация Т-клеток, секретирующих ряд цитокинов. В 1993 г. Н. Suzushima и соавт. у пациента с типичной клинической картиной гиперэозинофильного синдрома выявили цитогенетические поломки в популяции клеток, имеющих фенотип CD3+, CD4-, CD8. Позже Е. Cogan и соавт. сообщили о клональной пролиферации Т-хелперов типа 2, секретирующих ИЛ-5, у больного гиперэозинофильным синдромом. Далее появились работы, доказывающие, что у некоторых пациентов с необъяснимой эозинофилией удается обнаружить популяцию Т-клеток с аберрантным иммунофенотипом или имеющих явные цитогенетические поломки. В последующем у отдельных больных развивались лимфопролиферативные заболевания. Косвенным подтверждением роли Т-хелперов в развитии гиперэозинофильного синдрома может быть эффективное лечение циклоспорином А и хлордеоксиаденозином (2CDA), который, как известно, подавляет пролиферацию Т-хелперов. Возможно, у части больных с гиперэозинофильным синдромомна момент диагностики патологический Т-клеточный клон не удается выявить доступными методами.
В дальнейшем у этой категории больных по мере прогрессирования болезни и выявления признаков лимфопролиферации диагноз гиперэозинофильного синдрома может быть пересмотрен. Открытие реаранжировки позволило не только получить новые сведения об этиологии гиперэозинофильного синдрома, который может теперь рассматриваться как миелопролиферативное заболевание по крайней мере у части больных, но и объясняет эффективность лечения больных гиперэозинофильным синдромом гливеком. Независимо от этиологических факторов отсутствие адекватного лечения гиперэозинофильного синдрома (ГЭС) ведет к фатальному повреждению жизненно важных внутренних органов. – Также рекомендуем “Дифференциация гиперэозинофильного синдрома и хронического эозинофильного лейкоза (ХЭЛ)” Оглавление темы “Онкогематология”:
|
Источник
Гиперэозинофильный синдром является состоянием, которое характеризуется эозинофилией периферической крови с проявлениями поражения или дисфункции систем органов, обусловленных непосредственно эозинофилией у пациентов без паразитарных, аллергических или других вторичных причин эозинофилии. Симптомы разнообразны и зависят от того, дисфункция каких органов имеет место. Диагноз включает исключение других причин эозинофилии и дополнительно – исследование костного мозга и цитогенетические анализы. Лечение начинается с преднизолона и, при одном распространённом подтипе, включает иматиниб.
Гиперэозинофильный синдром раньше считался идиопатическим, а сейчас считается результатом различных заболеваний, некоторые причины которых известны. Одним ограничением традиционного определения является то, что оно не включает пациентов с наличием некоторых аналогичных патологий (например, хромосомных дефектов), которые являются широко известными причинами гиперэозинофильного синдрома, но не соответствуют его традиционным диагностическим критериям относительно степени или продолжительности эозинофилии. Еще одним ограничением является то, что некоторым больным с эозинофилией и повреждениями органов, которые характеризуют гиперэозинофильный синдром, необходимо начинать лечение ранее 6 месяцев, необходимых для подтверждения традиционных диагностических критериев. Эозинофилия любой этиологии может вызывать такие же виды повреждения тканей.
Гиперэозинофильный синдром является редким заболеванием, имеет неизвестную частоту распространения и чаще всего поражает людей в возрасте от 20 до 50 лет. Только у некоторых больных с длительной эозинофилией развивается дисфункция органов, которая характеризует гиперэозинофильный синдром. Хотя затронут может быть любой орган, но чаще всего это сердце, легкие, селезенка, кожа или нервная система. Вовлечение сердца может вызвать значительную заболеваемость и летальность.
Миелопролиферативный
Лимфопролиферативный
Миелопролиферативный вариант часто связан с небольшой интерстициальной делецией хромосомы 4 на участке CHIC2 которое вызывает связанный с FIP1L1/PDGFRA гибридный ген (имеющий тирозинкиназную активность, которая способна трансформировать гематопоэтические клетки). У больных часто наблюдается:
Спленомегалия
Тромбоцитопения
Анемия
Повышенный уровень витамина B12
Гипогранулярные или вакуолизированные эозинофилы
Миелофиброз
У пациентов с миелопролиферативным подтипом часто развивается эндомиокардиальный фиброз и редко возникает острая миелоидная лейкемия или острая лимфобластная лейкемия. Пациенты, имеющие связанный с FIP1L1/PDGFRA гибридный ген, чаще являются мужчинами и могут быть восприимчивы к приему низких доз иматиниба (ингибитор тирозинокназы).
Небольшая часть пациентов с миелопролиферативным вариантом гиперэозинофильного синдрома имеет цитогенетические изменения, которые затрагивают бета-рецептор тромбоцитарного фактор роста (PDGFRB) и может также отвечать на применение ингибиторов тирозин-киназы, таких как иматиниб (1). К другим цитогенетическим аномалиям относится реаранжировка гена рецепторов 1 фактора роста фибробластов (FGFR1) или гена янус-киназы-2 (JAK2).
Лимфопролиферативный вариант связан c клональной популяцией Т-клеток с аберрантным фенотипом. Метод ПЦР показывает клональную перестановку генов рецепторов Т-клеток. У больных часто наблюдаются:
Ангионевротический отек, кожные нарушения, или оба признака
Гипергаммаглобулинемия (особенно IgE)
Циркулирующие иммунные комплексы (иногда с сывороточной болезни)
Пациенты с лимфопролиферативным подтипом также восприимчивы к кортикостероидам, а иногда у них развивается Т-клеточная лимфома.
Другие формы гиперэозинофильного синдрома включают хронический эозинофильный лейкоз, синдром Глейча (циклическая эозинофилия и отек Квинке), семейный гиперэозинофильный синдром, отображаемый 5q 31-33, и другие специфические синдромы органов. При органоспецифических эозинофильных синдромах эозинофильная инфильтрация ограничивается одним органом (например, эозинофильное заболевание желудочно-кишечного тракта, хроническая эозинофильная пневмония—2).
Гиперлейкоцитоз может возникать у пациентов с эозинофилическим лейкозом и большим количеством эозинофилов (например, > 100 000 клеток/мкл). Эозинофилы могут образовывать агрегаты, которые закупоривают мелкие кровеносные сосуды, что приводит к ишемии тканей и микроинфарктам. Общие проявления включают гипоксию мозга или легких (например, энцефалопатия, одышка или дыхательная недостаточность).
Подтипы гиперэозинофильного синдрома
Характеристика | Миелопролиферативный | Лимфопролиферативный |
Генетика | Перестановка генов PDGFRA, PDGFRB, FGFR1 или JAK2 | Клональная популяция Т-клеток с аберрантным фенотипом |
Клинические проявления и результаты лабораторных исследований | Анемия Повышенный уровень витамина B12 Эндомиокардиальная Фиброз Гипогранулярные или вакуолизированные эозинофилы Миелофиброз Спленомегалия Тромбоцитопения | Ангионевротический отек Циркулирующие иммунные комплексы (иногда с сывороточной болезни) Гипергаммаглобулинемия (особенно IgE) Кожные аномалии |
Повышенный риск заболевания в будущем | Острый лимфобластный лейкоз Острый миелобластный лейкоз | Т-лимфоцитарная лимфома |
Восприимчивость к лекарственным препаратам | Иматиниб и другие ингибиторы тирозинкиназы | Кортикостероиды |
1. Apperley JF, Gardembas M, Melo JV, et al: Response to imatinib mesylate in patients with chronic myeloproliferative diseases with rearrangements of the platelet-derived growth factor receptor beta. N Engl J Med 347:481–487, 2002.
2. Gotlib J : World Health Organization-defined eosinophilic disorders: 2017 update on diagnosis, risk stratification, and management. Am J Hematol 92:1243–1259, 2017.
Клинические проявления
Аномалии у больных с гиперэозинофильным синдромом
Система | Распространенность | Проявления |
Конституционная | ≈ 50% | Анорексия Усталость Лихорадка Миалгии Слабость Снижение веса |
Кардиопульмональная | > 70% | Пристеночные тромбы с эмболами Рестриктивная или инфильтративная кардиомиопатия или митральная или трикуспидальная регургитация, сопровождаемая кашлем, одышкой, сердечной недостаточностью, аритмиями, эндомиокардиальной болезнью, легочными инфильтратами, и плевральными выпотами экссудатами |
Кожа | > 50% | Ангионевротический отек Дерматографизм Зуд Высыпания (включая экзему и крапивницу) |
Гематологические проявления | > 50% | Анемия Лимфаденопатия Спленомегалия Тромбоэмболические проявления Тромбоцитопения |
Неврологические симптомы | > 50% | Церебральные эмболы с очаговыми симптомами Диффузная энцефалопатия с измененным поведением и когнитивной функцией и мышечной спастичностью Периферическую нейропатию |
Желудочно-кишечные | > 40% | Колики в животе Диарея Тошнота |
Иммунологические | ≈ 40% | Циркулирующие иммунные комплексы при сывороточной реакции Повышенные уровни иммуноглобулинов (особенно IgE) |
Иногда у больных с тяжелой формой эозинофилии (например, количеством эозинофилов > 100 000/мкл) развиваются такие осложнения гиперлейкоцитоза, как проявления гипоксии мозга или легких (например, энцефалопатия, одышка, дыхательная недостаточность). Также могут возникать и другие тромботические проявления (например, пристеночные тромбы сердца).
Исключение вторичной эозинофилии
Тесты на определение поврежденного органа
Исследование костного мозга с проведением цитогенетического исследования
Обследование для выявления гиперэозинофильного синдрома должно быть проведено в случае, если уровень эозинофилов в периферической крови пациента >1500/мкл больше чем в одном необъяснимом случае, особенно когда есть симптомы поражения органов. Должно быть проведено исследование для исключения заболеваний, вызывающих эозинофилию.
Оценка поражения органов должна включать биохимические анализы крови (включая уровень ферментов печени, креатинкиназы, определение почечной функции и уровня тропонина); ЭКГ; эхокардиографию; исследование функции легких и КТ органов грудной клетки, брюшной полости, и таза. Для выявления связанного с FIP1L1/PDGFRA гибридного гена и других возможных причин эозинофилии проводят пункцию костного мозга и биопсию с использованием проточной цитометрии, цитогенетические анализы и ПЦР с обратной транскрипцией или флюоресцентную гибридизацию in situ (FISH).
К смерти обычно приводят нарушения в органах, особенно в сердце. Поражение сердца не предсказывается степенью или длительностью эозинофилии. Прогноз варьируется в зависимости от реакции на терапию. Реакция на иматиниб дает лучший прогноз течения болезни среди пациентов со связанным с FIP1L1/PDGFRA гибридным геном и другими восприимчивыми гибридными генами. Данная терапия улучшает прогноз.
Кортикостероиды для гиперэозинофилии и для продолжения лечения повреждений органов
Иматиниб для пациентов со связанным с FIP1L1/PDGFRA гибридным геном или другими сходными гибридными генами
Иногда применение препаратов для контроля содержание эозинофилов (например, гидроксимочевина, интерферон альфа, этопозид, кладрибин)
Поддерживающая терапия
Лечение включает немедленную терапию, радикальную терапию (лечение, направленное на устранение самого заболевания) и поддерживающую терапию (1).
Больным с очень тяжелой эозинофилией, осложнениями гиперлейкоцитоза или при обоих случаях одновременно (как правило, у пациентов с эозинофильным лейкозом) как можно скорее должны быть назначены высокие дозы кортикостероидов (например, преднизолон 1 мг/кг или его аналог). Если содержание эозинофилов намного ниже (например, на ≥ 50%) по истечении 24 ч, дозу кортикостероида можно повторять ежедневно. В противном случае начинают альтернативное лечение (например, гидроксимочвиной). Как только число эозинофилов начинает уменьшаться и лучше поддаваться контролю, можно начинать прием дополнительных препаратов.
Больных с FIP1L1/PDGFRA-ассоциированным гибридным геном (или сходными гибридными генами) обычно лечат с помощью иматиниба (2) и кортикостероидов, особенно при подозрении на поражение сердца. Если иматиниб неэффективен или плохо переносится можно использовать другой ингибитор тирозинкиназы (например, дазатиниб, нилотиниб, сорафениб), или же можно провести трансплантацию аллогеннных гемопоэтических стволовых клеток.
Пациентам без связанного с FIP1L1/PDGFRA гибридного гена, даже при бессимптомном течении, часто назначают одну дозу преднизона 60 мг (или 1 мг/кг) перорально, для определения восприимчивости к кортикостероидам (т. е., уменьшение уровня эозинофилов). У больных с симптомами и повреждениями в органе, такую же дозу преднизолона продолжают давать в течение 2 недель, затем снижают ее с каждым днем. Пациенты без симптомов и повреждения органов находятся под наблюдением в течение по крайней мере 6 месяцев для контроля за возможными осложнениями. Если употребление кортикостероидов не может быть легко снижено, то могут быть использованы кортикостероидо-щадящие препараты (например, гидроксимочевина, интерферон альфа).
Поддерживающая лекарственная терапия и операция могут потребоваться при симптомах нарушений сердца (например, инфильтративная кардиомиопатия, поражения клапанов сердца, сердечная недостаточность). Антитромбоцитарные препараты (например, аспирин, клопидогрел, тиклопидин) необходимы при тромботических осложнениях; антикоагулянты показаны если сохраняется пристеночный тромб левого желудочка или если, несмотря на использование аспирина, сохраняются транзиторные ишемические атаки.
Применение меполизумаба и других анти-интерлейкин-5-антител при лечении гиперэозинофильного синдрома на данный момент проходит клинические испытания. Меполизумаб является полностью гуманизированным моноклональным антителом, ингибирующим интерлейкин 5 (регулятор выработки эозинофилов). Меполизумаб уменьшает эозинофилию и потребность в терапии кортикостероидами в высоких дозах (3), в настоящее время он доступен для использования в США для пациентов с рефрактерным гиперэозинофильным синдромом.
Гиперэозинофильный синдром является эозинофилией периферической крови (> 1500/мкл) не вызванный паразитными, аллергическими, или другими вторичными причинами эозинофилии, которая длится ≥ 6 месяцев и вызывает или дисфункцию поражение органов.
По-видимому, гиперэозинофильный синдром является проявлением большого числа гематопоэтических нарушений, некоторые из которых имеют генетические причины.
Может быть поражен любой орган, но как правило, поражаются сердце, легкие, селезенка, кожа, и нервная система; поражение сердца может вызвать значительную заболеваемость и летальность.
Проводят анализы на вовлечение органов, включая ферменты печени; креатинкиназу и уровни креатинина и тропонина; ЭКГ и эхокардиографию; исследования функции легких; и КТ груди, брюшной полости, и таза.
Для выявления причины выполняют исследование костного мозга с цитогенетическим анализом.
При тяжелой эозинофилии и/или повреждения органаов назначают кортикостероиды. Ингибиторы тирозинкиназы, такие как низкие дозы иматиниба, могут оказывать благоприятное действие при подтипах, связанных с явными хромосомными расстройствами.
Источник

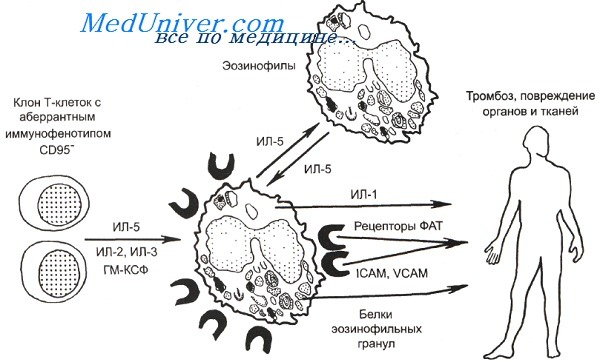 Патогенез лимфопролиферативного варианта гиперэозинофильного синдрома.
Патогенез лимфопролиферативного варианта гиперэозинофильного синдрома.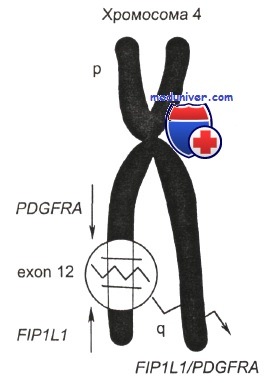 Хромосомная поломка при миелопролиферативном варианте гиперэозинофильного синдрома
Хромосомная поломка при миелопролиферативном варианте гиперэозинофильного синдрома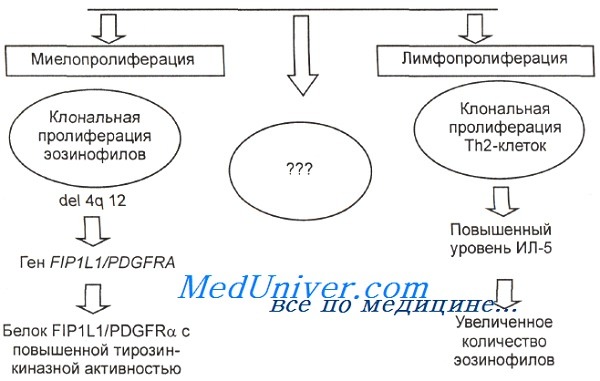 Этиология идиопатического гиперэозинофильного синдрома.
Этиология идиопатического гиперэозинофильного синдрома.