Гисо желудка код по мкб
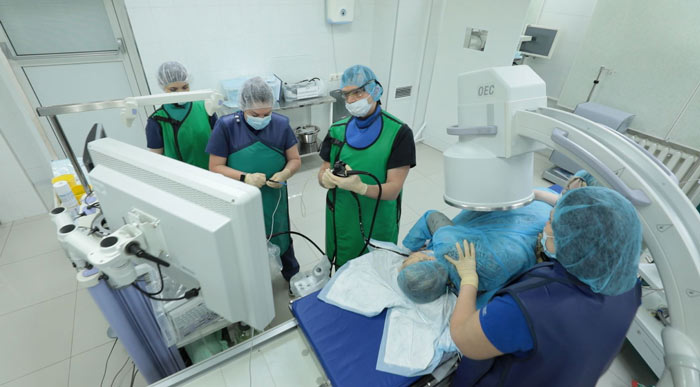
Гастроинтестинальные стромальные опухоли (ГИСО, ГИСТ) появились чуть больше 20 лет назад, когда усовершенствовали электронный микроскоп, их выделили из компании разнообразных лейомиом. ГИСТ — русскоязычная аббревиатура с английского. Это опухоли зрелого возраста, до 40 лет они встречаются очень редко, преобладают мужчины в середине седьмого десятка жизни. Предполагается, что заболеваемость не растет, просто диагностика стала лучше.

Причина стромальных опухолей
Стромальные опухоли происходят из мезенхимы, из которой у зародыша формируется соединительная ткань и мышцы, некоторые оболочки сосудов и кожа. Причина ГИСО — сбой в формировании гладкомышечной ткани. Подозревают, что родоначальником ГИСО становятся клетки, отвечающие за ритмичное сокращение — перистальтику органов желудочно-кишечного тракта. Они обладают электрической активностью и переносят возбуждение с нервного волокна на мышечное, поэтому носят сложное имя «возбудимые интерстициальные клетки Кахала». ГИСТ и клетки Кахала похожи по строению и обладают мутировавшим геном c-kit, кодирующим синтез определенного белка.
В ГИСО белок отвечает за все жизненно важные процессы, а поскольку он регулирует образование и жизнь опухолевых клеток, он становится онкобелком. Мутировавший с-KIT имеется в 95 из сотни гастроинтестинальных стромальных новообразований. ГИСО не наследуются, не имеют «своего предрака», возникают на фоне полного здоровья, не существует факторов риска. Если вы эпизодически ощущаете желудочный дискомфорт, пройдите обследование в Европейской онкологической клинике, специалисты которой знают всю патологию ЖКТ.
Диагностика ГИСО
В диагностике ГИСО возможности клиники определяют всё – нет возможностей — нет такого заболевания. Идеально сочетание эндоскопии с УЗИ — эндосонография, которая позволяет видеть внутри и за пределами желудка — состояние рядом находящихся структур и всю толщину желудочной стенки.
Главный диагностический критерий — иммуногистохимическое выделение в опухолевых клетках онкобелка KIT (CD117). Этот онкобелок синтезируют мелкоклеточный рак легкого и глиобластома, лейкоз из тучных клеток, метастазы меланомы и сосудистые образования, то есть возможен ложноположительный ответ при не гастроинтестинальной стромальной опухоли, к примеру, при поражении желудка или кишки лейкозом.
Дикими называют стромальные опухоли без с-KIT, таких пять на сотню всех гастроинтестинальных новообразований, внешне они ничем не отличаются от положительных по с-KIT, но течение и реакция на лекарственные препараты у них другая. Поскольку при диагностике с-KIT определяется только в двух экзонах из четырех, но в двух не исследуемых он может быть. В диких опухолях возможна мутация альфа-PDGFR или рецептора инсулинового фактора роста (IGF1R). Когда вообще не находят ни единого маркера, то выполняется молекулярно-генетический анализ, он способен выделить стромальную опухоль, негативную по всем известным критериям диагностики.
ГИСО растет под неизмененной слизистой, заметить маленький узел может только специалист с большим опытом наблюдения стромальных образований.
Симптомы стромальных опухолей желудка
Каждую пятую опухоль обнаруживают случайно при обследовании по другому поводу, узел же может постигать трети метра, ничем серьезным себя не проявляя. Причина частого бессимптомного течения — подслизистый рост, когда опухоль распластывается в стенке и выбухает наружу — в брюшную полость. К моменту обнаружения стромального образования у каждого третьего уже выявляются метастазы, преимущественно в печень, часто — канцероматоз брюшины, а вот легочная ткань поражается нечасто.
Никаких специфических проявлений нет, такие же симптомы возникают при других заболеваниях желудочно-кишечного тракта. В среднем от появления первых признаков неблагополучия до выявления патологического образования проходит почти полгода.

Клиника похожа на гастрит: быстрое насыщение малыми порциями еды, чувство распирания под ложечкой, может быть эпизодическое вздутие живота. По мере увеличения узла появляется тошнота и рвота недавно съеденным. Боли нехарактерны, они отмечаются только у каждого седьмого пациента и практически никогда не бывает клинической картины «острого живота». ГИСТ не прорастает в другие органы, а оттесняет их с анатомического «законного» места.
У половины пациентов имеются признаки желудочного кровотечения: слабость, анемичность крови, эпизоды жидкого черного стула из-за изъязвления слизистой над распадающейся крупной ГИСТ.
Что характерно только для ГИСТ?
Это не клинические симптомы, а сочетание стромальной опухоли с другими новообразованиями у девочек и молодых женщин. Синдром проявляется в сочетании ГИСО с параганглиомой, как правило, на шее или в животе, и доброкачественными гамартомами легких. Называется триада Карнея, сегодня таких пациентов чуть больше сотни. Гамартомы никак себя не проявляют, их обнаруживают при рентгеновском обследовании, а гормонально активная параганглиома вызывает повышение давления. Составляющие триаду процессы появляются с интервалом в несколько лет.
Когда гастроинтестинальное стромальное образование сопровождается множественными параганглиомами, то это синдром Карнея-Стратакиса, он генетически наследуется и вызван недостатком одного фермента, опять-таки поражает женщин. От врачей зависит своевременность выявления возможных метастазов, когда они хорошо лечатся. В Европейской онкологической клинике кумулирован опыт клинического наблюдения,что помогает изменить прогноз заболевания на благоприятный.
Лечение и химиотерапия
При любой злокачественной опухоли радикально лечит только удаление, и при ГИСТ ведущий метод — хирургический. При поражении желудка выполняются резекция или удаление всего органа — гастрэктомия, всё зависит от объема поражения. Лапароскопические операции следует делать только в специализированных учреждениях, поскольку имеется опасность разрыва неплотной псевдокапсулы с выбросом опухолевых клеток в брюшную полость.
Химиотерапия иматинибом имеет хорошую перспективу при наличии мутации гена с-KIT, применяется при метастатической стадии или рецидиве после операции, перед хирургическим этапом для уменьшения размера образования и объема операции. Доза иматиниба зависит от расположения мутации гена KIT, так она увеличивается двукратно при мутации в 9 экзоне. При прогрессировании на фоне химиотерапии используют лекарства второй линии: сунитиниб и дазатиниб. Их используют и при устойчивости ГИСО к иматинибу. В качестве третьей линии лечения применяется регорафениб.
Все ГИСТ активные химиопрепараты относятся к таргетным средствам — точно нацеленным, что не исключает токсические реакции на них. Химиотерапия не обязательно должна сопровождаться плохим качеством жизни, у специалистов Европейской онкологической клиники есть возможности минимизации побочных реакций. А при метастазах ГИСО в печени в клинике выполняется методика радиочастотной аблации, которой владеют единицы российских специалистов.
Источник
Гастроинтестинальные стромальные опухоли – новая разновидность сарком желудочно-кишечного тракта. В статье расскажем о симптомах и разновидностях заболевания, опишем лечение и профилактику
Это опухоли зрелого возраста, до 40 лет они встречаются очень редко, преобладают мужчины в середине седьмого десятка жизни.
Предполагается, что заболеваемость не растет, просто диагностика стала лучше.
Перед вами фрагмент клинической рекомендации из Медицинской экспертной системы Консилиум. Развернуть рекомендацию полностью вы можете в системе. Если вы не подписчик, воспользуйтесь пробным доступом.
Диагнозы по МКБ:
C15 Злокачественное новообразование пищевода
C16 Злокачественное новообразование желудка
C17.0 Злокачественное новообразование двенадцатиперстной кишки
C17.2 Злокачественное новообразование подвздошной кишки
C17.3 Злокачественное новообразование дивертикула Меккеля
C18 Злокачественное новообразование ободочной кишки
C19 Злокачественное новообразование ректосигмоидного соединения
C20 Злокачественное новообразование прямой кишки
C48.0 Злокачественное новообразование забрюшинного пространства
C48.1 Злокачественное новообразование уточненных частей брюшины
Жалобы и анамнез
Для выявления факторов, которые могут повлиять на выбор тактики лечения, необходим тщательный сбор жалоб и анамнеза у пациента
Физикальное обследование
Тщательный физикальный осмотр с оценкой нутритивного статуса.
Лабораторная диагностика
- развернутые клинический и биохимический анализы крови
- исследование свертывающей системы крови
- анализ мочи
Инструментальная диагностика
Предоперационное обследование включает следующие методы:
- клинические
- рентгенологические
- эндоскопические
Основными инструментальными методами в диагностике ГИСО являются эндоскопическое исследование и компьютерная томография (КТ) с в/в контрастированием.
Патоморфологический диагноз устанавливается на основании гистологического и обязательного иммуногистохимического исследования (CD117 и/или DOG1) биоптата или хирургически удаленной опухоли.
В CD117 и/или DOG1 негативных опухолях необходим анализ мутационного статуса опухоли.
- Эзофагогастродуоденоскопия (ЭГДС) при локализации опухоли в желудке и двенадцатиперстной кишке
- Тотальная колоноскопия – при гастроинтестинальной стромальной опухоли ободочной кишки
- УЗИ брюшной полости, забрюшинного пространства и малого таза для оценки распространенности опухолевого процесса.
- КТ органов брюшной полости и малого таза с внутривенным контрастированием.
КТ органов брюшной полости является стандартом диагностики у больных стромальными опухолями.
На практике данные исследования могут быть заменены УЗИ органов брюшной полости и малого таза у пациентов с небольшой местной распространенностью опухолевого процесса.
Рентгенография грудной клетки
МРТ органов брюшной полости и малого таза с в/в контрастированием при локализации опухоли в малом тазу или подозрении на ГИСО прямой кишки.
Магнитно-резонансная томография (МРТ) используется как уточняющий метод у пациентов с опухолевым поражением желудка или прямой кишки, а также для определения объема поражения печени (в частности, у больных с противопоказаниями к использованию рентгеноконтрастных препаратов).
Позитроно-эмиссионная томография (ПЭТ)
Позитронно-эмиссионная томография выполняется для оценки метаболического эффекта лечения, а также может применяться при сомнительных результатах компьютерной томографии.
Биопсия опухоли под контролем УЗИ/КТ для морфологической верификации опухоли
Чрескожная пункционная биопсия (core-биопсия) опухоли под контролем УЗИ нежелательна, поскольку может привести к разрыву капсулы опухоли и диссеминации по брюшине и по ходу пункционного канала.
Однако у больных с гигантскими размерами опухоли и/или местно-распространенным процессом core-биопсия допустима для гистологической верификации диагноза с целью определения показаний к предоперационной терапии иматинибом.
ЭКГ
При подготовке к хирургическому лечению с целью оценки функционального статуса по показаниям следует проводить дополнительное обследование:
- ЭхоКГ;
- холтеровское мониторирование сердечной деятельности;
- исследование функции внешнего дыхания;
- УЗДГ сосудов шеи и нижних конечностей;
- консультации кардиолога, эндокринолога, невропатолога и т.п.
Профилактика
Периодичность наблюдения после завершения лечения
В первые 1–2 года физикальный осмотр и сбор жалоб рекомендуется проводить каждые 3–6 месяцев.
На сроке 3–5 лет – 1 раз в 6–12 месяцев.
После 5 лет с момента операции визиты проводятся ежегодно или при появлении жалоб.
У пациентов с высоким риском рецидива перерыв между обследованиями может быть сокращен.
Объем обследования
- Анамнез и физикальное обследование.
- ФГДС или колоноскопия при гастроинтестинальной стромальной опухоли желудка и двенадцатиперстной кишки или ободочной и прямой кишки каждые 3–6 месяцев в зависимости от риска прогрессирования;
- УЗИ органов брюшной полости и малого таза каждые 3–6 месяцев в зависимости от риска прогрессирования;
- Рентгенография органов грудной клетки каждые 12 месяцев;
- КТ органов грудной и брюшной полости с в/в контрастированием каждые 6–12 месяцев в зависимости от риска прогрессирования.
Задачей наблюдения является раннее выявление прогрессирования заболевания с целью раннего начала таргетной терапии и хирургического лечения резектабельных метастатических очагов на фоне эффективного лекарственного лечения.
Полезные инструменты
Открыть справочники:
Стадирование гастроинтестинальных стромальных опухолей по системе TNM7 (2010)
Скачать критерии качества:
Материал проверен экспертами Актион Медицина
Критерии качества специализированной медицинской помощи взрослым при злокачественном новообразовании желудка
Критерии качества специализированной медицинской помощи взрослым при злокачественном новообразовании ободочной кишки, ректосигмоидного соединения, прямой кишки
Критерии качества специализированной медицинской помощи взрослым при злокачественном новообразовании пищевода
Алгоритмы лечения, протоколы первичного приема, новые формы ИДС, памятки для пациентов и врачей — читайте и скачивайте материалы на www.provrach.ru
Источник
- Типы злокачественности
- Причины развития
- Проявления и симптомы
- Диагностика
- Возможности лечения
- Факторы прогноза
GI стромальные опухоли (ГИСО) представляют собой новообразования с различным потенциалом злокачественности, от практически индолентных (низкой степени злокачественности) опухолей до быстро прогрессирующих злокачественных новообразований. ГИСО встречаются по всему кишечному тракту, и большинство из них содержат активирующую мутацию в KIT или тромбоцитарном факторе роста A (PDGFRA). Диагноз ставится с помощью иммуногистохимии, но молекулярный анализ с мутационным анализом имеет первостепенное значение для выбора соответствующей терапии.
Приблизительно 50-70% ГИСО происходят из желудка. Тонкая кишка становится вторым, наиболее распространенным местом, с 20-30% ГИСО. Менее частые места возникновения включают толстую кишку, прямую кишку (5-15%) и пищевод (<5%).
Отдаленные метастазы появляются поздно в большинстве случаев. В отличие от других опухолей мягких тканей, общими метастатическими участками ГИСО становятся печень и брюшина. Средний возраст при постановке диагноза — от 50 до 60 лет.
Классификация
Классификация на основе гистологической оценки клеточного состава опухоли свойственной неклассифицированным саркомам мягких тканей (эпителиоидные, веретеноклеточные и т.д.) сейчас неактуальна.
Вместо гистологической оценки ГИСО используется показатель митотического индекса.
Гастроинтестинальные стромальные опухоли принято делить в соответствии уровнем агрессивности на три подтипа:
- доброкачественные/индолентные;
- неопределенного злокачественного потенциала;
- злокачественные.
Отнесение конкретной опухоли к тому или иному подтипу выполняется путем комплексной оценки четырех показателей.
- Размер опухоли. Большие опухоли более склонны вести себя агрессивно, чем маленькие опухоли. Небольшая ГИСО с размером менее 2 см, может не вызвать проблем в будущем.
- Митотический индекс. Митотический счет – это количество активно делящихся клеток, видимых под микроскопом в заданной области опухоли. Оно говорит врачам о скорости размножения раковых клеток и служит показателем агрессивности опухоли. Низким считается индекс ≤ 5/50, что соответствует 5 видимым делениям в поле 5 мм².
- Место расположения. Опухоли в тонкой кишке и прямой кишке более агрессивны, чем опухоли в желудке.
- Разрыв опухоли. Если поверхность опухоли была повреждена во время операции по ее удалению или если опухоль не была интактной во время операции, существует вероятность того, что опухолевые клетки могли проникнуть в брюшную полость. Иногда это само по себе определяет опухоль как высокий риск.
Причины возникновения и факторы риска
Ученые обнаружили, что клетки могут расти неконтролируемым образом в результате нарушения в их ДНК. В ГИСО специфическая мутация заставляет клеточный фермент, известный как KIT, постоянно включаться.
KIT – это фермент (из группы внутриклеточных тирозинкиназ), ответственный за передачу сигналов роста и выживания внутри клетки. Если он включен, клетка растет или размножается. Выключение этого фермента переводит клетку в состояние покоя. Гиперактивный, неконтролируемый мутантный фермент KIT запускает быстрый рост и бесконечное размножение опухолевых клеток ГИСО.
Понимание этого процесса, уже помогло определить новые методы лечения этой неоплазии.
Факторы риска для ГИСО
Нейрофиброматоз
Наиболее существенным фактором риска для ГИСО становится наличие нейрофиброматоза. Он почти всегда связан с развитием таких новообразований.
Семейный анамнез
Есть редкие случаи появления наследственных ГИСО. Наследственные опухоли характеризуются унаследованными мутациями зародышевой линии в KIT или PDGFRA и дополнительными синдромами, такими как:
- кожная гиперпигментация;
- синдром раздраженного кишечника;
- дисфагия;
- дивертикулез кишечника.
95% ГИСО — KIT-положительные. Но 5% не демонстрируют определяемой экспрессии KIT. В части этих KIT-негативных ГИСО мутации происходят в гене PDGFRA, а не в KIT. Было показано, что иммуноокрашивание с помощью PDGFRA помогает различать KIT-негативные ГИСО и другие желудочно-кишечные поражения мезенхимы.
Мутации BRAF и протеинкиназа Сθ (PKCtheta) также были зарегистрированы в небольшом количестве ГИСО без KIT/PDGFRA. Первоначальные исследования показывают, что ГИСО с мутацией BRAF имеют склонность к тонкой кишке и не связаны с высоким риском злокачественности.
Симптомы
До 75% ГИСО обнаруживаются, когда они меньше 4 см в диаметре и либо бессимптомны, либо связаны с неспецифическими симптомами. Их часто диагностируют случайно во время рентгенологических исследований или эндоскопических или хирургических процедур, выполняемых для исследования заболевания желудочно-кишечного тракта или для лечения неотложных состояний. В Японии массовый скрининг на аденокарциному желудка с помощью верхней эндоскопии привел к увеличению случайных выявлений бессимптомных ГИСО.
В популяционном исследовании средний размер опухолей ГИСО, которые были обнаружены как случайные находки, составлял 2,7 см, по сравнению с 8,9 см для тех, которые были обнаружены на основании симптомов.
Верхнее кровотечение из желудочно-кишечного тракта — наиболее распространенное клиническое проявление ГИСО. Оно отмечается у 40-65% пациентов. Пациенты, которые испытали значительную потерю крови, могут сообщать о недомогании, усталости или одышке при физической нагрузке.
Обструкция может возникать в результате внутрипросветного роста эндофитной опухоли или из-за компрессии просвета из-за экзофитного поражения. Обструктивные симптомы могут быть органоспецифическими (например, затруднение глотания при опухоли пищевода, запор при ректальной опухоли, механическая желтуха при опухоли двенадцатиперстной кишки).
Другие симптомы:
- боль в животе;
- анорексия;
- тошнота;
- рвота;
- потеря веса;
- давление в эпигастрии;
- быстрая насыщаемость.
Методы диагностики
Точный диагноз можно поставить по биопсии. Предварительная диагностика проводится либо путем эндоскопии с одновременным УЗИ, либо с помощью компьютерной томографии (КТ) или МРТ.
При подозрении на метастазирование и для оценки ответа опухоли на лечение показано проведение ПЭТ-сканирования.
Лечение
Таргетная терапия
Хотя хирургическая резекция является предпочтительным методом лечения желудочно-кишечных стромальных опухолей (ГИСО) и предлагает единственный шанс на полное выздоровление, главную роль в лечении играют сейчас ингибиторы тирозинкиназы(TKI). И наиболее распространенными препаратами этой группы стали — Гливек® (Gleevec®) и Сутент® (Sutent®). Иматиниб и сунитиниб соответственно.
Сейчас при устойчивости опухоли к лечению этими препаратами широко используются новые лечебные агенты, такие как регорафениб, а США и Европе — сорафениб и другие.
Стандартные показания для использования ингибиторов тирозинкиназы:
- лечение неоперабельных и/или метастатичных ГИСО;
- предоперационное лечение новообразований, которые могут стать резектабельными с отрицательным краем;
- адъювантное лечение после полной грубой резекции неоплазии, для предотвращения рецидива.
Европейское сообщество медицинской онкологии (ESMO) рекомендует, чтобы оценка ответной реакции на лечение была сложной и что раннее прогрессирование, в частности, должно подтверждаться опытной командой. В большинстве случаев на противоопухолевую активность указывает уменьшение опухоли. Но иногда ответ опухоли определяется только уменьшением ее плотности. Или снижение плотности (с увеличением размера!) может предшествовать последующему уменьшению опухоли.
По данным ESMO, отсутствие прогрессирования опухоли через 6 месяцев лечения также является ответом опухоли.
Хирургическое лечение
До недавнего времени единственным методом лечения ГИСО была операция. Цель операции – полностью удалить опухоль. Однако одна только операция для больших или распространившихся новообразования, дает неутешительные результаты.
Хирургия осталась окончательной терапией для четко локализованных ГИСО. Несмотря на доказанный успех иматиниба и других более новых ингибиторов тирозинкиназы, хирургическая резекция остается выбором выбора и предлагает единственный шанс на полное избавление от ГИСО.
Учитывая способность иматиниба превращать неоперабельные опухоли в частично операбельные, может быть использована циторедуктивная хирургия — удаление максимально-возможного объема опухоли с целью достижения неполной ремиссии. Пациент получает неоадъювантную терапию в течение 6 месяцев, а затем проводится широкая резекция. Это нередко обеспечивает существенное увеличение выживаемости.
Преимущества лечения в Бельгии
- Доступность новейших препаратов. В Бельгии при резистентности опухоли к терапии иматинибом, сунитинибом и регорафенибом у больного есть возможность получить лечение новыми препаратами — сорафенибом, дасатинибом и нилатанибом. Это помогает продлевать жизнь даже в самых сложных случаях.
- Лапароскопическая малоинвазивная хирургия. Она используется в Бельгии при новообразованиях, не превышающих 5 см, расположенных в желудке и тонкой кишке. Преимущества лапароскопической резекции включают более быстрое возобновление нормального питания, более короткое пребывание в стационаре после операции и меньшее использование анальгезии. Краткосрочные результаты при этом остаются такими же, как и при открытой операции.
- Стоимость лечения. Она в Бельгии примерно на 30% ниже, чем в соседних странах Европы и на 60% ниже, чем в США. С учетом высокой стоимости лекарств, этот факт приобретает особую важность.
Прогноз
Согласно данным собранным за период с 2001 по 2011 годы, общая 5-летняя общая выживаемость для пациентов с ГИСО составляет:
- 77% для пациентов с локализованным заболеванием при постановке диагноза;
- 64% для пациентов с регионарным заболеванием;
- 41% для пациентов с метастатическим заболеванием.
Гастроинтестинальная опухоль желудка имеет лучший прогноз, чем неоплазия тонкой кишки схожего размера и митотической скорости. Также, гастроинтестинальная стромальная опухоль желудка имеет гораздо лучший прогноз, чем рак желудка.
Даже после полной резекции первичного ГИСО, по крайней мере, у 50% пациентов развивается рецидив или метастазирование.
Большие опухоли связаны с такими осложнениями, как кровотечение в ЖКТ, непроходимость желудочно-кишечного тракта и перфорация кишечника.
У пациентов с продвинутыми ГИСО, которые получают терапию ингибитором тирозинкиназы, может развиться связанное с опухолью внутрипросветное или внутрибрюшинное кровоизлияние, разрыв, фистула или обструкция, требующие неотложной хирургии.
Получите полную информацию о лечении сложных случаев гастроинтестинальных опухолей в Бельгии — закажите обратный звонок или задайте свой вопрос через форму обратной связи.
Источник
