Клинические проявления дефицита системы комплемента включают синдромы

Главная
- >>
Справочник заболеваний
- >>
Орфанные (редкие) заболевания
- >>
- Дефекты системы комплемента
„
Медсестра докладывает врачу:
– Когда я проверяю пульс у больного, у него усиливается сердцебиение.
Может быть, надо что-то сделать?
– Застегните получше халат.
”
показать еще
Орфанные (редкие) заболевания
Медучреждения, в которые можно обратиться
Общее описание
 Дефекты системы комплемента (ДСК) относятся к первичным иммунодефицитным состояниям человека, среди которых занимают чуть более одного процента случаев. Система комплемента представлена девятью компонентами, которые играют решающую роль в иммунном ответе организма на воздействие инфекционных патогенов. Соответственно, ДСК уменьшают устойчивость человека против болезней. Более часто встречается дефицит следующих факторов: C1, С2, С4, С6 и С10. Дефект каждого из компонентов системы имеет свои характерные клинические признаки.
Дефекты системы комплемента (ДСК) относятся к первичным иммунодефицитным состояниям человека, среди которых занимают чуть более одного процента случаев. Система комплемента представлена девятью компонентами, которые играют решающую роль в иммунном ответе организма на воздействие инфекционных патогенов. Соответственно, ДСК уменьшают устойчивость человека против болезней. Более часто встречается дефицит следующих факторов: C1, С2, С4, С6 и С10. Дефект каждого из компонентов системы имеет свои характерные клинические признаки.
Считается, что данная патология является генетически детерминированной. Наследование осуществляется по аутосомно-рецессивному типу: у гетерозиготных носителей количество дефектного белка комплемента понижено на 50% против нормы, что легко выявляется при лабораторном исследовании. ДСК ведет к развитию клинического пейзажа, характеризующегося развитием септических инфекций и аутоиммунных заболеваний, а дефекты компонента С3 могут закончиться летально. У ряда больных с ДСК инфекционные заболевания протекают без лейкоцитоза. Прогноз заболевания в целом неблагоприятный, однако при своевременной диагностике и непрерывном лечении возможна пролонгация жизни пациентов.
Симптомы дефектов системы комплемента
Заболевания, типичные для дефицита каждого из компонентов:
- Дефицит С1-компонента: системные васкулиты, персистирующие синуиты, отиты, пневмонии, остеомиелит, менингит, сепсис, наследственный ангионевротический отек, люпус-нефрит.
- Дефицит С2-компонента: ксеродерма, капилляротоксикоз, герпетиформный дерматит, ходжкинская лимфома, хронический лимфолейкоз.
- Дефицит С3-компонента: пневмонии, менингиты, флегмоны, перитониты, СКВ, реактивные артриты, дерматиты, гломерулонефрит, синдром Шегрена.
- Дефицит С4-компонента: инфекции не наблюдаются, зато случается СКВ, синдром Шегрена, гиперкератоз ладоней и стоп, инсулинозависимый сахарный диабет.
- Дефицит терминальных компонентов (С5-С9): развитие тяжелых инфекций, вызванных N. meningitidіs и N. Gonorrhoeae, проявляющихся повторяющимися менингококковыми ринофарингитами, пневмониями, менингококкцемией, менингококковым менингитом. Гонорея в этих случаях имеет тяжелое течение и резистентна к антибактериальным препаратам.
Диагностика дефектов системы комплемента
Возможна с помощью следующих лабораторных методик:
- ОАК: анемия, лейкопения, тромбоцитопения, эозинофилия;
- количественное определение IgJ, IgМ и IgA;
- детекция уровня общего IgE в сыворотке;
- исследование фагоцитов;
- определение изогемагглютининов для оценки уровня IgM в сыворотке;
- определение уровня хлора в поте и оценка экзокринной функции поджелудочной железы;
- постановка кожных аллергических проб;
- определение титра комплементной активности: сниженный или неопределяемый уровень титра комплементной активности свидетельствует о наследственной недостаточности системы комплемента;
- определение количества Т- и В-лимфоцитов, их субпопуляций;
- биопсия лимфоузлов, кишечника, тимуса.
Лечение дефектов системы комплемента
Начинается с соблюдения диетических (исключаются углеводы и растительный белок), гигиенических и асептических мероприятий: на первый план выходит профилактика инфекционных заболеваний. По мере необходимости используются антибиотики. Исключается введение живых вакцин и гемотрансфузии. Практически во всех случаях ДСК этиопатогенетическая и заместительная терапия невозможны. Поэтому проводится симптоматическая терапия с введением «дефицитных» ферментов, переливанием свежезамороженной плазмы, использованием андрогенных препаратов (даназол, станозолол).
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.
- Даназол (антигонадотропное средство). Режим дозирования: для предупреждения ангионевротического отека назначается внутрь в начальной дозе 200 мг, с последующим снижением в течение 1-3 мес.
- Станозолол (Винстрол) — анаболический стероид. Режим дозирования: взрослым назначают по 2 мг 3 р/день перед едой или во время еды; детям в возрасте от 2 до 6 лет — по 1 мг 2 р/день; в возрасте от 6 до 12 лет — по 2 мг 2 р/день.
Рекомендации
- Консультация гематолога.
- Консультация иммунолога.
- Консультация аллерголога.
Вопросы пользователей
(2)
Ирина
2018-02-07 03:49:00Здравствуйте. Скажите, пожалуйста, какое диагностическое значение имеет не пониженная, а повышенная активность С1 ингибитора? Сывороточные иммуноглобулины в норме, кроме igG, понижен; IgE тоже в… Наталья
2017-06-28 10:36:36Здравствуйте!
У ребенка выявлены гетерозиготный мутации системы комплемента. Сейчас ему 3 года, и у него поражён весь желудочно кишечный тракт по причине невозможности элиминации бесконечной условно…
Медучреждения, в которые можно обратиться:
Источник
Врожденный (первичный) дефицит компонентов комплемента
встречается чрезвычайно редко. Вместе с тем, сегодня описаны приобретенные
(вторичные) дефициты практически всех компонентов комплемента. Наиболее часто,
выявляются дефициты ранних компонентов комплемента – Clq, Clr, Cls, С4, С2, СЗ,
которые ассоциируются с системной красной волчанкой, гломерулонефритом и, с
меньшей частотой, с пиогенными инфекциями.
Дефицит СЗ комплемента ассоциируется с тяжелыми пиогенными
инфекциями, гломеруло-нефритом и системной красной волчанкой.
Дефициты конечных компонентов комплемента – С5-С9
ассоциируются, как правило, с рецидивирующей диссеминированной гонококковой
инфекцией.
Относительно альтернативного пути активации комплемента,
следует отметить, что дефицит фактора D ассоциируется с возвратной пиогенной
инфекцией, пропердина – с возвратной пиогенной инфекцией и фулминантной формой
менингококцемии, а дефицит фактора Н – с пиогенной инфекцией и
гломерулонефритом.
Врожденный дефицит С1-ИНГ комплемента ассоциируется с
наследственным ангионевро-тическим отеком, а приобретенный дефицит С1-ИНГ
комплемента, как правило, наблюдается у больных с лимфопролиферативными
нарушениями.
Специфические диагностические тесты. Наиболее информативным
скрининговым тестом для выявления дефицита комплемента является гемолитический
тест – СН-50.
При нулевом СН-50 следует думать о дефиците первых восьми
компонентов комплемента – от С1 до С8, а если он составляет 25-50% нормы – о
дефиците С9.
Дефицит фактора D и пропердина не выявляется с помощью
метода СН-50.
Дефицит фактора I, или фактора Н, ассоциируется с
потреблением СЗ комплемента и снижением СН-50.
Дефицит С1-ИНГ комплемента ассоциируется со снижением уровня
С4 и может быть выявлен с помощью функционального метода или количественного
определения специфического белка. У 85% больных с дефицитом С1-ИНГ уровень
белка снижен, а у 15% – нормальный или повышенный, что требует для подтверждения
диагноза применения функционального метода.
Нормальный уровень СЗ и С4 при отрицательном результате
теста СН-50 является убедительным доказательством врожденного дефицита
компонентов комплемента. В то же время сниженное количество СЗ и/или С4 с
отрицательными результатом СН-50 свидетельствует о том, что в данной ситуации
произошло потребление комплемента.
Оценка специфических компонентов комплемента и их
недостаточности должна проводиться в специализированных лабораториях.
Лечение. Какого-либо специфического лечения врожденного
дефицита компонентов комплемента нет. При дефиците С1-ИНГ комплемента введение
полусинтетического андрогена (например, даназола) ассоциируется со снижением у
больных частоты ангионевротического отека и увеличением уровня С1-ИНГ
комплемента (подробней см. соответствующую главу). Использование этих
препаратов у детей не рекомендуется из-за их андрогенного действия. Знания о
том, что данный больной имеет нарушения в системе комплемента чрезвычайно важны
для лечащего врача, так как свидетельствуют о высоком риске развития тяжелых
инфекций, и поэтому могут потребоваться более активные мероприятия по лечению
больных. Больные с дефицитом ранних компонентов комплемента относятся к группе
риска развития аутоиммунных заболеваний, в частности, системной красной
волчанки или гломерулонефрита.
Больные с врожденными или приобретенными нарушениями системы
комплемента с целью профилактики соответствующих заболеваний могут быть
иммунизированы вакцинами пневмококков, Haemofilus influenza и Neisseria
meningitidis. Для постановки диагноза нарушения в системе комплемента важным
является упоминание в семейном анамнезе о возможном наличии дефицита
компонентов комплемента у кого-то из родственников.
Поскольку активность компонентов комплемента чрезвычайно
быстро снижается после взятия крови при комнатной температуре, это может быть
очень частой причиной неправильных результатов исследований. Наиболее частой
причиной низких показателей или даже отсутствия активности комплемента по СН-50
как раз и является тот факт, что не во всех лабораториях следуют определенным
инструкциям для получения материала и проведения такого рода исследований.
Поэтому в случае низких значений СН-50 необходимо как можно более тщательно
провести дополнительные исследования.
В настоящее время получен очищенный С1-ИНГ комплемента и
начато его использование для лечения врожденного ангионевротического отека.
Кроме того, разрабатываются способы генной терапии дефицита компонентов
комплемента, и это может быть со временем альтернативным методом лечения такого
рода больных.
Говоря о взаимодействии врачей разных специальностей,
необходимо отметить, что, если у врача любой специальности будет наблюдаться
больной с рецидивирующими инфекциями, то этот врач обязан заподозрить нарушение
в системе иммунитета, в частности, в системе комплемента. Такой больной должен
быть проконсультирован у иммунолога-аллерголога для выявления того или иного
уровня нарушения в системе иммунитета и его оценки. Больные с явлениями
ангионевротического отека также должны быть проконсультированы у
иммунолога-аллерголога для оценки врожденного или приобретенного иммунодефицита
С1 -ИНГ комплемента. Больные с дефицитом комплемента должны наблюдаться и
лечиться у иммунологов-аллергологов.
Источник
Первичный дефицит компонентов системы комплемента встречается реже, чем все остальные первичные иммунодефицита: частота их составляет всего 1% общего количества первичных иммунодефицитов.
Генетические дефекты описаны для большинства компонентов ком-
племента — Clq, Clr, Cls, C2, C4, C3, C5, C6, C7, C8 и С9. Все они наследуются по аутосомно-рецессивному типу; гетерозиготы могут быть обнаружены при лабораторном обследовании: у них уровень дефектного белка комплемента снижен наполовину по сравнению с нормой. Наиболее часто в человеческой популяции выявляется дефицит С2: приблизительно один из 100 человек является гетерозиготным по дефекту этого белка. У представителей японской национальности наиболее часто обнаруживается дефицит Clq: приблизительно один из пятидесяти является гетерозиготными.
Наиболее частым клиническим симптомом, ассоциирующимся с дефектами ранних компонентов комплемента (С1, С2, С4), являются иммунокомплексные заболевания. В то время как врожденные дефекты поздних компонентов комплемента (от С5 до С8) ассоциируются с рецидивирующей гонококковой инфекцией. Дефицит СЗ клинически проявляется рецидивирующей пиогенной инфекцией. Таким образом, обнаруженные клинико-иммунологические ассоциации подтверждают важность системы комплемента: 1) в элиминации и/или солюбилизации (разрушении) иммунных комплексов; 2) в антибактериальной защите; 3) в механизмах опсонизации.
В клиническом плане важными являются также врожденные дефекты ингибиторов системы комплемента: Cl-ингибитора и СЗЬ-инакти- ватора (фактор I).
Дефицит ¦ Cl-ингибитора клинически проявляется врожденным ангионевротическим отеком. Наследуется по аутосомно-доминантному типу. Такие больные подвержены рецидивирующим атакам подкожных отеков, которые могут локализоваться в любой части тела. В табл. 8 приведены клинические проявления, связанные с дефицитом различных компонентов комплемента.
Таблица 8. Клинические проявления, связанные с дефицитом различных компонентов комплемента
| Компонеты комплемента | Клинические проявления |
| Clq | Высокая частота иммунокомплексной патологии (системная красная волчанка, гломерунефрит) |
| Clr | То же |
| С2 | » |
| С4 | » |
| СЗ | Рецидивирующая пио генная инфекция |
| С5 | Рецидивирующая гонококковая (нейсериальная) инфекция, высокая частота системной красной волчанки |
| С6 | Рецидивирующая гонококковая инфекция |
| Компонеты комплемента | Клинические проявления |
| С7 | То же |
| С8 | » |
| С9 | Протекает асимптоматически |
| С1-ингибитор | Ангионевротический отек |
| Фактор I (СЗЬ- инактиватор) | Рецидивирующая пиогенная инфекция |
| Фактор Н | То же |
| Пропердин | Рецидивирующая гонококковая инфекция |
Источник

Система комплемента — комплекс белков, постоянно присутствующих в крови, которые выполняют ряд важнейших функций. На данный момент комплекс насчитывает более трех десятков белковых молекул, среди которых основные белки — С1, С2, …, С9, а также ряд белков-регуляторов. Комплемент принято относить к факторам врожденного иммунитета, выполняющим защитную функцию, однако при определенных обстоятельствах сбой работы системы комплемента может стать звеном патогенеза некоторых заболеваний.
Вначале разберем механизмы работы системы комплемента, после чего рассмотрим их клиническое значение.
Активация системы комплемента
Существует три пути активации данной системы: классический, альтернативный и лектиновый. Все они приводят к ключевому событию: формированию С3-конвертазы.
В классическом варианте комплемент активируется через IgG и IgM, которые формируют иммунные комплексы с антигенами. Комплекс С1 (состоящий из q, r и s субъединиц) связывается с Fc-фрагментом иммуноглобулина. Происходит активация C1, комплекс приобретает протеолитическую активность и активирует C4 и C2. Последние формируют ключевой ферментативный комплекс — С3-конвертазу.
При альтернативном пути активация комплемента происходит без участия антител. Инициируют его поверхностные молекулы микробов и их внеклеточные структуры — например, углеводороды, полисахариды и т. д. С3 в клетках постоянно (даже когда нет активации системы комплемента) претерпевает диссоциацию на С3а и С3b, но в очень малых количествах.
Когда в клетке появляется инициирующий фактор (предположим, это бактерия), С3b связывается с ее поверхностными молекулами. К этому комплексу присоединяются другие молекулы-регуляторы: фактор В, фактор D, пропердин. Так появляется еще одна форма С3-конвертазы.
Лектиновый путь активируется через лектин, связывающий маннозу (фактор врожденного иммунитета — MBL) или группу лектинов Ficolin, которые связывают молекулы на поверхности патогенов — дрожжей, бактерий, паразитов и вирусов. MBL и Ficolin постоянно циркулируют в крови в виде MBL-ассоциированного комплекса (MASP). Когда MASP связывается с вышеназванными молекулами, комплекс претерпевает изменения конформации и активирует уже знакомый путь C4 и C2, что приводит к формированию С3-конвертазы, как и в классическом случае.
Итак, вне зависимости от пути активации различия оканчиваются на формировании ключевого фермента — С3-конвертазы. Последняя расщепляет С3 на два фрагмента: С3а и С3b. Отметим, что С3b выполняет функцию опсонина, С3а — анафилотоксин, способный воздействовать на тучные клетки с высвобождением гистамина.
Однако С3b также способен присоединиться к С3-конвертазе и модифицировать ее, превратив в С5-конвертазу. Этот фермент проделывает то же самое с С5, образуя С5а и С5b. По аналогии, С5а — анафилотоксин, С5b — опсонин.
И снова С5b присоединяется к С5-конвертазе, вовлекая в каскад С6–С9 с формированием т. н. мембраноатакующего комплекса (MAC) [1].
.
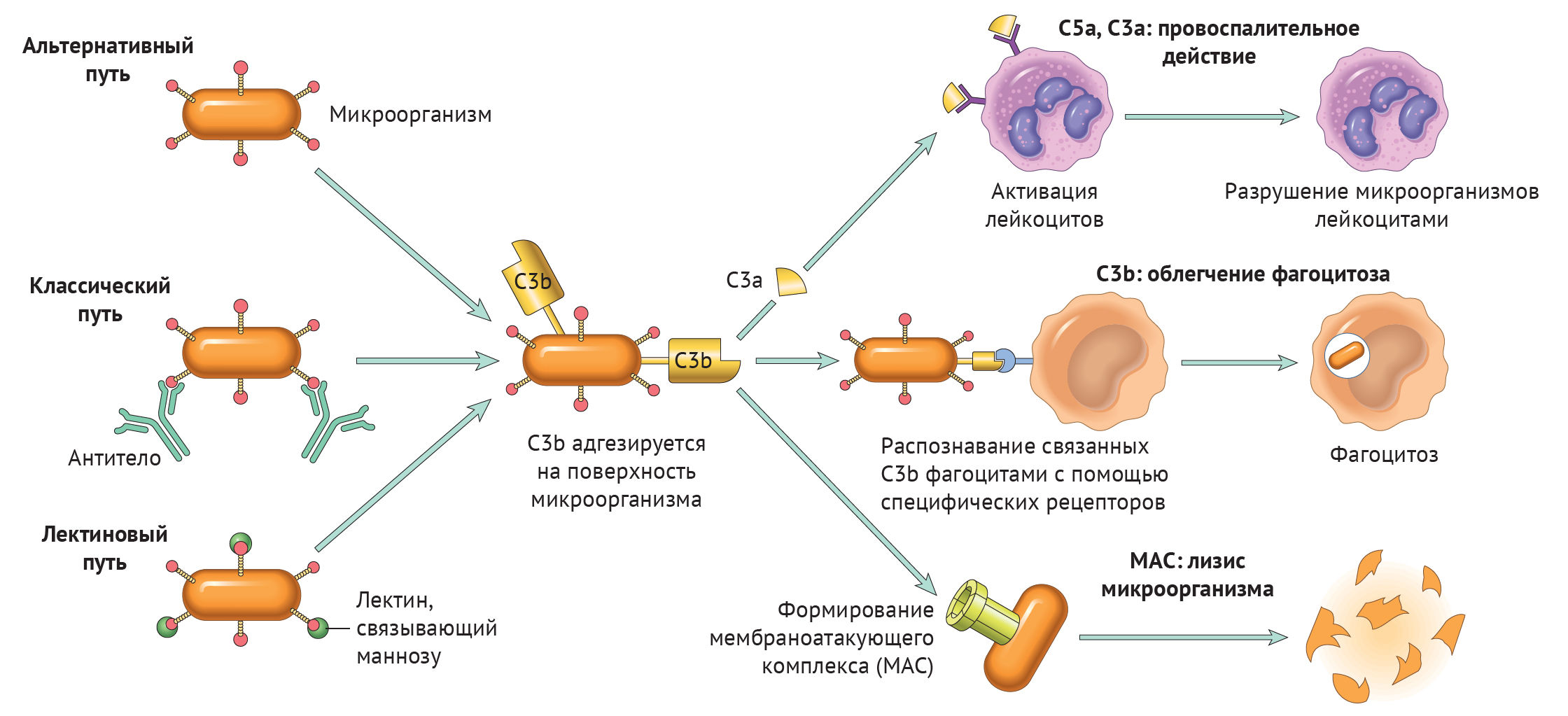
Рисунок 1
Любой из трех путей активации системы комплемента приводит к формированию С3-конвертазы, которая расщепляет С3-компонент на С3а и С3b. Последний участвует в опсонизации патогенов и облегчает таким образом фагоцитоз, а также инициирует каскад формирования МАС. С3а вместе с С5а (и в меньшей степени С4а) — побочные продукты реакций, которые обладают провоспалительным действием («Robbins Basic Pathology», 10nd ed — 2018, p 76).
Таким образом, систему комплемента можно разделить на три функциональные группы: анафилотоксины, опсонины и мембраноатакующий комплекс — МАС.
.

Анафилотоксины
К ним относятся С3а, С4а и С5а. В целом, их роль сводится к провоспалительному действию, что выражается в повышении проницаемости сосудов микроциркуляторного русла (МЦР), вазоконстрикции. В нейтрофилах, эозинофилах и макрофагах анафилотоксины инициируют респираторный взрыв, в базофилах и тучных клетках — высвобождение гистамина. Кроме того, анафилотоксины регулируют синтез эозинофильного катионного белка, адгезию и хемотаксис эозинофилов [2].
В здоровом организме роль анафилотоксинов по большому счету этим и ограничивается. Однако в случае реакций гиперчувствительности данные молекулы могут стать ключевым звеном патогенеза. Одним из наиболее ярких примеров является бронхиальная астма.
Эпителий и гладкомышечные клетки дыхательных путей содержат рецепторы к анафилотоксинам — C3aR и C5aR. При аллергических реакциях происходит активация системы комплемента, который в свою очередь активирует иммунокомпетентные клетки (ИКК), среди которых — нейтрофилы, эозинофилы, макрофаги, дендритные клетки. Последние под влиянием стимула (например, аллергена) способны в свою очередь вновь активировать комплемент — так замыкается порочный круг.
Помимо поддержания системного воспаления, анафилотоксины ответственны и за ремоделирование дыхательных путей. Под их влиянием происходит гиперплазия мерцательного эпителия и гладкомышечных клеток, неоваскуляризация и фиброзирование паренхимы [3,4].
Также анафилотоксины играют важную роль в патогенезе синдрома системного воспалительного ответа (SIRS). При сепсисе, когда микробы в больших количествах попадают в кровоток, происходит системная активация цитокинов, хемокинов и, конечно, системы комплемента. Повышение концентрации анафилотоксинов при сепсисе, к слову, считается неблагоприятным прогностическим фактором [5].
В случае с сепсисом и SIRS анафилотоксины становятся звеном патогенеза. Наибольшая роль в данной ситуации принадлежит С5а. Предположительно, избыточный синтез этого белка приводит к дисфункции нейтрофилов, апоптозу лимфоидных клеток, способствует развитию кардиомиопатий, ДВС-синдрома и полиорганной недостаточности.
В связи с этим постепенно разрабатываются препараты, ингибирующие синтез С5а. На биологических моделях было показано, что блокада данного фактора действительно улучшает прогноз при сепсисе и SIRS [6].
МАС
Данный комплекс может формироваться на поверхности грамотрицательных бактерий и напрямую участвовать в их уничтожении (более всего действие МАС направлено против Neisseria). Описаны также случаи образования МАС на поверхности грамположительных бактерий, паразитов и мембране собственных клеток. Состоит он из последних 5 белков комплемента: С5 — С9.
Специфического рецептора, инициирующего образование комплекса, нет. Белки комплемента адгезируются на наружной поверхности клеточной стенки бактерии, после чего комплекс приобретает ферментативную активность и перфорирует мембрану. Нарушается концентрация ионов и воды — клетка погибает [7].
Недавние исследования показывают, что у МАС имеется и провоспалительное — «сублитическое» — действие. При образовании комплекса на поверхности нейтрофилов или макрофагов происходит локальная утечка провоспалительных медиаторов, а в случае атаки мезангиальных клеток и микроглии — высвобождение цитокинов. Также МАС вызывает образование инфламмасомы путем активации Nod-подобного рецептора [8].
Не допустить образование МАС на собственных клетках помогает рецептор CD59. Генетический дефект CD59 приводит к появлению пароксизмальной ночной гемоглобинурии [7]. А поскольку МАС способен поддерживать системное воспаление, он также вовлекается в патогенез различных воспалительных заболеваний (см. ниже).
Возрастная макулярная дегенерация
Возрастная макулярная дегенерация (ВМД) — основная причина слепоты у пациентов старше 50 лет в цивилизованных странах. В макуле (как и во всей сетчатке) происходят дистрофически-дегенеративные процессы, вследствие чего нарушается способность фокусировать свет в определенной точке, в результате исчезает ясность и четкость зрения. Существует две формы ВМД: влажная (быстро прогрессирующая, экссудативная) и сухая (атрофическая форма). Иногда выделяют рубцовую форму, которая скорее является завершающей стадией заболевания.
Одним из ключевых звеньев этиопатогенеза ВМД является дефект фактора комплемента H — одного из основных регуляторов системы комплемента. Функция его заключается в ингибировании С3-конвертазы (если точнее — является кофактором для протеазы, которая осуществляет катализ С3-конвертазы). Существует несколько форм гена фактора Н, один из наиболее известных — Y402H, который существенно повышает риск развития ВМД. Есть и другие, более редкие варианты [9].
В случае влажной формы ВМД происходит неоваскуляризация сетчатки — аномальное разрастание сосудов под действием VEGF (фактор роста эндотелия сосудов). В опытах было показано, что высвобождение VEGF и неоваскуляризация невозможны без действия MAC [10].
Также в обоих вариантах ВМД важная роль приписывается локальному хроническому воспалению под воздействием системы комплемента. Установлена взаимосвязь между активацией комплемента (особенно по альтернативному пути) и риском развития ВМД [10].
Разумеется, эти данные невозможно было проигнорировать, вследствие чего начали разрабатывать ингибиторы факторов системы комплемента для предотвращения ВМД. На данный момент существуют и моноклональные антитела (анти-фактор D, Экулизумаб), и рекомбинантный фактор Н, и антагонисты различных белков системы комплемента, но пока ни один из них не рекомендован для лечения ВМД [10].
Болезнь Альцгеймера
Воспалительный процесс в нервной ткани сегодня рассматривается как основное патогенетическое звено в развитии БА и других нейродегенеративных заболеваний. Также существуют данные, что прием противовоспалительных препаратов (НПВС) существенно снижает риск развития БА [11].
Однако помимо воспалительных цитокинов, важная роль в развитии локального воспаления принадлежит и системе комплемента. В ликворе пациентов с болезнью Альцгеймера обнаруживается повышенная концентрация С3 в сравнении со здоровыми пациентами. Также активность системы комплемента у пациентов с БА существенно выше [12].
Наследственный ангионевротический отек
НАО — редкое и потенциально фатальное заболевание, этиологическим фактором которого является генетический дефект (НАО 1 типа) или дисфункция (НАО 2 типа) ингибитора С1-компонента комплемента (iС1). В норме iС1 — регулятор, который блокирует весь путь активации системы комплемента. При его дефиците происходит гиперактивация начальных компонентов комплемента, следствием чего является повышение проницаемости сосудов, что приводит к различным отекам.
Проявляется НАО в основном в возрасте после 20 лет отеками конечностей, реже — шеи и лица, которые длятся 1–3, максимум — 7 дней, после чего самостоятельно проходят. Сначала пациент может их даже не замечать, однако со временем частота и выраженность отеков нарастают, может происходить отек слизистой ЖКТ, что проявляется болью, тошнотой, иногда — клиникой острого живота. Наиболее опасен отек гортани, который может сопровождаться асфиксией.
Но ситуация с лечением не так уж и плоха. Ингибитор С1 можно вводить внутривенно для профилактики приступов, для купирования — подкожно [13,14].
Пароксизмальная ночная гемоглобинурия
ПНГ — редкое заболевание, в основе которого лежит клональная экспансия гемопоэтических клеток с мутацией PIGA. Результатом данной мутации является недостаточность ГФИ-заякоренных белков, а именно — CD55 и CD59 (гликозилфосфатидилинозитол или ГФИ-якорь — гликопептид, присоединяющийся к белкам в процессе посттрансляционных модификаций).
Проявляется заболевание гемолитической анемией, костномозговой недостаточностью, тромбофилией.
В норме CD55 ингибирует С9-компонент и предотвращает формирование МАС, а CD59 — ингибирует образование С3-конвертазы и предотвращает протеолиз С3-компонента.
Патогенез начинается с внутрисосудистого гемолиза, который происходит ввиду дефицита CD55. На поверхности эритроцитов с мутацией формируется С3-конвертаза, которая запускает дальнейший синтез МАС. Образование последнего ничего не сдерживает из-за дефекта CD59. МАС перфорирует мембрану эритроцита, и клетка погибает.
Все клинические проявления — гемоглобинурия, анемия (апластическая), тромбоз/эмболия, гастроинтестинальные и неврологические симптомы, так или иначе, являются следствием данного механизма [15,16].
В качестве лечения используется трансплантация гемопоэтических клеток, гемотрансфузии, симптоматическая и поддерживающая терапия. Также достаточно перспективным является использование ингибиторов системы комплемента, например, Экулизумаба (Солириса), который, по данным некоторых публикаций, устраняет все значимые симптомы заболевания [15].
Однако по данным Кохрейна, доказательную базу Экулизумаба нельзя назвать достаточной [17].
Атипичный гемолитико-уремический синдром
Для АГУС характерными симптомами являются гемолитическая анемия, тромбоцитопения и почечная недостаточность с уремией. Этиологией данного заболевания могут быть различные генетические дефекты регуляторов системы комплемента.
Зачастую это мутация CFH, отвечающего за экспрессию уже знакомого читателю фактора Н. Таких мутаций существует более 80, они могут быть наследственными или спорадическими. Также встречаются мутации генов, ответственных за фактор В, С3-компонент комплемента, тромбомодулин и др. [18].
В лечении АГУС также может быть использован экулизумаб [19], однако и здесь ощущается нехватка доказательной базы. В основном же терапия АГУС осуществляется с помощью гемотрансфузий/плазмообмена, диализа, почечной трансплантации — и снова ни одна из названных процедур не способна избавить пациента от болезни [18]. Таким образом, наиболее перспективна разработка ингибиторов системы комплемента и проведение РКИ с их участием.
Помимо перечисленных заболеваний, система комплемента принимает непосредственное участие в патогенезе аутоиммунных кожных заболеваний [20], воспалительных заболеваний почек [21], разнообразных аллергических и аутоиммунных заболеваний.
Разработка ингибиторов комплемента уже сегодня является перспективным направлением, а некоторые препараты данной группы (экулизумаб) уже могут применяться в ряде случаев.
Источники:
- J. V. Sarma and P. A. Ward, ‘The complement system’, Cell Tissue Res., vol. 343, pp. 227–235, 2011.
- J. Kohl, ‘Anaphylatoxins and infectious and non-infectious inflammatory diseases’, Mol. Immunol., vol. 38, no. 2–3, pp. 175–187, 2001.
- M. A. Khan, A. M. Assiri, and D. C. Broering, ‘Complement mediators: Key regulators of airway tissue remodeling in asthma’, J. Transl. Med., vol. 13, no. 1, pp. 1–9, 2015.
- Y. Laumonnier, A. V. Wiese, J. Figge, and C. Karsten, ‘Regulation and function of anaphylatoxins and their receptors in allergic asthma’, Mol. Immunol., vol. 84, pp. 51–56, 2017.
- C. E. Hack et al., ‘Elevated plasma levels of the anaphylatoxins C3a and C4a are associated with a fatal outcome in sepsis’, Am. J. Med., vol. 86, no. 1 C, pp. 20–26, 1989.
- R. S. Hotchkiss, L. L. Moldawer, S. M. Opal, K. Reinhart, I. R. Turnbull, and J.-L. Vincent, ‘Sepsis and septic shock’, Nat. Rev. Dis. Prim., vol. 2, no. 16045, pp. 1–47, 2017.
- C. Bayly-Jones, D. Bubeck, and M. A. Dunstone, ‘The mystery behind membrane insertion: A review of the complement membrane attack complex’, Philos. Trans. R. Soc. B Biol. Sci., vol. 372, no. 1726, 2017.
- B. P. Morgan, ‘The membrane attack complex as an inflammatory trigger’, Immunobiology, vol. 221, no. 6, pp. 747–751, 2016.
- E. C. Schramm, S. J. Clark, M. P. Triebwasser, S. Raychaudhuri, J. M. Seddon, and J. P. Atkinson, ‘Genetic variants in the complement system predisposing to age-related macular degeneration: A review’, Mol. Immunol., vol. 61, no. 2, pp. 118–125, 2014.
- R. Troutbeck, S. Al-Qureshi, and R. H. Guymer, ‘Therapeutic targeting of the complement system in age-related macular degeneration: A review’, Clin. Exp. Ophthalmol., vol. 40, no. 1, pp. 18–26, 2012.
- P. L. McGeer, J. Rogers, and E. G. McGeer, ‘Inflammation, antiinflammatory agents, and Alzheimer’s disease: The last 22 years’, Handb. Infect. Alzheimer’s Dis., vol. 54, pp. 11–15, 2017.
- H. Krance, C. W. Yi, and Z. Huiyan, ‘The complement cascade in Alzheimer ’ s disease : a systematic review and meta-analysis’, Mol. Psychiatry, 2019.
- K. Bork et al., ‘Guideline: Hereditary angioedema due to C1 inhibitor deficiency: S1 Guideline of the German Society for Angioedema (Deutsche Gesellschaft für Angioödeme, DGA), German Society for Internal Medicine (Deutsche Gesellschaft für Innere Medizin, DGIM), German S’, Allergo J. Int., vol. 28, no. 1, pp. 16–29, 2019.
- H. Longhurst et al., ‘Prevention of hereditary angioedema attacks with a subcutaneous C1 inhibitor’, N. Engl. J. Med., vol. 376, no. 12, pp. 1131–1140, 2017.
- A. Kumar, ‘Paroxysmal Nocturnal Hemoglobinuria’, Blood, vol. 124, no. 18, pp. 1462–1470, 2014.
- C. Parker et al., ‘Diagnosis and management of paroxysmal nocturnal hemoglobinuria’, Rev. Transl. Hematol., vol. 106, no. 12, pp. 3699–3709, 2005.
- A. J. Martí-Carvajal, V. Anand, A. F. Cardona, and I. Solà, ‘Eculizumab for treating patients with paroxysmal nocturnal hemoglobinuria’, Cochrane Database Syst. Rev., vol. 2013, no. 2, 2013.
- M. Progress, ‘Atypical Hemolytic–Uremic Syndrome’, N. Engl. J. Med., 2010.
- C. M. Legendre et al., ‘Terminal complement inhibitor eculizumab in atypical hemolytic-uremic syndrome’, N. Engl. J. Med., vol. 368, no. 23, pp. 2169–2181, 2013.
- G. Edwards, G. F. H. Diercks, M. A. J. Seelen, B. Horvath, M. B. A. Van Doorn, and J. Damman, ‘Complement activation in autoimmune bullous dermatoses: A comprehensive review’, Front. Immunol., vol. 10, no. JUN, pp. 1–8, 2019.
- K. Koåcielska-Kasprzak, D. Bartoszek, M. Myszka, M. Åabińska, and M. Klinger, ‘The complement cascade and renal disease’, Arch. Immunol. Ther. Exp. (Warsz)., vol. 62, no. 1, pp. 47–57, 2014.
Источник
