Лечение хронического болевого синдрома в онкологии принципы воз
23 апреля 2019 г.
Просмотров: 2001
Согласно определению Международной ассоциации по изучению боли (IASP), к хронической относят боль, которая сохраняется более 3 месяцев. Это достаточно типичная ситуация для онкологического больного. При прогрессировании опухолевого процесса хроническая боль отягощает жизнь пациента и окружающих его людей, представляет серьезную медицинскую и социальную проблему. У онкологических пациентов болевые ощущения не являются временными или преходящими, в них нет биологической целесообразности, они не играют защитной роли. Возникшая у онкологического пациента боль ведет к дезадаптации, к ненормальному восприятию болевых импульсов и сопровождается различными нарушениями функции центральной нервной системы (ЦНС).
Клиническая картина болевого синдрома зависит от локализации очага поражения, патогенетического типа боли, индивидуального порога болевой чувствительности, предшествующего болевого опыта.
Этиология
Выделяют следующие основные причины хронической боли у онкологических больных:
- боль, вызванная самой опухолью (поражение костей, мягких тканей, кожи, внутренних органов, органов пищеварительной системы, окклюзия сосудов и др.);
- боль при осложнениях опухолевого процесса (патологический перелом, некроз, изъязвление, воспаление, инфицирование тканей и органов, тромбозы);
- боль при паранеопластических синдромах (артро-, нейро- и миопатии);
- боль как следствие астенизации (пролежни, трофические язвы, запор);
- боль, обусловленная противоопухолевым лечением:
- при осложнениях хирургического лечения рака (фантомная боль, боли при спайках, рубцах, отеках);
- при осложнениях химиотерапии (мукозиты, полинейропатия, генерализованная миалгия, асептический некроз, артралгии);
- при реакциях и осложнениях лучевой терапии (поражение кожи и слизистых оболочек, костей, фиброз, неврит, плексит, миелопатия и др.).
Типы боли и механизм их развития
Выделяют три патогенетических типа боли: ноцицептивный, нейропатический и психогенный. При ноцицептивном типе боли происходит раздражение специфических периферических болевых рецепторов (ноцицепторов), которые расположены во всех органах и тканях: в коже, слизистых оболочках, стенках полых органов, капсулах паренхиматозных органов, в костях и надкостнице.
Повреждения, сопровождающие опухоли, приводят к деструкции клеточных мембран, в результате этого запускается цепь гистохимических реакций с высвобождением тканевых альгогенов, к числу которых в настоящее время относят более 30 различных субстанций. Важнейшими из них принято считать простагландин Е2 (ПГЕ2), гистамин, серотонин и другие биоактивные вещества. В патологическом очаге также активны альгогены, поступающие из плазмы. К ним относятся брадикинин и каллидин. Как плазменные, так и тканевые альгогены взаимодействуют с соответствующими структурами на поверхности болевых рецепторов,резко повышая их чувствительность.
Особенность формирования ноцицептивной боли при онкологическом процессе — способность болевых рецепторов активироваться не только при взаимодействии с воспалительными альгогенами, но и при воздействии на них специфических опухолевых факторов, что способствует усилению потока болевых импульсов. При этом ноцицепторы взаимодействуют как с продуктами метаболизма опухолевых клеток, так и с факторами повреждения или воспаления тканей. На ноцицепторы при онкологической боли воздействуют внеклеточные ионы водорода Н+, эндотелин 1, интерлейкины разных типов и фактор некроза опухоли.
В результате этих разнообразных и частых воздействий генерируются болевые импульсы. По афферентным нервным волокнам болевой импульс поступает в задние рога спинного мозга, откуда по спиноталамическому тракту — в вышележащие отделы ЦНС, ядра таламуса. В дальнейшем вся сенсорная болевая информация поступает в нейроны серого вещества проекционных зон коры больших полушарий, где происходят ее обобщение, обработка и анализ (перцепция), после чего организм осознает боль и степень опасности произошедшего повреждения.

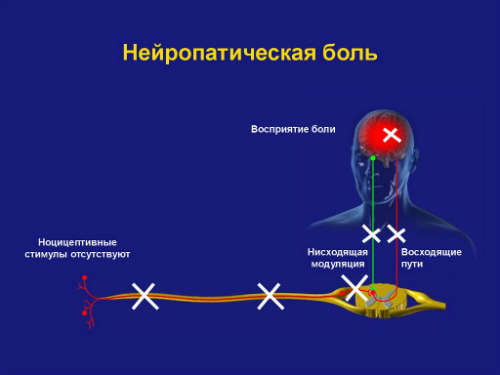
Нейропатическая боль имеет принципиальное отличие от ноцицептивной в механизмах формирования. Нейропатическая боль у онкологических пациентов может возникать как результат повреждений на разных уровнях нервной системы — от периферических нервов до нейронов коры головного мозга.
При повреждении головного или спинного мозга развивается центральная нейропатическая боль. При повреждениях структур периферической нервной системы (корешков спинномозговых нервов, нервных сплетений, периферических нервов) развивается периферическая нейропатическая боль.
Нейропатическая боль у онкологических пациентов часто гетерогенна, так как может иметь одновременно несколько причин, например, компрессия нервов (79%), деафферентационное повреждение нервов (16%), симпатически усиленная боль (5%). Симпатически усиленная боль — каузалгия, которая проявляется локальной вазодилатацией, гипертермией, повышенным потоотделением, трофическими расстройствами, извращенными сенсорными реакциями.
Опухоли, неудержимо разрастаясь в объеме, способны сдавливать структуры периферической нервной системы либо прорастать непосредственно в нервные сплетения, корешки и ветви периферических нервов, вызывая боль, нарушая сенсорную и моторную функции. Длительно существующая опухолевая компрессия, как и инфильтрация нервных структур, приводит к повреждению волокон нерва, вызывая дегенеративные изменения и деафферентацию (централизацию) боли.
Нейропатическая боль у онкологического больного может сопровождаться разнообразной неврологической симптоматикой, в которой присутствуют симптомы усиления чувствительности: жгучая или простреливающая боль высокой интенсивности, гиперестезия, гипералгезия, боль в ответ на неболевое раздражение (аллодиния), симптомы выпадения или ослабления сенсорных ощущений.
Психогенная боль возникает в ответ на индивидуальное эмоционально значимое переживание (депрессия, стресс, страх, истерия, бред, боли, галлюцинации и т.п.). Эти эмоциональные проявления могут вызывать изменения в симпато-адреналовой системе, системе выработки гипофизарных гормонов, что ведет к дисбалансу в работе висцеральных систем.
Лекарственная терапия хронической онкологической боли
Основным методом симптоматического лечения хронической боли онкологического генеза является системная фармакотерапия. Принципы медикаментозного лечения хронической боли включают следующие основные положения:
- подход к назначению лечения должен быть индивидуализированным;
- выбор препарата осуществляется в зависимости от патофизиологического типа и ее интенсивности;
- лечение осуществляется «по восходящей» в соответствии с «анальгетической лестницей ВОЗ»;
- преимущество отдается неинвазивным путям введения препаратов (пероральному и трансдермальному) и соответствующим лекарственным формам анальгетиков;
- препараты следует назначать в фиксированное время суток, «по часам», а не «по требованию»;
- препараты следует назначать в адекватных дозах;
- необходимо предотвращать развитие нежелательных эффектов и бороться с ними при их возникновении.
При лечении ноцицептивной боли ВОЗ рекомендует трехступенчатую схему использования анальгетиков («анальгетическую лестницу ВОЗ»). На первой ступени обезболивания, при наличии слабой боли, назначают препараты неопиоидного ряда, ненаркотические анальгетики (парацетамол,метамизол) или НПВП. При усилении боли и недостаточной эффективности ненаркотических анальгетиков и НПВП к ним добавляют сначала слабые (трамадол, кодеин, дигидрокодеин), а затем сильные опиоиды (бупренорфин, морфин, оксикодон, фентанил). Также при наличии тех или иных симптомов или при развитии нежелательных явлений от применения анальгетиков в терапию включаются адъювантные средства.
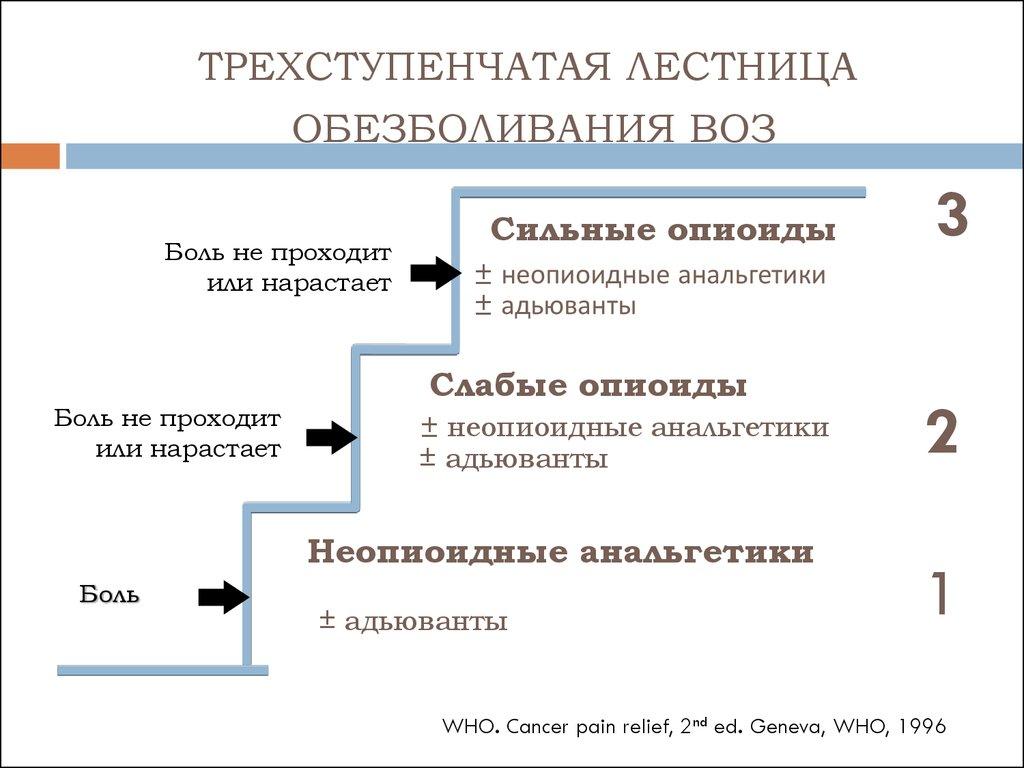
«Анальгетическая лестница ВОЗ»
1-я ступень НЕНАРКОТИЧЕСКИЙ АНАЛЬГЕТИК или НПВП (с возможным добавлением адъювантов)
2-я ступень СЛАБЫЙ ОПИАТ + НЕНАРКОТИЧЕСКИЙ АНАЛЬГЕТИК или НПВП (с возможным добавлением адъювантов)
3-я ступень СИЛЬНОДЕЙСТВУЮЩИЙ ОПИАТ + НЕНАРКОТИЧЕСКИЙ АНАЛЬГЕТИК или НПВП (с возможным добавлением адъювантов)
В целом такая тактика лечения хронической боли позволяет достичь удовлетворительного обезболивания у 77-90% онкологических больных. В России зарегистрированы основные лекарственные препараты как из группы НПВП, так и из группы опиоидов для лечения хронической боли, рекомендуемые ВОЗ.
По мнению экспертов ВОЗ, для длительной терапии хронической боли анальгетики следует использовать в удобных для пациентов неинвазивных формах, предназначенных для введения: внутрь, трансбуккально, подъязычно, трансдермально, ректально.
Для длительной плановой терапии предпочтительны в лекарственные формы продленного действия (депо-формы).
К 1-й ступени «лестницы обезболивания» ВОЗ относят препараты из группы ненаркотических анальгетиков (парацетамол, метамизол) и препараты из группы НПВП (кеторолак, диклофенак, кетопрофен, лорноксикам, нимесулид, мелоксикам, целекоксиб).
Применение НПВП показано на всех этапах терапии боли у онкологических больных. У больных с опухолями и/или метастазами, поражающими мягкие ткани и кости, всегда развивается выраженное перифокальное воспаление. В начале 70-х годов ХХ века было установлено, что болеутоляющее, жаропонижающее и противовоспалительное действие НПВП обусловлено подавлением синтеза простагландинов. НПВП снижают продукцию простагландинов за счет ингибирования фермента циклооксигеназы (ЦОГ).

На сегодня выделяют три изоформы ЦОГ. Считают, что избирательное угнетение ЦОГ-2 приводит к подавлению воспаления и боли. В то же время сохранение активности ЦОГ-1 определяет репаративные процессы в желудке, кровоток в почках. Было отмечено, что парацетамол и метамизол слабо влияют на синтез простагландинов в периферических тканях, но подавляют продукцию простагландинов в ЦНС. В последние годы появились сведения о том, что в ЦНС имеется третий, отличный от первых двух тип ЦОГ, названный ЦОГ-3. Ингибирование ЦОГ-3 головного мозга сопровождается подавлением боли и снижением температуры тела при лихорадке.
Все НПВП могут вызывать осложнения со стороны желудочно-кишечного тракта (ЖКТ): диспепсию, язвы, кровотечения и перфорацию верхних и нижних отделов ЖКТ, железодефицитную анемию.
Все НПВП могут вызывать осложнения со стороны сердечно-сосудистой системы (ССС): дестабилизацию артериальной гипертензиии сердечной недостаточности, повышают риск «кардиоваскулярных катастроф» (инфаркт миокарда, ишемический инсульт) и летальности.
Все НПВП могут оказывать негативное влияние на функцию почек и печени (особенно при наличии заболеваний последних), а в ряде случаев вызывать серьезные нефро- и гепатотоксические реакции.
Препараты группы противопоказаны при эрозивно-язвенных поражениях желудочно-кишечного тракта (ЖКТ) в стадии обострения, состояниях гипокоагуляции (в том числе при гемофилии, геморрагическом диатезе, тромбоцитопении), при бронхиальной астме, тяжелой хронической сердечной недостаточности, гиповолемии, тяжелой почечной и печеночной недостаточности, состояниях, сопровождающихся гиперкалиемией, могут вызвать обострение и осложнения воспалительных заболеваний кишечника (ВЗК).
НПВП могут вызывать кожные реакции и бронхоспазм. Риск развития осложнений со стороны указанных органов и систем существенно отличается при использовании различных НПВП. Для предотвращения осложнений необходим учет факторов риска и выбор наиболее безопасного НПВП.
Для снижения риска развития НПВП гастропатии необходимо дополнительное назначение препаратов из группы ингибиторов протонной помпы и применение низких доз аспирина для снижения риска кардиоваскулярных осложнений. В настоящее время НПВП классифицируются по степени селективности ингибирующей активности в отношении разных изоформ ЦОГ.
В клинике «Медицина 24/7» работает круглосуточный хоспис для онкологических больных. Весь коллектив клиники работает на то, чтобы продлить жизнь человека и устранить болезненные симптомы. Наши врачи назначают и проводят паллиативное лечение для облегчения состояния пациента, а также подбирают наиболее подходящую схему обезболивания. Наши медсестры и санитарки готовы обеспечить достойный уход пациенту на терминальной стадии рака.
Литература:
- Исакова М.Е. Болевой синдром в онкологии. — М.: Практическая медицина, 2011. — 384 с.
- Каприн А.Д., Абузарова Г.Р., Хороненко В.Э. и др. Фармакотерапия хронического болевого синдрома у онкологических пациентов. Медицинская технология. — М.: МНИОИим. П.А. Герцена, 2015. — 48 с.
- Машфорт М.Л., Купер М.Г., Кохен М.Л. и др. Боль и аналгезия. Руководство для практикующих врачей / Перевод сангл. А.Н. Редькин; ред. рус. изд. Бунятян А.А., НасоновЕ.Л., Никода В.В. — М.: Литтерра, 2004. — 488 с.
- Новиков Г.А., Осипова Н.А. Лечение хронической боли онкологического генеза: учебное пособие. Москва. — 83 с.
- Новиков Г.А. Контроль симптомов в паллиативной медицине. — М.: ГЭОТАР-Медиа, 2013. — 248 с.
- Осипова Н.А., Абузарова Г.Р., Петрова В.В. Принципы клинического применения наркотических и ненаркотических аналгетических средств при острой и хронической боли. Методические указания. Практическое руководство для врачей. М., 2005. — 79 с.
- Штрибель Х.В. Терапия хронической боли. Практическое руководство / Пер. с нем.; ред. Осипова Н.А., ДаниловаА.Б., Осипова В.В. — М.: ГЭОТАР-Медиа, 2005. — 303 с.
- Ahmedzai S.H., Leppert W., Janecki M., Pakosz A., LomaxM., Duerr H., Hopp M.
- Long-term safety and efficacy of oxycodone/naloxoneprolonged-release tablets in patients with moderate-to-severechronic cancer pain. Support Care Cancer. 2015 Mar; 23 (3):823-30.
- Caraceni A., Hanks G., Kaasa S. et al. Use of opioid analgesicsin the treatment of cancer pain: evidence-basedrecommendations from the EAPC // Lancet Oncol. 2012 Feb;13 (2): e 58-68.
- Mystakidou K., Parpa E., Tsilika E. et al. Pain management ofcancer patients with transdermal fentanyl: a study of 1828 stepI, II, & III transfers. // J. Pain. 2004; 5: 119–13212. Skaer T.L. Transdermal opioids for cancer pain. // HealthQual. Life Outcomes. 2006 Mar 31; 4: 2413. World Health Organization. Cancer pain relief: with a guide toopioid availability. 2. Geneva: WHO; 1996.14. Zech D.F., Grond S., Lynch J., Hertel D., Lehmann K.A.Validation of World Health Organization guidelines forcancer pain relief: A 10-year prospective study. Pain. 1995;63: 65–76.
Источник: Научно-практический журнал «Паллиативная медицина и реабилитация» № 1. 2018.
Источник
Онкологи Юсуповской больницы уделяют большое внимание лечению пациентов, страдающим от боли, причиной которой являются злокачественные новообразования. В клинике онкологии работают кандидаты и доктора медицинских наук, врачи высшей категории. Они для лечения пациентов и купирования болевого синдрома используют наиболее эффективные лекарственные препараты, обладающие минимальным спектром побочных эффектов.
Врачи применяют стандарты и протоколы ведущих стран мира, рекомендации Всемирной организации здравоохранения по лечению болевого синдрома в онкологии. Онкологи индивидуально подходят к подбору препаратов и их доз каждому пациенту. Для того чтобы выявить онкологическое заболевание и установить распространённость патологического процесса используют современные методы обследования. Юсуповская больница оснащена новейшим диагностическим оборудованием, позволяющим своевременно выявить злокачественное новообразование. Наиболее сложные диагностические процедуры и анализы пациенты имеют возможность пройти в клиниках-партнёрах. Пациентам, требующим постороннего ухода, оказывают помощь сиделки и медсестры.
Болевой синдром при онкологических заболеваниях
Болевой синдром у пациентов, страдающих онкологическими заболеваниями, может развиться на любой стадии патологического процесса. Боль бывает острой и хронической. Длительность острой боли – 3 месяца, а о хронической боли врачи говорят, когда она беспокоит пациента больше трёх месяцев. Острая боль – это сигнал тревоги. Она свидетельствует о наличии заболевания. Врачи Юсуповской больницы проводят комплекс диагностических процедур для определения причины болевого синдрома.
Хроническая боль является постоянным патологическим раздражителем. Она нарушает качество жизни пациента. Интенсивность онкологической боли не зависит напрямую от типа или распространённости опухолевого процесса. У некоторых пациентов небольшое новообразование вызывает сильную боль, в то время как многие больные с наличием множественных метастазов боли не ощущают.
В случае онкологического заболевания врачи говорят о болевом синдроме, в котором симптомы являются результатом суммы эпизодов острых болей, превратившихся в хронические. В начале онкологического заболевания боль беспокоит только 10-20% пациентов. Врачи Юсуповской больницы при обращении пациентов с жалобами на постоянную, не снимающуюся анальгетиками боль, проявляют повышенную онкологическую настороженность. Они используют все диагностические методы, позволяющие выяснить причину болевого синдрома.
Довольно часто боль является признаком рецидива опухоли. Болевой синдром сопутствует далеко зашедшим стадиям заболевания. Боль нередко является результатом противораковой терапии, и онкологи Юсуповской больницы купируют её для того, чтобы избежать перехода в хроническую стадию.
Методы обезболивания в онкологии
Врачи Юсуповской больницы используют эффективные обезболивающие препараты, которые не имеют побочного действия и не дают быстрого привыкания. При слабой боли назначают неопиоидные анальгетики, при усилении болевого синдрома – «лёгкие» опиоидные препараты. Если боль сильная, онкологи применяют наркотическое обезболивание и адъювантную терапию.
Врачи индивидуально подбирают обезболивающий препарат, который устраняет или заметно уменьшает боли за 2–3 дня. Они назначают анальгетики таким образом, чтобы пациент получал очередную дозу препарата до прекращения действия предыдущей дозы. Вначале пациент принимает максимально слабо действующую дозу, а затем минимальную сильнодействующую.
При подборе анальгетика и начальной дозы учитывают следующие факторы:
- возраст пациента;
- степень его истощения;
- интенсивность боли;
- ранее применявшиеся обезболивающие средства и их эффективность;
- состояние функции почек, печени, степень усвоения препарата.
Сначала онкологи для снятия болевого синдрома назначают парацетамол, ибупрофен, мелоксикам, диклофенак. Нестероидные противовоспалительные препараты действуют на периферические болевые рецепторы. Иногда пациенты в течение первых дней приёма лекарств чувствуют сонливость и общую усталость. Эти симптомы проходят самостоятельно или после корректировки дозы препарата. Если после приёма таблеток боль не уменьшается, переходят к инъекционному введению обезболивающих лекарств.
Когда нестероидные противовоспалительные препараты становятся неэффективными, к ним подключают слабые опиаты – трамадол и кодеин. Болеутоляющий эффект достигают за счёт воздействия на опиатные рецепторы и замещения эндорфинов. Трамадол назначают в форме таблеток или инъекций. Препарат принимают совместно с нестероидными противовоспалительными средствами, так как трамадол воздействует на центральную нервную систему, а нестероиды – на периферическую нервную систему.
Если пациент испытывает мучительные, непрекращающиеся боли, ему назначают сильные опиаты, ключевым из которых является морфин. Врач может сначала назначить более щадящие лекарственные средства, вызывающие меньшее привыкание. К ним относится бупренорфин, пиритрамид или фентанил. Принимать их начинают с минимальной дозы, которую постепенно увеличивают.
На каждом этапе лечения онкологических больных врачи назначают коанальгетики. Это группа лекарственных средств, обладающих, кроме основного действия, эффектами, за счет которых они могут уменьшать боли: кортикостероиды, трициклические антидепрессанты, антиэпилептические препараты.
Кортикостероиды включают почти во все химиотерапевтические протоколы. Их применяют для симптоматического лечения за счёт мощного противовоспалительного, противоотёчного и кальцийснижающего действия. Кортикостероидные препараты снижают внутричерепное давление и компрессию спинного мозга. Их назначают в комбинации с обезболивающими препаратами при поражении опухолью нервных сплетений и костных метастазах.
В лечении нейрогенных болей у онкологических больных часто используют трициклические антидепрессанты. Они усиливают действие опиоидов, оказывают прямое обезболивающее действие, улучшают настроение независимо от анальгезирующего эффекта. Препаратом выбора является амитриптилин. В комбинации с морфином он эффективен при онкологической боли.
При сильных, стреляющих неврогенных болях применяют антиэпилептические препараты. Пациенты хорошо переносят карбамазепин в сочетании с антидепрессантами. При появлении побочных эффектов (сонливости, сухости во рту, гипотензии, запоров) врачи корригируют дозу препарата.
Если приём таблеток и инъекции обезболивающих препаратов не снимают боль, онкологическим больным лекарство вводят в эпидуральное пространство. Врачи также используют нейролизис – процесс разрушения болевого нервного пути. Анальгетик вводят через желудочно-кишечный тракт под ультразвуковым эндоскопическим контролем. Такие методы местного обезболивания применяют при злокачественных новообразованиях поджелудочной железы. У 90% пациентов обезболивающий эффект сохраняется больше месяца, в то время как наркотические анальгетики классическим способом пришлось бы вводить постоянно.
Миофасциальный болевой синдром выражается в спазме мышц и появлении в напряженных мышцах болезненных уплотнений, которые называются триггерными точками. Они болезненны при нажатии. После инъекции обезболивающего препарата в триггерную зону проходит боль и улучшается подвижность участка тела.
Вегетативные блокады предполагают введение препарата в место проекции нерва, который связан с поражённым органом. Процедуру проводят раз в год, раз в полгода или каждую неделю. После неё отмечается минимальное количество негативных последствий.
Хронический болевой синдром в онкологии
Хронический болевой синдром – это самостоятельное заболевание. Он не исполняет защитной функции. Хроническая боль ведёт к дезадаптации, ненормальному восприятию болевых импульсов и сопровождается различными нарушениями функций центральной нервной системы. Клиническая картина зависит от расположения очага поражения, конституции и психики пациента, индивидуального порога болевой чувствительности.
Основная причина возникновения хронического болевого синдрома – длительно существующая постоянная боль, вызывающая дисбаланс в работе периферической и центральной нервной системы. Болевые раздражители постоянно стимулируют спинной и головной мозга. Боль продолжается даже после устранения её причины.
Боль, вызванная опухолевым процессом, имеет свою специфику. Раковые клетки быстро растут, сдавливают прилежащие здоровые ткани или периферические и центральные структуры нервной системы. В процессе роста и развития опухоль выделяет специфические вещества, которые возбуждают или повышают восприимчивость периферических рецепторов и нервных волокон к раздражителям. Опухолевые клетки вырабатывают протеолитические ферменты. Они постоянно возбуждают и дестабилизируют сенсорную симпатическую иннервацию. Это приводит к нейропатической боли.
Хроническую боль вызывают метастазы опухоли. Ноцицептивная висцеральная боль возникает при повреждении органов, иннервируемых симпатической нервной системой. Помощь онкологическим больным, страдающим хронической болью, в Юсуповской больнице оказывают специалисты отделения паллиативной помощи. Опытные медицинские сёстры знают особенности течения опухолевого процесса. Они помогают пациентам справиться с болью.
Выбор конкретного метода обезболивания при раке зависит от многих факторов. Запишитесь на приём к онкологу по телефону. Врачи Юсуповской больницы индивидуально подберут схему обезболивания.
Источник
