Лечение нефротического синдрома при скв
Нефротический синдром – это симптомокомплекс, развивающийся на фоне поражения почек, включающий массивную протеинурию, нарушения белково-липидного обмена и отеки. Патология сопровождается гипоальбуминемией, диспротеинемией, гиперлипидемией, отеками различной локализации (вплоть до анасарки и водянки серозных полостей), дистрофическими изменениями кожи и слизистых. В диагностике важную роль играет клинико-лабораторная картина: изменения в биохимических анализах крови и мочи, ренальная и экстраренальная симптоматика, данные биопсии почки. Лечение нефротического синдрома консервативное, включающее назначение диеты, инфузионной терапии, диуретиков, антибиотиков, кортикостероидов, цитостатиков.
Общие сведения
Нефротический синдром может развиваться на фоне широкого круга урологических, системных, инфекционных, хронических нагноительных, метаболических заболеваний. В современной урологии данный симптомокомплекс осложняет течение заболеваний почек примерно в 20% случаев. Патология чаще развивается у взрослых (30-40 лет), реже у детей и пожилых пациентов. Наблюдается классическая тетрада признаков: протеинурия (свыше 3,5 г/сут.), гипоальбуминемия и гипопротеинемия (менее 60-50 г/л), гиперлипидемия (холестерин более 6,5 ммоль/л), отеки. При отсутствии одного или двух проявлений говорят о неполном (редуцированном) нефротическом синдроме.
Нефротический синдром
Причины
По происхождению нефротический синдром может быть первичным (осложняющим самостоятельные заболевания почек) или вторичным (следствием заболеваний, протекающих с вторичным вовлечением почек). Первичная патология встречается при гломерулонефрите, пиелонефрите, первичном амилоидозе, нефропатии беременных, опухолях почек (гипернефроме).
Вторичный симптомокомплекс может быть обусловлен многочисленными состояниями: коллагенозами и ревматическими поражениями (СКВ, узелковым периартериитом, геморрагическим васкулитом, склеродермией, ревматизмом, ревматоидным артритом); нагноительными процессами (бронхоэктазами, абсцессами легких, септическим эндокардитом); болезнями лимфатической системы (лимфомой, лимфогранулематозом); инфекционными и паразитарными заболеваниями (туберкулезом, малярией, сифилисом).
В ряде случаев нефротический синдром развивается на фоне лекарственной болезни, тяжелых аллергозов, отравлений тяжелыми металлами (ртутью, свинцом), укусов пчел и змей. Иногда, преимущественно у детей, причину нефротического синдрома выявить не удается, что позволяет выделить идиопатический вариант заболевания.
Патогенез
Среди концепций патогенеза наиболее распространенной и обоснованной является иммунологическая теория, в пользу которой свидетельствует высокая частота возникновения синдрома при аллергических и аутоиммунных заболеваниях и хороший отклик на иммуносупрессивную терапию. При этом образующиеся в крови циркулирующие иммунные комплексы являются результатом взаимодействия антител с внутренними (ДНК, криоглобулинами, денатурированными нуклеопротеидами, белками) или внешними (вирусными, бактериальными, пищевыми, медикаментозными) антигенами.
Иногда антитела образуются непосредственно к базальной мембране почечных клубочков. Осаждение иммунных комплексов в ткани почек вызывает воспалительную реакцию, нарушение микроциркуляции в клубочковых капиллярах, развитие повышенной внутрисосудистой коагуляции. Изменение проницаемости клубочкового фильтра при нефротическом синдроме ведет к нарушению абсорбции белка и его попаданию в мочу (протеинурия).
Ввиду массивной потери белка в крови развивается гипопротеинемия, гипоальбуминемия и тесно связанная с нарушением белкового обмена гиперлипидемия (повышение холестерина, триглицеридов и фосфолипидов). Появление отеков обусловлено гипоальбуминемией, снижением осмотического давления, гиповолемией, уменьшением ренального кровотока, усиленной продукцией альдостерона и ренина, реабсорбцией натрия.
Макроскопически почки имеют увеличенные размеры, гладкую и ровную поверхность. Корковый слой на разрезе бледно-серый, а мозговой – красноватый. Микроскопическое изучение тканевой картины почки позволяет увидеть изменения, характеризующие не только нефротический синдром, но и ведущую патологию (амилоидоз, гломерулонефрит, коллагенозы, туберкулез). Собственно нефротический синдром в гистологическом плане характеризуется нарушениями структуры подоцитов (клеток капсулы клубочков) и базальных мембран капилляров.
Симптомы
Признаки нефротического синдрома однотипны, несмотря на различие вызывающих его причин. Ведущим проявлением служит протеинурия, достигающая 3,5-5 и более г/сутки, причем до 90% выводимого с мочой белка составляют альбумины. Массивная потеря белковых соединений вызывает снижение уровня общего сывороточного белка до 60-40 и менее г/л. Задержка жидкости может проявляться периферическими отеками, асцитом, генерализованным отеком подкожной клетчатки (анасаркой ), гидротораксом, гидроперикардом.
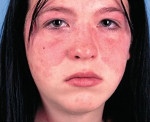
Прогрессирование нефротического синдрома сопровождается общей слабостью, сухостью во рту, жаждой, потерей аппетита, головной болью, тяжестью в пояснице, рвотой, вздутием живота, поносом. Характерным признаком служит олигурия с суточным диурезом менее 1 л. Возможны явления парестезии, миалгия, судороги. Развитие гидроторакса и гидроперикарда вызывает одышку при движении и в покое. Периферические отеки сковывают двигательную активность больного. Пациенты вялые, малоподвижные, бледные; отмечают повышенное шелушение и сухость кожи, ломкость волос и ногтей.
Нефротический синдром может развиваться постепенно или бурно; сопровождаться менее и более выраженной симптоматикой, что зависит от характера течения основного заболевания. По клиническому течению различаются 2 варианта патологии – чистый и смешанный. В первом случае синдром протекает без гематурии и гипертензии; во втором может принимать нефротически-гематурическую или нефротически-гипертоническую форму.
Осложнения
Осложнениями нефротического синдрома могут стать периферические флеботромбозы, вирусные, бактериальные и грибковые инфекции. В отдельных случаях наблюдается отек мозга или сетчатки, нефротический криз (гиповолемический шок).
Диагностика
Ведущими критериями распознавания нефротического синдрома служат клинико-лабораторные данные. Объективный осмотр выявляет бледные («перламутровые»), холодные и сухие на ощупь кожные покровы, обложенность языка, увеличение размеров живота, гепатомегалию, отеки. При гидроперикарде отмечается расширение границ сердца и приглушение тонов; при гидротораксе – укорочение перкуторного звука, ослабленное дыхание, застойные мелкопузырчатые хрипы. На ЭКГ регистрируется брадикардия, признаки дистрофии миокарда.
В общем анализе мочи определяется повышенная относительная плотность (1030-1040), лейкоцитурия, цилиндрурия, наличие в осадке кристаллов холестерина и капель нейтрального жира, редко – микрогематурия. В периферической крови – увеличение СОЭ (до 60-80 мм/ч), преходящая эозинофилия, увеличение числа тромбоцитов (до 500-600 тыс.), небольшое снижение уровня гемоглобина и эритроцитов. Нарушение свертываемости, выявляемые с помощью исследования коагулограммы, могут выражаться в небольшом повышении или развитии признаков ДВС-синдрома.
Исследование биохимического анализа крови подтверждает характерную гипоальбуминемию и гипопротеинемию (менее 60-50 г/л), гиперхолестеринемию (холестерин более 6,5 ммоль/л); в биохимическом анализе мочи определяется протеинурия свыше 3,5 г в сутки. Для выяснения степени выраженности изменений почечной ткани может потребоваться проведение УЗИ почек, УЗДГ почечных сосудов, нефросцинтиграфии.
С целью патогенетической обоснованности лечения нефротического синдрома крайне важно установление причины его развития, в связи с чем требуется углубленное обследование с выполнением иммунологических, ангиографических исследований, а также биопсии почки, десны или прямой кишки с морфологическим исследованием биоптатов.
Лечение нефротического синдрома
Терапия проводится стационарно под наблюдением врача-нефролога. Общими лечебными мероприятиями, не зависящими от этиологии нефротического синдрома, служат назначение бессолевой диеты с ограничением жидкости, постельного режима, симптоматической лекарственной терапии (диуретиков, препаратов калия, антигистаминных средств, витаминов, сердечных средств, антибиотиков, гепарина), инфузионное введение альбумина, реополиглюкина.
При неясном генезе, состоянии, обусловленном токсическим или аутоиммунным поражением почек, показана стероидная терапия преднизолоном или метилпреднизолоном (перорально или внутривенно в режиме пульс-терапии). Иммуносупрессивная терапия стероидами подавляет образование антител, ЦИК, улучшает почечный кровоток и клубочковую фильтрацию. Хорошего эффекта лечения гормонорезистентного варианта патологии позволяет добиться цитостатическая терапия циклофосфамидом и хлорамбуцилом, проводимая пульс-курсами. В период ремиссии показано лечение на специализированных климатических курортах.
Прогноз и профилактика
Течение и прогноз тесно связаны с характером развития основного заболевания. В целом устранение этиологических факторов, своевременное и правильное лечение позволяет восстановить функции почек и достичь полной стабильной ремиссии. При неустраненных причинах синдром может принимать персистирующее или рецидивирующее течение с исходом в хроническую почечную недостаточность.
Профилактика включает раннее и тщательное лечение почечной и внепочечной патологии, которая может осложниться развитием нефротического синдрома, осторожное и контролируемое применение лекарственных средств, обладающих нефротоксическим и аллергическим действием.
Источник

Волчаночный нефрит — это деструкция гломерулярного аппарата почек вследствие аутоиммунного воспаления при системной красной волчанке. Проявляется отеками, уменьшением диуреза, макрогематурией, повышением АД, нарастающей интоксикацией, которые обычно усугубляют основную симптоматику СКВ, реже являются самостоятельными симптомами волчанки. Диагностируется с помощью общего анализа мочи, определения уровней сывороточного креатинина, аутоантител, волчаночного антикоагулянта, пункционной биопсии почек с гистологическим исследованием биоптата. Для лечения применяют цитостатики, кортикостероиды, ингибиторы рецепторов ангиотензина, проводят ЗПТ, трансплантацию почки.
Общие сведения
Клинические признаки волчаночного гломерулонефрита определяются почти у половины больных с установленным диагнозом СКВ. Судя по результатам биопсий, распространенность почечной патологии при волчанке может превышать 90%. Заболевание одинаково часто поражает женщин и мужчин, страдающих волчанкой, однако у пациентов мужского пола волчаночный нефрит отличается более ранним началом, тяжелым и агрессивным течением. При возникновении в возрасте старше 40 лет гломерулонефрит имеет меньшую активность и протекает благоприятнее. Актуальность своевременной диагностики нефрологической патологии у больных СКВ обусловлена ухудшением общего прогноза при аутоиммунном поражении почек. Активный люпус-нефрит остается второй по частоте причиной смерти от волчанки и составляет до 23% в структуре летальности при этом заболевании.
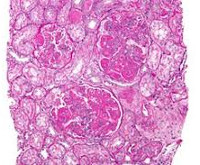
Волчаночный нефрит
Причины
Поражение почек при СКВ обусловлено характерными нарушениями иммунитета. Непосредственной причиной нефрита становится повреждение паренхимы и интерстиция вследствие специфической аутоиммунной деструкции тканей. Специалистами в сфере клинической урологии, нефрологии и ревматологии выявлено два этиологических фактора развития почечной патологии у пациентов, страдающих системной красной волчанкой:
- Иммунные комплексы. При СКВ неконтролируемо усиливается образование антител к собственным клеткам организма. Осаждение циркулирующих иммунных комплексов (ЦИК) в почках потенцирует возникновение специфического воспалительного процесса (гломерулонефрита).
- Волчаночный антикоагулянт. Антифосфолипидные антитела, вытесняя фосфолипид-связывающие протеины, провоцируют усиление коагуляции. Возникающие артериальные и венозные микротромбозы приводят к ишемии и атрофии почечной паренхимы, усугубляя течение нефрита.
Патогенез
Ключевым звеном в развитии волчаночного нефрита является повреждение почечных тканей вследствие аутоиммунной деструкции. В результате поликлональной активации B-лимфоцитов, недостаточной активности T-супрессоров, низкой толерантности к аутоантигенам в организме больного в большом количестве образуются антитела к ДНК, нуклеосомам, кардиолипину, некоторым фракциям комплемента. Первыми в гломерулах обычно осаждаются иммунные комплексы, антигеном в которых являются нуклеосомы, тропные к анионным участкам базальных мембран. В дальнейшем происходит осаждение ЦИК с другими антигенами.
Накопление иммунных комплексов под эндотелием, эпителием, в базальных мембранах, межуточной ткани нарушает мембранную проницаемость, активирует нейтрофилы, цитокины, систему комплемента и другие эффекторные механизмы воспалительного ответа. В конечном итоге пролиферируют клетки клубочков, расширяются мезангиальные пространства, в виде «проволочных петель» утолщаются базальные мембраны капилляров, подвергаются фибриноидному некрозу и склерозируются капиллярные петли. Ситуация усугубляется повреждениями эндотелия и ишемией тканей из-за микротромбозов ренальных сосудов, вызванных развитием волчаночного варианта антифосфолипидного синдрома.
Классификация
В качестве основного критерия систематизации вариантов люпус-нефрита использованы морфологические изменения почечных структур, их распространенность и клинические проявления. Такой подход позволяет максимально точно спрогнозировать течение заболевания и подобрать оптимальную схему лечения. Эксперты ВОЗ различают 6 классов волчаночного нефрита:
- Класс I – мезангиальный нефрит с нормальными клубочками. Морфологические изменения мезангия не выражены, при электронной или иммунофлуоресцентной микроскопии в нем определяются иммунные комплексы. Клиническая симптоматика отсутствует. Наиболее прогностически благоприятный вариант патологии. Пациенты нуждаются в динамическом наблюдении и скрининговых исследованиях для контроля над состоянием почек.
- Класс II – пролиферативный мезангиальный нефрит. Отмечается расширение мезангия, увеличение количества мезангиальных клеток, наличие осажденных ЦИК. В осадке мочи могут выявляться эритроциты, суточная протеинурия не превышает 500 мг. Клинические симптомы поражения почек отсутствуют. Прогноз благоприятный. Базисная терапия предполагает прием блокаторов ангиотензиновых рецепторов, глюкокортикостероидов в низких и средних дозировках.
- Класс III – пролиферативный очаговый гломерулонефрит. До половины гломерул подверглись эндо- и экстракапиллярной клеточной пролиферации. Участки воспаления сегментарно распределены в паренхиме. Определяется протеинурия и гематурия. Гипертензия, нефротический синдром, повышение концентрации сывороточного креатинина наблюдаются редко. Кроме кортикостероидов назначают цитостатические препараты. Прогноз различный.
- Класс IV – пролиферативный диффузный гломерулонефрит. Иммуновоспалительному некрозу и склерозированию подверглось больше половины гломерул. В клинической картине кроме лабораторных изменений часто выявляется повышение давления, нефротический синдром. Уровень сывороточного креатинина обычно увеличен. Необходима комплексная терапия цитостатиками и стероидами. Прогноз серьезный.
- Класс V – мембранозный гломерулонефрит. Гломерулярная мембрана утолщена. Обнаруживается субэпителиальное и интрамембранозное отложение иммунных комплексов. Преобладает клиника нефротического синдрома, у некоторых больных возможно увеличение АД, появление эритроцитов в моче, изредка повышается уровень креатинина. Рекомендована иммуносупрессорная терапия разными препаратами и ЗПТ. Прогноз сомнительный.
- Класс VI – склерозирующий гломерулонефрит. Склерозировано более 90% клубочковых капилляров. Быстро возникает и нарастает хроническая почечная недостаточность при минимальных изменениях мочевого осадка. Прогноз неблагоприятный. Пациентам требуется раннее назначение заместительной почечной терапии и пересадка почек. Без радикального лечения заболевание переходит в терминальную стадию.
Отечественными специалистами предложена классификация люпус-нефрита с учетом тяжести, особенностей течения и исходов патологического процесса. Быстропрогрессирующую форму аутоиммунного воспаления почек с нефротическим синдромом, злокачественной гипертензией, ранним возникновением ХПН, плохим прогнозом выявляют у 10-12% больных СКВ. Активный нефрит с признаками волчаночного нефротического синдрома обнаруживают у 30-40% пациентов. В 30-33% случаев определяется активный гломерулонефрит, в картине которого преобладает мочевой синдром. У 15-30% больных нефрит протекает латентно и диагностируется только лабораторно.
Симптомы волчаночного нефрита
Заболевание развивается в среднем через год после постановки диагноза СКВ, хотя может быть и единственным висцеральным проявлением волчанки. В 40% люпус-нефрит имеет бессимптомное течение и выявляется лабораторно. В клинике обычно преобладают признаки основной патологии (поражения суставов, характерная эритема, серозиты), к которым присоединяются отеки, локализованные на лице и наиболее выраженные по утрам, уменьшение суточного количества мочи. 2-5% больных отмечают появление видимой примеси крови в моче. При прогрессировании процесса у 60-70% пациентов возникает стойкая артериальная гипертензия с высокими значениями диастолического давления, рефрактерная к традиционным гипотензивным препаратам. Общее состояние зависит от выраженности морфологических изменений, при нефрите легкой степени нарушения отсутствуют, при тяжелом течении нарастают симптомы интоксикации, появляется кожный зуд, сильные головные боли.
Осложнения
Заболевание часто приводит к формированию или обострению сердечно-сосудистой патологии. Наиболее распространенными осложнениями волчаночного нефрита, развивающимися вследствие поражения сосудов при симптоматической артериальной гипертензии с дислипидемией, являются ишемическая болезнь сердца, инсульты. У пациентов могут возникать тяжелые инфекционные процессы (сепсис, некурабельные пневмонии, туберкулез), связанные с резким снижением иммунитета при длительном лечении кортикостероидами и цитостатиками. Нефрит при волчанке повышает риск злокачественной трансформации клеток, в частности – лейкоцитов с развитием В-клеточных лимфом. Почечная недостаточность как исход волчаночного гломерулонефрита обнаруживается у 10-15% больных. У 36% пациентов с быстропрогрессирующим заболеванием наблюдается ДВС-синдром.
Диагностика
Постановка диагноза волчаночного нефрита обычно не представляет сложностей при наличии характерной симптоматики заболевания. Диагностика может быть затруднена, если гломерулонефрит является единственным органным проявлением СКВ. При подозрении на волчаночный генез поражения почек рекомендованы следующие методы исследований:
- Общий анализ мочи. Соответственно клиническому варианту люпус-нефрита в осадке могут определяться эритроциты, лейкоциты, цилиндры. Для всех форм волчаночного гломерулонефрита кроме I класса характерна протеинурия от 200 до 3000-3500 мг белка/сут и более.
- Содержание креатинина в крови. Обычно показатель повышен у пациентов с диффузным пролиферативным люпус-нефритом, реже — при очаговом, мембранозном поражении, склерозирующей форме заболевания. Высокий креатинин служит прогностически неблагоприятным признаком.
- Исследование крови на антитела. Обнаруживается наличие антинуклеарного фактора, антинуклеарных антител, антител к ds-ДНК, нуклеосомам, гистонам. С1q. При проведении анализа применяют иммунофлуоресцентные и иммуногистохимические методы.
- Волчаночный антикоагулянт (LA). Умеренные и высокие показатели теста характерны для сочетания нефрита с антифосфолипидным синдромом. Положительные результаты свидетельствуют о повышенном риске усугубления аутоиммунного воспаления тромботическими процессами.
- Пункционная биопсия почек. Гистологическое исследование биоптата позволяет выявить патогномоничные морфологические изменения тканей. Проводится всем больным с подозрением на люпус-нефрит при измененном общем анализе мочи или повышенном сывороточном креатинине.
В общем анализе крови часто определяется снижение уровня лейкоцитов, эритроцитов, тромбоцитов, ускорение СОЭ. В качестве вспомогательных методов, позволяющих оценить выраженность структурных изменений и функциональную состоятельность почечной паренхимы, могут выполняться УЗИ, КТ, МСКТ, МРТ почек, экскреторная урография, нефросцинтиграфия, комплексное биохимическое исследование крови, нефрологический комплекс, оценка системы гемостаза. Дифференциальная диагностика люпус-нефрита проводится с быстропрогрессирующим и хроническим гломерулонефритом, лекарственной нефропатией, поражениями почек при ревматоидном артрите, других системных заболеваниях соединительной ткани, миеломной болезни, аутоиммунном гепатите, геморрагическом васкулите, первичном и наследственном амилоидозе. По показаниям пациента кроме уролога, нефролога и ревматолога консультирует терапевт, гепатолог, гематолог, онколог, онкогематолог, токсиколог.
Лечение волчаночного нефрита
Основными терапевтическими задачами при ведении пациентов с СКВ, у которых диагностирован специфический гломерулонефрит, являются индукция ремиссии, максимально долгое сохранение функциональной состоятельности паренхимы, профилактика рецидивов и осложнений, улучшение качества жизни и показателей выживаемости. При выборе схемы лечения учитывают активность аутоиммунного процесса, потенциальную обратимость деструктивных изменений, выраженность почечной недостаточности. Больным с неактивным процессом (I класс люпус-нефрита) рекомендован периодический скрининг состояния почек и назначение препаратов для коррекции других клинических проявлений СКВ.
При волчаночном гломерулонефрите II класса терапию начинают с ингибиторов АПФ, оказывающих антигипертензивный и нефропротективный эффекты за счет снижения системного артериального давления без ущерба ренальному кровотоку. Терапевтическая резистентность состояния, нарастание протеинурии, появление признаков гематурии является основанием для дополнительного применения глюкокортикостероидов и имидазольных цитостатиков. Больным с активным люпусным воспалением гломерул III-V класса в качестве базисных назначают иммуносупрессивные лекарственные средства:
- Цитостатические препараты. Являются обязательным элементом индукционного и поддерживающего лечения. При агрессивном течении заболевания предпочтительна пульс-терапия сверхвысокими дозами алкилирующих производных диамидофосфата, которые ингибируют активность B-лимфоцитов. В последующем больных переводят на поддерживающие дозировки имидазольных цитостатиков или селективных производных микофеноловой кислоты.
- Глюкокортикостероиды. В качестве монопрепаратов в настоящее время практически не используются. Эффективно дополняют цитостатическую терапию, обеспечивая более длительное сохранение почечных функций и лучшие показатели выживаемости. Обычно назначаются в низких дозировках и альтернирующих режимах приема. На начальных этапах лечения возможно проведение активной пульс-терапии высокими дозами.
Альтернативными методами ведения больных с терапевтически резистентными вариантами волчаночного гломерулонефрита являются применение ингибиторов кальциневрина, синтетических моноклональных антител к CD20 и CD22-антигенам мембран B-лимфоцитов, антицитокиновых препаратов, молекулярных блокаторов иммунной реакции. Апробируются и внедряются технологии тотального облучения лимфоидной ткани, костного мозга с последующей трансплантацией стволовых клеток.
Симптоматическая терапия люпус-нефрита направлена на коррекцию отдельных клинических проявлений заболевания. При развитии артериальной гипертензии и значительной протеинурии рекомендован прием ингибиторов АПФ или селективных блокаторов рецепторов ангиотензина II. Для устранения возможной дислипидемии используются статины. Пациентам с признаками антифосфолипидного синдрома показаны антикоагулянты и антиагреганты. Нарастание признаков почечной недостаточности, особенно при волчаночных гломерулонефритах V-VI класса, служит основанием для проведения ЗПТ (гемодиализа, перитонеального диализа, гемофильтрации, гемодиафильтрации и др.), а затем трансплантации почки после 3-6-месячного снижения активности аутоиммунного воспаления.
Прогноз и профилактика
Хотя развитие почечной патологии в целом ухудшает прогноз СКВ, при своевременной диагностике и адекватной терапии пятилетняя выживаемость наблюдается у 80-85% больных с тяжелыми формами гломерулонефрита и у 95% с процессами средней тяжести. Первичная профилактика волчаночного нефрита заключается в скрининговых обследованиях пациентов из группы риска по СКВ с целью раннего выявления и назначения комплексного лечения основной патологии, что позволяет снизить вероятность развития поражения почек. Для предупреждения прогрессирования уже имеющегося нефрита необходимо проведение длительной поддерживающей терапии.
Источник
